电解锰阳极液脱硒渣中硒和铁回收工艺探索
王周亮,王雨红,粟海锋
(1. 西南能矿集团有限公司,贵州 贵阳 550001; 2. 广西大学 化学化工学院, 广西 南宁 530004)
0 前 言
硒是一种重要的工业原料,也是动物和人体所必需的微量元素之一[1]。工业上广泛使用二氧化硒添加到锰电解液中以提高电流效率[2]。电解锰阳极液是电解金属锰生产过程中经过阳极室流出的溶液,由于阳极液中含有大量的硫酸锰、硫酸铵及硫酸,因此工业上一般将其补加硫酸作为浸出剂循环使用,但在浸出过程中,由于矿物中硅酸盐的吸附作用,导致阳极液中部分锰、氨、硒、硫酸根会随着锰矿浸渣排放而损失,其中,硒的损失达到85%[3]。无机硒是一种剧毒致癌物质,锰矿浸渣一般都是露天堆放,雨水冲刷会把硒带入周边的土壤和水源中,危害环境和人畜健康[4],且硒价格高昂。因此,对电解锰阳极液中的硒进行回收利用,将给电解锰企业带来经济环保的双重利益。
本文采用还原铁粉脱除锰阳极液中硒,硒以单质形式沉淀,渣中以硒和未溶解完全的铁为主[5]。针对硒渣中的硒,目前提取方法主要分为火法和湿法。其中火法包括硫酸化焙烧法、氧化焙烧法、苏打焙烧法等[6-9]。然而火法过程能耗大,烟气污染严重。湿法主要采用氧化剂或还原剂,将渣中不同形式的硒浸出。李倩等[10]采用煤油脱硫—氯酸钠氧化浸出—还原沉硒法处理硒酸泥,制备粗硒,硒的浸出率达到97.76%。郑雅杰等[11]采用Na2SO3从硒渣中浸出Se,当Na2SO3溶液浓度为2 mol/L时,Se浸出率达到66.78%。侯晓川等[12]在H2SO3-HCl-H2O复合体系中浸出镍钼矿冶炼烟尘中的Se,硒的浸出率大于98%。这些方法都能较好的解决相应硒渣中硒的回收,且湿法工艺能耗小、效率高,是硒回收的好的途径之一。
本文以电解锰阳极液经铁粉浸出后的残渣为研究对象,采用双氧水浸出硒渣中的硒,考察各影响因素对硒、铁回收过程的影响,硒渣经还原后获得硒酸及亚硒酸,直接返回到电解锰体系作为添加剂使用,残渣可作为铁精矿使用,从而实现硒资源循环利用的目的。
1 实验部分
1.1 实验原料
本文所使用的电解锰阳极液来自于广西某一大型电解锰企业,分析结果见表1,阳极液含锰13.56 g/L,含硒0.012 g/L,含硫酸33.10 g/L。实验所用还原铁粉含铁量大于98%。
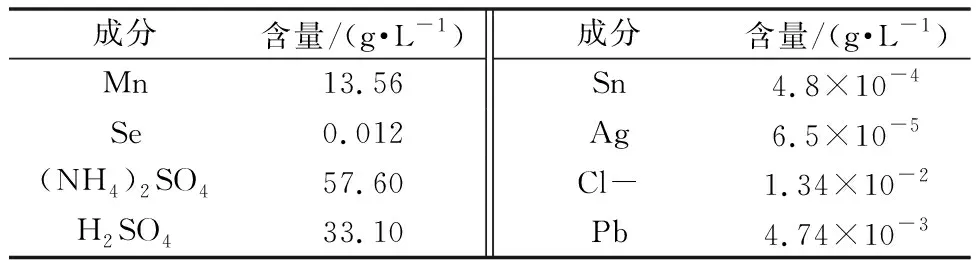
表1 锰阳极液的元素成分
脱硒渣是用铁粉还原脱除阳极液中硒后所剩残渣,反应条件为阳极液3 L,铁粉用量18 g,搅拌速度600 r/min,反应温度为90 ℃时,含硒量为94.16%。
1.2 试剂和仪器
主要试剂包括:硫酸、双氧水、硝酸、盐酸羟胺、1,10-菲罗啉、乙酸钠。主要仪器包括:电子分析天平,DF-101S集热式恒温加热磁力搅拌器、电热鼓风干燥箱、超级恒温水浴锅、721型分光光度计、JP-303型极谱分析仪、S-3400N型扫描电子显微镜及D/MAX2500 V型X射线衍射仪。
1.3 实验方法和步骤
1) 滤渣的制备。实验将3 L阳极液加入到5 L的烧杯中,置于超级恒温水浴中,开启搅拌装置,当温度达到设置温度后,加入一定量铁粉,开始计时,当反应结束后,过滤物料,取滤渣即硒渣放入烘箱中,120℃干燥2 h;
2) 硒渣浸出反应。将干燥好的滤渣研磨过0.15 mm(100 目)筛,称取一定量的硒渣放入小烧杯中,加入一定量的双氧水,开始计时,反应结束后,过滤物料,取滤液分析硒和铁的浸出率,其中硒采用催化极谱法测定[13],铁采用邻二氮杂菲分光光度法测定[13]。
2 结果与讨论
2.1 浸出工艺的单因素实验
2.1.1 不同反应条件下反应获得硒渣的影响
采用不同温度条件下反应的硒渣,并分别在相应反应温度下干燥24 h,获得50℃硒渣(含硒量33.40%),70℃硒渣(含硒量89.11%),80℃硒渣(含硒量97.56%),90℃硒渣(含硒量99.65%),0.200 0 g渣,在30℃反应,分别添加双氧水1.4 mL,不加硫酸,待达到反应时间后,过滤,分别测定溶液和硒渣中硒和铁的含量,计算硒、铁浸出率,结果如图1所示。
数据显示,随着制备硒渣的反应温度越高,产品中硒的含量也越高,当反应温度达到90℃时,产品中硒含量达到99.65%,相比30℃制备的硒渣中含硒量为12.47%有较大提高。从图1中可以看出,随着制备硒渣的反应温度提高,硒渣越易被双氧水浸出,这可能硒的结晶形态有关,当反应温度大于80℃时,红硒能够转变成灰硒。为了进一步确认,对硒渣进行了XRD和SEM分析,结果见图2~3。

图1 不同浸出时间条件下硒、铁浸出实验结果
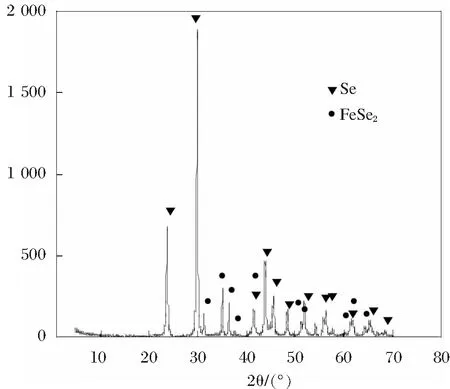
图2 固体产物的XRD图谱
从图2中可以看出,90℃反应的固体产物晶型发育较好,硒峰明显增强,产物中只存在Se和FeSe2两种物相,即锰阳极液中的硒还原成Se(-Ⅰ)和Se(0)两种形式,通过图3可以看出,硒结晶形态为球形的灰硒,这与30℃时形成的结构完全不同,可能也是导致硒浸出率高的原因。因此选取90℃渣完成后续试验。

图3 固体产物的SEM图谱
2.1.2 双氧水用量的影响
取90℃硒渣(含硒量99.65%)0.200 0 g,在30℃反应150 min,分别添加不同量的双氧水,不加硫酸,待达到反应时间后,过滤,分别测定溶液和硒渣中硒和铁的含量,计算硒、铁浸出率,结果如图4所示。
从图4中可以看出,随着双氧水用量的增加,硒、铁浸出率均显著增加,当双氧水的用量大于1.1 mL时,硒、铁浸出曲线趋于平缓,一般来说,单质Fe是不能与双氧水发生反应的,且在无酸的条件下,铁不能溶解,但图4(b)中,铁的浸出率随着双氧水用量的增加,结合XRD图2,进一步说明90 ℃反应后的硒渣中不存在单质铁的形式,硒渣中FeSe2与双氧水发生反应,导致Fe释放出来进入溶液中,因此,铁的浸出率会不断增大。后续试验选取双氧水用量为1.1 mL来进行。
2.1.3 硫酸用量的影响
由于在酸性条件下,双氧水具有很强的氧化性,且体系中有Fe2+存在时,会形成Fenton反应,产生羟基自由基,羟基自由基的氧化电位为2.8 V,仅次于氟,具有超强的氧化能力,其反应如式(1)~(2)所示。因此,通过试验,考察了不同硫酸用量对硒、铁浸出率的影响。

图4 双氧水用量对硒渣中硒、铁浸出影响
Fe2++H2O2→Fe+3+OH·+OH-
(1)

·HO2+H+
(2)
取90℃硒渣(含硒量99.65%)0.200 0 g,在30℃反应150 min,添加双氧水1.1 mL,分别添加硫酸0,0.1,0.3,0.5,0.8,1.1 mL,待达到反应时间后,过滤,分别测定溶液和硒渣中硒和铁的含量,计算硒、铁浸出率,结果如图5所示。
从图5(a)中可以看出,硒的浸出率随着硫酸用量的增加,先增后减,在硫酸用量为0.1 mL时最大,达到95.56%,继续增加硫酸用量,硒的浸出率逐步减小,但是变化不大,一般来说,增大酸用量会加快双氧水的分解,使浸出率急剧下降,但是本研究中变化不大,主要是因为直接添加浓硫酸的缘故,部分单质硒直接与硫酸形成亚砜结构而促进硒的溶解,因此,硒整体浸出率下降不明显,而随着硫酸浓度的增加,铁的浸出率逐渐增加,因此,从节约成本角度出发,选择添加硫酸0.1 mL进行后续试验。

图5 硫酸用量对硒渣中硒、铁浸出影响
2.1.4 温度的影响
温度升高,可以降低液相粘度,增加离子运动的速度,减小扩散阻力,有利于传质过程的进行,同时表面反应加快,可以显著提高浸出率。因此,本研究考察了反应温度对硒、铁浸出率的影响。取90℃硒渣(含硒量99.65%)0.200 0 g,分别在30,50,70,90℃反应150 min,添加双氧水1.1 mL,添加硫酸0.1 mL,待达到反应时间后,过滤,分别测定溶液和硒渣中硒和铁的含量,计算硒、铁浸出率,结果如图6所示。

图6 温度对硒渣中硒、铁浸出影响
从图6中可以看出,随着温度的升高,硒、铁浸出率都下降,这是因为温度越高,双氧水分解越严重,能参与反应的有效含量降低,从而导致硒、铁浸出率均降低,从成本及效果出发,后续反应温度选定30℃为宜。
2.2 浸出工艺的正交实验
为了探索双氧水浸出常温脱硒渣中硒的最佳工艺条件,分别以硒和铁的浸出率为目标函数,经过探索实验,确定影响硒、铁浸出率的主要因素为双氧水用量A、硫酸用量B、反应温度C、反应时间D,取0.200 0 g硒渣为定量,无搅拌,设计五因素四水平正交试验 L16 (54), 实验结果见表2。
2.2.1 硒的正交实验结果分析
将双氧水浸出常温硒渣中硒和铁的正交实验结果分析见表3。

表2 正交试验结果

表3 浸出硒渣中硒的正交试验结果
正交实验直观分析结果表明,双氧水用量,硫酸用量,反应温度,反应时间这4个因素对90℃脱硒渣中硒的浸出影响大小为:
双氧水用量>反应温度>硫酸用量>反应时间
正交实验中硒浸出的最优方案为:A4B3C3D3。
即反应时间130 min,双氧水用量1.4 mL,反应温度70 ℃,硫酸用量0.6 mL,此时硒的浸出率达到99.51%。
2.2.2 铁的正交实验结果分析
铁的正交试验结果分析见表4。
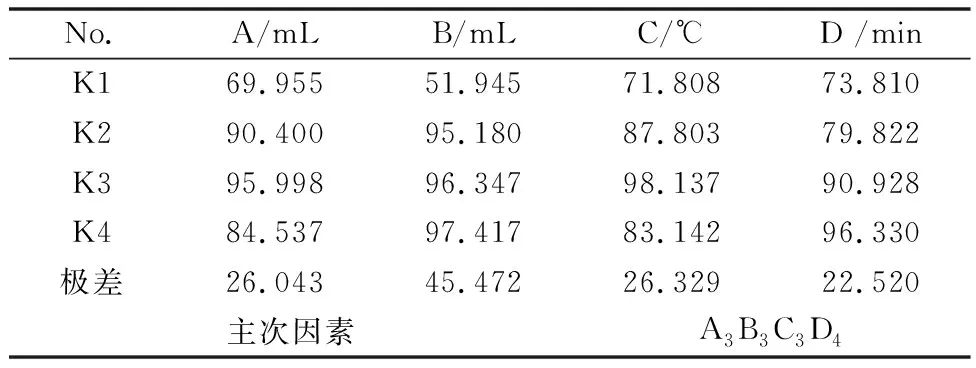
表4 浸出脱硒渣中硒的正交试验结果
从表4可知:硫酸浓度,双氧水用量,硫酸用量,反应温度,反应时间对90 ℃脱硒渣中铁的浸出影响大小为:硫酸浓度>反应温度>双氧水用量>反应时间。
正交实验中铁浸出的最优方案为:A3B3C3D4。
即硫酸浓度0.6 mL,反应温度70℃,反应时间180 min,双氧水用量1.1 mL,此时铁的浸出率达到100%。
由于在脱硒渣铁的浸出过程中,最好实现硒的完全溶解,而铁不发生反应,以达到分离的目的,因此选择不添加硫酸,反应时间130 min,双氧水用量1.4 mL,反应温度70℃,作为最优条件,此时硒的浸出率达到98.51%。
3 结 论
1) 不同反应条件下制备的硒渣,随着反应温度越高,渣中含硒量也越高,也越易被双氧水浸出,经研究,90℃制备的硒渣产物中只存在Se和FeSe2两种物相,硒结晶形态为球形的灰硒,这与30℃时形成的结构完全不同,可能是导致硒浸出率高的原因。
2) 双氧水用量越大,硒、铁浸出率也随之增大;硫酸用量的增加,对硒浸出率影响不大,可能是因为单质硒与硫酸形成亚砜结构;温度越高,双氧水分解越厉害,从而导致有效成分的减少,降低了硒、铁浸出率。
3) 单因素实验表明,90℃制备的硒渣在反应温度30℃情况下,添加双氧水1.1 mL,硫酸0.1 mL,反应150 min,硒的浸出率达到95.56%,铁的浸出率达到92.93%。
4) 正价实验结果表明,对90℃脱硒渣中硒的浸出影响大小为:双氧水用量>反应温度>硫酸用量>反应时间。正交实验中硒浸出的最优方案为:反应时间130 min,双氧水用量1.4 mL,反应温度70℃,硫酸用量0.6 mL,此时硒的浸出率达到99.51%。
5) 反应时间对90℃脱硒渣中铁的浸出影响大小为:硫酸浓度>反应温度>双氧水用量>反应时间。正交实验中铁浸出的最优方案为:硫酸浓度0.6 mL,反应温度70℃,反应时间180 min,双氧水用量1.1 mL,此时铁的浸出率达到100%。
6) 综合正交实验中铁和硒的浸出考虑,得出较优方案为:不添加硫酸,反应时间130 min,双氧水用量1.4 mL,反应温度70℃,作为最优条件,此时硒的浸出率达到98.51%,铁的浸出率达到94.18%。

