小剂量地塞米松预防经皮肾镜取石术并发全身炎症反应综合征的疗效观察
徐辉 谢天朋 肖日海 邹晓峰 袁源湖 伍耿青 王晓宁 刘佛林 张兆林 夏维 郭桂军 肖观称 黄若辉 张国玺
1赣南医学院第一附属医院泌尿外科 赣南医学院泌尿外科研究所 341000 江西赣州
泌尿系结石是临床常见的疾病之一,微创技术的发展推动了泌尿系结石的治疗,PCNL已逐步代替了传统的开放手术,成为上尿路结石最主要的治疗手段之一。随着PCNL技术在我国的推广及普及,PCNL手术并发出血、感染等并发症逐渐被泌尿外科医生认知,感染性休克是PCNL手术最为凶险的并发症之一,临床报道为0.6%~1.5%[1],死亡率高达20%~40%[2]。
全身炎症反应综合征(systemic inflammatory responsible syndrome, SIRS)是感染性休克的初级级联反应,降低PCNL并发SIRS是控制术后感染性休克的早期措施。如何运用干预手段来减少SIRS的发生,目前的研究报道很少,我们于2014年5月开始运用小剂量地塞米松对有SIRS高危因素的患者行PCNL手术治疗时予以干预,观察其效果,现报告如下。
1 资料与方法
1.1 临床资料
1.1.1研究对象 分析2014年5月~2015年8月在我院行PCNL患者资料,手术均由有100例以上手术经验泌尿外科副高职称的医师完成。纳入标准:①接受一期单侧PCNL手术上尿路结石者;②ASA为Ⅰ~Ⅱ级;③有SIRS高危因素之一者(术前存在尿路感染,结石负荷≥500 mm2,术中碎石手术时间≥120 min)。排除标准:①术前体温、心率、呼吸及血液分析检查结果异常可能干扰术后SIRS诊断者;②术前已行肾造瘘或放置输尿管支架管者;③肾功能异常者[3, 4]。
1.1.2SIRS诊断标准 以美国胸科医师学会和危重病医学会联席会议诊断为标准。包括下列两项或两项以上体征:体温>38℃或<36℃;呼吸频率>20次/min或PCO2<4.256 kPa(32 mm Hg);心率>90次/min;外周血白细胞计数>12×109/L或<4×109/L或未成熟细胞>10%。上述4项标准符合≥2项者诊断成立[5]。
1.2 手术方法
参考文献[6]的方法,建立F18~20通道,行钬激光碎石,清除结石后留置双J管及肾造瘘管结束手术。
1.3 研究方法及监测指标
术前记录患者术前一般情况包括年龄、性别、ASA分级、糖尿病,收集术前患者尿液分析情况、中段尿培养结果、结石负荷情况。患者随机分为常规组和地塞米松组,术前给予预防性和治疗性的抗生素治疗,地塞米松组在碎石30 min时予以静推地塞米松注射液(0.1 mg/kg)或碎石超过120 min时使用,常规组术中不予地塞米松,术后监测SIRS各指标及感染性休克的发生率情况。
1.4 统计学方法
2 结果
共入选54例患者,其中男17例,女37例,平均(43.4±9.2)岁。其中左侧29例,右侧25例。术前诊断均为上尿路结石,尿液分析32例提示尿路感染(WBC +~++++),中段尿培养出细菌11例,其中大肠埃希氏杆菌5例,肺炎克雷伯杆菌3例,粪肠球菌3例,尿路感染患者术前根据培养结果或经验性用药治疗3~5 d再行手术治疗。常规组和地塞米松组患者在年龄、性别、ASA、糖尿病、尿路感染和结石负荷无明显差异(P>0.05)(表1)。手术均获成功,无需输血患者。手术均为单一通道,术后SIRS异常情况如表2,术后共有8例患者诊断为SIRS,其中2项指标达诊断标准者5人,3项2人,4项1人,术后常规组诊断为SIRS者7例(25.9%),地塞米松组1例(4%),诊断SIRS的患者予积极治疗后大部分明显好转;常规组1例患者4项指标达标者术后感染严重,并发感染性休克,后经抢救治疗后痊愈。与常规组相比,地塞米松组术后并发SIRS的发生率较低,差异有统计学意义(P<0.05)。54例结石取净率92.6%,3例患者后行二期PCNL取石。
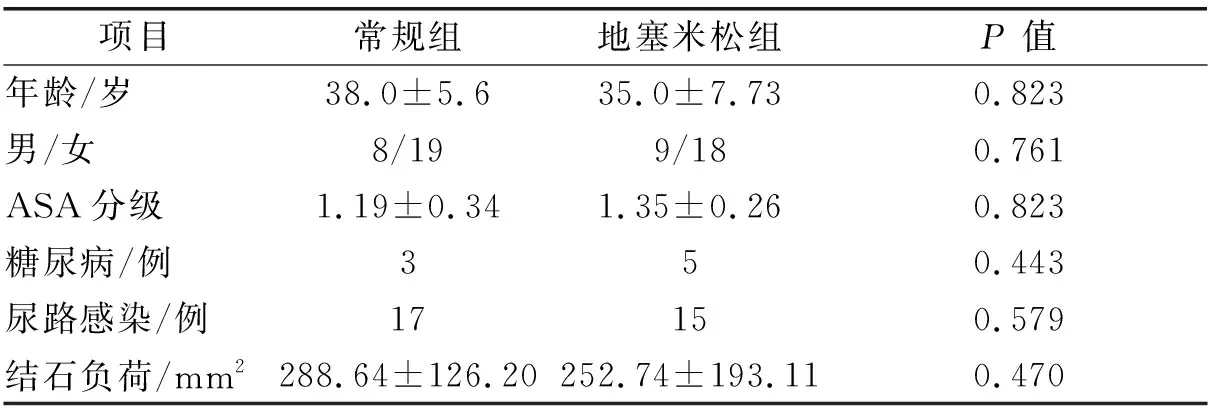
表1 两组患者术前指标比较
3 讨论
SIRS是20世纪90年代初提出来的概念,认为感染、创伤、休克最后均通过一条共同的路径发展至多脏器功能衰竭,这一共同的路径即SIRS[7]。SIRS是整个病理生理过程一个可逆转的中间环节。机体受损开始到出现全身炎症发应呈现一个动态级联过程,依次为轻度发热、SIRS、感染中毒性休克及多器官功能衰竭。现有的研究发现,SIRS的诊断对于预测感染性休克患者的预后是一个简单而有意义的预测指标。故我们选择研究预防SIRS的发生对于防止PCNL术后感染导致进一步严重后果,以期降低术后感染相关并发症发生率具有重要意义[8]。
国内学者很早开始了PCNL术后SIRS变化与疾病进展的研究,陈仙等[9]2009年在一组280例PCNL超声碎石术后分析发现,在并发症、二次感染、血小板减少、C反应蛋白增高方面,PCNL超声碎石术后并发SIRS患者机体损害的发生率高于未并发SIRS的患者。其他学者的研究也发现预防SIRS的发生对降低术后并发症的发生有重要意义[10]。
在感染性休克现代治疗中,激素得到广泛应用,现有的研究推荐小剂量生理剂量替代治疗,已不推荐应用大剂量糖皮质激素,并于应用1周后逐渐减量是较为一致的认识[11]。激素治疗感染性休克是通过稳定血液动力学指标起治疗作用,且早期应用是关键,故对于临床有SIRS高危因素的患者,我们使用小剂量激素干扰感染所引起的“多米诺骨牌效应”,在抗生素治疗的同时,术中单次加用小剂量激素试图降低SIRS的发生,以达到预防感染性休克的目的。
本研究选择了术前存在尿路感染,结石负荷≥500 mm2,术中碎石手术时间≥120 min作为PCNL术后并发SIRS的高危因素。对于经皮肾镜术后并发SIRS的高危因素分析,已有多位学者对此进行了研究,周少丽等[3]认为手术时间≥120 min、尿培养阳性、术前尿中白细胞数、右美托咪定是有独立作用的影响因素。亦有学者研究认为术前存在尿路感染、患侧上尿路完全梗阻、结石负荷≥500 mm2、术中碎石手术时间≥120 min、术中发现脓肾是高危的因素[4]。我们选取结石负荷≥500 mm2、手术时间≥120 min和尿路感染作为高危因素,未选择尿培养阳性作为高危因素,是因为存在完全上尿路梗阻合并感染,但尿培养阴性的情况。结石负荷和手术时间有可能是相关因素,但亦可能是独立因素,故分别考虑。对于术中发现脓肾的患者,我们常规改为肾造瘘后行二期手术,故此类病例亦未列入研究,对于铸型结石患者,我们多采用F20通道,以达到降低肾盂内压力,提高取石效率的目的。
本资料患者术中生命体征均平稳,术后共有8例患者(常规组7例,地塞米松组1例)诊断为SIRS,其中2项指标达诊断标准者5例,3项2例,4项1例,常规组的发生率(25.9%)高于一般经皮肾镜手术,和多数有高危因素手术报道类似[3],地塞米松组发生率4.0%,低于已有报道的高危组SIRS发生率[4]。本组的手术医师均为手术操作熟练的副高以上人员,避免了主观因素的导致的偏差。本研究中排除多通道因素,没有考虑多通道的因素。无输血患者,则术中无大的血管损伤,减少了术中细菌及毒素入血的机会。减少了此情况对此研究的影响。我们研究表明地塞米松组术后并发SIRS的发生率低于常规组(25.9%vs. 4.0%),差异有统计学意义(P<0.05),提示对于术前诊断有SIRS高危因素的患者,经皮肾镜取石术中早期预防性应用小剂量地塞米松能够减少SIRS的发生。
尽管糖皮质激素的应用饱受争议,但不可否认其在感染性休克治疗中使用广泛,严格说来,激素只有在应用抗生素的基础上才能真正起到治疗作用,这是运用小剂量地塞米松的前提,也是理解地塞米松作用基础[11]。并且小剂量地塞米松可改善应激状态下的肾上腺皮质功能[12],从而减少术后SIRS的发生。Minneci等[13]的Meta分析结果显示,短期疗程使用生理剂量的糖皮质激素,可提高治疗成功率。近年的研究显示,小剂量的激素有助于休克的治疗,降低器官功能损害,提高存活率[14]。我们的研究也表明,手术期间使用单次小剂量激素安全,无明显副作用。但亦要认识到单纯依靠激素无法治愈感染,必须同时使用抗生素才能取得感染治疗的成功,对于有适应征的患者,我们均按照指南在术前给予治疗性和预防性的抗生素治疗。