利拉鲁肽对糖尿病合并急性心肌梗死患者的疗效
岳晓燕 张大卫
中国糖尿病患者数量多年位列世界第一,2017年患病人数1.144亿,死亡人数84万,其中约半数(男47.5%,女49.7%)死于心血管疾病[1]。另一方面,我国近年急性心肌梗死(acute myocardial infarction,AMI)死亡率快速上升[2],由于冠心病合并糖尿病者的病程进展迅速[3],发生AMI后虽然通过急诊经皮冠状动脉介入术(percutaneous coronary intervention,PCI)的积极治疗,术后发生心源性休克、恶性心律失常、心力衰竭及死亡的风险仍远高于非糖尿病患者。因此,兼具降糖及心血管保护作用的新型降糖药物胰高血糖素样肽-1(Glucagon-like peptide-1,GLP-1)类似物利拉鲁肽(liraglutide),在此类患者中所发挥的作用日益受到关注[4]。本文选取2型糖尿病(type 2 diabetes mellitus,T2DM)合并急性ST段抬高型心肌梗死(ST-segment elevation myocardial infarction,STEMI)者50例,行PCI后加用利拉鲁肽观察其降糖及心血管保护作用。
1 资料与方法
1.1 临床资料
选取2016年10月—2018年5月收治的T2DM并STEMI行急诊PCI者100例,随机分为试验组和对照组。两组一般资料差异无统计学意义(P>0.05),见表1。排除标准:(1)合并酮症酸中毒;(2)胰腺炎或恶性肿瘤史;(3)陈旧心梗或冠状动脉旁路移植术史;(4)心肺复苏>30 min;(5)妊娠哺乳期女性;(6)血液透析。
1.2 研究方法
采用经桡动脉途径行冠脉造影术,病变符合给予置入雷帕霉素药物涂层支架。试验组PCI术后在原有降糖方案基础上加用利拉鲁肽(生产厂家:丹麦诺和诺德公司,批准文号:国药准字J20110026)0.6~1.8 mg/d,治疗12周,既往胰岛素治疗者将胰岛素剂量减量。对照组继续原有降糖方案,应用降糖药物(包括二甲双胍、磺脲类、格列奈类、α-糖苷酶抑制剂)及(或)胰岛素严格控制血糖,治疗12周。余治疗按《STEMI诊疗指南》[5]进行。
1.3 观察指标
术前、术后2 w、12 w的HbA1c、FBG、BMI、TC、TG、LDL-C、LVEF、LVED、E/A;主要心血管事件(恶性心律失常、心源性死亡、再次心梗)、药物副反应。
1.4 统计方法
采用SPSS 19.0软件进行统计分析,计量资料用(±s)表示,同时间点的组间指标采用t检验;计数资料采用χ2检验,以P<0.05为差异有统计学意义。
表1 两组患者一般资料比较[n/(±s)]
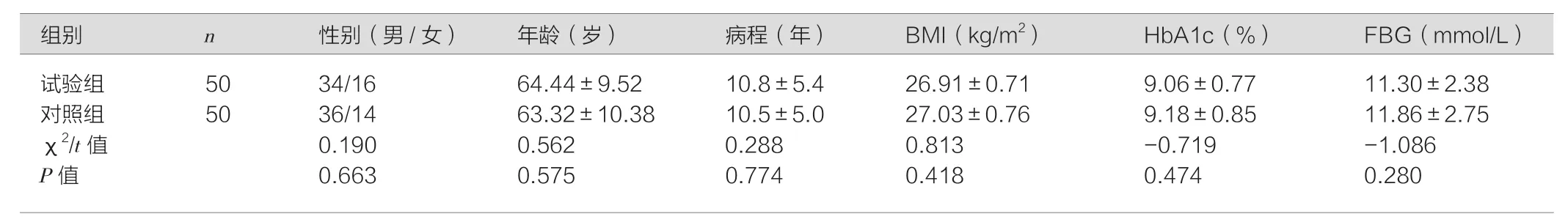
表1 两组患者一般资料比较[n/(±s)]
试验组 5034/1664.44±9.5210.8±5.426.91±0.719.06±0.7711.30±2.38对照组 5036/1463.32±10.3810.5±5.027.03±0.769.18±0.8511.86±2.75 χ2/t值 0.1900.5620.2880.813 -0.719 -1.086 P值 0.6630.5750.7740.4180.4740.280
2 结果
术后12 w试验组身体质量指数(BMI)、总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白(LDL-C)、左室射血分数(LVEF)、左室舒张末期内径(LVED)、舒张早期最大峰值速度/舒张晚期最大峰值速度(E/A)优于对照组(P<0.05),见表2、表3。对照组死亡1例,可能为心脏破裂。试验组有一过性恶心腹泻6例,能耐受。
3 讨论
2017年全球糖尿病患者4.25亿,其中20~64岁占比76.8%,发病年龄呈低龄化趋势[1],且发生冠心病的风险比非糖尿病者高出2~3倍[6],严重影响了劳动力人口的生活质量及预期寿命。当发生急性心梗时,高血糖损伤血管内皮,加快动脉粥样硬化进程,干扰心肌细胞代谢影响收缩舒张功能,降低机体代偿能力,限制心梗区域侧支循环开放,增加不良预后风险[7]。GLP-1的生理作用主要有:促进胰岛素分泌,促进β细胞再生,增加静息时能耗,抑制食欲,降低体质量[8]。另外,国内外多项研究都证实了GLP-1在发生急性心血管事件时的保护作用,其可能机制如下:改善血管内皮细胞功能,改善心肌细胞代谢,减少细胞凋亡,减少梗死面积,增加左心射血分数,改善心室重构,降低收缩压,恢复血管舒张功能[9-11]。
本文中,两组患者术后2 w的临床生化、心功能指标差异无统计学意义(P>0.05)。但随着随访时间的延长,术后12 w试验组在BMI、TC、TG、LDL-C、LVEF、LVED及E/A方面的控制情况优于对照组(P<0.05)。Chen WR等[12]研究证实,心梗患者在PCI治疗前给予利拉鲁肽保护受损心肌,术后与对照组相比LVEF水平明显升高,与本文结果一致。程向娟等[9]为研究GLP-1对心肌损伤的保护作用,以动物实验为基础建立大鼠心肌缺血模型,试验组于术前给予7天的利拉鲁肽治疗,再灌注后与对照组相比心肌梗死面积减少,心肌细胞凋亡数量减少。本文试验组应用利拉鲁肽治疗2 w后的心血管指标较对照组差异无统计学意义,提示临床获益时间与动物模型的获益时间尚存在一定差距;但术后12 w的LVEF、LVED及E/A均优于对照组(P<0.05),证实了利拉鲁肽在增加左室心功能和射血分数,降低左心室舒张末期压力,改善心室重构方面的作用。另外,利拉鲁肽心血管结局研究(LEADER研究)[13]指出,利拉鲁肽可将合并心血管疾病的T2DM患者心血管死亡风险降低22%。Beiroa D等[14]通过动物实验证实,利拉鲁肽可减少小鼠下丘脑摄食中枢饥饿信号的传导,从而增加饱食感,减少食物摄入;另一方面,利拉鲁肽可抑制脂肪生成转录因子水平减少内脏脂肪堆积,并增加非脂肪组织的能量消耗,从而降低小鼠体质量。本文试验组术后12 w的TC、TG、LDL-C、BMI指标优于对照组(P<0.05),同样证实了利拉鲁肽在降脂减重、保护血管内皮方面的作用。纪立农等[15]也充分肯定了利拉鲁肽疗效的可靠性及安全性。因此,推荐T2DM患者在发生STEMI行PCI后尽早加用利拉鲁并长期应用,以得到更多的心血管获益。
表2 两组不同时间生化指标比较(±s)

表2 两组不同时间生化指标比较(±s)
注:#与对照组相比,P<0.05,差异有统计学意义
试验组 术前 9.06±0.7711.30±2.3826.91±0.716.71±0.363.87±0.625.26±0.48术后2 w 7.57±0.556.63±1.2326.87±0.645.81±0.262.61±0.623.99±0.34术后12 w 6.36±0.445.93±0.8224.68±0.74# 3.97±0.31# 1.41±0.33# 2.67±0.29#对照组 术前 9.18±0.8511.86±2.7527.03±0.766.65±0.463.93±0.525.30±0.40术后2 w 7.68±0.537.02±1.0626.96±0.635.83±0.372.72±0.504.02±0.27术后12 w 6.53±0.486.13±0.8926.15±0.664.22±0.321.82±0.402.91±0.39 t值 术后2 w -1.024 -1.671 -0.742 -0.309 -1.023 -0.489 P值 0.3080.0980.4600.7580.3090.626 t值 术后12 w -1.819 -1.156 -10.460 -3.964 -5.549 -3.433 P值 0.0720.2510.0000.0000.0000.001
表3 两组不同时间心功能指标比较(±s)
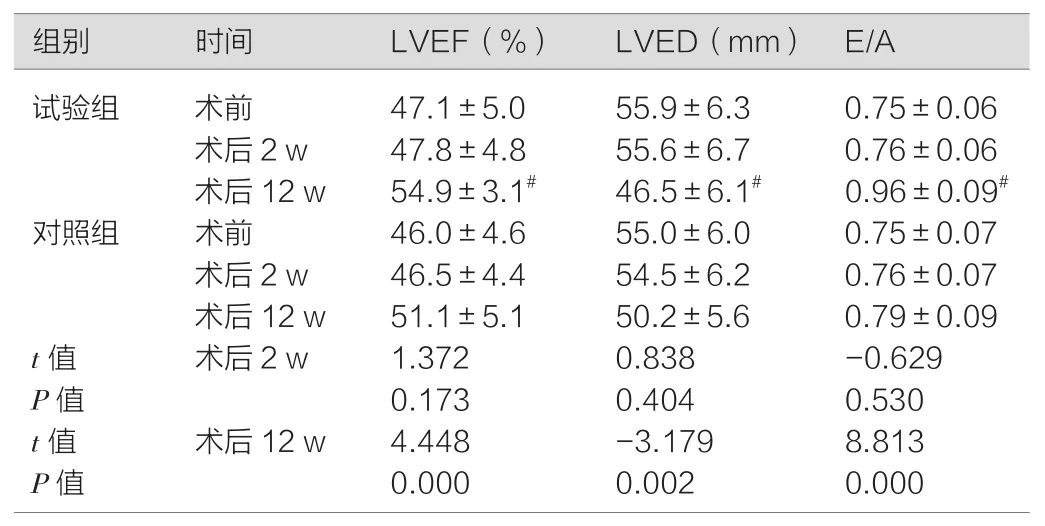
表3 两组不同时间心功能指标比较(±s)
注:#与对照组相比,P<0.05,差异有统计学意义
试验组 术前 47.1±5.055.9±6.30.75±0.06术后2 w 47.8±4.855.6±6.70.76±0.06术后12 w 54.9±3.1# 46.5±6.1# 0.96±0.09#对照组 术前 46.0±4.655.0±6.00.75±0.07术后2 w 46.5±4.454.5±6.20.76±0.07术后12 w 51.1±5.150.2±5.60.79±0.09 t值 术后2 w 1.3720.838 -0.629 P值 0.1730.4040.530 t值 术后12 w 4.448 -3.1798.813 P值 0.0000.0020.000

