HLA-G基因多态性对哮喘儿童缓解期肺功能的影响
为了解哮喘儿童缓解期肺功能情况及其可能的影响因素,对哮喘儿童进行随访检测缓解期肺功能情况,并分析HLA-G基因多态性、家族史、喂养史、合并变应性疾病等因素与肺功能障碍之间的相关性。
1 资料与方法
1.1 一般资料
选取2014年1月—2015年12月我院收治的84例哮喘儿童,符合《儿童支气管哮喘诊断与防治指南》[1]中的相关诊断标准。2016年1月—2017年12月随访检测肺功能68例(失访16例,失访率19%),复查肺功能检查时判断病情处于临床缓解期。平均起病年龄(3.19±0.23)岁;平均随访年龄(6.28±0.87)岁。其中男36例,女32例;汉族50例,壮族18例。
1.2 基因多态性检测
采用荧光PCR检测法检测患儿基因多态性,仪器采用全自动PCR基因检测仪(北京柯尔特生物仪器有限公司),检测过程严格按照临床检测标准进行[2-3]。
1.3 肺功能检测
应用德国Jaeger Master ScreeTM肺功能仪进行肺通气功能检测和脉冲震荡肺功能检测,仪器购于上海浦科生物仪器有限公司,检测指标包括患儿用力肺活量(FVC)、最大呼气流量(PEF)、第1秒用力呼气量占预计值百分比(FEV1)的变化。
1.4 统计学分析
采用SPSS 23.0统计学软件进行数据分析,正态计量资料用(±s)表示,计数资料采用例数或百分比表示,样本率的比较采用χ2检验或Fisher确切概率法,多因素分析采用Logistic回归模型,P<0.05为差异有统计学意义。
2 结果
2.1 肺功能测定结果
68例哮喘儿童在缓解期仍有25例(36.8%)存在肺功能指标异常,患儿PEF为(3.96±0.54)L/s,FVC为(2.13±0.58)L,FEV1为(2.14±0.51)L。
2.2 HLA-G和IL-10基因多态性与环境因素交互作用对哮喘儿童肺功能的影响
GMDR分析得到有统计学意义的最优模型为HLA-G rs1063320和生后4~6个月龄内的喂养史,见表1。HLA-G rs1063320的GG基因型、同时生后早期人工喂养,使得哮喘儿童发生肺功能异常的风险增加了1倍(OR=2.265,P=0.008),见表2。
3 讨论
哮喘是一种多基因遗传性疾病。本课题组之前的研究结果发现HLA-G基因的rs1063320的CC基因型与儿童哮喘易感相关;rs 1800871的TT基因型与儿童哮喘高IgE水平相关。为探讨儿童哮喘控制期肺功能异常与基因和环境因素的相关性,本文进行了回顾性研究[4-7]。
小气道是指光镜对传导气道数字成像时直径小于2 mm的部分,包括细支气管和终末支气管。哮喘为气道慢性炎症性疾病,已证实小气道炎症在哮喘的所有病程阶段均存在并且在发病机制中占重要作用[8-10]。哮喘时小气道可以对组胺产生过高的反应性,慢性炎症的存在还使得小气道被气道黏液及炎症细胞分泌物所堵塞,并出现管壁增厚、管腔狭窄,甚至关闭,进一步导致气道阻力增高,呼气受限和呼气困难。
特应性是哮喘的表型特征,而人类白细胞抗原(HLA)在抗原加工提呈和调节免疫应答中的关键作用中影响免疫反应特应性。HLA决定对抗原起反应的辅助T淋巴细胞基因,在抗原加工提呈和调节免疫应答过程中起关键作用,因而影响免疫反应的特应性。前期研究表明广西哮喘儿童HLA-DR等位基因遗传易感性呈一定特点。本课题组之前的研究显示HLA-G rs1063320的GG基因型是儿童哮喘的易感基因型。本研究中,虽然未发现该基因型与哮喘患儿的小气道功能障碍相关,但发现HLA-G基因与母乳喂养史存在交互作用。HLA-G rs1063320的GG基因型与人工喂养史同时作用可使得哮喘儿童发生小气道障碍的风险升高(OR=2.265,P=0.008)。这一发现符合哮喘受遗传与环境共同影响的认识。提示,母乳喂养对具有哮喘易感遗传因素的人群具有一定的保护作用,与一项荟萃分析结论一致[11-12]。
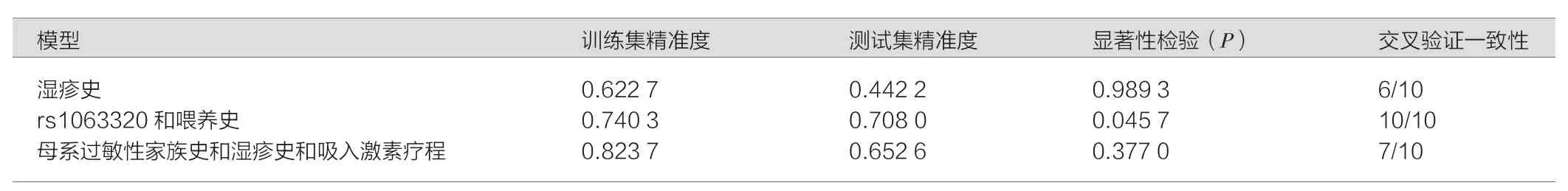
表1 GMDR分析肺功能异常影响因素的最优模型
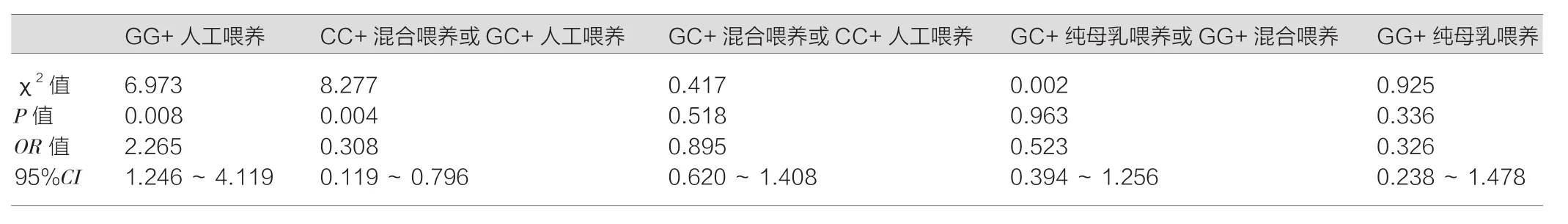
表2 HLA-Grs1063320和母乳喂养史不同组合与肺功能异常的关联分析
综上所述,哮喘儿童在缓解期仍有较高比例病例存在小气道功能障碍。湿疹史、HLA-G rs1063320的GG基因型与生后早期人工喂养可能增加哮喘小气道功能障碍的风险。

