一个铜掺杂的缺位Keggin型链状杂化材料的合成与表征
刘亚冰,李明阳,裴桐鹤
(吉林建筑大学 材料科学与工程学院,长春 130118)
Keggin型多金属氧酸盐(Polyoxometalates,POMs)作为金属氧簇家族具有划时代意义的一个重要分支,以其在工业催化、光催化降解有机污染物、医药化学及化学传感等领域具有广泛的应用前景而引起超分子化学、固体无机化学、配位化学及材料化学界的广泛关注。制备电子结构独特的光、电、磁学性能优异的Keggin型金属氧酸盐簇阴离子作为建筑块(Building block)的1D、2D和3D无机-有机杂化材料是材料学科及配位化学学科的重要研究热点[1-5]。近年来,随着水热合成技术在金属-氧簇合成中的广泛应用,大量具有新颖结构的抗病毒、光催化和工业催化等特性的经典、非经典的Keggin型簇及其衍生物被合成[6-11]。然而,相较于过渡金属取代、二帽、四帽及过渡金属配合物阳离子支撑等非经典金属氧簇及其衍生物,以缺位Keggin型簇阴离子为建筑块,尤其是以过渡金属取代的缺位Keggin型簇阴离子为建筑块,构筑多维新颖结构且具有优良功能特性的簇基材料却鲜有报道,自组装合成此类结构材料仍具有极大的科学挑战性[12,13]。
本文采用水热合成法,制备出一个以过渡金属取代的缺位Keggin型簇阴离子为建筑块,通过碱金属和过渡金属配合物阳离子连接成的一维“梯子”型双链状簇聚物{K(H2O)2[Cu0.5(en)][CuSiW11O39]}(H2en)2(1,en=乙二胺),并经元素分析、X射线单晶衍射、X射线光电子能谱、红外光谱等对其组成和晶体结构进行了表征,并研究了该材料的光催化降解性能。
1 实验部分
1.1 仪器与试剂
2400系II CHNS/O CHN型元素分析仪(美国Perkin-Elmer公司);3300D系ICP等离子体发射光谱仪(美国Perkin-Elmer公司);Spectrum One FTIR型红外光谱仪(测定范围250~4000cm-1,KBr压片;美国Perkin-Elmer公司);TGA7型热重(TG)分析仪(美国Perkin-Elmer公司);AXS Smart Apex 1000型X射线单晶衍射仪(德国Bruker公司);Thermol ESCALAB型X射线光电子能谱仪(XPS)(美国热电公司)
实验用K8SiW11O39·13H2O按文献的方法制备并经红外光谱及热重分析法确定结晶水的数目[14]。对氨基苯甲酸、氯化铜和乙二胺等化学试剂均为分析纯,购自国药集团上海化学试剂有限公司,使用之前未经进一步的纯化处理。
1.2 化合物的制备过程
在室温下将K8SiW11O39·13H2O(1.65g,0.5mmol),CuCl2·2H2O(0.34g,2.0mmol),C7NO2H7(对氨基苯甲酸)(0.185g,1.35mmol)和H2O(18mL,1000mmol)充分混合并放置在磁力搅拌器上持续搅拌120min,然后用0.2mL乙二胺(3.1mmol)调节反应体系的pH至5.5,装入30mL套有聚四氟乙烯内衬的不锈钢水热反应釜中,经密封后放置于160°C的烘箱中加热72h,关闭烘箱,逐渐冷却至室温,用蒸馏水充分清洗、分离、干燥、称量得到0.886g不规则块状晶体,按W计算产率为57.1%。元素分析及ICP实测值(%,C6H32Cu1.5KN6O41SiW11计算值),C,2.43(2.38);H,1.21(1.06);Cu,3.11(3.15);N,2.63(2.77);Si,0.864(0.927);K,1.31(1.29);W,66.81(66.76)(%)。
1.3 化合物晶体结构测定
尺寸为0.22mm×0.19mm×0.17mm的化合物1单晶被放置于Smart CCD单晶衍射仪样品支架上,296K温度下采用带有石墨单色器的Mo Kα射线(λ=0.071073nm)X光为辐射源,以ψ-ω扫描方式在1.12-28.38o的角度范围内共收集29636个衍射点,其中10233个独立衍射点[R(int)=0.0643]。衍射数据使用SAINT程序进行还原,并采用直接法运用SHELX-97程序完成晶体结构解析和数据精修。用全矩阵最小二乘法对所有的非氢原子坐标及各向异性参数进行了修正[15]。相关的结晶学数据和结构精修参数见表1。
2 结果与讨论
2.1 化合物的晶体结构
单晶X-ray衍射分析结果表明,化合物1是由一个新的过渡金属取代的缺位的Keggin型簇阴离子[CuSiW11O39]6-,碱金属和过渡金属配合物阳离子{K(H2O)2[Cu0.5(en)]}2+和两个充当抗衡作用的双质子化的乙二胺分子组成。传统的过渡金属取代的缺位Keggin型簇阴离子是由经典的Keggin型簇阴离子[SiW12O40]4-脱去一个[WO]4+基团得到了[SiW11O39]8-,过渡金属Cu2+取代[WO]4+基团的位置,形成[CuSiW11O39]6-[16]。本文报道的缺位簇阴离子与传统结构有所不同,它是在两个W的位置各缺失0.5,缺失的部分由过渡金属Cu取代,形成无序的簇阴离子结构。如图1所示,{SiO4}四面体居于簇阴离子的中心,以共边和共角的方式连接十个{WO6}八面体、1个{MO6}八面体和1个{MO5}四方椎形成过渡金属取得的缺位Keggin型簇结构。M为无序原子,M=0.5W+0.5Cu,两个无序原子的配位环境一个与钨原子相同,为畸变的八面体,另一个为畸变的四方锥。M-O键长的变化范围为1.91(3)-2.38(3)Å,O—M—O键角的变化范围为74.2(10)-170.5(10)˚。Si—O键长范围为1.62(2)-1.67(2)Å,O—Si—O键角范围为106.4(14)-111.3(14)˚。按照配位环境的不同,与W和M原子配位的氧可分为:(a)端氧(Ot):仅与一个金属原子配位的氧原子,共11个;二桥氧(O2b):与同一个三金属簇内的两个金属原子配位的氧原子,共12个;三桥氧(O3b):与不同三金属簇内的三个金属原子配位的氧原子,共12个;中心氧(Oc):同时与中心原子和金属原子配位的氧原子,共4个。W—Ot键的键长范围为1.69(2)-1.76(3)Å;W—O2b的键长范围为1.83(2)-1.93(2)Å;W—O3b的键长范围为1.86(3)-1.98(3)Å;W—Oc的键长范围为2.26(2)-2.39(2)Å。

表1 化合物1的晶体学数据

图1 化合物1的分子结构图,乙二胺分子、水分子上的H原子已删除
如图2所示,化合物1结构的独特性表现在一个簇阴离子通过{M(11)O6}上的O35原子与另一个簇阴离子的{M(12)O5}以M(11)-O(35)-M(12)的方式相连,形成了无限的1D簇阴离子链{[CuSiW11O39]8-}n,M-O键的键长分别为1.93(3)和2.02(3)Å。化合物1结构的另一个新颖性表现在结构中存在两种阳离子:Cu(1)2+和K(1)+。Cu(1)2+处于结构对称位置(对称码:-x+1,y,-z+1/2,占有率为0.5),Cu(1)2+被两个en上的四个N原子和一个水分子OW1配位,Cu(1)-OW1之间的距离是2.42(3)Å,Cu(1)-N之间的距离范围为2.04(4)-2.05(4)Å;K+分别和OW1、OW2两个水分子配位,K(1)-OW1和 K(1)-OW2之间的距离分别是2.67(4)Å和2.68(4)Å。这样,配位的Cu2+和K+离子通过OW1连接起来,形成{K(H2O)2[Cu0.5(en)]}2+混合金属配合物阳离子。同时,K+分别与相邻两个簇阴离子链上的O(16)、O(21)、O(25)和O(37)通过共价键作用相连接形成了新颖的一维“T”字形双链结构,K-O键的键长范围为2.82(4)-2.91(3)Å,主要的键长、键角列于表2中。经查阅文献所知,如此新颖结构被发现尚属首次。

图2 化合物1的一维“T”字型链状结构球/棍模型
如图3所示,相邻的“T”字型双链又通过O…Ow1…O、O…Ow2…O和N-H…O等氢键相互作用,形成新颖的三维超分子网络结构。典型的氢键相互作用如表3所示。

图3 化合物1由1-D链和水分子通过氢键链接的三维超分子网络图(乙二胺分子已去掉)

表2 化合物1的主要键长和键角

表3 化合物1的主要氢键
2.2 化合物1的红外光谱
图4为化合物1的红外吸收谱图,其测试范围是在200~4000cm-1范围内。主要的红外吸收峰为(KBr pellet,ν/cm-1):676.8(w),786.1(w),868.6(s),946.0(s),1053.2(s),1098.0(m),1168.5(w),1267.4(w),1395.1(w),1458.4(w),1582.3(s),2887.9(w),2941.6(w),3263.4(w),3311.0(w),3432.9(s)。其中,868.6cm-1是Si-O键的振动吸收峰,676.8、786.1、946.0和1053.2cm-1为W-O-W的反对称伸缩振动峰以及W=O伸缩振动吸收峰。3263.4-3432.9cm-1为O-H及N-H的伸缩振动;2887.9和2941.6cm-1为C-H的伸缩振动。

图4 化合物1的红外光谱
2.3 化合物1的光电子能谱(XPS)
图5为化合物1的光电子能谱(XPS)。W原子的XPS谱如图5(a)所示,得到35.8和38.1eV两个峰位,归属于W6+4f7/2、W6+4f5/2的电子结合能;Si原子的XPS谱图如5(b)所示,得到102.4eV的一个峰位,归属于Si4+2p3/2的电子结合能。

图5 化合物1的XPS
2.4 化合物1的TG研究
化合物1的TG分析是在空气环境下以每分钟10OC的升温速度在44℃~800℃的温度范围内测得的。如图6所示,在40℃~420℃温度范围内,化合物1的失重可分为两步。第一步在44℃-145℃失重1.22%,归属与两个结晶水分子;第二步在145℃~420℃范围内共失重5.99%,归属与三个乙二胺分子。这与理论计算值1.19%和5.95%均相吻合。

图6 化合物1的TG曲线
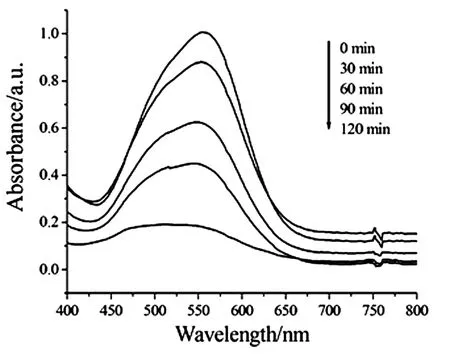
图7 化合物1光催化降解RhB溶液的吸光曲线和降解率变化图
2.5 化合物1的光催化性能研究
化合物1的光催化性能研究是选择典型的染料污染物罗丹明B(RhB)来模拟评价其纯化工业废水能力。将5mg化合物1在玛瑙研钵中研磨约10分钟以获得细粉末,然后将粉末分散在100mL浓度为1.0×10-5mol·L-1RhB溶液中。悬浮液在黑暗中磁力搅拌约30min,取悬浮液3mL,经离心分离后,取清液进行紫外光谱分析。之后暴露于400W Xe灯的照射下,保持液体表面和Xe灯之间的距离为5cm。在照射期间约790~800rpm搅拌速率下搅拌悬浮液。同样以30min的间隔,取5mL样品,以10000rpm离心5分钟,随后使用UV-vis光谱分析,图6显示了化合物1光催化降解RhB溶液的吸光曲线和降解率与光照时间的函数关系。从图中可以看出,在催化剂的作用下,RhB溶液的最大吸收峰随着紫外辐照时间的延长而逐渐减小,降解速率逐渐增大。经紫外线照射120min时,化合物1对RhB的降解率为81.5%,进而表现出良好的光催化活性。
3 结论
采用水热合成技术制备了一种具有新颖结构的簇基杂化材料,并对其进行了结构及性能表征。X-ray单晶结构分析表明:新颖的过渡金属取代的Keggin型缺位簇阴离子通过碱金属和过渡金属配合物阳离子连接成“梯子”型的一维链,链与链之间又经水分子连接成三维超分子网络,双质子化的乙二胺分子填充与网络中间。光催化性能研究表明,化合物1存在较强的催化降解能力。该簇基材料的成功合成再次证明水热合成法的优越性,其良好的光催化降解性能也展现了广阔的应用前景。

