血清脂蛋白相关磷脂酶A2在子痫前期的应用价值研究
刘 倩,兰 静,高 铮,赵 丹
(河北省保定市第一中心医院东院妇产科 071000)
子痫前期是在患者妊娠20周后所发生,在临床上主要表现为高血压与蛋白尿等妊娠阶段特有的,在初产妇和经产妇中子痫前期的发病率分别为3%~7%和1%~3%[1]。该疾病起病急,且无显著前驱症状,疾病发生后,是妊娠晚期、产后患者死亡的主要因素之一[2]。目前在临床上诱发子痫的原因及发病机制还不够明确,在临床上诊断、预防及治疗上存在一定的难度。子痫前期女性存在着较为明显的糖代谢异常、脂代谢异常。脂蛋白相关磷脂酶A2(Lp-PLA2)是一种特定的非依赖性的磷脂酶,在调节低密度蛋白上起到一定作用[3]。而Lp-PLA2是否参与子痫前期的发生发展,相关文献报道较少。本研究中探讨了子痫前期中脂代谢紊乱和Lp-PLA2水平的相关性,现将结果报道如下。
1 资料与方法
1.1一般资料 选择2014年1月至2016年1月在本院行剖宫产术终止妊娠的孕妇63例,其中正常妊娠组31例,年龄18~37岁,平均(27.81±4.15)岁;孕周35~40周,平均(39.4±1.1)周。子痫前期组患者32例,其中轻度子痫前期组15例,年龄21~39岁,平均(29.22±5.52)岁;孕周38~40周,平均(38.7±0.7)周;重度子痫前期组17例,年龄22~36岁,平均(28.07±4.25)岁;孕周32~39周,平均(37.53±1.72)周。轻度子痫诊断标准[4]:妊娠20周后血压(BP)≥140/90 mm Hg,尿蛋白≥0.3 g/24 h,上腹部不舒适,头部有疼痛症状。重度子痫诊断标准[5]:妊娠20周后BP≥160/110 mm Hg,尿蛋白≥2.0 g/24 h,或血清肌酐>106 μmol/L,或血小板<1.0×1011/L,或谷氨酸氨基转移酶和天门冬氨酸氨基转移酶水平上调,或有持续性头痛,或持续上腹不适。入组研究对象均无内外科相关疾病,即慢性高血压、肝肾功能损坏,以及其他可以影响患者血脂代谢的疾病等,体质量指数(BMI)正常,无其他妊娠并发症,未进入产程,均已剖宫产结束分娩。
本研究通过本院伦理委员会一致同意,全部研究对象均签署了知情同意书,并详细地了解研究的基本内容。
1.2方法 对产妇的基本情况进行收集,包括年龄、身高、收缩与舒张压、孕产数、孕周及BMI等信息。孕妇入院后空腹8~12 h,抽取静脉血4 mL,3 000 r/min,离心15 min分离血清。采用酶联免疫吸附试验(ELISA)检测Lp-PLA2(美国R&D公司)。应用生化分析仪对患者的血清总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、极低密度脂蛋白胆固醇(VLDL-C)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)和游离脂肪酸(FFA)进行检测。利用所得出的血脂结果对动脉硬化指数(AI)进行计算,公式为AI=(TC水平-HDL-C水平)/HDL-C水平[6]。
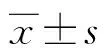
2 结 果
2.1各组研究对象一般资料比较 4组研究对象的BMI比较,差异无统计学意(P>0.05);子痫前期组收缩、舒张压和新生儿体质量与正常妊娠组比较,差异有统计学意义(P<0.05);重度子痫前期组和轻度子痫前期组的收缩压、舒张压和新生儿体质量比较,差异有统计学意义(P<0.05)。见表1。
2.2各组血脂水平比较 子痫前期组TC、TG、VLDL-C、LDL-C、FFA和AI显著高于正常妊娠组,HDL-C显著低于正常妊娠组,差异有统计学意义(P<0.05);重度子痫前期组TC、TG、VLDL-C、LDL-C、FFA和AI显著高于轻度子痫前期组,差异有统计学意义(P<0.05)。见表2。

表1 各组一般资料比较
注:与正常妊娠组比较,*P<0.05;与轻度子痫前期组比较,#P<0.05

表2 各组血脂水平比较
注:与正常妊娠组比较,*P<0.05;与轻度子痫前期组比较,#P<0.05
2.3各组Lp-PLA2比较 正常妊娠组血清Lp-PLA2为(16.79±6.99)μmol/L,子痫前期组Lp-PLA2为(30.56±9.45)μmol/L,子痫前期组Lp-PLA2显著高于正常妊娠组,差异有统计学意义(P<0.05);轻度子痫前期组Lp-PLA2为(26.38±9.49)μmol/L,重度子痫前期组Lp-PLA2为(34.46±10.69)μmol/L,重度子痫前期组Lp-PLA2显著高于轻度子痫前期组,差异有统计学意义(P<0.05)。
2.4Lp-PLA2和其他指标相关性分析 Lp-PLA2和TC呈正相关(r=0.551 5,P<0.05);Lp-PLA2和TG呈正相关(r=0.539 3,P<0.05);Lp-PLA2和LDL-C呈正相关(r=0.709 2,P<0.05);Lp-PLA2和HDL-C呈负相关(r=-0.466 4,P<0.05)。
2.5子痫前期相关因素Logistic回归分析 经过Logistic回归分析发现,Lp-PLA2、TG和LDL-C是子痫前期的独立危险因素(P<0.01),HDL-C是子痫前期的保护因素(P<0.01)。见表3。
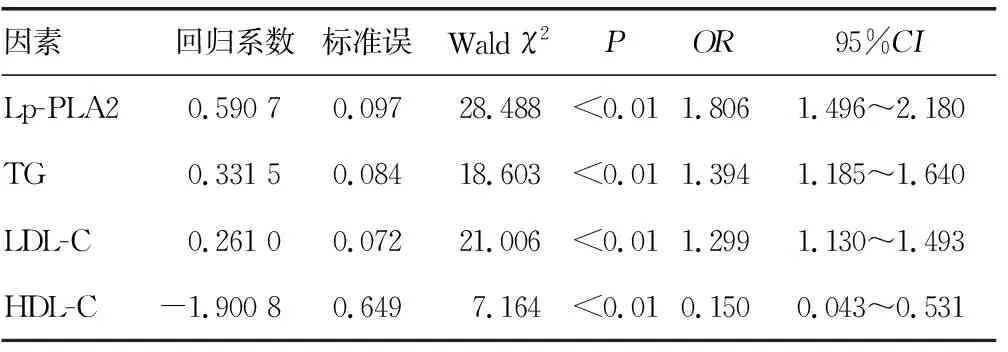
表3 子痫前期相关因素的Logistic回归分析
3 讨 论
子痫前期是妊娠阶段患者特发的疾病,它的基础病理变化是全身性的小血管痉挛,引发管腔内部狭窄,周围存在的阻力加大,提高其通透程度,渗出患者蛋白质与体液,在临床上一般表现为蛋白尿、高血压、血液浓缩及水肿等[7]。子痫前期的生理变化由全身小血管痉挛导致的全身各脏器灌流减少。子痫前期患者容易并发多种疾病(如脑血管意外、心力衰竭、胎盘早剥、弥散性血管内凝血等),从而导致患者及胎儿严重损伤,严重者导致死亡[8-9]。
对子痫前期确切病因及发病机制相关的研究为妇产科领域探讨的主要内容,相关学者对发生子痫前期的影响因素及发病机制存在着不同的分歧,主要有胎盘缺血及氧化应激学说、脂质代谢紊乱学说、血管内皮损伤学说、胰岛素抵抗学说、免疫学说、炎症学说、营养不良学说、遗传学说等[10-11]。本研究中,通过将子痫前期组与正常妊娠组比较,得出子痫前期组血清TC、TG、AI、VLDL-C、FFA、LDL-C高于正常妊娠组,HDL-C降低,在研究中得出子痫前期患者内部脂质代谢过程异常,粥样硬化的风险增加。有研究显示,孕10~20周即可测得孕妇TG、TC、LDL-C和VLDL-C显著高于怀孕前,表明妊娠期女性在妊娠早期已经存在一定的脂代谢紊乱[12]。妊娠期间脂代谢增高可用于满足胎儿生长发育,但过度的升高将呈现出血管内皮功能性紊乱、胰岛素抵抗、胰岛素敏感性降低等病理特征,进一步导致患者子宫胎盘受到伤害,在交换母胎功能上减退,对胎儿生长发育上起到不良影响[13]。
目前,子痫前期尚无统一有效的诊断标准。而临床子痫前期经确诊时,母婴已经受到不同程度的伤害。该病的诊断方法包括翻身试验、利用超声波对子宫动脉血流、血清钙、血清尿酸、人绒毛膜促性腺激素(β-HCG)等进行检测,但灵敏度、特异度均不高。Lp-PLA2是磷脂酶A2超家族中的一员,在血液中大部分与通过载脂蛋白B与低密度脂蛋白结合,少部分结合于高密度脂蛋白或密度较低的脂蛋白。体外研究显示Lp-PLA2能与高密度脂蛋白结合,参与抗炎和抗动脉粥样硬化形成[14]。本研究中,子痫前期组Lp-PLA2显著高于正常妊娠组(P<0.05),Lp-PLA2和TC、TG和LDL-C呈正相关(r=0.539 3,P<0.05),与HDL-C呈负相关(r=-0.460 4,P<0.05),且Lp-PLA2是子痫前期的独立危险因素。周宇恒[15]研究中也发现子痫患者血清Lp-PLA2较健康孕妇升高,且在产后持续升高,其推断可能是由于孕期脂代谢异常导致单核细胞产生代谢记忆有关。而洪岩[16]的研究中指出血清Lp-PLA2是妊娠期高血压疾病的独立危险因素,MTHFR基因启动子区甲基化可能是导致子痫前期发病的原因之一。
综上所述,子痫前期中存在脂质代谢紊乱,Lp-PLA2水平与子痫前期的发生密切相关,高Lp-PLA2水平可作为子痫前期预测的重要指标。

