小剂量他克莫司在危重型胸腺瘤并重症肌无力术后的应用*
林庆,柳阳春,徐全,彭雷,章晔,周鑫,吴昊,陈立如
(江西省人民医院胸心外科,南昌 330006)
重症肌无力(MG)是一种自身免疫性疾病,通常由针对神经肌肉接头的乙酰胆碱受体(AChR)抗体介导,其特征是骨骼肌无力[1]。其中部分患者可能合并胸腺瘤,而手术切除是其重要治疗方法[2]。但对于某些病例,尤其是OssermanⅢ级和OssermanⅣ级MG,术后仍有可能会迅速恶化甚至出现肌肉萎缩危象,这可能导致呼吸衰竭甚至死亡[3,4]。因此,他们的治疗仍然是一大挑战。他克莫司是一种钙调神经磷酸酶抑制剂,通常用于预防器官移植后的排斥反应,目前在临床上已经用于治疗MG[5]。并且,一些研究表明他克莫司作为MG患者的免疫抑制剂有一定疗效且具有良好的耐受性[6,7]。本研究通过危重型胸腺瘤合并重症肌无力患者术后应用他克莫司,从而对其疗效和安全性进行观察研究。
1 资料与方法
1.1 研究对象 选取2014年8月-2017年12月在我院确诊住院的危重型胸腺瘤合并重症肌无力的患者68例,随机分成实验组和对照组。排除标准:⑴合并心、肺、肝、肾功能不全、糖尿病、高血压等基础疾病;⑵有感染等严重并发症;⑶合并其他恶性肿瘤或免疫功能缺陷患者;⑷因药物过敏不能服用他克莫司;⑸备孕、孕妇女或需哺乳;⑹精神、心理疾病致不能配合治疗;⑺注册在其他临床试验;⑻曾接受他克莫司治疗;⑼年龄≤18岁或≥65岁。
1.2 研究方法 所有病人在全麻下行胸腺瘤切除+纵膈脂肪清扫术,手术方式为胸骨正中切口、胸骨上段J型小切口或全胸腔镜,术后均予以溴吡斯的明及强的松,根据病情需要给予机械通气或血浆置换,实验组病人在此基础上,于术后24h经口服或经胃管鼻饲他克莫司(FK-506)2~3mg/d,分 2 次服用:早 1.0-1.5mg,晚 1.0~1.5mg,饭后 2h 服用。 所有病人术前进行Osserman分期、改良美国MG基金会(MGFA)量表、徒手肌力量表(MMT)以及MG日常生活量表(ADL)评定。 治疗后第 1、4、8、12 周第 6、9、12、18、24个月分别重复改良美国 MG基金会(MGFA)量表、徒手肌力量表(MMT)以及MG日常生活量表(ADL)测定,每次肌力评定均在服用嗅吡斯的明后2h进行。根据患者肌力改善情况逐步减少激素用量。观察期间,定期监测药物相关不良反应。
1.3 统计方法 采用SPSS 20.0软件进行统计分析。计量数据通过平均值±标准差表示,并且应用t检验或单因素方差分析来比较组间的差异。计数数据用数字或百分数表示,并且使用χ2检验进行组间比较。P<0.05表明差异有统计学意义。
2 结果
2.1 患者一般情况 实验组和对照组两组在性别、初始发病年龄、发病至接受手术病程、OSSERMAN分型方面的差异无没明显统计学意义。(表1)
2.2 疗效比较
2.2.1 两组各项评分情况 实验组与对照组MGFA评分、ADL评分及MMT评分在术前比较无明显差异,具有可比性。术后1周两组各项评分均有所下降,但两组之间评分差异仍然没有统计学意义,但是从12周开始,实验组各项评分明显低于对照组,且两组间的MGFA评分、ADL评分及MMT评分差异具有统计学意义,说明加用他克莫司比单纯使用激素更有效果,提高患者生活质量。(表2)
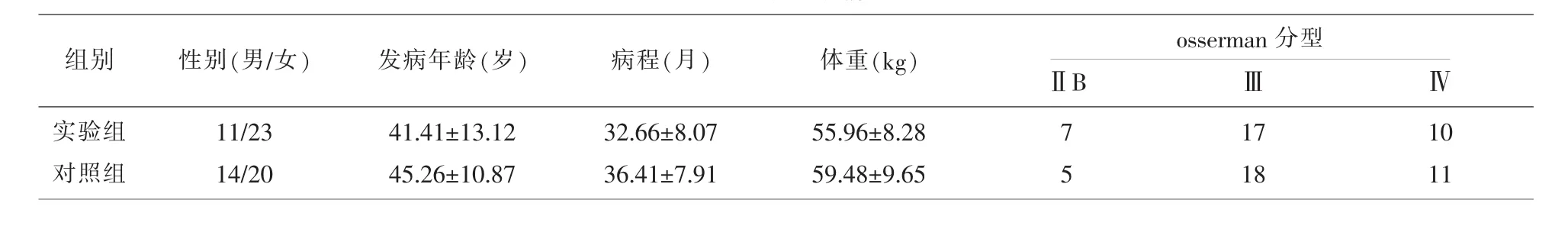
表1 患者一般情况

表2 两组患者术前及术后MGFA评分、ADL评分及MMT评分对比
2.2.2 激素减药量及不良反应 两组患者术后均长期口服强的松,其中实验者术后首次强的松给药量为(37.51±17.49)mg,术后 12、24、48 周强的松服用量分别为 (16.23±2.37)mg、(8.53±1.71)mg、(3.99±1.02)mg (P<0.05),而对照组在观察期内减药量较少。两组患者术后均有患者出现药物相关不良反应,但无严重不良反应,主要包括呼吸道感染,尿路感染,带状疱疹,皮疹,皮肤瘙痒,脱发,满月脸,血糖水平升高和高血压,24周之内两组患者不良反应率差异不大,但是24-48周,实验组新发不良反应为5例 (14.70%),对照组为14例(41.23%),差异具有统计学意义。
3 讨论
MG是一种针对神经肌肉接头的自身免疫性疾病,可导致B淋巴细胞活化以及神经肌肉连接突触下膜乙酰胆碱受体抗体介导作用[8]。此外,MG还表现为眼外肌、内脏平滑肌和全身骨骼肌无力。有和没有胸腺瘤的胸腺切除术已被广泛接受作为重症肌无力(MG)患者的治疗方式[2]。自布拉洛克等报告了6例患者通过去除胸腺使得MG症状缓解后,外科胸腺切除术在MG的管理中逐渐发挥了核心作用[9]。然而,腺体与疾病之间的关系尚未完全明确,胸腺切除术的确切作用机制尚不清楚,可能的解释包括去除持续抗原刺激的来源,减少B细胞分泌乙酰胆碱受体抗体和免疫调节[10,11]。另一方面,关于胸腺切除术治疗非胸腺瘤MG的有效性的辩论仍在继续[12]。一般来说,胸腺切除术的益处会延迟数月或数年,众所周知,缓解率会随着时间的推移而改善[13]。
在胸腺切除术后潜伏期内经常给予免疫调节剂,包括强的松,硫唑嘌呤,环磷酰胺和环孢菌素,直至完全缓解完全巩固。皮质类固醇对MG的长期免疫调节有效,其主要作用是通过减少炎性细胞因子的表达并在免疫细胞中诱导细胞凋亡来抗炎。然而,每个患者对常规免疫抑制剂如强的松,硫唑嘌呤,环孢菌素和环磷酰胺的反应不均匀,一部分患者对常规免疫抑制剂的反应可能较差或产生不可耐受的副作用,一旦出现这些副作用则需停止使用。他克莫司是一种新型的在移植领域使用广泛的免疫抑制剂,其起效快,效果好,毒副反应较小,自20世纪90年代开始应用于MG治疗,且越来越多的临床研究表明,他克莫司对于MG患者,甚至是难治性MG患者是一种有效且安全的治疗药物[14,15]。在我们的研究中两组患者均出现了一些药物相关不良反应,但是严重程度低,此外在24周至48周这段时间内,实验组新发不良反应为5例(14.70%),对照组为14例(41.23%),实验组新发药物不良反应明显少于对照组,进一步支持了他克莫司联合强的松的治疗在危重型重症肌无力合并胸腺瘤术后患者中比单用强的松相比更有利。然而他克莫司的药物不良反应在报道中并不少见,其主要不良反应为肾毒性和神经毒性[14],此外2005美国FDA曾发出他克莫司有致癌风险的警告。我们此次研究样本量较少,随访观察时间短,不能完全评估他克莫司的毒副作用。笔者在进行本临床研究过程中,曾治诊治过2例移植术后患者,之前分别行肝、肾移植术,移植前均排除恶性肿瘤,术后长期联合使用他克莫司及其它免疫抑制剂,3-5年后发现肺部肿块,术后病理证实为原发性肺癌。
有研究者曾报道了接受小剂量他克莫司治疗的患者其ADL评分显著改善,并且在用药期间内可逐渐减少平均激素用量[15]。在我们的研究当中,术后用药观察期间内,我们四次评估两组患者肌无力情况,接受他克莫司治疗的患者MGFA、MGADL、MMT评分随着时间的推移,评分显著降低,特别是12周之后,实验组各项评分明显低于对照组,说明联合使用他克莫司相比于单用强的松更能促进患者肌力恢复,改善患者生活质量。
综上所述,在危重型胸腺瘤合并重症肌无力术后的患者使用小剂量他克莫司比单独使用溴吡斯的明+强的松更加有利于改善患者肌无力情况,减少激素使用量。

