PI-RADS V2在3.0 T MR前列腺中央腺体癌诊断中的应用价值
李鹏,黄云海,张进,景晶
1 材料与方法
1.1 一般临床资料
收集我院2013年1月至2015年12月间50例前列腺癌(prostate cancer,Pca)患者的多参数磁共振成像(mutli-parameter magnetic resonance imaging,Mp-MRI)资料和临床资料,患者年龄58~86岁。临床表现:前列腺特异抗原(prostate specific antigen,PSA)升高,排尿困难,血尿和尿频。PSA:5.5~100 ng/ml。Pca穿刺标本Gleason评分:平均6.60分,范围6~9分。50例患者均经临床检查、实验室检查、影像学检查。影像学检查前未经任何治疗手段,均由穿刺活检取得病理结果,27例经根治术后,进一步病理切片证实。
入组标准:①临床疑诊Pca;②Mp-MRI检查符合前列腺影像报告和数据系统第2版(prostate image report and data system V2,PI-RADS V2)技术要求,图像资料完整;③穿刺活检术操作符合诊疗规范[1-3],穿刺针数“10+X”,每一针穿刺标本均明确标注具体穿刺部位;④病理结果在MRI检查后8周内获得。排除标准:①不符合入组标准中任意一条者;②MP-MRI示中央腺体明显增生挤压外周带,使其形成外科包膜或T2WI两者结构无法分辨者;③病灶同时侵及中央腺体和外周带;④有显著包膜外侵犯者;⑤穿刺和(或)术后病理切片显示外周带有癌变者;⑥临床及实验室检查提示癌变,而穿刺及MR检查均未发现者。
1.2 检查方法
使用3.0 T SIEMENS Verio超导型全身磁共振成像系统,16通道表面相控线圈。常规扫描参数:①前列腺轴位FSE-T2WI:TR=450 ms,TE=15 ms;层厚:3 mm;层间隔:0.8 mm;FOV:240 mm×240 mm;覆盖整个前列腺和精囊。②矢状位和冠状位FSE-T2WI:TR=550 ms,TE=9.5 ms;层厚:3 mm;层间隔:0.8 mm;FOV:380 mm×380 mm。扩散加权成像(diffused weighted imaging,DWI)扫描参数:采用单次激发平面回波成像(single-shot echo planar imaging,SS-EPI)序列,TR=5700 mm,TE=90 mm;FOV:260 mm×260 mm;层厚:3.6 mm;层间隔:1 mm;b值=0、800 s/mm。动态增强扫描(dynamic contrast enhancement,DCE)参数:前列腺轴位,TR=5700 mm,TE=90 mm;FOV:260 mm×260 mm;矩阵:128×128;层厚:3.6 mm;层间隔1 mm;范围:包括整个前列腺;扫描同时经静脉团注射对比剂[钆双胺注射液,欧乃影,通用电气药业(上海),剂量0.1 mmol/kg,速率2.5 ml/s],前后分别注入20 ml生理盐水;总扫描时间:4~5 min。
1.3 病理检查
所用病例均采用相同穿刺方式,直肠超声引导下前列腺“10+X”点穿刺活检术,标准化穿刺10针基础上,对可疑区域加穿1~2针[1,3]。
1.4 图像分析和评分诊断标准
1.4.1 前列腺分割模型
结合穿刺中的10针定位标准,在前列腺纵轴上将前列腺自上而下3等分为底、体、尖3个部分,每一部分以正中线为界将前列腺中央腺体分成6个区域。将Mp-MRI各序列轴位层数除以3,得到前列腺底、体、尖3部分的层数,如不能整除,则去除上部靠近精囊腺层面或尖部外周带组织较少的层面。
1.4.2 Mp-MRI前列腺分区的预定义
有效预定义分区是指有相应病理结果匹配的前列腺分区,及对应的MP-MRI图像,由影像科医师、超声科医师及病理科医师取得一致意见,共同确认。无效预定义分区是指:①分区没有相应的病理结果;②分区位置与穿刺点不能完全匹配,或穿刺点不能匹配到对应的分区;③穿刺点不能明确在前列腺分带结构中的具体定位。
1.4.3 Mp-MRI图像分析和评分诊断标准
由两名参加工作10年以上从事MRI诊断的副主任医师作为观察者,采用盲法各自独立对入组病例的MP-MRI图像进行评分诊断,评分诊断标准:PI-RADS V2[2]。间隔4周后,2位观察者各自独立对入组病例图像进行常规阅片。常规阅片指不借助任何评分系统及辅助手段,凭主观经验阅片判断。
1.5 统计学方法
观察者间评分结果一致性采用Kappa检验,极佳:K>0.80;高度:0.60<K≤0.80;中度:0.40<K≤0.60;低度:K≤0.40。用受试者工作特征(receiver operating characteristic,ROC)曲线分析观察者PI-RADS V2评分诊断前列腺中央腺体癌的效能,包括特异度、准确度、敏感度、阳性预测值、阴性预测值和约登指数。采用独立样本t检验比较PI-RADS V2评分诊断与常规阅片之间特异度、准确度、敏感度的差异,P<0.05表示差异有统计学意义。

表1 前列腺分区相匹配的穿刺病理结果(例)Tab.1 Pathological results of prostatic partition matching(case)
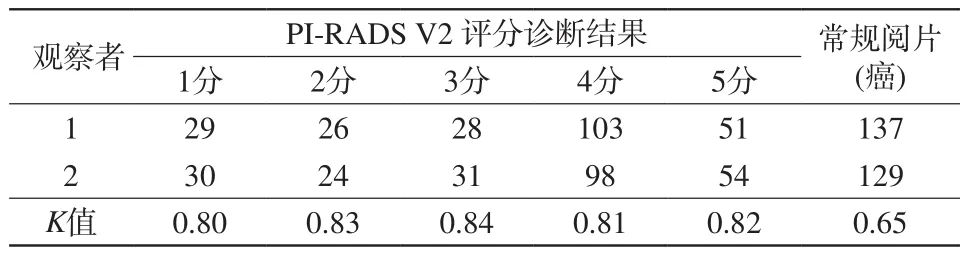
表2 两位观察者的PI-RADS V2 评分诊断结果及常规阅片诊断结果(个)Tab.2 PI-RADS V2 scoring and routine examination of two observer (n)
2 结果
2.1 基于穿刺病理结果的前列腺分区预定义结果
50例患者均经穿刺活检取得的病理组织证实,27例患者在Pca根治术后经病理组织切片证实,其中病理证实癌的有32例,非癌的有18例。在总计300个前列腺分区中,中央腺体有效预定义分区237个,无效预定义分区107个(表1)。
2.2 观察者诊断结果一致性分析
两位观察者的PI-RADS V2评分诊断结果的一致性极佳(K=0.81~0.84)。两位观察者常规阅片的结果一致性为高度(K=0.65),差异有统计学意义(P<0.05)。以“4”为诊断“癌”的界值,两位观察者PI-RADS V2评分结果与常规阅片结果差异有统计学意义(P<0.05)(表2)。
2.3 PI-RADS V2量表对前列腺分区评分诊断的效能分析
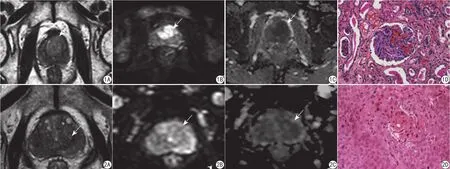
图1 73岁男性患者,PSA:32.0 ng/ml。A:T2WI中央腺体区不规则等信号结节;B、C:DWI结节样高信号,表观扩散系数(apparent diffusion coef ficient,ADC)低信号,最大径>1.5 cm;D:病理结果:前列腺癌。医师PI-RADS V2评分:5分,常规阅片诊断为前列腺癌 图2 63岁男性患者,PSA:22.0 ng/ml。A:T2WI中央腺体区不规则等信号,结节最大径<1.5 cm;B、C:DWI/ADC等信号;D:穿刺病理:前列腺炎症伴增生改变。医师PI-RADS V2评分:3分,常规阅片:前列腺癌可能Fig. 1 Male, 73 years old, PSA: 32.0 ng/ml. A: T2WI: irregular signal nodules in central gland region; B, C: DWI: hyper signal, ADC low signal,maximum diameter >1.5 cm; D: Pathological results: prostate cancer. PI-RADS V2: 5 points, regular reading: prostate cancer. Fig. 2 Male, 63 years old,PSA: 22.0 ng/ml. A: T2WI: irregular signal in central gland region, nodule maximum diameter <1.5 cm; B, C: DWI/ADC: normal signal; D: Pathology:prostatitis with hyperplasia. PI-RADS V2: 3 points, regular reading: probably prostate cancer.
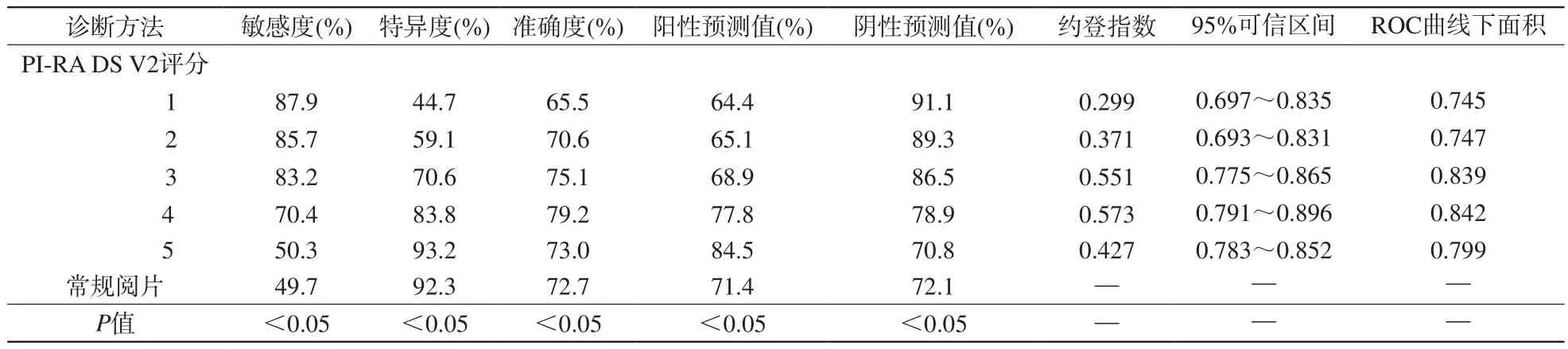
表3 前列腺分区评分诊断结果Tab.3 Diagnostic results of prostatic partion
对PI-RADS V2评分诊断的5个等级进行诊断效能分析。ROC曲线结果显示,评分“4分”作为诊断癌的界值时,约登指数(正确诊断指数)最大,为0.573,诊断效能达到最优点(表3,图1、2)。PIRADS V2评分“4”分(最佳诊断界值)时的诊断效能与常规阅片差异有统计学意义(P<0.05),优于常规阅片。
3 讨论
前列腺癌是男性常见的恶性肿瘤,在世界范围内居男性所有恶性肿瘤第2位,在我国男性恶性肿瘤中排第6位[3]。磁共振成像具有无辐射、多序列、多参数和多方位成像的特点,是目前公认的最佳影像学检查方法[4]。前列腺癌多发生在外周带,同时有30%的前列腺癌发生在中央腺体区,且诊断困难[5]。
3.1 PI-RADS及PI-RADS V2 的产生背景及应用现状
Mp-MRI为影像科医师提供了多方位的影像学信息,使诊断的准确性得到提高的同时,也使影像科医师与临床医师之间对信息掌握程度出现了不对等,影像报告难以理解[2]。欧洲泌尿放射委员会(European Society of Urinary Radiology,ESUR)在2012年推出了《ESUR prostate MR guidelines 2012》,提出了“PI-RADS”的概念,目的在于规范化、标准化前列腺Mp-MRI报告,减少模糊的影像描述,便于更好地与泌尿外科医生之间的沟通[2,4]。2014年,ESUR推出了PI-RADS V2,对第1版PI-RADS作了进一步修改和完善。PI-RADS V2主要基于ESUR专家的经验共识,准确性还有待于大样本量研究资料的进一步证实。Moritz等[6]报道诊断中央腺体区病灶的ROC曲线下面积为0.82~0.85,PI-RADS V2为0.75~0.77,敏感度提高,特异度减低。曾浩等[7]研究发现PI-RADS V2检出移行带Pca的诊断效能较PI-RADS有所提升,敏感度提高,特异性有所减低。特异度减低分析原因可能为:PI-RADS V2降低了DWI及DCE在Mp-MRI诊断中央腺体癌中的权重,第1版各个参数的权重是一致的,DWI及DCE提高了诊断的特异度[8]。
3.2 PI-RADS V2检查序列的构成及优化运用
《ESUR prostate MR guidelines 2012》[4]对Mp-MRI的设备条件的基本要求是:3.0 T磁共振设备配备专用盆腔相控线圈,可以达到最佳的诊断图像要求。Mp-MRI是在常规T1WI及T2WI的基础上,增加功能MRI检查序列DWI、DCE、磁共振波谱成像(magnetic resonance spectrum imaging,MRSI)等,为病变的诊断提供多个序列的诊断信息。Moritz等[6]研究表明将MRSI纳入PI-RADS评分系统中进行评分诊断研究,相比PI-RADS V2中的T2WI、DWI和DCE各序列联合评分诊断,MRSI并未显著提高Pca诊断的准确度。胡毅等[8]研究发现,联合应用T2WI+DWI+DCE在PI-RADS V2 评分诊断中的应用价值高于单一序列。参照之前的研究结果,笔者认为,中央腺体区的评分诊断虽以DWI为主导,但同时参考T2WI及DCE 仍是非常必要的。
3.3 PI-RADS V2的诊断效能及诊断结果一致性
本研究中应用PI-RADS V2在中央腺体区癌的诊断较常规阅片有较高的准确度(应用PI-RADS V2的准确度为78.9%,常规阅片的准确度为65.4%),与Barentsz等[9]的研究结果相符,可能原因为:良性前列腺增生大多数发生在该区域,同时约30%的前列腺癌发生在中央腺体[1],而良性前列腺增生和炎症的Mp-MRI信号特征可类似于癌灶,使得中央腺体癌灶的检出要难于外周带[10]。中央腺体癌较外周带癌灶缺少特征性表现,更大程度上依赖医师的经验积累,而PI-RADS V2针对各序列的异常征象进行标准化,使得如何判断图像表现是否异常更容易判断,更容易接受,医师之间更容易达成共识。Arnaldo等[11]和Rosenrantz等[12]分别用病理大切片验证PI-RADS V2对中央腺体Pca的诊断效能,结果表明,PI-RADS V2在中央腺体癌中的诊断结果与最终病理结果的一致性的K值为0.85,是Pca有效的评分诊断方法。
PI-RADS V2是带有一定客观性的主观评分诊断评价标准[13],本研究结果显示同年资医师间对中央腺体癌分别应用PI-RADS V2进行评分诊断结果的一致性较高,与Barentsz等[9]的研究结果相符。
本研究的不足:文中两位观察者资历相仿,而不同临床经验医师间应用PI-RADS V2评分诊断结果的一致性有待于进一步研究,不同年资的医师标准图像的解读存在差异,以及对前列腺不同分带中癌灶诊断效能的差异也有待深入的研究。

