不规则趋化因子在急性肺栓塞后的表达及机制研究
谢小娜,蔡学定
(1.浙江中医药大学附属温州中医院呼吸内科,浙江温州 325000;2.温州医科大学附属第一医院呼吸与危重症医学科,浙江温州325000)
急性肺栓塞(acute pulmonary embolism,APE)后引起严重的肺损伤和急性肺动脉高压(pulmonary hypertension,PAH)是导致死亡的直接原因。有报道发现,APE后形成的PAH与肺动脉的机械阻塞作用密切相关[1],甚至认为肺栓塞后血栓的机械阻塞是导致PAH的直接原因。近年来随着研究的深入还发现,肺动脉机械阻塞严重程度与肺动脉压力的增高有时不成正相关,当机械性阻塞基本解除后,仍发现肺动脉压力持续升高的现象。此外,有研究结果显示,APE时大量炎症细胞聚集浸润在栓塞血管的周围,这些聚集稍微炎症细胞释放的细胞因子进一步加重肺血管内皮损伤,因此,这些细胞因子在APE性PAH的形成中扮演重要的角色[2]。其中,不规则趋化因子(fractalkine,FKN)又名趋化因子CX3CLl,是趋化因子CX3C亚族的独有成员,具有可溶和膜结合两种形式,既有趋化性蛋白的功能也有细胞黏附分子的功能,还具有促进平滑肌细胞增殖的生长因子作用[3]。PERROS等[4]在PAH模型中发现,肺动脉病变周围的炎症细胞中FKN表达增加且在血管平滑肌细胞中的表达也明显增加。本文研究大鼠APE后FKN的表达变化及其机制,从而探讨肺栓塞后炎症反应的作用机制。
1 材料与方法
1.1材料 (1)动物:SPF级健康雄性SD大鼠72只,体质量300~350 g,由温州医科大学动物实验中心生产提供,实验动物合格证为SCXK(浙)2005-0019。动物置于相同环境和条件饲养。(2)试剂与仪器:BCA 蛋白浓度检测试剂盒购自Thermo Fisher Scientific公司;DAB显色试剂盒购自福建迈新生物技术开发有限公司(MXB Biotechnologies);兔抗大鼠磷酸化p38抗体、兔抗大鼠总P38抗体和山羊抗兔HRP二抗购自美国CST(Cell Signaling Technology)公司;兔抗大鼠FKN抗体购自美国Biolegend公司。
1.2方法
1.2.1实验动物分组 按照完全随机的方法将72只SD大鼠分为对照组、溶剂组、APE组,每组24只;再将每组分为处理后1、4、8 h 3个亚组,每组8只。
1.2.2APE大鼠模型建立 (1)自体血栓制备:取聚维酮碘棉球对大鼠颈部进行消毒,内径1.1 mm头皮针(19G)置入左颈动脉取血并静置10 min凝血,再将血块置于37 ℃水中20 min,切成统一规格1.1 mm×3.0 mm的栓子,并用无菌生理盐水轻柔冲洗3 遍,放入对应试管内,加无菌生理盐水2 mL,4 ℃冷藏备用,所有操作均为无菌操作。(2) APE模型的建立:使用5%水合氯醛(3 mg/kg)经腹腔注射麻醉大鼠,暴露颈正中线并行纵行切口,分离大鼠颈外静脉并剪一小口,插入19G聚乙烯导管,通过导管注入之前准备的栓子约50个(不致大鼠死亡),附以无菌生理盐水0.6 mL(0.1 mL/min),血栓伴随循环血液汇聚并嵌顿于肺动脉,行核素扫描检测发现栓塞部位核素摄取量明显减少,证明APE大鼠模型建立成功。对照组不作任何处理;溶剂组大鼠除注入等量的生理盐水外,余操作同APE组。在成功建立APE模型后,分别于1、4、8 h 3个时间点处死大鼠,经胸腔取大鼠肺组织。
1.2.3免疫组织化学(IHC)检测 摘取大鼠左肺上叶组织,固定于4%多聚甲醛液24 h,经漂洗、脱水、透明、浸蜡、和包埋后再行切片,通过IHC检测FKN、p38蛋白的表达。组织切片经脱蜡、水化、封闭及微波修复后,滴加抗FKN抗体(1∶50)或抗p38抗体(1∶50)于4 ℃过夜后,加入山羊抗兔二抗(1∶50),DAB显色终止后行苏木素复染,最终脱水、透明中性树胶封片。置于显微镜下观察p38、FKN在肺组织中的表达。
1.2.4Western blot检测p38丝裂原活化蛋白激酶(p38 mitogen-activated protein kinases,p38MAPK)表达 称取各组大鼠等量新鲜肺组织加入细胞裂解液后充分研磨,再经超声细胞粉碎仪充分破碎,于低温超速离心机12 000 r/min 4 ℃离心 10 min,取上清液加入等体积2×上样缓冲液及相应体积PBS充分震荡混匀并分装至PCR管经PCR仪维持99 ℃运行5 min,多余蛋白于-70 ℃冰箱保存备用。进行10 mol/L SDS-PAGE(电压浓缩胶80 V,分离胶120 V)蛋白电泳,电泳后将蛋白转印至PVDF膜(转膜电流300 mA,30 min)后用5 g/L 脱脂奶粉在室温下封闭1 h,分别加入5%牛血清清蛋白(BSA)稀释的磷酸化p38单克隆抗体(1∶1 000,兔抗大鼠)和总p38单克隆抗体(1∶1 000,兔抗大鼠) 4 ℃冰箱孵育过夜后,用TBST充分洗涤条带3 min后,室温下孵育标记辣根过氧化物酶(HRP)的羊抗兔二抗(1∶2 000)1 h,再次用TBST充分洗涤3 min,使用ECL试剂显色及暗室内胶片曝光。使用图像分析系统对所得条带进行扫描保存及灰度分析。
1.2.5RT-PCR检测FKN mRNA表达 使用Trizol试剂盒提取肺组织总RNA并测出A值,A260 nm/A280 nm为1.8~2.0。用日本TakaRa 公司RT-PCR 试剂盒进行逆转录扩增,逆转录扩增条件:65 ℃ 1 min,30 ℃ 5 min,65 ℃ 15 min,98 ℃ 5 min,5 ℃ 5 min,转录成cDNA后,各组取5 μL加入PCR反应体系,PCR扩增条件:94 ℃预变性5 min,94 ℃ 1 min,56.2 ℃退火1 min,72 ℃延伸1 min,循环30次。各组PCR产物等量注入2 %琼脂糖凝胶孔中行水平电泳并在紫外凝胶成像系统下观察、摄像,随后进行吸光度值(OD)分析。各样本的基因表达量计算方法为产物胶上条带OD与β-action基因条带OD的比值。

2 结 果
2.1APE大鼠FKN的表达部位 IHC检测结果显示,FKN在APE大鼠的肺实质、肺动脉血管壁上均有不同程度的表达;p38在APE大鼠的肺实质、肺动脉血管壁细胞核内均有表达。
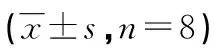
表1 各组大鼠各时间点磷酸化P38蛋白OD比值比较
a:P<0.05,与APE组比较
2.2各组大鼠各时间点肺组织磷酸化p38OD比值比较 APE组各时间点大鼠肺组织磷酸化p38OD比值高于对照组和溶剂组(P<0.05),见表1、图1。

图1 各组大鼠处理后8 h磷酸化p38的表达水平
2.3各组大鼠各时间点肺组织FKN mRNAOD比值比较 APE组各时间点大鼠肺组织FKN mRNAOD比值明显高于对照组和溶剂组(P<0.05),见表2。
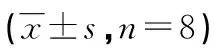
表2 各组大鼠各时间点FKN mRNA的OD比值比较
a:P<0.05,与APE组比较

图2 各组大鼠处理后8 h肺组织FKN mRNA的表达水平
3 讨 论
3.1FKN在APE后的表达及其作用 FKN是1997 年由BAZAN等[5]在用趋化因子的基因探针检索表达序列标签数据库时发现的,是目前CX3C-类趋化因子中惟一成员,它是含有多个结构域的大分子蛋白,人的FKN基因定位在染色体16q13[6]。膜结合型Fractalkine 存在于活化的细胞表面,主要起着黏附作用;分泌型Fractalkine主要是对单核、NK细胞等具有强有力的趋化作用[7-8]。近年来有报道指出,炎症反应时,FKN在单核细胞和T细胞募集到血管壁的过程中起重要作用,而且FKN还具有类似于生长因子促肺动脉平滑肌细胞增殖的作用[3]。在APE后,对FKN的研究较少报道。
本研究结果显示,APE后FKN、p38在肺血管内皮、肺泡上皮、支气管内皮上有明显表达(P<0.05)。本研究结果显示,APE组各时间点大鼠肺组织FKN mRNA的表达量明显高于对照组和溶剂组(P<0.05)。目前研究认为,APE后PAH的形成可能与栓塞后血管周围大量炎症细胞浸润及其释放的细胞因子进一步损伤肺动脉内皮有关[9],而表达增多的FKN对炎症细胞的聚集起到促进作用。
3.2p38MAPK通路在APE后被激活从而上调FKN的表达 1993年科学家研究发现p38MAPK信号转导通路,该通路一旦被激活,细胞质中的非磷酸化p38MAPK转化为磷酸化p38MAPK,再移位到细胞核内[10]。本研究中采用Western blot检测肺组织磷酸化p38的表达,结果显示随时间延长磷酸化p38的表达有明显增高趋势(P<0.05),提示在大鼠APE后,p38MAPK通路被激活。因此本课题组推测,APE后p38MAPK通路被激活,上调了FKN的表达,使得FKN在APE后明显升高。
此外,有研究报道FKN在PAH的发生、发展中起到重要作用,值得注意的是损伤的内皮细胞可过度表达FKN[11-12],其是否在APE后PAH的形成中起作用有待进一步研究。也有研究显示FKN 所引起的趋化白细胞、纤维化、凋亡等均可能是心力衰竭的诱因[13-15]。右心功能不全也是APE后PAH的形成的原因之一。
综上所述,本研究结果显示在APE后8 h内,大鼠肺组织中FKN的表达即明显升高,作为炎症趋化因子,FKN对APE后肺部炎症反应有明显促进作用,从而加重了APE后炎症反应及PAH的形成。

