μ阿片受体激动剂PL017对内脏痛和胃肠功能的调节作用
张兆伟,秦妮娜,陈 锴,邹雨霞
(延安大学附属医院麻醉科,延安 716000)
阿片类药物被广泛用于缓解中重度疼痛,其中吗啡、杜冷丁和羟考酮等镇痛药多是通过μ阿片受体介导[1-5]。[MePhe3,D-Pro4]morphiceptin (PL017),是基于μ阿片受体激动剂morphiceptin(Tyr-Pro-Phe-Pro-NH2)修饰所得,对μ阿片受体有较高的选择性和亲和力[6-8]。热板实验结果显示,PL017在中枢水平和外周水平都表现出强效的剂量依赖性的镇痛。PL017在中枢水平和外周水平均可显著抑制小鼠的胃肠推进,有效缓解腹泻症状,且缓解腹泻的有效剂量远低于它抑制胃肠推进所需的剂量,提示PL017治疗腹泻时不会造成胃肠功能紊乱[9-10]。研究表明,PL017跨血脑屏障的水平有限,因此,本实验试图探究PL017在外周水平对小鼠内脏痛(经典的外周痛醋酸扭体模型)、末端结肠(结肠排珠实验)和排便的调节。
1 仪器与材料
1.1仪器 AR2140型电子天平(美国Adventurer公司);DHG-9030B型电热恒温鼓风干燥箱(上海煜南仪器有限公司)。
1.2试药 μ阿片受体激动剂PL017和μ阿片受体拮抗剂cyprodime (Tocris公司);冰醋酸(天津永晟精细化工有限公司)。
1.3动物 雄性昆明系成年小鼠,体质量23±1 g,由西安交通大学医学院实验动物中心提供,饲养于严格控温22±1 ℃、控光12/12 h昼夜循环的动物房,保障充足的鼠粮、饮水,并保持鼠房、鼠笼的清洁。
2 方法
2.1醋酸扭体模型 醋酸扭体模型很好地模拟了腹腔炎症引起的腹痛症状,是研究外周镇痛的经典模型。参考文献方法[11-12],将新鲜配制的醋酸溶液(6 mL·L-1,0.2 mL)注入小鼠(6~8只·组-1)腹腔,观察并记录皮下注射PL017或生理盐水15 min内的扭体次数。
2.2结肠排珠实验 参照文献方法[13-14],在小鼠皮下注射PL017或生理盐水,于10 min后用玻璃棒辅助将预热的玻璃珠(37 ℃,直径3 mm)塞入小鼠(6~8只·组-1)末端结肠(深2 cm),并迅速将小鼠单只置于鼠笼中,观察并记录小鼠排出玻璃珠的潜伏期。
2.3排便实验 为避免皮下给药时刺激小鼠的排便,选择异氟烷吸入轻度麻醉。迅速皮下注射PL017或生理盐水,并于10 min后将小鼠(6只·组-1)单只放在金属网格为底的鼠笼中,小心收集30 min内的粪便颗粒,置于60 ℃烘箱中过夜烘干,记录粪便颗粒数和干质量[15-16]。
2.4数据分析 应用Origin软件进行统计分析,采用单因素方差分析的Bonferroni法检验组间的显著性。以P<0.05 为差异有统计学意义。
3 结果
3.1PL017在醋酸扭体模型中的镇痛作用 见表1。
表1皮下注射PL017对醋酸扭体的调节
Tab.1 Effects of subcutaneous PL017 on the acetic acid-induced writhing


分组剂量 /μg·kg-1扭体次数P动物数/只生理盐水050.38±2.26-8PL017 347.86±2.690.487PL0171029.43±2.644.02×10-57PL017309.71±1.441.82×10-97PL017506.14±1.588.58×10-107
注:-表示与生理盐水组不进行显著性比较。
由表1可知,与生理盐水组相比,皮下注射PL017(3~50 μg·kg-1)能有效地减少15 min内醋酸模型小鼠的扭体次数。其中3 μg·kg-1组小鼠的扭体次数略低于生理盐水组,差异无统计学意义;而PL017在高剂量时(30和50 μg·kg-1),几乎将醋酸诱发的扭体反应完全消除。结果表明,皮下注射PL017对醋酸诱发的炎性痛有强效镇痛作用,且呈现一定的剂量依赖性(ED50=9.76±1.36 μg·kg-1)。
3.2PL017镇痛调节中的受体参与 参考文献方法[17],提前60 min腹腔注射μ阿片受体拮抗剂cyprodime(1 mg·kg-1,0.2 mL)。见表2。由表2可知,与生理盐水组相比,cyprodime自身对醋酸诱发的扭体行为无显著影响(48.29±2.44,P=0.54);与只注射30 μg·kg-1PL017的小鼠相比,预注射的cyprodime却能够完全拮抗PL017而表现出与生理盐水组相近的扭体次数(51.5±1.99,P=4.08×10-10),表明PL017在醋酸扭体模型的镇痛作用是通过激活μ阿片受体介导的。
3.3PL017对结肠排珠的调节 见表3。由表3可知,生理盐水组小鼠排出玻璃珠的时间为394±33.49 s。与生理盐水组相比,在扭体镇痛ED50的10倍剂量(50 μg·kg-1)时,PL017对小鼠的排珠潜伏期无显著的调节作用;而只有10倍于镇痛ED50的100 μg·kg-1,PL017可有效延迟小鼠的排珠潜伏期(559.75±67.98 s,P=0.046)。
表2提前60min预注射μ阿片受体拮抗剂cyprodime对PL017镇痛的影响
Tab.2 The influence of 60 min pre-treated μ opioid receptor antagonist cyprodime on PL017-produced analgesic effects in the mice writhing test
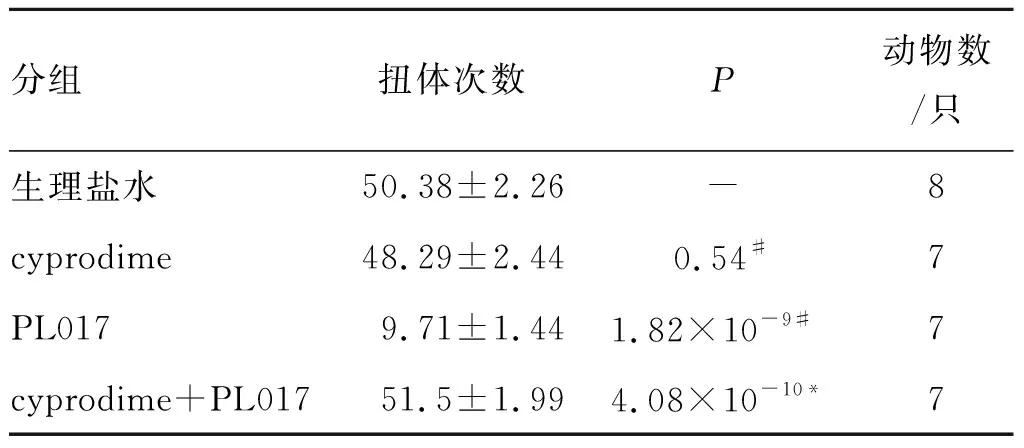
分组扭体次数P动物数/只生理盐水50.38±2.26-8cyprodime48.29±2.440.54#7PL0179.71±1.441.82×10-9#7cyprodime+PL01751.5±1.994.08×10-10*7
注:#表示与生理盐水组进行显著性比较;*表示与PL017组进行显著性比较;-表示与生理盐水组不进行显著性比较。
表3皮下注射PL017(50~100μg·kg-1)对结肠排珠的调节
Tab.3 The effects of subcutaneous PL017 (50-100 μg·kg-1) on bead expulsion latency

分组剂量/μg·kg-1排珠潜伏期/sP动物数/只生理盐水0394±33.49-8PL01750437±51.980.4907PL017100559.75±67.98 0.0468
注:-表示与生理盐水组不进行显著性比较。
3.4PL017对排便的调节 考虑到阿片类药物相关性便秘是药物调节胃肠蠕动及消化液分泌等的综合表征[18-19],以粪便颗粒的数量和干质量为指标来评价皮下注射PL017对小鼠排便的调节。相较于生理盐水组(6.33±0.49个,71.17±6.69 mg),300 μg·kg-1PL017组小鼠的粪便颗粒数(4.17±0.6个,P=0.019)和粪便颗粒干质量(43.67±5.28 mg,P=0.009)明显减少。100 μg·kg-1PL017虽然能一定程度上抑制小鼠的排便数量(5.50±0.76个,P=0.380)和粪便干质量(60.00±10.19 mg,P=0.210),但差异不显著。见表4。
表4皮下注射PL017(100~300μg·kg-1)对小鼠排便的调节
Tab.4 The effects of subcutaneous PL017 (100-300 μg·kg-1) on fecal pellet output in mice

分组剂量/μg·kg-1数量/个P干质量/mgP动物数/只生理盐水06.33±0.49-71.17±6.69-6PL0171005.50±0.76 0.380 60.00±10.19 0.2106PL0173004.17±0.60 0.01943.67±5.280.0096
注:-表示与生理盐水组不进行显著性比较。
4 讨论
作为μ阿片受体激动剂阿片的类似物,PL017的稳定性和生物活性都有了明显的提升[6,9]。在中枢水平上,侧脑室注射的PL017在热板实验中表现出强有力的镇痛效果(ED50=0.012 μg·只-1),对胃肠推进有显著的抑制作用(ED50=0.038 μg·只-1)。PL017在镇痛和胃肠调节中的ED50相差3.16倍,意味着侧脑室注射PL017的镇痛药效与胃肠不良反应在一定程度上是可以分开的[10]。鉴于热板实验的缩足行为有高位中枢的参与及PL017极其有限的血脑屏障通透性,因此比较PL017在外周皮下给药时对热板急性痛(ED50=30.2 mg·kg-1)与胃肠推进(ED50=0.37 mg·kg-1)的调节活性不合理[9]。因此,本实验选择经典的外周痛模型(醋酸扭体模型)来评价PL017的外周镇痛效力。此外,通过末端结肠排珠和排便实验,进一步评价PL017在外周水平对胃肠的调节作用。
与相同给药途径的热板镇痛相比(ED50=30.2 mg·kg-1)[9],皮下注射PL017在醋酸扭体模型中表现出更强效的镇痛作用(ED50=9.76±1.36 μg·kg-1),见表1。该镇痛效果可被cyprodime完全阻断,表明PL017可能是通过激活μ阿片受体发挥其外周镇痛的,见表2。皮下注射50 μg·kg-1PL017不会延迟小鼠的排珠潜伏期,而30 μg·kg-1PL017却能有效地抑制胃肠推进(ED50=0.37 mg·kg-1)[9]。也就是说,与上消化道相比,末端结肠对PL017表现出更高的敏感性,这或许是因为μ阿片受体在结肠和直肠比在上消化道有更广泛的表达和分布[20]。在外周皮下给药时,PL017调节胃肠推进、结肠排珠、排便的有效剂量远高于其镇痛剂量,意味着PL017在发挥其外周镇痛效力时,不会造成胃肠功能紊乱等不良反应。
综上所述,本实验探究了μ阿片受体激动剂PL017在经典的外周炎性痛醋酸扭体模型中的镇痛活性;相对较低的有效镇痛剂量,表明PL017具有一定的治疗外周内脏痛的潜力。

