Er 3+,Yb3+共掺杂NaY(WO4)2上转换荧光粉的制备及其发光性能
史忠祥 卢 杨 王 晶*, 关 昕 时 军 江 豪
(1大连交通大学,辽宁省无机超细粉体制备及应用重点实验室,大连 116028)
(2营口理工学院化材系,营口 115014)
(3承德石油高等专科学校化学工程系,承德 067000)
0 引 言
稀土离子掺杂的上转换发光材料因具有优异的光学特性及特殊的发光机理,使其在物理、化学、生物等多学科交叉领域备受关注[1],同时也推动了其在可见上转换激光器[2]、三维立体显示[3]、温度传感[4]、生物成像[5]、太阳能电池[6]等诸多先进技术的快速发展。特别地,当作为生物探针使用时,其良好的发光效率以及更深的穿透能力是传统有机染料所无法比拟的。因此,对于研究上转换材料的制备方法以及深入了解上转换发光过程的机理是很有必要的。
基质材料可为激活离子提供适宜的晶体场,同时其声子能量的高低也是影响发光效率的重要因素,NaYF4因具有较低的声子能量成为研究者们首选的基质材料。因此,近年来关于稀土离子掺杂NaYF4上转换发光材料的报道屡见不鲜,且多集中于通过热分解及其衍生方法合成形貌可控的小尺寸微/纳米颗粒[7-9],但合成时所使用的前驱体如三氟乙酸盐以及大量用到的十八烯、油酸、油胺等有机配体,不仅价格昂贵而且会产生多种有毒副产物和有毒气体,对环境造成污染,与绿色化学的理念相悖。若采用传统的热液法合成,则NaYF4多以发光效率较低的立方相存在,此时常需要辅以高温焙烧才能实现由立方相到六方相的转变。因此,选择适宜的基质材料以及简便有效的合成方法则显得尤为重要。作为无机材料的重要组成部分,复式钨酸盐NaLn(WO4)2(Ln=Y,La,Gd)具有与 CaWO4类似的白钨矿型结构,该结构材料具备良好的热稳定及化学稳定性,并且对稀土离子具有较大的容纳能力。此外,与传统二价碱金属钨酸盐相比,稀土激活离子与NaLn(WO4)2中的Ln3+属于同价态替换,因此,不会引起晶格畸变或晶格缺陷,亦无需电荷补偿。目前,已有大量关于稀土离子掺杂NaY(WO4)2荧光材料的报道,其中以Eu3+掺杂NaY(WO4)2红色荧光粉的报道居多[10-13]。随着研究的深入,NaY(WO4)2材料优良的光学性质以及较低的声子能量吸引了研究者们的注意。近年来,关于NaY(WO4)2基质的上转换材料也逐渐成为关注的热点[14-16]。此外,对于制备具有特殊形貌的发光粒子而言,常辅以高分子有机物作为表面活性剂,通过控制晶体的各向异性生长,实现对产物尺寸、形貌的有效控制。但目前,鲜有关于仅通过调节pH值即能合成出具有八面体、拟立方体、片状形貌的NaY(WO4)2微米颗粒的报道。
鉴于此,本工作主要报道了采用水热法在未加入表面活性剂条件下合成出纯相NaY(WO4)2微米颗粒,通过调节pH值实现对材料形貌的有效控制,并研究了形貌演变过程的机理。此外,通过掺杂Er3+/Yb3+离子合成出 NaY(WO4)2∶Er3+,Yb3+上转换发光粉,讨论了Er3+激发态能级可能的布居过程以及Yb3+与Er3+间的能量传递过程。
1 实验部分
1.1 试 剂
六水合硝酸钇[Y(NO3)3·6H2O]、六水合硝酸铒[Er(NO3)3·6H2O]、五水合硝酸镱[Yb(NO3)3·5H2O]均为高纯试剂,纯度99.99%(购自安耐吉化学试剂有限公司);二水合钨酸钠[Na2WO4·2H2O],纯度≥99.5%(购自阿拉丁试剂);分析纯、无水乙醇、氨水及硝酸(购自天津大茂化学试剂厂)。实验中所需去离子水为实验室设备自制。
1.2 制备NaY(WO4)2基质材料
首先,将1.979 2 LNa2WO4·2H2O在磁力搅拌条件下溶于50 mL去离子水中形成透明溶液,记为A。之后,准确移取10 mL Y(NO3)3(0.2 mol·L-1)溶液至100 mL烧杯中,记为B。随后,将溶液A缓慢地滴入溶液B中,形成白色乳浊液C,并在磁力搅拌下持续搅拌30 min至均匀。上述步骤完成后,利用氨水及硝酸调节溶液C的pH值分别为5.0,6.0,7.0,7.5,8.0与9.0,最后将该溶液移入带有聚四氟乙烯内衬的不锈钢水热釜中,180℃条件下保温24 h。待水热反应完成后自然冷却至室温,将沉淀物取出离心,并用去离子水及无水乙醇各洗涤3次,60℃干燥10 h,获得NaY(WO4)2基质材料。
1.3 制备Er 3+/Yb3+共掺杂NaY(WO4)2上转换荧光粉
按 照 配 方 NaY0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07)准确移取适量的 Y(NO3)3(0.2 mol·L-1)、Er(NO3)3(0.01 mol·L-1)及Yb(NO3)3(0.01 mol·L-1)溶液,并在磁力搅拌条件下充分混合。取1.979 2 LNa2WO4·2H2O溶于50 mL去离子水中。随后将溶解好的Na2WO4溶液逐滴加入到上述稀土硝酸盐混合液中,并将乳浊液的pH值调至8左右,继续搅拌30 min后,将该溶液移入带有聚四氟乙烯内衬的不锈钢反应釜中180℃恒温24 h,收集反应釜底部白色沉淀,离心,用去离子水及无水乙醇洗涤若干次后,60℃干燥10 h,得到NaY(WO4)2∶Er3+,Yb3+上转换发光粉。
1.4 样品表征
采用荷兰帕纳科公司的Empyrean型X射线衍射仪测试样品的物相结构,靶材为Cu靶,Kα辐射(λ=0.154 06 nm),工作电压与电流分别为40 kV和40 mA,扫描范围 2θ=10°~80°;利用德国卡尔蔡司公司的SUPRA 55型场发射扫描电子显微镜 (工作电压5.0 kV)及日本电子株式会社生产的JEM-2100F型透射电子显微镜(加速电压200 kV)对样品的微观形貌进行放大观察;使用英国马尔文公司的Mastersizer 2000型激光粒度分析仪测定样品的粒度分布,当遮光度大于6.0%时自动开始测试;采用日本Hitachi公司的F-4600型荧光光谱仪记录样品的上转换光谱,扫描范围400~700 nm,扫描速率1 200 nm·min-1,激发光源为980 nm光纤激光器,且激光器最大输出电流为5.0 A。
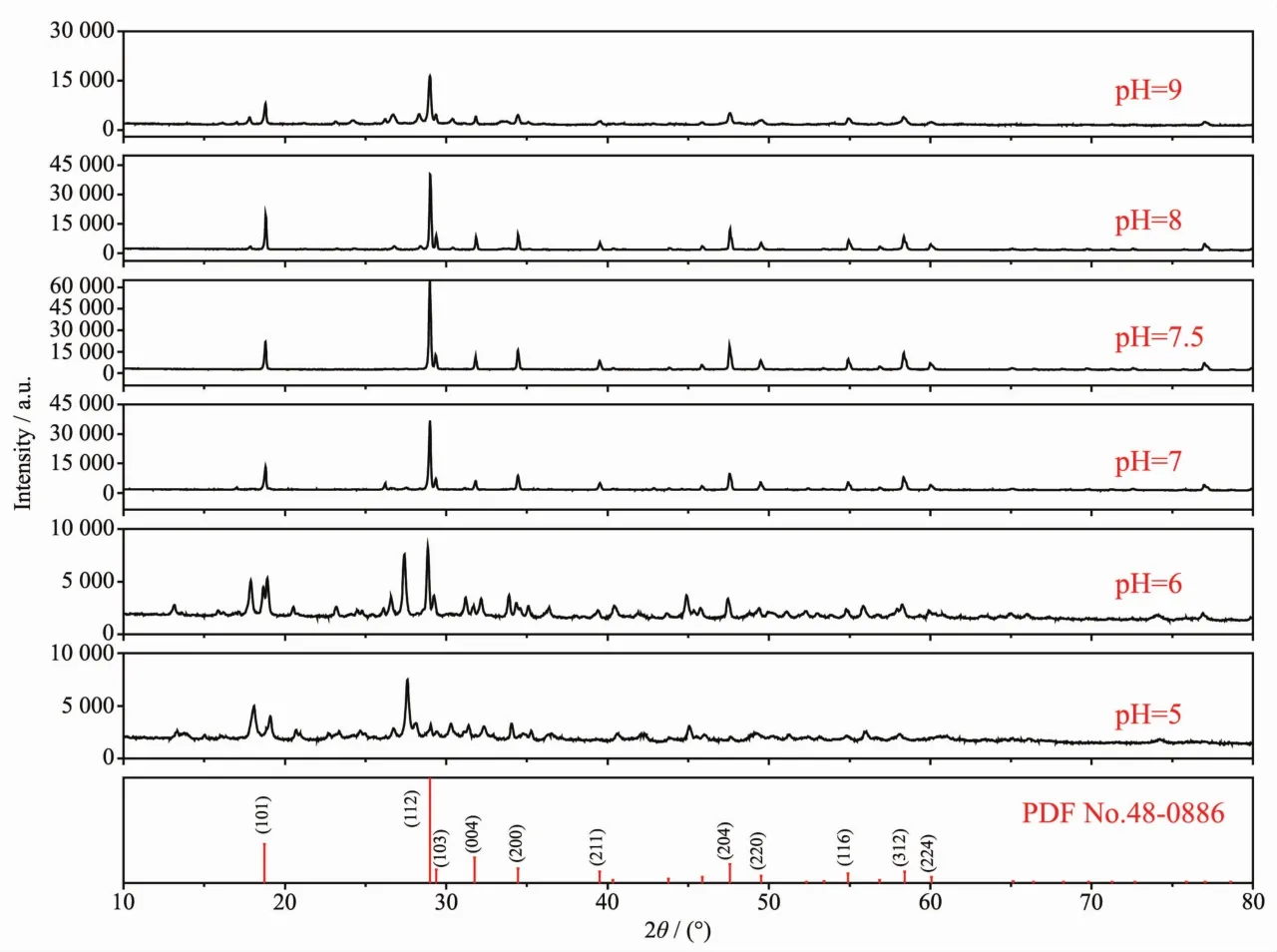
图1 不同pH值下合成样品的XRD图FiL.1 XRD patterns of the samples synthesized at different pH values
2 结果与讨论
2.1 pH值对NaY(WO4)2基质材料的晶体结构及形貌的影响
众所周知,在利用水热法、溶剂热法等湿化学方法合成粉体材料时,pH值的变化对于材料的晶体结构、形貌及性能具有很大的影响。对于钨酸根而言,在不同pH环境中有 [WO4]2-、[HW6O20]3-、[HW6O11]6-等多种不同的存在形式。而作为原料之一的Na2WO4只有在偏碱性溶液中才会以[WO4]2-的形式存在,在偏酸性条件下则以偏钨酸根和仲钨酸根的形式存在[17]。因此,为保证合成产物为纯相的NaY(WO4)2有必要了解pH值变化对其晶体结构的影响,同时也为后续稀土Er3+、Yb3+离子的掺杂奠定基础。鉴于此,图1给出了在不同pH值条件下经180℃水热反应24 h后样品的XRD图。如图所示,当pH值小于7时尚未形成四方相的NaY(WO4)2,样品中存在多处其他相衍射峰,主要对应WO3、Y2WO6、Y6WO12等多酸化合物。而在pH值等于7时,上述多酸化合物衍射峰基本消失。继续调节pH值至7.5或8,图中所有衍射峰均与NaY(WO4)2的标准卡片PDF No.48-0886匹配,说明在该条件下合成的样品为纯四方相的NaY(WO4)2,空间群为I41/a(88)。当pH值为9时,衍射峰强度有所减弱。因此,在合成Er3+、Yb3+共掺杂NaY(WO4)2上转换发光粉时选择pH等于8。
图2为不同pH值条件下经180℃水热反应24 h后样品的SEM图。根据前文XRD结果可知,当pH值小于7时样品的物相结构与目标产物NaY(WO4)2不符,因此在进行SEM表征时,选择pH值等于7、7.5、8及9的样品进行测试 (图2)。由图可见,在不同pH值条件下,样品的形貌发生了很大变化。当pH值为7时,样品主要呈不规则块状,同时还伴有少量片状颗粒组成的微米球,在部分位置还能观察到少量八面体状微晶,其中块状粒子的粒径约为2.5μm,微米球的粒径在2μm左右。调节pH值为7.5,多数颗粒呈轮廓清晰的八面体,颗粒间的分散性较好,另有少量细小颗粒分散在八面体粒子周围,其中八面体微晶的尺寸约为2μm,小颗粒的粒径在400~600 nm之间。当pH值为8时,样品以拟立方体状微晶为主,且立方体表面附着有片状颗粒,拟立方体状微晶的尺寸约为2.3μm。继续调节pH值至9,样品厚度及尺寸减小颗粒全部呈片状,且不规则片状颗粒相互组合形成一个大的团聚体,其中片状颗粒的尺寸约为200~500 nm。

图2 不同pH值下合成样品的SEM图FiL.2 SEM imaLes of the samples synthesized at different pH values
根据上文分析发现,pH值对样品的形貌具有显著的影响,通过调节pH值可以实现由八面体到拟立方体再到片状微粒的转变,引起这种形貌间演变的主要原因是,控制pH值以改变晶面的表面能,从而改变沿各晶面的生长速率,实现对微晶形貌的有效控制。对于图2中晶体可能的生长机理分析如下:通常,晶体的生长速率与其表面能有关,更快的生长方向出现在具有较高表面能的晶面上。通过调节pH值,溶液中的OH-可优先选择吸附在(001)晶面上,使其表面能降低,同时可促进沿其他等效方向上的生长速率。根据Donnay-Harker提出的理论[18],对于具有四方相结构 NaY(WO4)2,(001)晶面的表面能高于(101)晶面,这使得沿着(001)晶面方向的生长速率要高于(101)晶面,因此可以形成(101)晶面暴露的双椎体,即八面体。继续升高溶液pH,吸附在(001)晶面上的OH-数量增多,使该晶面上Na+和Y3+的堆积密度高于其他晶面,导致具有更高表面能的(001)晶面的生长速率降低,而(001)晶面将会在最终的形貌中予以保留,因此,在较高pH值条件下倾向于形成拟立方体。此外,体系中OH-继续增多的同时的数量也随之增加,这时体系中的阳离子经历一个简单的离子交换过程,使得空间中部分Na+被取代,而离子半径较大的可使空间膨胀导致层面位移,在碱性溶液的辅助下离子交换的范围逐渐扩大,有利于更多层状结构的形成。于此同时,水热过程中与水分子始终存在可逆反应,这样一来便难以提供足够量的正电荷来维持层状结构的稳定,导致层状结构被剥离并形成薄片产物。此外,结合XRD分析,当pH值等于9时,衍射峰的半峰宽变宽且强度减弱,因此尺寸减小。
图3(a~d)分别为pH=8,180℃水热反应24 h后样品的SEM、粒度分布、TEM及HRTEM图。由图3(a)可见,在当前合成条件下,样品主要由拟立方体形的块状颗粒及分散在其表面和周围的片状颗粒组成,其中拟立方体的边长约为3μm,片状颗粒的尺寸在500~600 nm之间。根据图3(b)的粒度分布曲线得到样品的d0.5=2.312μm,即组成该样品的所有粒径颗粒中,小于2.312μm的颗粒占50%,该结果与SEM图观察到的结果基本一致。图3(c)的TEM图显示出与SEM图类似的结果,拟立方体形貌规整,4条边清晰可辨,并有少量亚微米级片状颗粒附着其表面。如图3(d)所示,在HRTEM图中可以观察到明显的晶格条纹,表明合成样品具有较高的结晶度。经计算得到2个相邻条纹间的距离约为0.303 nm,该结果与纯四方相NaY(WO4)2晶体中的(112)晶面对应。
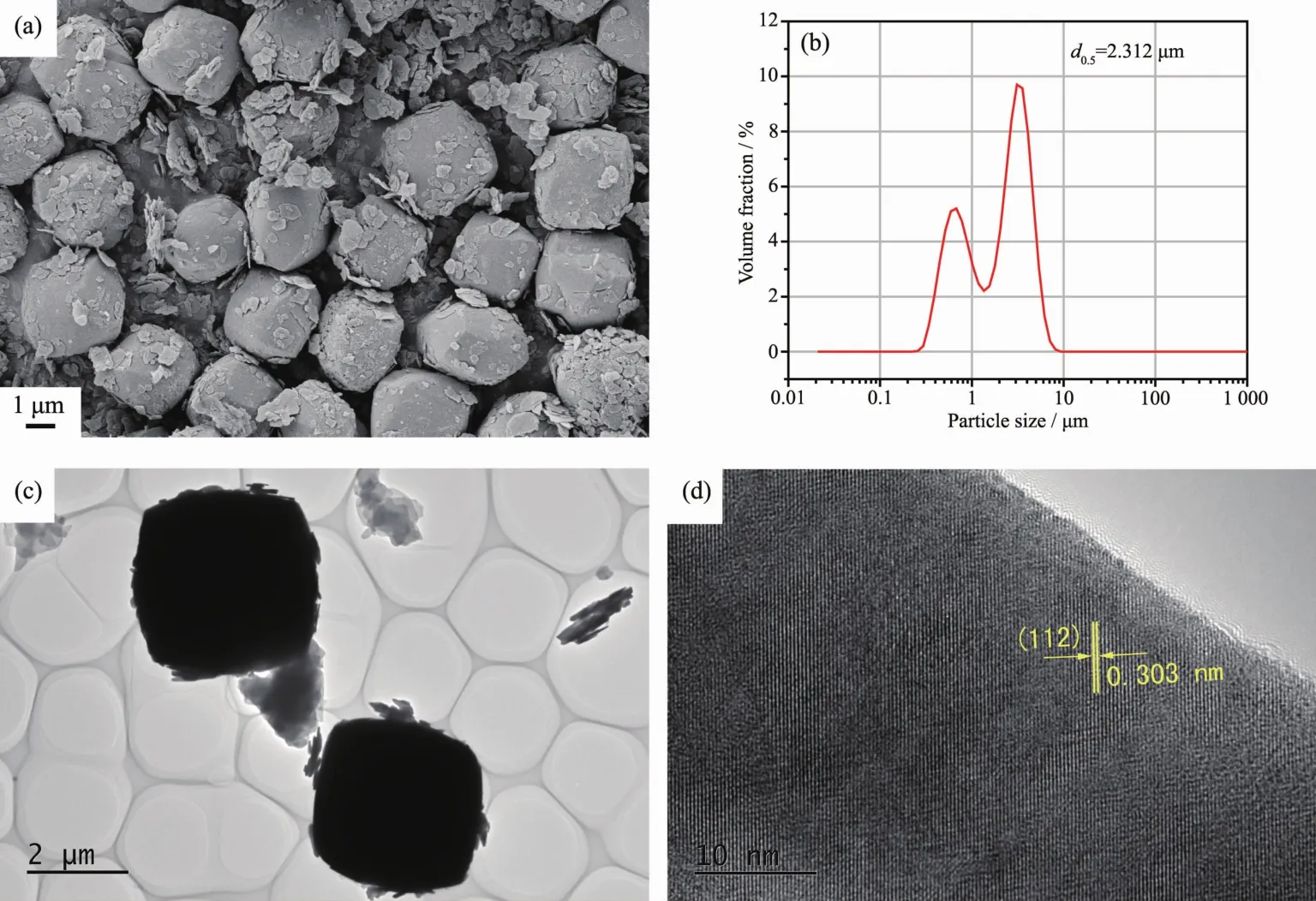
图3 样品的SEM、粒度分布、TEM及HRTEM图FiL.3 (a)SEM,(b)particle size distribution,(c)TEM and(d)HRTEM imaLes of sample
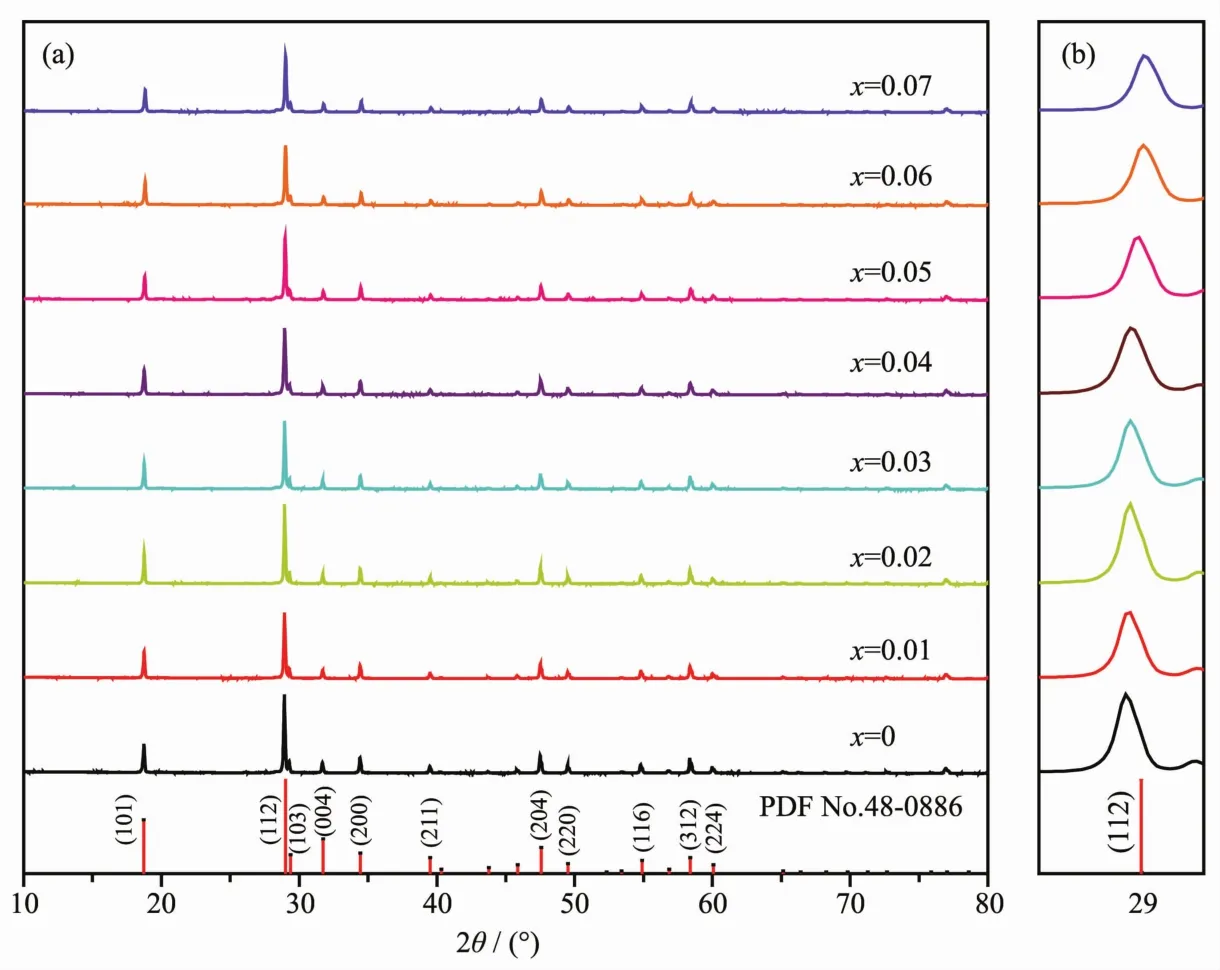
图 4 (a)NaY0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07)样品的 XRD 图及NaY(WO4)2标准卡片PDF No.48-0886;(b)(112)晶面衍射峰放大图FiL.4 (a)XRD patterns of NaY0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07)samples and the standard card of NaY(WO4)2;(b)Amplified(112)diffraction peaks
2.2 Yb3+掺杂量对 NaY(WO4)2∶Er 3+,Yb3+荧光粉晶体结构的影响
图 4(a)为样品 NaY0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07)的 XRD 图。图中各样品的衍射峰均与标准卡片PDF No.48-0886吻合,且无杂相峰出现,说明样品是与NaY(WO4)2同构的纯相,而掺入的Er3+和Yb3+离子并未引起NaY(WO4)2晶体结构的改变。此外,衍射峰尖锐明显,半高宽较窄,表明样品结晶程度良好。随着Yb3+浓度的增加,样品(112)晶面对应的衍射峰逐渐向高 2θ角度方向位移(图 4(b))。这是由于 Er3+(0.100 4 nm)和Yb3+(0.098 5 nm)的离子半径小于Y3+(0.101 9 nm), 当 Er3+与 Yb3+进入晶格取代 Y3+后,导致晶面间距减小,因此衍射峰逐渐向大角度偏移。一般而言,在稀土离子掺杂的荧光材料中被取代离子与掺杂离子之间的半径百分比之差(Dr)应小于30%,上述关系可表示成[19]:

式中,Rs为被取代离子的有效离子半径,RD为掺杂离子的有效离子半径。计算得到Y3+/Er3+与Y3+/Yb3+的Dr值分别为1.47%和3.37%。很明显该结果远远小于30%,因此可进一步证实Er3+、Yb3+离子可取代Y3+的格位进入到基质NaY(WO4)2晶格中。
2.3 上转换发光性能分析
根据文献[20]所述,在制备 NaY(WO4)2∶Er3+,Yb3+上转换荧光粉时,选择Er3+的浓度为2.0%(n/n)。为了解 NaY0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07) 荧光粉的上转换发光性能,分别测试了不同Yb3+浓度样品在980 nm光激发下的上转换发射光谱,(图5)。图中谱线由三部分组成,包括中心波长位于525和553 nm处的强绿光发射,对应 Er3+的2H11/2→4I15/2与4S3/2→4I15/2跃迁。以及 650~680 nm之间的弱红光发射,归属于Er3+的4F9/2→4I15/2跃迁。此外,随着Yb3+浓度的增加,绿光和红光的发射强度呈先增强后减弱的趋势,当x=0.05时,绿色及红色上转换光强度均达到最大值。Yb3+掺杂浓度与553 nm处绿光及657 nm处红光发射强度之间的关系曲线,见图5插图。不难发现,与未掺杂Yb3+样品相比以上2组发射峰强度均得到不同程度的提高,说明Yb3+与Er3+之间存在强而有效的能量传递。稀土离子间的能量传递效率E可用下式表示[21]:

式中R为2个稀土离子之间的距离,当Yb3+的浓度增加时,Er3+与Yb3+之间的距离逐渐缩短,能量传递效率随之增加,因此Er3+的特征发射增强。而x大于0.05时,由于临近离子的相互作用增强,产生能量共振传递,导致浓度猝灭,所以发光强度减弱。
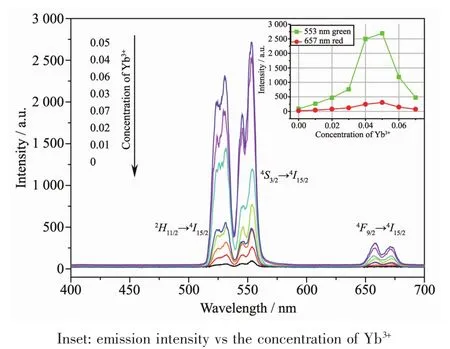
图 5 NaY0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07)荧光粉在 980 nm光激发下的上转换发射光谱FiL.5 Upconversion emission spectra of NaY 0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07)phosphors excited by 980 nm laser
2.4 上转换发光强度的制约关系与发光机理
上转换发光是一种典型的多光子参与的发光行为,且上转换发光强度Iup与激光器泵浦功率P之间满足[22]:

式中,a为常数,n代表发射出一个可见光子所需吸收的红外光子数。此外,由于光纤激光器的输出功率P与激光器的工作电流i呈线性相关,可表示成:

其中,i0表示光纤激光器的阀值电流,P0为常数。结合(3),(4)两式得到上转换发光强度Iup与激光器工作电流i之间的关系,如下式:

依据上文确定的双光子过程,图7给出了Er3+与Yb3+的能级结构及980 nm光激发下NaY(WO4)2∶Er3+,Yb3+荧光粉可能的上转换发光机制。对于单掺杂Er3+的上转换材料而言,Er3+发光能级的布居主要通过基态吸收(GSA)及激发态吸收(ESA)来实现。由于Yb3+在980 nm波长附近的吸收截面远大于Er3+的吸收截面,并且Yb3+对Er3+具有较高的能量传递几率,因此在掺入Yb3+后,Yb3+→Er3+的能量传递将占主导,具体过程如下:处于基态2F7/2上的Yb3+吸收一个980 nm光子能量后跃迁至激发态2F5/2,之后通过 ET1:2F5/2(Yb3+)+4I15/2(Er3+)→2F7/2(Yb3+)+4I11/2(Er3+)完成对Er3+的能量传递,使之跃迁至4I11/2能级。此时,处于4I11/2上的Er3+一部分继续吸收1个Yb3+传递的能量,经 ET2:2F5/2(Yb3+)+4I11/2(Er3+)→2F7/2(Yb3+)+4F7/2(Er3+),使Er3+跃迁到4F7/2能级,之后经连续无辐射跃迁(NR)至2H11/2、4S3/2及4F9/2能级;而另一部分处于4I11/2能级的Er3+则无辐射跃迁(NR)到4I13/2能级,并通过 ET3:2F5/2(Yb3+)+4I13/2(Er3+)→2F7/2(Yb3+)+4F9/2(Er3+)使其达到4F9/2能级,至此完成对各发光能级的布居。2H11/2、4S3/2及4F9/2能级上的Er3+分别向下辐射跃迁至对应能级完成上转换绿、红光发射[23-25]。值得一提的是,当Yb3+浓度过高时,临近离子的相互作用增强,出现反向能量传递(EBT),使Er3+发光能级的布居数减少,从而失去对上转换发光的贡献,导致发光强度明显减弱。
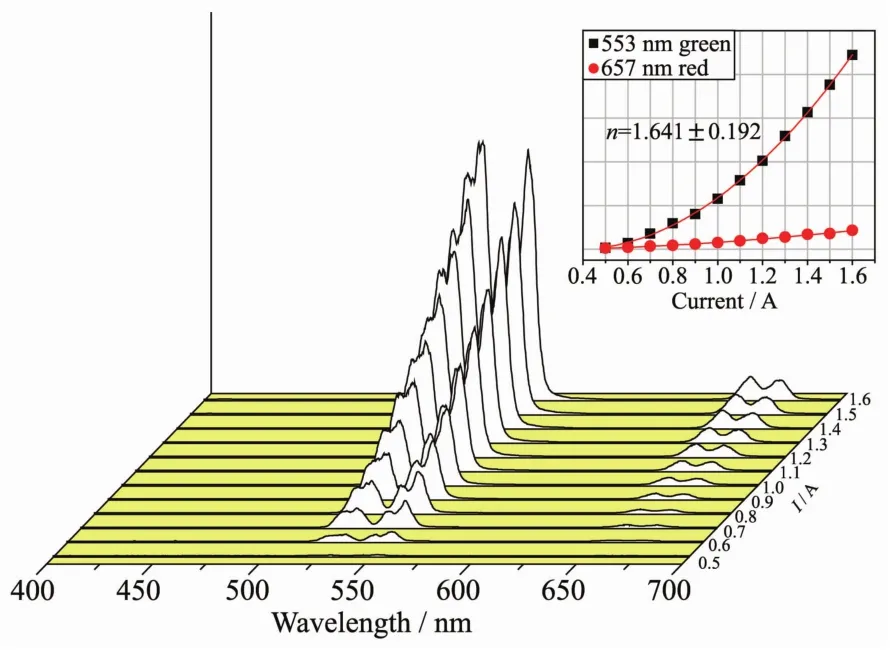
图 6 NaY0.93(WO4)2∶0.02Er3+,0.05Yb3+样品在 980 nm光激发下不同工作电流时的上转换发射光谱及绿、红光发射强度与工作电流间的关系曲线FiL.6 Upconversion emission spectra of NaY0.93(WO4)2∶0.02Er3+,0.05Yb3+sample excited by 980 nm laser at different workinLcurrents and the dependence ofred and Lreen emission intensities on the laser workinLcurrent
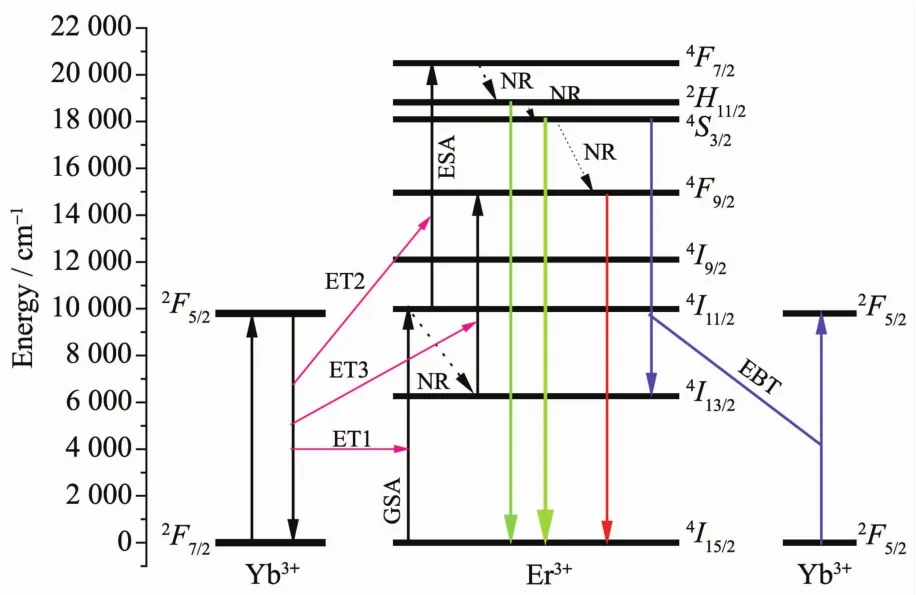
图7 980 nm光激发下Er3+和Yb3+的能级结构及其上转换发光机理FiL.7 EnerLy level diaLram of Er3+and Yb3+ions as well as possible UCmechanism under the excitation of 980 nm
2.5 CIE色度图分析
为表征 NaY0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07)系列荧光粉的色度,实验测试了样品的CIE色度坐标随Yb3+掺杂浓度的变化图(图8)。在980 nm近红外光激发下,所有样品的发光颜色均处于绿光区,与前文发射光谱描述的结果一致。此外,通过调节Yb3+的浓度可实现纯度较高的绿光发射,使荧光粉表现出良好的可控单色发光特性,这对于生物标记具有重要的实际意义。
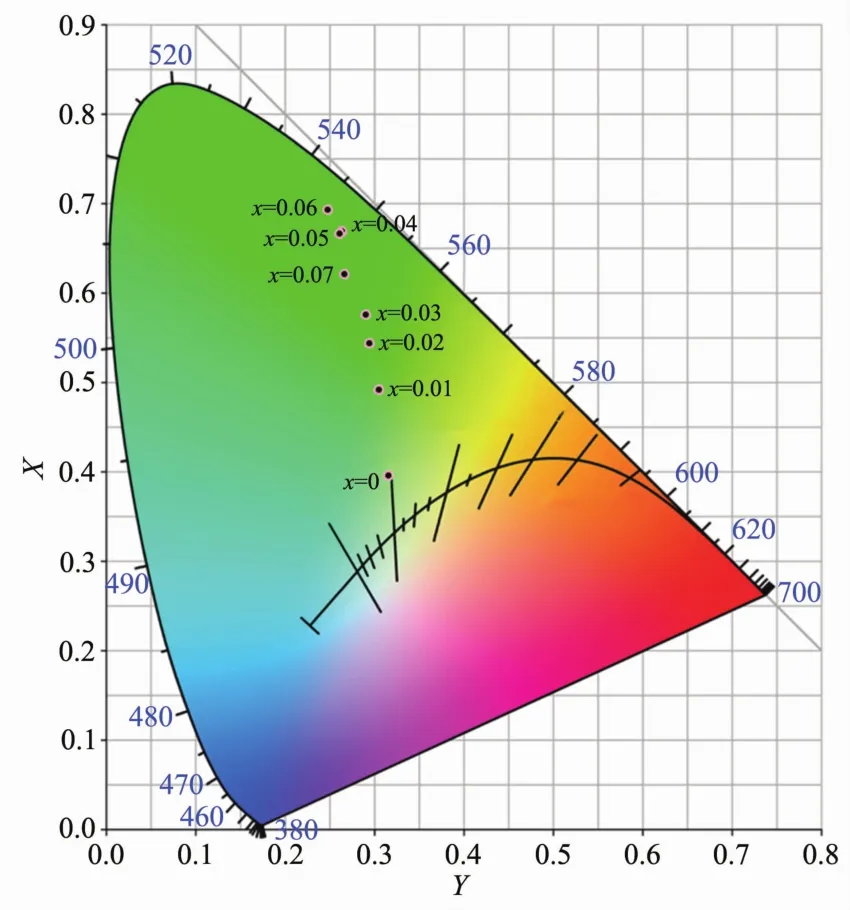
图 8 NaY0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07)样品的 CIE 色度图FiL.8 CIE chromaticity diaLram of NaY0.98-x(WO4)2∶0.02Er3+,x Yb3+(x=0,0.01,0.02,0.03,0.04,0.05,0.06,0.07)samples
3 结 论
(1)采用水热法成功合成出具有四方白钨矿结构的NaY(WO4)2微米颗粒。通过调节pH值可实现由八面体到拟立方体再到片状颗粒的形貌演变,且该变化过程与溶液中的OH-数量以及OH-对(001)晶面的优先选择吸附有关。
(2)在pH=8条件下合成出一系列Er3+/Yb3+共掺杂NaY(WO4)2上转换发光粉。利用980 nm激光器作为激发光源,实现了Er3+在525、553及650~680 nm之间的绿、红光特征上转换发射,其发射强度明显高于单掺杂Er3+体系,说明Yb3+与Er3+之间存在能量传递,且上转换绿、红光均属于双光子过程。
(3) 通 过 调 节 NaY(WO4)2∶Er3+,Yb3+上转换 荧 光粉中Yb3+的浓度,可完成对绿光色度的精确调控,这对于生物成像中对单一组分的荧光标记具有重要的实际意义。

