基于石墨烯和壳聚糖复合膜构建的电化学传感器检测尿酸研究
高牧丛,张 盼,周 强,常 东,潘洪志
(1.泰州市中医院,江苏泰州 225300; 2.哈尔滨医科大学公共卫生学院,哈尔滨 150081;3.枣庄市立医院,山东枣庄 277000;4.复旦大学附属浦东医院,上海 201209;5.上海健康医学院,上海 201308)
尿酸(uric acid,UA)是生理过程中重要的生化分子[1]。如果机体产生过多或排泄机制下降均可导致体内潴留过多,进而并发多种代谢疾病,因此尿酸的检测在临床应用方面具有重要意义[2,3]。近年来,电极法测定尿酸因其成本低、制备容易、灵敏度高、反应速度快等特点而被广泛关注[4~7]。石墨烯(graphene,GR)导电性能高,比表面积大,是十分优良的电极材料。壳聚糖(chitosan,CHI)具有良好的生物相容性,不仅有亲水基团和疏水基团,还有可使石墨烯均匀分散的-NH2和-OH。本实验用石墨烯和壳聚糖构建电化学传感器来检测尿酸,为临床尿酸研究提供了良好的应用前景。
1 材料与方法
1.1 实验样本 尿酸、多巴胺、抗坏血酸标准品购自美国Sigma公司。采集2017年9月24日三名实验人员晨尿进行检测。
1.2 试剂与仪器 石墨烯(南京吉仓纳米科技有限公司);壳聚糖、冰醋酸、铁氰化钾、亚铁氰化钾、氯化钾、磷酸氢二钠、磷酸二氢钠(国药化学试剂有限公司);其他试剂均为国产分析纯试剂;实验用水为超纯水。CHI660C型电化学工作站(上海辰华仪器有限公司);常规三电极系统:修饰玻碳电极为工作电极,铂丝为对电极,Ag/AgCl为参比电极;SU-8010型扫描电子显微镜(SEM,日本日立公司);pH酸度计(上海精密科学仪器有限公司);电子天平AR1140(梅特勒-托利多仪器上海有限公司);KQ-100型超声波清洗器(昆山市超声仪器有限公司);微量移液器(北京吉尔森科技有限公司);Al2O3(1 μm,0.05 μm)研磨剂和电极抛光布(上海辰华仪器有限公司)等。
1.3 实验方法
1.3.1 电极预处理:将玻碳电极用1 μm和0.05 μm的Al2O3抛光粉抛光,并依次用乙醇、1∶1硝酸、去离子水超声清洗5 min,使用前在铁氰化钾溶液中进行循环伏安法扫描(-0.1 V~ 0.6 V,50 mV/s),直至△Ep <70 mV。最后将电极用去离子水洗涤并干燥备用。
1.3.2 修饰电极的制备:1 g/dl壳聚糖溶液(100 ml):用电子天平称取壳聚糖1 g,置入小烧杯中,加入1 ml冰醋酸后转移至100 ml容量瓶中双蒸水定容,充分混匀,常温放置,需要超声数小时备用;取适量石墨烯(GR)溶于上述制得的1 g/dl壳聚糖溶液中得到0.5 g/L混悬液,备用。取6 μl的CHI/GR混悬液滴在处理好的干净玻碳电极上,室温下干燥即为CHI/GR/GCE修饰电极,将所制备的电极置于4℃冰箱中备用。
1.3.3 表征和检测方法:通过扫描电子显微镜对石墨烯进行形貌分析;采用循环伏安法、差分脉冲伏安法和交流阻抗法等研究尿酸在石墨烯/壳聚糖修饰的玻碳电极上的电化学行为,并评估其检测性能。
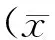
2 结果
2.1 修饰材料的形貌分析 见图1。由图1的石墨烯(GR)的扫描电子显微镜图可知,电极表面的石墨烯薄膜呈波浪状的皱褶形貌,这与文献描述一致[8]。这些皱褶可以形成很多纳米孔道和空穴,从而增大电极的比表面积,增强电极的导电性能。

图1 GR的SEM照片
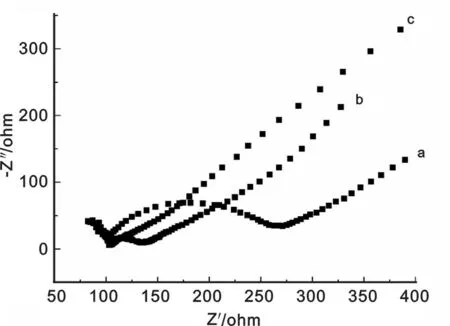
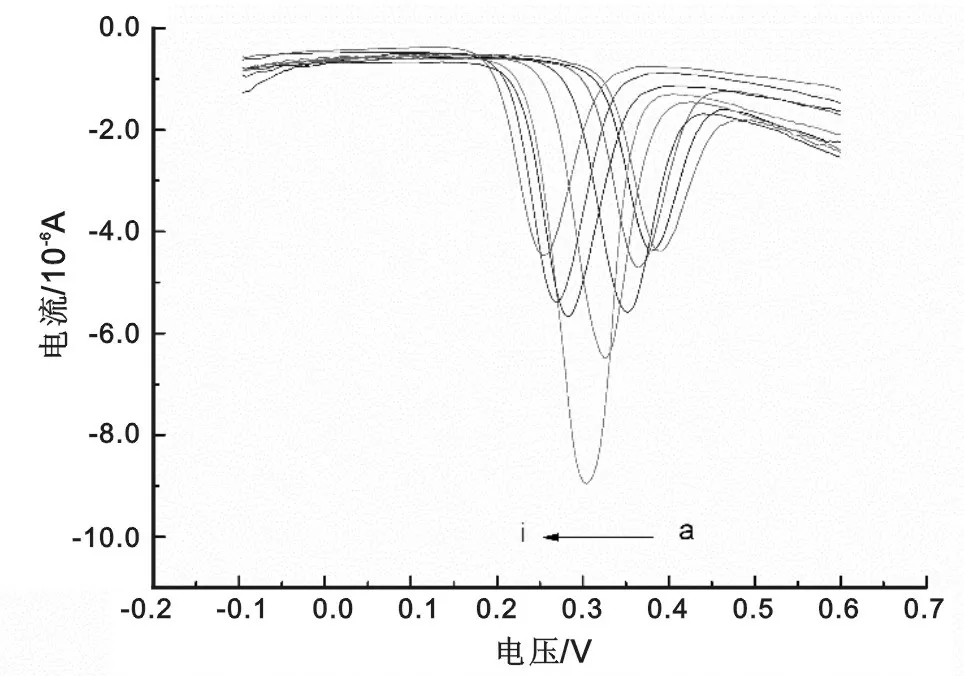
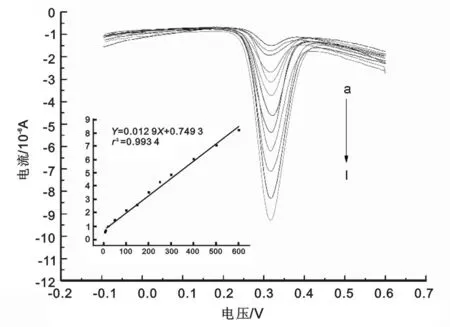
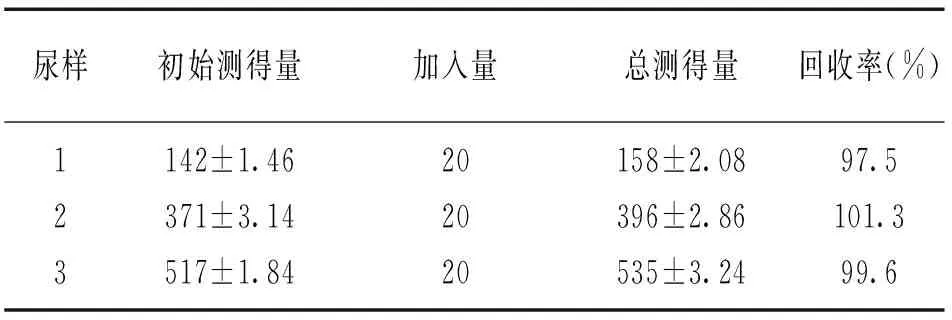
2.2 修饰电极的表征 见图2。图2是不同修饰电极在循环底液中的循环伏安曲线。图中曲线a,b,c分别为GCE电极、GR/GCE电极和CHI/GR/GCE电极的CV曲线。在扫描的电位范围内有一对明显的氧化还原峰,峰电流由小到大依次为:a 图2 不同修饰电极在5 mmol/L K3Fe(CN)6+0.1mol/L KNO3中的循环伏安图 图3 不同电极在5 mmol/L K3Fe(CN)6/K4Fe(CN)6+0.1 mol/L KNO3溶液中的交流阻抗图谱 2.3 电解液pH的优化 见图4。图4为CHI/GR/GCE电极在不同pH值下的200 μmol/L尿酸中的差分脉冲曲线。尿酸的氧化峰电位随着缓冲溶液pH值的增加而负移,这说明尿酸的电化学反应过程伴有质子的参与。当pH值为6.5时,尿酸的峰电流相对较大,因此在后续实验中选择pH 6.5的0.1 mol/L PBS作为支持电解质。 图4 CHI/GR/GCE电极在不同pH值的200 μmol/L尿酸中的差分脉冲曲线图 2.4 扫速的优化 CHI/GR/GCE修饰电极在pH 6.5的200 μmol/L尿酸中以不同的扫描速度进行的循环伏安实验见图5。尿酸在修饰电极上的氧化峰电流随扫速的增加而增大。由峰电流与扫速的线性关系曲线可知,峰电流与扫速的平方根在20~500 mV/s范围内呈良好的线性关系,线性方程为:Ip(10-5A)=0.011 8v(mV/s)+0.260 2(R2=0.9936),符合典型的表面化学过程。这说明尿酸在CHI/GR/GCE电极上的反应速率受电极的表面电化学过程控制。 From a to m:20,40,60,80,100,200,300,400,500 mV/s;Inset:plot of oxidation peak potential versus scan rate 图5 CHI/GR/GCE电极在200 μmol/L尿酸中不同扫速下的循环伏安图 2.5 尿酸的检测 在最佳实验条件下,对不同浓度的尿酸进行测定。由不同浓度的尿酸在修饰电极上的差分脉冲伏安曲线见图6,可知随尿酸浓度的增大,电流值也逐渐增大。在6~600 μmol/L的浓度范围内峰电流与相应尿酸浓度具有良好的线性关系,线性方程为Ip(10-6A)=0.012 9c(μmol/L)+0.749 3,相关系数R2=0.993 4。信噪比为3时(S/N=3),根据3σ规则计算可得尿酸的检出限为0.33 μmol/L,具有较好的灵敏度。 图6 不同浓度UA在CHI/GR/GCE电极上的差分脉冲图 (A)100 μmol/L UA;(B)100 μmol/L UA+1 000 μmol/L DA;(C)100 μmol/L UA+1 000 μmol/L G;(D)100 μmol/L UA+1 000 μmol/L AA。 图7不同干扰物对100 μmol/L UA测定的影响 2.7 实际样品及加标回收率测定 采集实验人员的晨尿进行尿酸测定及其加标回收试验。本文采用差分脉冲(DPV)技术,将尿样在3 500 r/min下离心15 min后分别取1 ml尿样1,2,3进行测定,结果见表1,其回收率在97.5%~101.3%之间。 尿样初始测得量加入量总测得量回收率(%)123142±1.46371±3.14517±1.84202020158±2.08396±2.86535±3.2497.5101.399.6 本文基于石墨烯与壳聚糖复合膜构建了一种检测尿酸的新方法。石墨烯是片层的二维结构;壳聚糖不仅有亲水基团和疏水基团,而且还有可使石墨烯均匀分散的-NH2和-OH的基团,使其具有较好的生物相容性。CHI/GR复合材料不仅具有石墨烯的良好导电性还具有很好的成膜性,可更好地吸附尿酸,进而提高尿酸检测的灵敏度。实验结果表明,该电化学传感器测定尿酸时具有良好的稳定性、抗干扰性、电催化性及较宽的线性范围。将该电极用于实际样品的测定时尿酸的回收率在97.5%~101.3%之间,这在实际样品中的检测具有良好的应用前景。本实验对临床尿酸的检测及其相关疾病的预防、诊断具有重要的意义,在临床生物诊断中具有较高的应用价值。由于高灵敏度和高选择性的分析方法是电分析化学研究追求的目标之一,加之固有电极的清洁问题可能导致可靠性问题,因此仍然需要进一步地开发一次性的微型总分析系统来对相应的临床尿酸检测进行研究。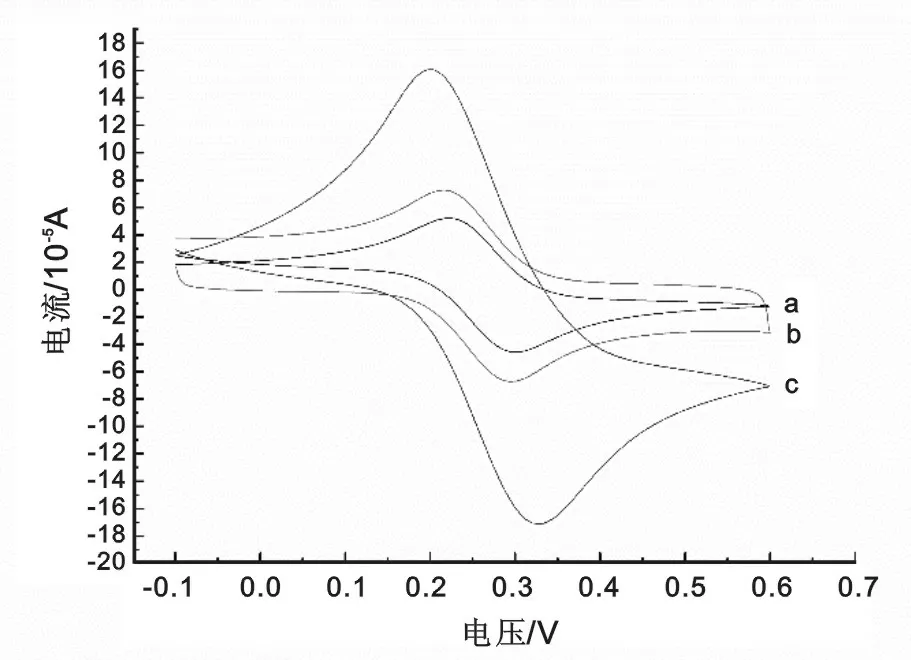



3 讨论

