电-多相臭氧催化技术处理金刚烷胺制药废水
马富军,李新洋*,宗博洋,于晓华,孙绍斌,姚 宏*
电-多相臭氧催化技术处理金刚烷胺制药废水
马富军1,李新洋1*,宗博洋2,于晓华1,孙绍斌1,姚 宏1*
(1.北京交通大学土木建筑工程学院,北京 100044;2.同济大学环境科学与工程学院,上海 314051)
采用电-多相臭氧催化(E-catazone)技术处理高COD、高含盐、难生化的金刚烷胺制药废水.对比研究电-多相臭氧催化、多相臭氧催化(Catazone)、电催化氧化(EO)对金刚烷胺制药废水的处理效果,在此基础上进一步研究了电流密度、pH值以及气相O3浓度对电-多相臭氧催化技术处理效果的影响,同时优化实验条件.实验结果表明,在原水pH值为12.5,电流密度为15mA/cm2,O3进气流速0.4L/min,O3浓度为60mg/L的条件下,经过60min反应,电-多相臭氧催化技术获得了62%的COD去除和44%的总有机碳(TOC)去除,其效果显著优于多相臭氧催化(COD 44%,TOC 29% )与电催化氧化(COD 13%,TOC 17%);同时,电-多相臭氧催化不仅氧化能力强,而且氧化速率快,获得的伪一级COD去除速率常数是多相臭氧催化和电催化氧化的1.81倍和8.22倍, 更为重要的是,电-多相臭氧催化技术还可以高效、快速地提高废水的生化性,提高约2个数量级, 结果表明,电-多相臭氧催化技术是一种有潜力的高级氧化技术,可以实现高效、快速去除有机污染物以及提高废水的可生化性.
金刚烷胺;制药废水;电-多相臭氧催化;二氧化钛
金刚烷胺是近年来广泛使用的抗流感药物,在工业生产过程中主要产生于溴化废水和胺化废水[1-2],是高浓度有机废水,具有成分复杂、高COD、高无机盐、生化性差、微生物抑制作用强等特点,如果不经处理直接排入河流,影响河流生态环境,目前,国内外主要处理金刚烷胺废水的方法有络合萃取法[3]、双极膜电渗析法[4]等,这些技术虽取得了一定的成果,但还存在处理效率低、速率低、需要投加化学药剂、产生二次污染等不足[5],因此,亟待开发高效、快速、绿色的金刚烷胺制药废水深度氧化技术.
电-多相臭氧催化技术是本课题组此前开发的新型高级氧化技术[6],具有矿化效率高、反应速率快、无二次污染等特点,该氧化体系主要由自主开发的负载TiO2纳米花管状多孔钛为阳极,钛网作阴极组成,该负载TiO2纳米花阳极巧妙地将电极、曝气器、电催化氧化以及多相臭氧催化整合于一体,当在该阳极上同时施加正向偏电位并通入O3时,表面负载的TiO2纳米花催化层在其电催化/多相臭氧双催化活性的作用下,可以实现阳极界面的电催化氧化与多相臭氧催化的协同作用,羟基自由基等活性物质产率的大幅提高,最终实现污染物地快速去除,同时该曝气阳极三维多孔结构以及特有的流通式构型,O3气体可以在强制对流作用下穿过电极内部进行传质,使得O3/电极界面扩散层厚度显著降低到文献报道的20mm[7]的百分之一,极大地促进了O3/电极间传质,提高了反应速率,另外,电-多相臭氧催化系统还具有装置简洁、紧凑的特点,曝气阳极的使用还将传统电化学-臭氧装置(阳极/曝气装置/阴极)极大简化为现有体系(曝气阳极/阴极),显著促进了气-液-固三相反应,但此前的电-多相臭氧技术主要针对蒽醌类染料[8]模拟废水进行研究,对于成分复杂且难降解实际工业废水的处理尚无研究报道.
本文基于电-多相臭氧催化技术,开展该技术对金刚烷胺制药废水处理的可行性研究,通过对比研究,考察电-多相臭氧催化技术、多相臭氧催化、电催化氧化等不同氧化体系对污染物的去除效率、速率以及可生化性改善效果,在此基础上,在电-多相臭氧催化体系中,考察初始pH值、O3浓度、电流密度对COD去除的影响,并优化体系的运行参数,旨在为电-多相臭氧催化处理实际废水提供参考.
1 材料与方法
1.1 实验用水
所用金刚烷胺制药废水来自某金刚烷胺制药企业生产车间排放的废水,其水质指标如表1所示;实验用水使用前用0.22μm微孔滤膜抽滤,去除大部分废水中的悬浮性固体后,在4℃冰箱中保存,

表1 金刚烷胺废水水质特征
1.2 试剂和仪器设备
1.2.1 试剂 重铬酸钾、浓硫酸、磷酸、硫酸亚铁铵、硫酸银、硫酸汞、叔丁醇、甲醛、乙酸铵、乙酰丙酮均为分析纯,由国药生产公司提供.
1.2.2 仪器 臭氧发生器(3S-J5000,北京同林高科科技有限公司);稳压直流电源(PS-305DM,香港龙威仪器仪表有限公司);管状多孔钛(长20mm/Φ5mm,平均孔径51μm,宝鸡英高金属材料有限公司);O3浓度检测仪(3S-J5000,北京同林高科科技有限公司);转子流量计(LZB-3WB,天津斯秘特精密仪表股份有限公司);TOC分析仪(vario TOC,大昌华嘉商业有限公司);COD快速测定仪(5B-1,连华科技有限公司); DO测定仪(Multi 3420,德国WTW);生化培养箱(LRH-250A,广东医疗器械厂);真空干燥箱(DZF- 6092,上海一恒科学仪器有限公司);Milli-Q纯水系统(A10,Milipore公司);溶剂过滤器(T-50,天津津腾试验设备有限公司);隔膜真空泵(GM-0.33A,天津津腾试验设备有限公司).
1.3 实验方法
1.3.1 对比实验 在避光的条件下,取经0.22μm混合纤维滤膜抽滤过的澄清金刚烷胺制药废水各500mL于3个相同的玻璃柱反应器中(图1),分别用电-多相臭氧催化、多相臭氧催化和电化学氧化技术进行处理.在电-多相臭氧催化体系中,使用负载TiO2的多孔钛曝气头为阳极[9]、钛网作为阴极, O3和O2混合气体经臭氧发生器以0.4L/min的恒定流量通入反应器.通入O3的同时,向曝气阳极施加一定的恒定电流;在多相臭氧催化体系中仅使用负载TiO2的多孔钛曝气头, O3通过曝气头通入体系;在电催化氧化体系,同样使用负载TiO2的多孔钛曝气头为阳极、钛网作为阴极,仅通过直流电源施加恒定电流,不通入O3;电-多相臭氧催化、多相臭氧催化和电催化氧化的羟基自由基产量反应条件:pH=12.5,以0.1mol/L Na2SO4溶液为电解质,其他条件与对比实验相同.每组实验反应为60min,每隔10min取样进行分析.

图1 电-多相臭氧催化实验示意
1.O2瓶;2. O3发生器;3.转子流量计;4. O3检测器;5.稳压直流电源;6.反应器;7.负载TiO2纳米花管状多孔钛曝气器;8.钛网阴极;9.O3检测器
1.3.2 优化实验 在电-多相臭氧催化实验中,逐次改变电流密度、气相O3浓度和初始pH值的大小,其他条件与对比实验相同,分别研究不同参数下,水中COD、速率常数()和O3利用率的变化情况.电-多相臭氧催化示意图如图1.
O3利用率的计算公式如下:
O3利用率=(反应器进口O3浓度-反应器出口O3
浓度)´100%/反应器进口O3浓度 (1)
1.4 分析方法
总有机碳(TOC)由TOC分析仪测定;COD用重铬酸钾法测定;pH值采用PHS-3C型精密pH计测定;O3浓度由O3检测器检测;DO用膜电极法进行测量;BOD5采用稀释接种法测定;×OH浓度测量用叔丁醇进行捕获,用Hantzsch显色法测量叔丁醇分解产物(甲醛)浓度[8].每个成分测3次,分别计算平均值,并且用单因素统计方法分析对比实验.
2 结果与讨论
2.1 电-多相臭氧催化、多相臭氧催化、电催化氧化处理金刚烷胺制药废水的对比
如图2(a)所示,电-多相臭氧催化技术对于TOC的去除效能显著地优于多相臭氧催化和电催化氧化技术,如表2所示,1-0.1(2,6)<<1-0.05(2,6).经过60min反应,电-多相臭氧催化技术获得TOC的去除率达到44%,分别是多相臭氧催化(29%)的1.52倍和电催化氧化(15%)的2.59倍;同样的,电-多相臭氧体系获得的COD去除率也显著优于多相臭氧催化和电催化氧化,如表3所示,1-0.1(2,6)<<1-0.05(2,6).其中电-多相催化获得COD的去除率达到62%,分别是多相臭氧催化(44%)的1.41倍和电催化氧化(13%)的4.77倍,如图3(a)所示.更为重要的是在反应前期(前30min), 电-多相臭氧催化对COD、TOC的去除速率符合伪一级反应动力学特征(图2(b)和图3(b)),获得的速率常数远高于多相臭氧催化以及电催化氧化.其中对于COD的去除,电-多相臭氧催化(3.26× 10-2min-1)比多相臭氧催化(1.81×10-2min-1)和电催化氧化(3.97×10-3min-1)分别高1.81倍和8.22倍;对于TOC地去除,电-多相臭氧催化技术(1.21×10-2min-1)比多相臭氧催化(7.06×10-3min-1)和电催化氧化(4.73×10-3min-1)分别高1.71倍和2.55倍.电-多相臭氧催化快速矿化金刚烷胺制药废水的主要原因在该体系中可以产生高浓度的强氧化剂(·OH),该研究结果与倪金雷等[10]研究效果相似.

图2 不同技术去除金刚烷胺制药废水中TOC的对比
(a)电-多相臭氧催化,电催化氧化和臭氧催化对TOC的去除率;(b)伪一级反应曲线;(c)羟基自由基产量
如图2(c)所示,电-多相臭氧催化技术在反应进行60min后,产生并积累的是多相臭氧催化的35倍,并且高出电催化氧化3个数量级.相比单纯的多相臭氧催化以及电化学氧化体系,电-多相催化体系的高·OH产率正是由于曝气阳极上负载的TiO2纳米花催化剂,该催化剂具有电催化/多相臭氧催化的双活性,可以实现电/多相臭氧催化的协同作用.当在TiO2表面施加正偏电位时, TiO2表面会快速失去电子产生正电空穴,该空穴会快速与O3分子相互作用并进一步引发O3链式反应产生羟基自由基(·OH),同时O3也会分解生成表面原子氧并进一步转化产生羟基自由基.然而单一的电化学氧化体系由于没有O3的参与,只能通过电化学反应在电极界面产生微量的·OH.同样的,单一的多相臭氧催化体系由于没有电化学作用参与,TiO2表面并不能有效地空穴化,与O3界面反应速率较低,因此导致·OH产率也较低,该体系也因而更多凭借O3的直接氧化作用降解有机物,所以氧化能力比较有限.此外,电-多相催化体系对金刚烷胺制药废水高效、快速的去除效果也归因于曝气阳极其优异的气-液-固三相传质性能.以往电化学/臭氧耦合体系中多为阳极∣曝气器∣阴极构型,气-液-固传质阻力较大.在电-多相臭氧催化体系中采用的是曝气阳极∣阴极构型,由于曝气阳极将曝气器、催化剂和电极三者有机结合,加之TiO2纳米花催化剂高比表面积以及三维多孔结构[11-12],因此,极大地缩短了气-液-固之间传质距离,提高了传质效率,提高了·OH产率,最终实现COD高效去除.

表2 电-多相臭氧催化、多相臭氧催化和电催化氧化去除TOC的统计分析
注:影响因素是指电-多相臭氧催化、多相臭氧催化和电催化;表中数据为反应进行60min时,电-多相臭氧催化、多相臭氧催化和电催化氧化对TOC的去除效率进行统计分析.
更值得关注的是,本研究中除了发现电-臭氧催化可以实现金刚烷胺中难降解有机物的高效、快速去除,还可以显著地提高废水的可生化性.电-多相臭氧催化技术可将BOD5/COD显著提升约2个数量级(104倍),从由原来的0,004提高到0.423,而多相臭氧催化与电催化氧化将BOD5/COD仅提升了74倍与48倍,如图4所示.经过60min反应后,虽然电-多相臭氧催化、多相臭氧催化、电催化氧化技术对BOD5的提升效果相同,但是电-多相臭氧催化体系对COD的去除效率(62%)明显优于多相臭氧催化(43%)和电催化氧化(13%),因此有效地降低金刚烷胺制药废水中COD值,显著地增大了废水中BOD5/COD值,为后续的生物处理单元提供优异的条件.
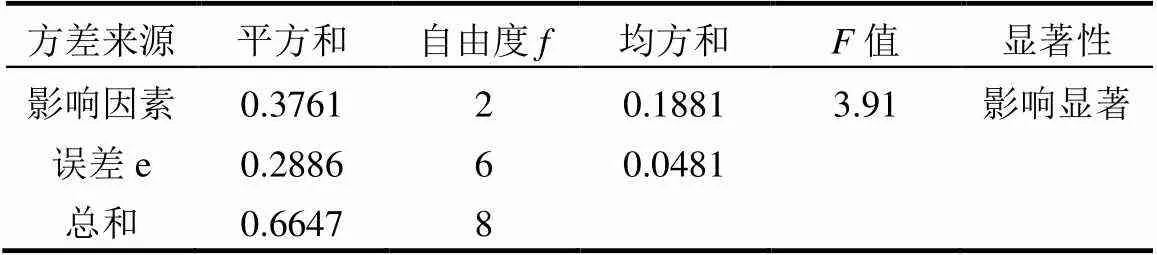
表3 电-多相臭氧催化、多相臭氧催化和电催化氧化去除COD的统计分析
注:影响因素是指电-多相臭氧催化、多相臭氧催化和电催化;表中数据为反应进行60min时,电-多相臭氧催化、多相臭氧催化和电催化氧化对COD的去除效率进行统计分析.

图3 不同技术去除金刚烷胺制药废水中COD的对比
(a)电-多相臭氧催化,电催化氧化和臭氧催化对COD的去除率;(b)伪一级反应曲线

图4 电-多相臭氧催化,多相臭氧催化和电催化氧化在反应60min后的BOD5/COD值和增大倍数
2.2 电-多相臭氧催化技术影响因素的研究
2.2.1 初始pH值对电-多相臭氧催化技术的影响 研究结果表明,在碱性条件下(如金刚烷胺原水pH=12.5),电-多相臭氧催化技术对COD的去除效能明显优于酸性和中性条件,如图5(a)所示.经过30min反应,pH=12.5时,电-多相臭氧催化技术获得的COD去除率为52%,分别是pH=7.0(15%)和pH=5.0(9%)的3.5倍和5.8倍;并且电-多相臭氧催化技术在不同pH值条件下对COD的去除速率符合伪一级反应动力学特征(图5(b)),碱性条件下的速率常数远远大于酸性条件下的速率常数;在电-多相臭氧催化反应体系中,pH=12.5=7.3×10-1min-1分别是pH=7=1.6×10-1min-1和pH=5=9×10-2min-1的4.6倍和8.1倍.因此,碱性条件下,电-多相臭氧催化技术能够高效、快速地去除金刚烷胺制药废水中的COD.
更值得关注的是,在碱性条件下(如pH=12.5),电-多相臭氧催化体系也有效地提高了臭氧利用率,如图6所示,使电-多相臭氧催化体系能够更加高效地利用臭氧,该实验效果与曾萍等[1]研究结果相同.在pH=12.5和pH=11.0时,电-多相臭氧催化体系中O3利用率达到85%,远远高于pH=7.0和pH=5.0时的37%和25%.这主要是因为在酸性条件下,反应体系中的H+与·OH反应生成水,如反应式(1),消耗了反应系中的·OH,使得COD去除率较低;同时在碱性条件下,可能会促进液相臭氧与OH-的链式反应[13],如式(2)和(3),进而促进·OH的产生,同时pH值越高,OH-浓度越大,对臭氧的利用率越大.
H++ ·OH → H2O (2)
O3+ OH-→ HO2-(3)
HO2-+O3→ ·OH + OH-(4)

图5 不同pH值条件下电-多相臭氧催化技术去除COD的对比
(a) COD去除率的比较;(b)伪一级反应曲线;(c)反应过程中pH值的变化
如图5(c)所示,在电-多相臭氧催化氧化体系中,不同初始pH值情况下去除TOC和COD的过程中,pH值不随时间的变化而发生改变,这可能是因为随着反应的进行,金刚烷胺制药废水中部分物质或是中间产物之间形成缓冲体系,使废水pH值没有明显变化,这与李兆欣等[14]研究结果有一定的差异,可能是因为处理水质的差异.

图6 电-臭氧催化技术体系中对O3的利用率随初始pH值变化的曲线

图7 电-多相臭氧催化技术随O3浓度变化对COD的去除率的影响
2.2.2 气相O3浓度对电-多相臭氧催化技术的影响 如图7所示,研究结果表明,在电-多相臭氧催化体系中,气相O3浓度显著地影响金刚烷胺废水中COD的去除效率.经过30min反应,O3浓度为60mg/L时对COD的去除效率达到60.9%,分别是O3浓度为40mg/L(39.7%)和20mg/L(11.1%)的1.5倍和3.0倍,极大地提高了金刚烷胺制药废水中COD的去除率.主要是因为负载TiO2纳米花结构的阳极表面有大量空穴,能够与大量O3分子相互作用并进一步引发O3链式反应,提升·OH的产率;并且高浓度的O3可以有效地促进臭氧分子从气相向液相地传递,可能促进电催化过程中H2O2的产生[15],进一步促进H2O2与O3分子之间的反应,产生更多的·OH,使得废水中的有机污染物和无机还原性物质更迅速的被氧化.

图8 不同电流密度对电-多相臭氧催化技术去除COD的的影响
(a) COD去除率的比较;(b)伪一级反应曲线
2.2.3 电流密度对电-多相臭氧催化体系的影响 研究结果表明,在电-多相臭氧催化体系中,较大的电流密度能够高效、快速地去除金刚烷胺废水中的COD,如图8(a)所示.经过60min反应,电流密度为15mA/cm2时对COD的去除效率是61%,明显优于电流密度10mA/cm2(47.6%)和5mA/cm2(43%);更值得注意的是,经过30min反应后,电流密度为15mA/cm2的反应速率常数为15=7.3×10-1min-1,分别是电流密度为10mA/cm2(10=4.05×10-1min-1)的1.8倍和5mA/cm2(5=2.87×10-1min-1)的2.5倍,电流密度的增加可以有效地提高电-多相臭氧催化体系对COD的降解速率(图8(b)).主要是因为电流密度增大,可以增加TiO2表面的正电空穴[16-18],产生更多的活性位点,能够高效、快速地与O3分子相互作用引发O3链式反应产生羟基自由基(·OH).并且可能是因为增加电流密度,可以增加H2O2在阳极的产生速率[18],从而能够较多的与O3反应生成∙OH,更加有效快速地降解溶液中的COD[19-20],此研究效果与袁石等[21]研究结果相似.
3 结论
3.1 电-多相臭氧催化技术处理金刚烷胺制药废水是可行的,且电-多相臭氧催化技术不仅能够快速高效地去除金刚烷胺废水中COD(62%)和TOC(44%),并且有效地提高废水中的BOD5/COD值(提高104倍),为后续的生物处理提供优异的条件.
3.2 金刚烷胺废水的pH值显著影响COD的去除效率;在原水pH值(pH=12.5)条件下,电-多相臭氧催化技术能够高效快速地去除金刚烷胺制药废水中的COD,去除效率为62%,因此本文研究的金刚烷胺废水无需添加任何化学药剂.
3.3 气相臭氧浓度和电流密度显著影响电-多相臭氧催化技术对COD的去除效率,在臭氧浓度为60mg/L和电流密度为15mA/cm2时,对COD的去除效率分别是62%和61%.
[1] 曾 萍,宋永会, Dresely,等,金刚烷胺模拟废水Fenton氧化及其中间产物分析[J]. 环境工程技术学报, 2011,1(6):455-459.
[2] 宋永会,魏 健,马印臣,等,金刚烷胺制药胺化废水与溴化废水的中和络合萃取处理[J]. 中国环境科学, 2014,34(10):2522-2527.
[3] 樊 杰,金刚烷胺制药废水Fenton-超声氧化处理及溴化氢双极膜电渗析回收[D]. 北京:北京林业大学, 2013.
[4] Bobu M, Yediler A, Siminiceanu I, et al, Comparison of different advanced oxidation processes for the degradation of two fluoroquinolone antibiotics in aqueous solutions, Journal of environmental science and health [J]. Part A, Toxic/hazardous substances & environmental engineering, 2002,36(4):1034-1042.
[5] 宋永会,魏 健,马印臣,等.络合萃取法处理金刚烷胺制药废水[J]. 环境科学研究, 2014,27(12):1513-1518.
[6] 曾 萍,宋永会,樊 杰,等,超声、Fenton及其联合工艺预处理金刚烷胺制药废水效果对比[C]//北京:中国环境科学学会学术年会论文A集, 2014:4492-4496.
[7] Wang Y J, Li X Y, Zhen L M, et al. Electro-Fenton treatment of concentrates generated in nanofiltration of biologically pretreated landfill leachate [J]. Journal of Hazardous Materials, 2012,115(3):229- 230.
[8] 刘永泽,高级氧化过程中OH×和SO4-定量分析及溴代副产物生成规律研究[D]. 哈尔滨:哈尔滨工业大学, 2015.
[9] Li X Y, Liu G C , Shi M, et al, A novel electro-catalytic ozonation process for treating Rhodamine B using mesoflower-structured TiO2-coated porous titanium gas diffuser anode [J]. Water Science and Technology, 2016,165(1):154-159.
[10] 倪金雷.不同物相TiO2催化臭氧(/H2O2)体系的氧化效能[D]. 浙江:浙江工业大学, 2015.
[11] Li X Y, Sun S B, Zhang X, et al,Combined electro-catazone/electro- peroxone process for rapid and effective Rhodamine B degradation [J]. Separation and Purification Technology, 2017,178:189–192.
[12] Li X Y, Liu G C, Shi M, et al. Using TiO2Mesoflower Interlayer in Tubular Porous Titanium Membranes for Enhanced Electrocatalytic Filtratio [J]. Electrochimica Acta, 2016,218:318–324.
[13] Chemlal R, Azzouz L, Kernani R, et al. Combination of advanced oxidation and biological processes for the landfill leachate treatment [J]. Ecological Engineering, 2014,73:281-289.
[14] 李兆欣,甄丽敏,李新洋,等.BDD电极阳极氧化垃圾渗滤液纳滤浓缩液[J]. 环境工程学报, 2014,8(11):4662-4668.
[15] Wang H J, Yuan S, Zhan J H, et al. Mechanisms of enhanced total organic carbon elimination from oxalic acid solutions by electro- peroxone process [J]. Water Research, 2015,80:20-29.
[16] Komtchou S, Dirany A, Drogui P, et al, Removal of atrazine and its by-products from water using electrochemical advanced oxidation processes [J]. Water Research, 2017,125:91-103.
[17] Oulego P, Collado S, Laca A, et al. Impact of leachate composition on the advanced oxidation treatment [J]. Water Research, 2016,88:389- 402.
[18] Li X Y, Zhu W, Wang C G, et al. The electrochemical oxidation of biologically treated citric acid wastewater in a continuous-flow three- dimensional electrode reactor (CTDER) [J]. Chemical Engineering Journal, 2013,232(10):495–502.
[19] Kishimoto N, Sugimura E, Feasibility of an electrochemically assisted Fenton method using Fe2+/HOCl system as an advanced oxidation process [J]. Water Science and Technology, 2010,62(10):2321-2329.
[20] Yao W K, Wang X F, Yang H G, et al, Removal of pharmaceuticals from secondary effluents by an electroperoxone process [J]. Water Research 2015,88:826-83.
[21] 袁 实.电催化臭氧水处理技术的开发和研究 [D]. 北京:清华大学, 2014.
致谢:本实验的现场采样工作金煤化工水处理公司的员工协助完成,在此表示感谢.
Study on electrochemical heterogeneous catalytic ozonation process for treatment of amantadine pharmaceutical wastewater,
MA Fu-jun1, LI Xin-yang1*, ZONG Bo-yang2, YU Xiao-hua1, SUN Shao-bin,1YAO Hong1*
(1.School of Civil Engineering and Architecture, Beijing Jiaotong University, Beijing 100044, China;2.College of Environmental Science and Engineering, Tongji University, Shanghai 314051, China)., 2018,38(10):3713~3719
Electrochemical heterogeneous catalytic ozonation (E-catazone) process was studied for treating amantadine wastewater, which was of high COD, high salinity and nonbiodegradable. The amantadine removal efficiency of E-catazone process was compared with catalytic ozonation (Catazone) and electrochemical oxidation (EO) processes, Besides, the effects of current density, pH and ozone concentration on the amahadine treatment efficiency were further investigated to obtain optimized experimental conditions. Electro-catalytic ozonation obtained 62% of the COD removal efficiency and 44% removal of TOC under pH 12.5, current density 15mA/cm2, O3flow rate 0.4L/min and O3concentration 60mg/L, The performance was significantly better than that of Catazone (COD 44%, TOC 29%) and EO (COD 13%, TOC 17%), E-catazone process demonstrated strong oxidizing power and fast oxidation rate, and the pseudo-first order of COD removal rate constantwas 1.81times and 8.22times of Catazone and EO, More importantly, the E-catazone could improve the biochemical properties of wastewater efficiently and rapidly, and increased by about two order of magnitude. The results showed that the E-catazone was a potential advanced oxidation technology, which could realize high efficiency, fast removal of organic pollutants and improve the biodegradability of wastewater.
amantadine;pharmaceutical wastewater;electrochemical heterogeneous catalytic ozonation;titanium dioxide
X505
A
1000-6923(2018)10-3713-07
马富军(1994-),男,宁夏固原人,北京交通大学硕士研究生,主要从事高级氧化降解污染物研究.
2018-03-19
中央基本科研业务费(2017JBM342;2016JBZ008);中国铁路总公司科技研究开发计划重点课题(2017Z003-F)
* 责任作者, 姚宏, 教授, yaohongts@163,com; 李新洋, 讲师, lixinyang928@163,com

