氢氧化镁铝改良滨海盐碱土机理与效果研究
田 露,赵 林,杨永奎,乔 治
(天津大学环境科学与工程学院,天津 300072)
土地盐渍化是由自然环境和人类活动引起的盐分在土壤表层积聚的一种环境问题,目前所采用的改良措施有物理、化学和生物三类,物理措施基础投资大、成本高,化学措施易引入其他污染物而造成二次污染,生物措施对技术要求高、见效慢[1-2]。总体来说大都没有从土壤的微观层面研究脱盐改良,忽视土壤自身特性,不能解决根本性问题。盐碱土中盐分离子主要有两种存在形式,一种是存在于土壤溶液中的游离态,另一种是靠静电作用吸附在土壤胶体上的可交换态,可交换态离子很难淋洗脱除,其中交换性Na是造成盐碱土理化性质恶劣的主要危害离子,它使得土壤遇水泥泞膨胀、孔隙度低、透水性差[3]。可交换性离子与土壤胶体带电性能及其所形成的双电层有关,土壤胶体表面负电荷数越多,所能吸附的交换性离子量越大。
双电层的扩散层重叠是指在同一体系中正、负电荷的胶体颗粒由于静电引力相互靠近而导致二者的扩散层发生部分重叠的现象[4]。关于土壤双电层间的相互作用,30多年前就曾有欧美土壤学家提出高度风化的可变电荷土壤中带相反电荷胶体颗粒的扩散双电层可能相互重叠;近年来随着对可变电荷土壤研究增多,Qafoku和Sumner[5]提出可变电荷土壤中带相反电荷胶体颗粒表面双电层重叠的假说解释了美国老成土淋溶实验;随后,徐仁扣等[6-9]在土壤或黏土矿物与Fe/Al氧化物的混合体系中也观察到了类似的现象并对此进行了进一步研究。研究表明[6-9]正负电荷胶体双电层间的扩散层重叠能降低土壤表面有效负电荷,从而有利于Na+、Mg+、Ca2+等交换态阳离子从土壤上解吸,并且其解吸量随着Fe/Al氧化物添加量增加而增加。
类水滑石化合物氢氧化镁铝(MAH)是由正电荷金属氢氧化物层和层间负电荷阴离子构成的层状双金属氢氧化物,其正电荷来源于Mg2+和Al3+同晶置换作用[10-11]。本文利用正电荷MAH和负电荷盐碱土胶体间的扩散层重叠降低土壤胶体对盐分离子的吸附,进而实现盐碱土的脱盐改良。以天津滨海盐碱土为研究对象,研究MAH与盐碱土胶体间的扩散层重叠现象和MAH改良盐碱土的效果,并从5种不同镁铝摩尔比的MAH中筛选出最佳材料及用量,从土壤微观层面为盐碱土脱盐改良提供新的思路和理论依据。
1 材料和方法
1.1 供试土壤
土样于2016年11月19日取自天津中新生态城(117°45′40″E,39°7′55″N)。天津滨海地区属于海退地和吹填造陆区,土壤和潜水原生含盐量较高,地势低平,地下水位埋深浅,在半干旱气候条件下土壤中的水分蒸发强烈,盐分大量向土壤表层积聚,土壤盐渍化现象普遍发生,其中盐分主要为NaCl。土样采集0~20 cm的表层土壤,为棕色黏壤质土壤,将其置于室内通风处风干一周,然后碾碎混匀后过2 mm标准筛。供试土样基本理化性质见表1,分析方法参照《土壤农化分析》[12]。
1.2 实验方法
1.2.1 MAH胶体的制备与表征
本文使用的MAH是用氯化镁、氯化铝和氨水在一定的制备条件[13-14]下通过共沉淀方法制得。制备方法:将一定比例的氯化镁和氯化铝混合溶于超纯水,在搅拌同时加入稀释3倍的浓氨水,直至无新沉淀产生为止,继续缓慢搅拌2 h,随后胶溶9 h后离心洗涤数次,最后真空干燥、保存备用。按照不同镁铝摩尔比制备 5 种 MAH,Mg∶Al分别为 3∶1(MAH-1)、2∶1(MAH-2)、1∶1(MAH-3)、1∶2(MAH-4)和 1∶3(MAH-5)。对其进行扫描电镜图(SEM)和X射线衍射(XRD)分析,测定其粒径、pH和不同pH下MAH悬浮液的Zeta电位进行表征。
1.2.2 MAH胶体与土壤胶体扩散层重叠实验
本实验采用离心法[15]提取盐碱土胶体,以MAH-1为例研究盐碱土和MAH胶体间的扩散层重叠现象。将MAH-1胶体分散在0.1 mmol·L-1的NaCl溶液中,保持溶液中土壤胶体的浓度为0.25 g·L-1,分别按盐碱土胶体∶MAH-1为10∶5、10∶3和10∶1加入MAH-1,超声分散1 h,再将其混合悬浮液的pH调节至3~10,测定其Zeta电位。
1.2.3 不同MAH配比下盐碱土盐分溶出实验
在50 mL离心管中加入1 g土样,按照目前滨海盐碱土改良使用广泛的石膏添加量范围设置添加量梯度[3],按0、10、25、50、75、100 mg·g-1添加MAH,并加入25 mL超纯水混合均匀,25℃恒温振荡2 h,最后8500 r·min-1离心15 min测其上部水溶液的pH、主要阴阳离子浓度(Na+、K+、Ca2+、Mg2+、Cl-、SO2-4、HCO-3和CO2-3)以及TP、TN,土壤溶液含盐量采用主要阴阳离子的加和,每个处理进行3个平行实验。

表1 供试土壤基本理化性质Table 1 Basic physical and chemical properties of experimental soil
1.3 分析方法
MAH的粒径和Zeta电位使用纳米粒度及Zeta电位仪测定,使用场发射扫描电子显微镜和X射线粉末衍射仪对MAH进行SEM和XRD表征。土壤溶液pH使用pH计测定,土壤溶液过0.45 μm滤膜后使用ICP-OES测定溶液中Na+、K+、Ca2+和Mg2+浓度,离子色谱测定Cl-和浓度,滴定法测定和浓度,分光光度计测定TP和TN。
1.4 数据处理
采用Microsoft Excel 2016、Origin 2016软件对数据进行整理分析并作图。
2 结果与讨论
2.1 MAH胶体基本特性
表2为5种不同镁铝摩尔比的MAH胶体的粒径和pH。从中可以看出,5种MAH的粒径较小(大都在100~200 nm),其中MAH-1的粒径最大,这与王松林等[16]的研究结果一致,MAH-1更接近自然界水滑石的镁铝摩尔比例,结构比较稳定。由于镁铝摩尔比不同,5种MAH的pH存在差异,MAH-1、MAH-2和MAH-3显碱性,MAH-4和MAH-5显酸性,其酸碱性主要与镁氢氧化物的碱性和铝氢氧化物的酸性有关。
图1和图2分别为MAH-1的SEM图和XRD图,从图1可以观察出MAH-1微观形貌,大体呈六边形片状结构。图2的XRD图可以看出,样品具有水滑石的典型结构,低角度的衍射峰比较尖锐,高角度的衍射峰较弱[17],表现出明显层状结构特征,图谱基线低且平稳,主要衍射峰尖而窄,基本没有杂峰存在,说明产物纯度与结晶度高。
2.2 pH对MAH胶体Zeta电位的影响
5种MAH是正电荷胶体,其正电性不随pH变化,但其所带正电荷数量却会受pH影响。由图3可知,pH在3~10的变化范围内MAH的Zeta电位一直是正值,这就验证其正电性来源于Mg2+被Al3+同晶替换的作用。但图3中MAH的Zeta电位却随pH升高总体呈现先下降、再上升、最后下降的趋势。
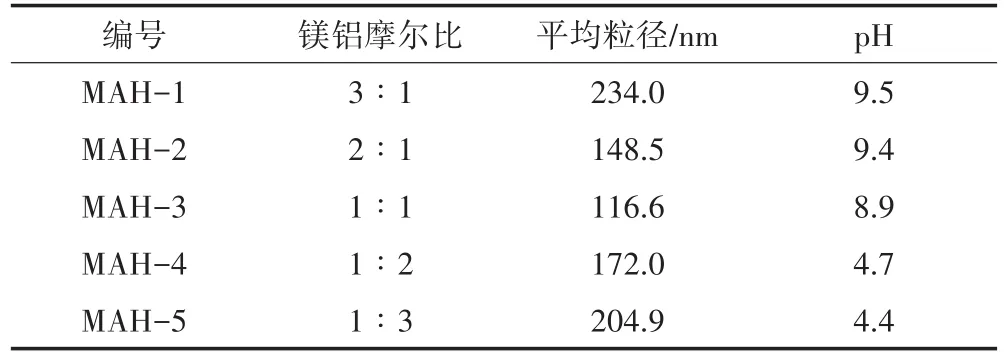
表2 氢氧化镁铝胶体的粒径和pHTable 2 Particle size and pH of magnesium aluminum hydroxide colloids

图1 氢氧化镁铝胶体的SEM图(×100 000倍)Figure 1 Scanning electron microscopy(SEM)of magnesium aluminum hydroxide colloids(×100 000 times)
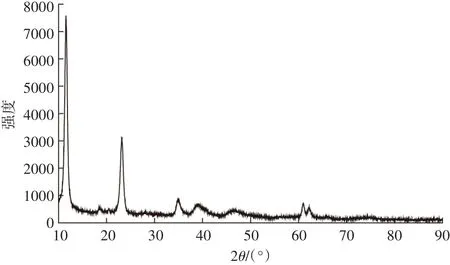
图2 氢氧化镁铝胶体的XRD图Figure 2 X-ray diffraction(XRD)of magnesium aluminum hydroxide colloids
MAH的Zeta电位变化趋势主要与MAH中Mg和Al存在形态有关。较低pH下MAH发生酸性水解,OH-被部分中和,部分镁铝以聚阳离子形式存在,正电荷增加,Zeta电位较高;随着pH升高,MAH水解减少,正电荷相应减少,Zeta电位呈下降趋势;随着pH升高至碱性,溶液中OH-增加,部分氢氧化铝先从MAH中释放,MAH中镁铝比例增大,Zeta电位升高,5种MAH在pH为7~8时Zeta电位升高至峰值;随着pH 进一步上升(pH>8),过多 OH-使 Al(OH)3变成Al(OH)-4,Zeta电位反而降低[16]。因此,pH 是影响MAH胶体Zeta电位的一个重要因素,并且MAH较高的Zeta电位出现在pH为3和7~8左右。
2.3 MAH胶体与土壤胶体的扩散层重叠现象
Zeta电位与胶体颗粒表面电荷状况密切相关,其数值和正负性决定于胶体颗粒的表面电荷状况[9],Ze⁃ta电位与胶体颗粒表面电荷的正负性一致,Zeta电位绝对值大小与胶体颗粒表面电荷多少一致。因此本文以其作为研究MAH和盐碱土胶体扩散层重叠的指标,表征土壤胶体表面电荷的情况。
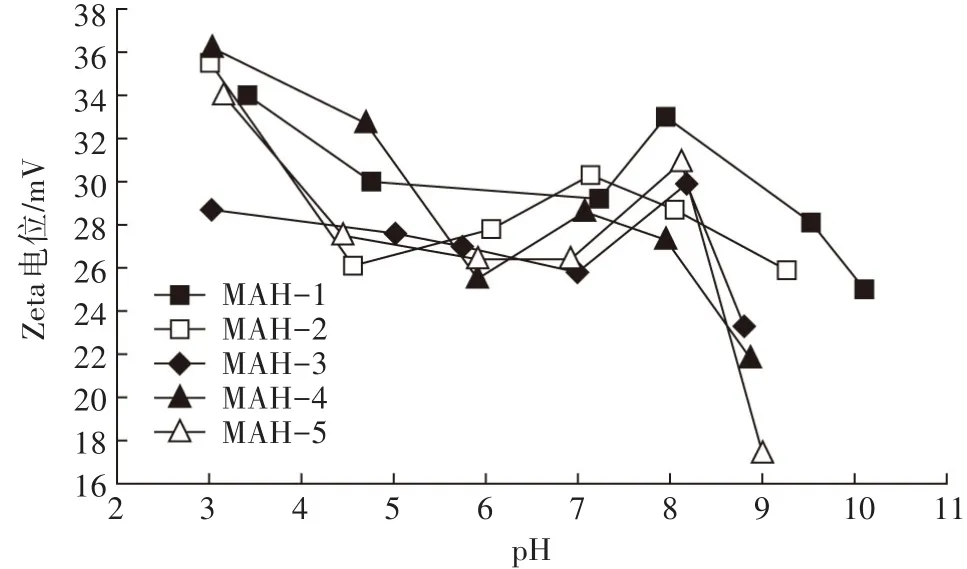
图3 pH对MAH的Zeta电位的影响Figure 3 Effect of pH on Zeta potential of MAH
图4 是以MAH-1为例研究混合体系pH及MAH-1添加量对土壤和MAH胶体间扩散层重叠现象的影响。在所研究的pH范围内单一体系盐碱土胶体的Zeta电位为负值,其Zeta电位随pH升高向负值方向移动,碱性土壤环境对盐基离子吸附力更强,这就解释了盐碱土含盐量高的问题。盐碱土和MAH-1胶体混合体系的Zeta电位随pH升高也存在相似现象。混合体系的Zeta电位相对于盐碱土单一体系向正值方向移动,这就验证了盐碱土和MAH-1胶体间的扩散层重叠现象,混合体系中带负电荷的盐碱土和带正电荷的MAH-1胶体颗粒由于静电吸引相互靠近,二者扩散层发生部分重叠使得盐碱土胶体表面的有效负电荷密度降低。随着混合体系中MAH-1含量增加,Zeta电位向正值方向移动的幅度增大,双电层相互作用程度增加,盐碱土胶体上有效负电荷密度降低程度增大。
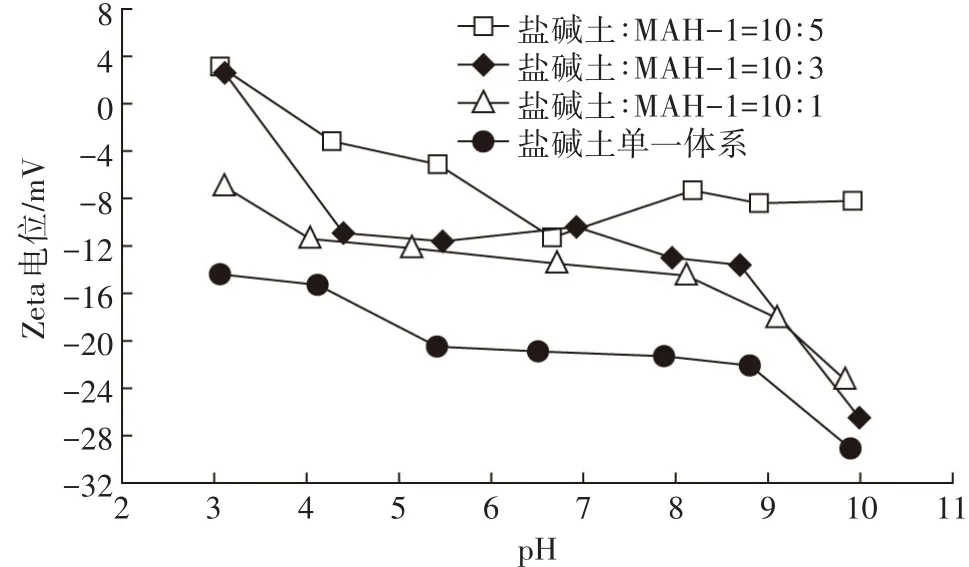
图4不同pH下盐碱土单一体系及土壤和MAH-1胶体混合体系的Zeta电位Figure 4 Zeta potential of single system of saline-alkali soil and mixed system containing soil and MAH-1 in different pH
图4 中混合体系在碱性环境中Zeta电位相对于盐碱土胶体单一体系向正值方向有所提升,尤其当盐碱土∶MAH-1达到10∶5时,在pH>7时Zeta电位随pH增加趋于平缓。这是区别于徐仁扣等[6-9]在土壤或黏土矿物与Fe/Al氧化物的混合体系中所观察到的结果,在他们的研究中,当pH>8时混合体系Zeta电位向土壤或粘土矿物单一体系趋近,几乎没有提升。这主要与MAH和Fe/Al氧化物所带电荷的来源有关,MAH正电荷来源于同晶替换作用,是一种永久正电荷[10-11];而Fe/Al氧化物表面电荷来自羟基的质子化作用,会受到介质pH的影响[9,18],在偏碱性环境中解离出H+而带负电荷使得扩散层重叠现象减弱甚至消失。
由以上分析可知,利用负电荷盐碱土胶体和正电荷MAH胶体双电层的扩散层重叠现象可以降低土壤胶体表面有效电荷密度,从而降低土壤对盐基阳离子的吸附能力,在该研究中MAH能在碱性环境中很好地发挥扩散层重叠作用,进而能够实现盐碱土的脱盐改良,并且MAH是一种类水滑石化合物,能够在自然环境中稳定存在,二次污染风险较低。
2.4 MAH种类及其添加量对盐碱土脱盐改良效果的影响
2.4.1 MAH对土壤溶液pH和含盐量的影响
土壤pH值是盐碱土酸碱度指标,是盐碱土基本性质和肥力的重要影响因素,影响盐碱土中养分存在状态、转化及有效性,进而影响植物生长[19]。土壤全盐量是盐碱土的另一个重要指标,是影响植物生长的一个主要障碍因素[20]。因此,pH值是改良盐碱土的重要参考指标,而改良盐碱土的重点就是降低土壤盐分。
图5和图6分别是MAH种类及添加量对盐碱土溶液pH值及含盐量的影响情况,间接说明MAH对盐碱土的脱盐改良效果。由图5可见,5种MAH的加入都有利于降低土壤溶液的pH,并且随着MAH添加量的增加土壤溶液的pH逐渐下降。在添加量范围内3种碱性MAH-1、MAH-2和MAH-3使得土壤溶液pH降低了0.3,2种酸性MAH-4和MAH-5使得土壤溶液pH降低了1.6,2种酸性MAH对土壤溶液pH的改善效果更加显著,说明MAH的pH是改良盐碱土pH的重要因素。从图6中可知,随着MAH的添加,土壤溶液的含盐量接近于线性增加,说明从土壤中脱出的盐分随着MAH的添加而增加。5种MAH中2种酸性MAH的脱盐效果优于3种碱性MAH,而2种酸性MAH中酸性稍强的MAH-5脱盐效果最佳,尤其在添加量为10 mg·g-1时MAH-5的脱盐效果明显优于其他4种,在最大添加量100 mg·g-1下加入MAH-5土样的脱盐量是原土样的1.7倍。
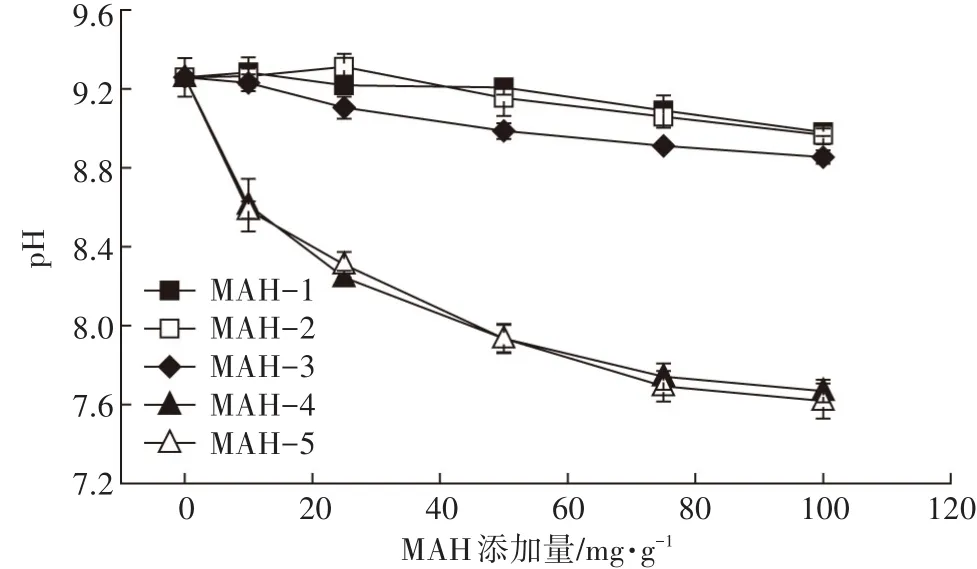
图5 MAH种类及添加量对土壤溶液pH的影响Figure 5 Effect of type and additive amount of MAH on pH of soil solution
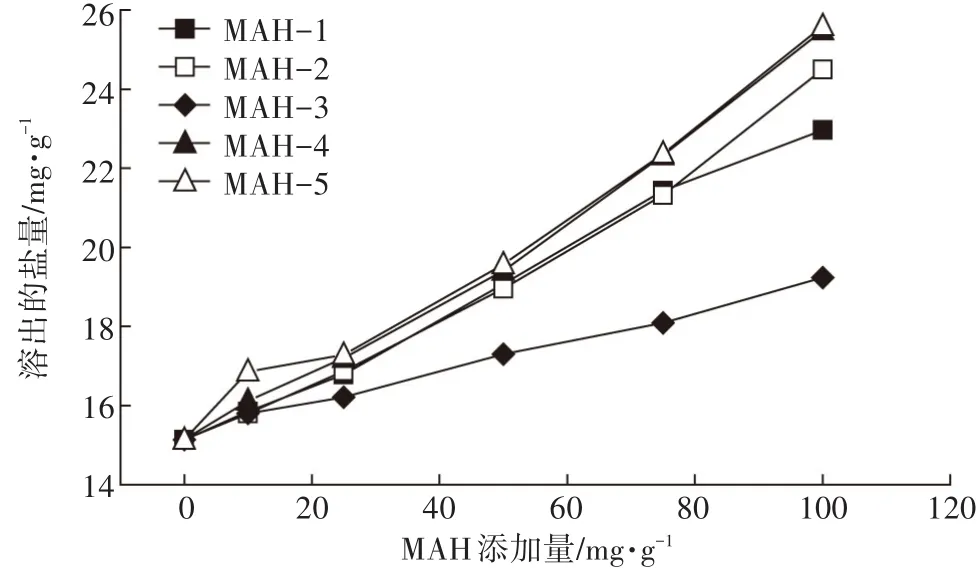
图6 MAH种类及添加量对土壤溶液含盐量的影响Figure 6 Effect of type and additive amount of MAH on salt content of soil solution
加入MAH后,MAH与盐碱土胶体产生扩散层重叠,使得盐碱土壤胶体表面的有效负电荷密度降低,对正电荷离子的吸附能力下降,盐基阳离子发生解吸,产生交换性H+和交换性Al3+以平衡土壤颗粒表面的负电荷,这就解释了土壤溶液pH下降、含盐量增加的原因。综上分析,5种MAH中酸性最强的MAH-5对滨海盐碱土的脱盐改良效果最佳。
2.4.2 MAH-5的添加对土壤溶液中主要阳离子及养分N、P的影响
由图7可知,随着MAH-5添加量的增加,K+脱出量几乎保持不变;Mg2+脱出量的变化幅度不大,在最大添加量下 Mg2+脱出量提升了 0.3 mg·g-1;Ca2+脱出量呈线性增加,在最大添加量下Ca2+脱出量提升了3.8 mg·g-1;Na+脱出量在MAH-5添加量为10 mg·g-1下就能达到最大,并且随MAH-5添加量的增加没有显著变化。加入MAH-5的盐碱土中大量Ca2+脱出除了交换性Ca,还有随盐碱土pH降低而溶出的难溶性钙盐;而盐碱土中多溶出的Na大都是交换性Na,在MAH-5添加量为10 mg·g-1下溶出444×10-3mg·g-1,盐碱土胶体上交换性Na的脱除率达到65%。
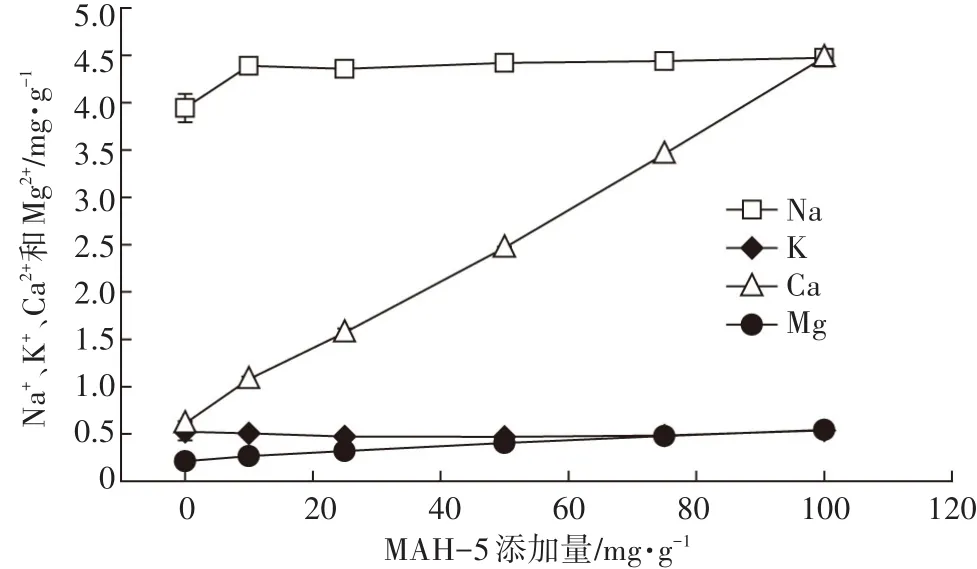
图 7 MAH-5添加量对盐碱土溶出Na+、K+、Ca2+、Mg2+含量的影响Figure 7 Effect of additive amount of MAH-5 on Na+,K+,Ca2+and Mg2+content dissolved from saline-alkali soil
图8 是盐碱土中养分N、P的脱出情况,随着MAH-5的添加,P的脱出量几乎没有变化,脱出量在2.3×10-3mg·g-1左右,相对于盐碱土的全P含量401.1×10-3mg·g-1来说可以忽略;而N的脱出量随着MAH-5添加显著增加,在最大添加量下N的脱出量可以达到62×10-3mg·g-1,这可能与盐碱土中氨氮的脱出有关,MAH-5与盐碱土胶体产生扩散层重叠,使得NH+4发生解吸。
在确定最佳用量时,Na+的脱出情况应该成为首要考虑的因素,再结合Ca2+和养分N的脱出趋势,综合考虑以上因素,确定MAH-5最佳用量为10 mg·g-1,即按1%添加MAH-5。
3 结论
(1)pH值是影响MAH的Zeta电位的重要因素,随着pH上升,MAH的Zeta电位呈现先下降、再上升、最后下降的趋势,pH值通过影响MAH中Mg和Al的存在形态从而影响MAH的Zeta电位。

图8 MAH-5添加量对盐碱土溶出的养分N、P的影响Figure 8 Effect of additive amount of MAH-5 on nutrient N and P dissolved from saline-alkali soil
(2)MAH和盐碱土胶体间存在扩散层重叠现象,二者扩散层重叠程度随着MAH添加量的增加而增大,随着pH值的升高而减弱。所研究的扩散层重叠现象在碱性环境中存在,说明MAH可通过降低盐碱土对盐分离子的吸附进而实现盐碱土脱盐改良。
(3)MAH的添加能够降低盐碱土的pH和含盐量,5种MAH中酸性MAH对盐碱土的pH和脱盐改良效果优于碱性MAH,酸性最强的MAH-5改良效果最佳,综合分析筛选出的最佳脱盐改良方案为按1%添加MAH-5,在此方案下对盐碱土中交换性Na脱除率达到65%。

