酞菁化合物合成及光谱性能研究
许 浩,刘 珩
(陆军工程大学,江苏 南京 210007)
1 引 言
高、超光谱成像技术结合遥感技术和测谱技术的优势,已具备从卫星和飞机平台上探测目标光谱细节的能力,对现有伪装和隐身技术是空前的挑战[1]。传统绿色伪装颜料或涂料可仿造植物的颜色,却模拟不了植物的光谱特性,不能满足先进光学侦察下的隐身要求。绿色植物的叶绿素卟啉结构,使其在光学和近红外波段具有显著的光谱特征:波长550 nm处的光谱反射峰,波长670 nm附近的光谱吸收峰以及680~780 nm范围反射率陡升[2]。酞菁与卟啉结构很相似,可看成是卟啉分子中四个吡咯环外围并四个苯环形成的,其光谱曲线基本形状与植物相似,苯环结构导致酞菁吸收峰较植物产生了100 nm左右的红移。
酞菁具有很强的配位能力,中心及周边位置可进行金属离子[3]、取代基团[4-5]置换或取代,分子结构变化导致前线分子轨道(HOMO-LUMO)能级改变[6],形成光谱性能可调的酞菁化合物[7-8]。在有机染(颜)料、太阳能电池材料等领域具有重要的应用和潜在应用价值[9-12]。
酞菁合成一般以金属离子为模板,酞菁分子碎片(邻苯二甲腈等)在一定的反应条件下环绕模板形成具有特定性能的酞菁化合物[13-14]大连理工大学夏道成通过该方法合成了1,11,15,25-四羟基-4,8,18,22-二(桥联二丙羧基)酞菁铜并表征其紫外-可见光谱[15];东华大学陈大俊合成了不同的八羧基金属酞菁染料,并研究其光谱响应范围、水溶性等性质[16]。二者均未涉及酞菁类染料拟合植物光谱的研究,且目前针对光学伪装需求的有机酞菁颜料合成及光谱性能研究未见报道。
本文根据能级跃迁公式ΔE=ћc/λ,ΔE、λ分别为轨道能级差和吸收波长,围绕峰值波长减小、轨道能级差增大为目标,设计以第四周期过渡金属为中心、α-NO2取代的单层平面结构。采用DBU催化合成法[17],利用自制装置合成酞菁化合物,探究最佳合成条件工艺和提纯方法,研究中心金属离子与聚集方式对酞菁化合物光谱性能的影响,合成与植物“同谱同色”的酞菁类颜料,为对抗高、超光谱成像侦察下目标伪装技术提供新方法和新材料。
2 实 验
2.1 合成原理
DBU催化法是指在加热条件下,以DBU(有机碱1,8-二氮杂双环[5,4,0]-7-十一烯)为催化剂,邻苯二甲腈与金属盐在有机溶剂中进行反应,分子碎片包围金属模板合成金属酞菁,该方法反应温度低,副产物少。本文以4-硝基邻苯二甲腈与金属氯盐在DMAC溶剂(二甲基乙酰胺)中进行反应制得α-四硝基金属酞菁(TNMPC),合成原理见图1。

图1 金属酞菁DBU催化合成原理示意图 Fig.1 A schematic diagram of DBU catalytic synthesis of metal phthalocyanine
2.2 仪器与试剂
电子天平、真空干燥箱、微量进推器、比色皿、集热式磁力搅拌器、柱层析装置、冷凝装置、紫外-可见光-近红外分光光度计,所用试剂见表1。
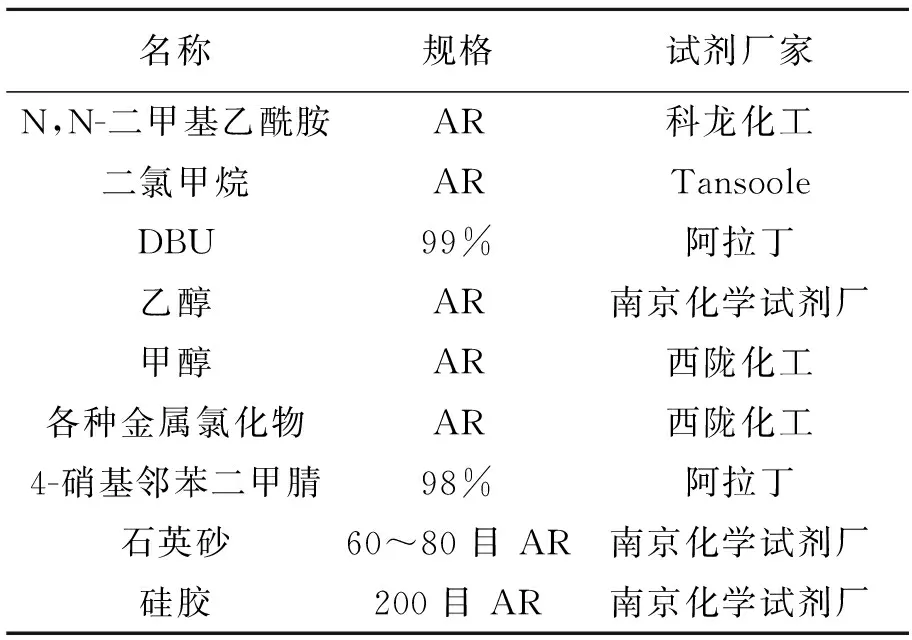
表1 原料剂表Tab.1 Ingredient list
2.3 合成与提纯
合成装置及合成工艺示意图如图2所示。称取4-硝基邻苯二甲腈 0.004 mol,金属氯化物0.001 mol,DMAC 5 mL(溶剂),倒入三口烧瓶常温搅拌充分溶解。将烧瓶置于铁架台,放入聚四氟乙烯磁子,插上冷凝管、温度计、塞口后移至集热式磁力搅拌器固定。根据金属离子及取代基不同,设定220~270 ℃恒温油浴加热。调整旋钮使磁子保持稳定旋转并以微量进推器向反应溶液注射催化剂DBU 0.075 mL,开始反应直至溶液彻底变色反应完全,记录反应时间。
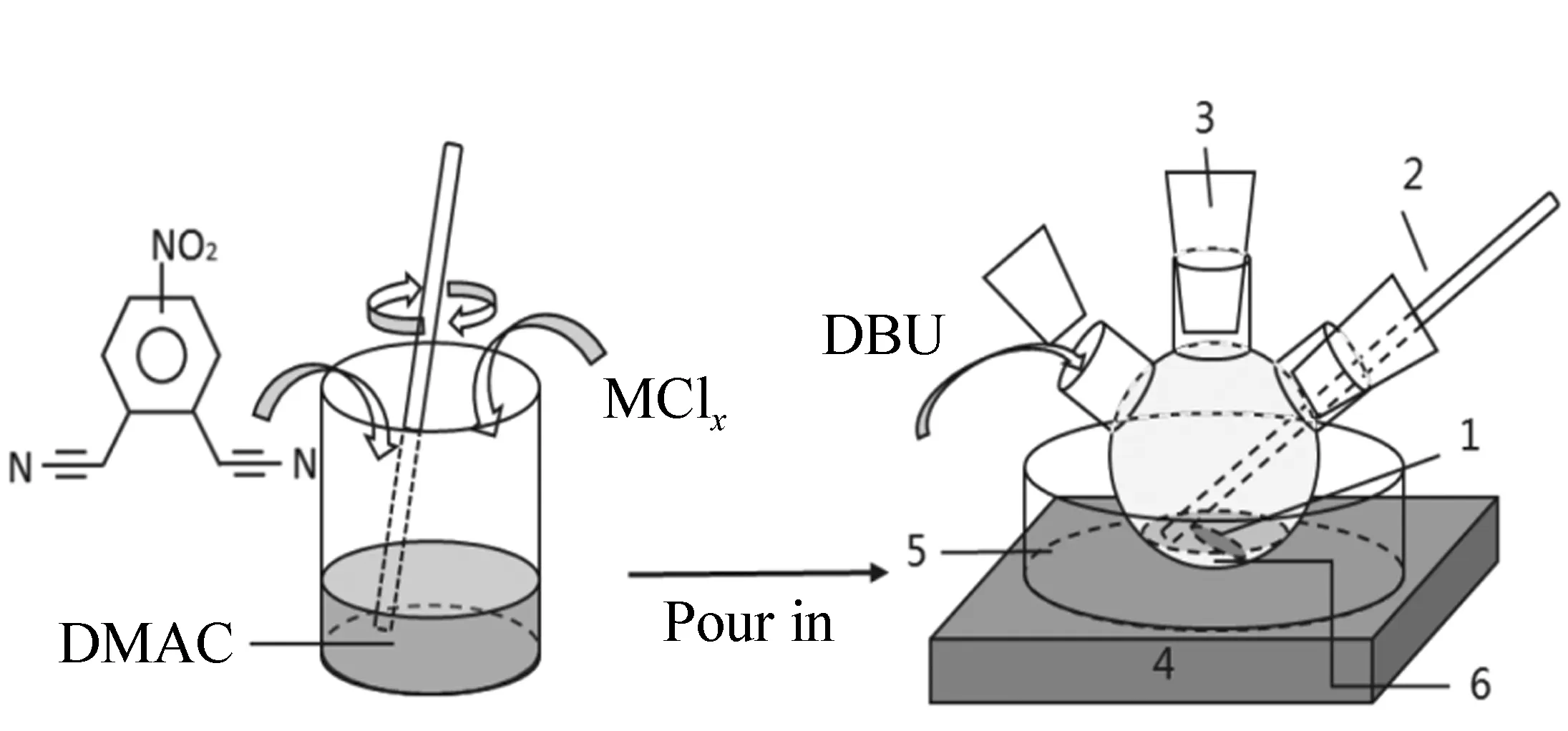
图2 自主设计合成装置及合成工艺示意图 (1.聚四氟乙烯磁子, 2.高温温度计, 3.冷凝管, 4.集热式磁力搅拌器, 5.甲基硅油油浴锅, 6.反应液) Fig.2 Schematic diagram of self-designed synthesis device and synthetic process(1.Teflon polyethylene magneton; 2.High temperature thermometer; 3.Condensing tube; 4.Heat magnetic mixer; 5.Methyl silicone oil bath wok; 6.Reaction liquid)
提纯过程示意图见图3。将反应液倒入烧杯再置于相同反应温度下的油浴中加热去除溶剂DMAC,直至不产生气泡为止。取出烧杯,常温冷却至样品呈固态,倒入乙醇搅拌、沉淀、倒去上层清液,反复直至上层清液为无色,将沉淀物置于阴凉处挥发干燥得到产物。

图3 提纯过程示意图 Fig.3 Schematic diagram of purification process
2.4 性能测试
(1)吸收光谱样品制备:取合成产物0.1 g溶入二氯甲烷制成浓溶液,将二氯甲烷、甲醇以固定比例(铁酞菁样品2∶1,其他样品4∶1)配制洗脱液,过层析柱取下层深色柱层。经溶解过滤蒸发,得到深色固体粉末样品。通过计算后,取0.000 1 mol样品溶于10 mL二氯甲烷,置于比色皿中,采用分光光度计进行吸收光谱测试。
(2)反射光谱样品制备:取过量样品溶于二氯甲烷得浓溶液,均匀涂布于滤纸,溶剂挥发后,采用分光光度计进行反射光谱测试。
(3)产物产率:0.001 mol金属酞菁的理论质量记为w1,提纯挥发后的产物质量记为w2,产率%=w2/w1×100%。
3 结果分析与讨论
3.1 合成条件对产物、产率的影响
本文基于DBU催化合成法,利用自行设计装置合成金属酞菁化合物,通过调控反应时间、温度进行大量对照实验,以产率为标准,探究各金属酞菁的最佳合成条件。
由于初始反应液颜色(浅黄至浅绿色)、中间产物颜色(血红至紫红色)、目标产物颜色(墨绿色至深蓝色)存在较大差异,故而实验初期反应液颜色可以用于判断合成程度。图4为在不同温度下各金属酞菁反应液彻底变色所需时间。从图中可看出,反应时间随反应温度升高而缩短直至稳定不变,除铁酞菁在270 ℃外,其余金属酞菁在240~250 ℃时反应时间达到最短。随着温度升高,分子活化能增加,有利于金属离子从氯化物中分离并与分子碎片形成更稳定的酞菁化合物,但温度继续升高,反应达到平衡,反应时间不再变化。

图4 不同中心金属的反应时间与反应温度 Fig.4 Reaction time and reaction temperature of different central metals
在最佳反应温度下各金属酞菁产率随时间的变化关系如图5所示。从图中可看出,在最佳反应温度下,产物产率先随反应时间增加而提高,一段时间后反应达到平衡,产率不再增加,除铁酞菁在50 min,其余金属酞菁在20~30 min内产率达到最高。本文金属离子均为第四周期过渡族元素,外层电子相同,不同的是内壳层电子数,决定化学反应和化学性能的恰是最外层电子,因此,达到最佳反应温度的反应时间及产物产率变化不大。铁酞菁的合成条件较其他金属酞菁反应条件苛刻的原因可能是由于三价铁与氯离子结合紧密,破坏原有的离子键需要能量较大。
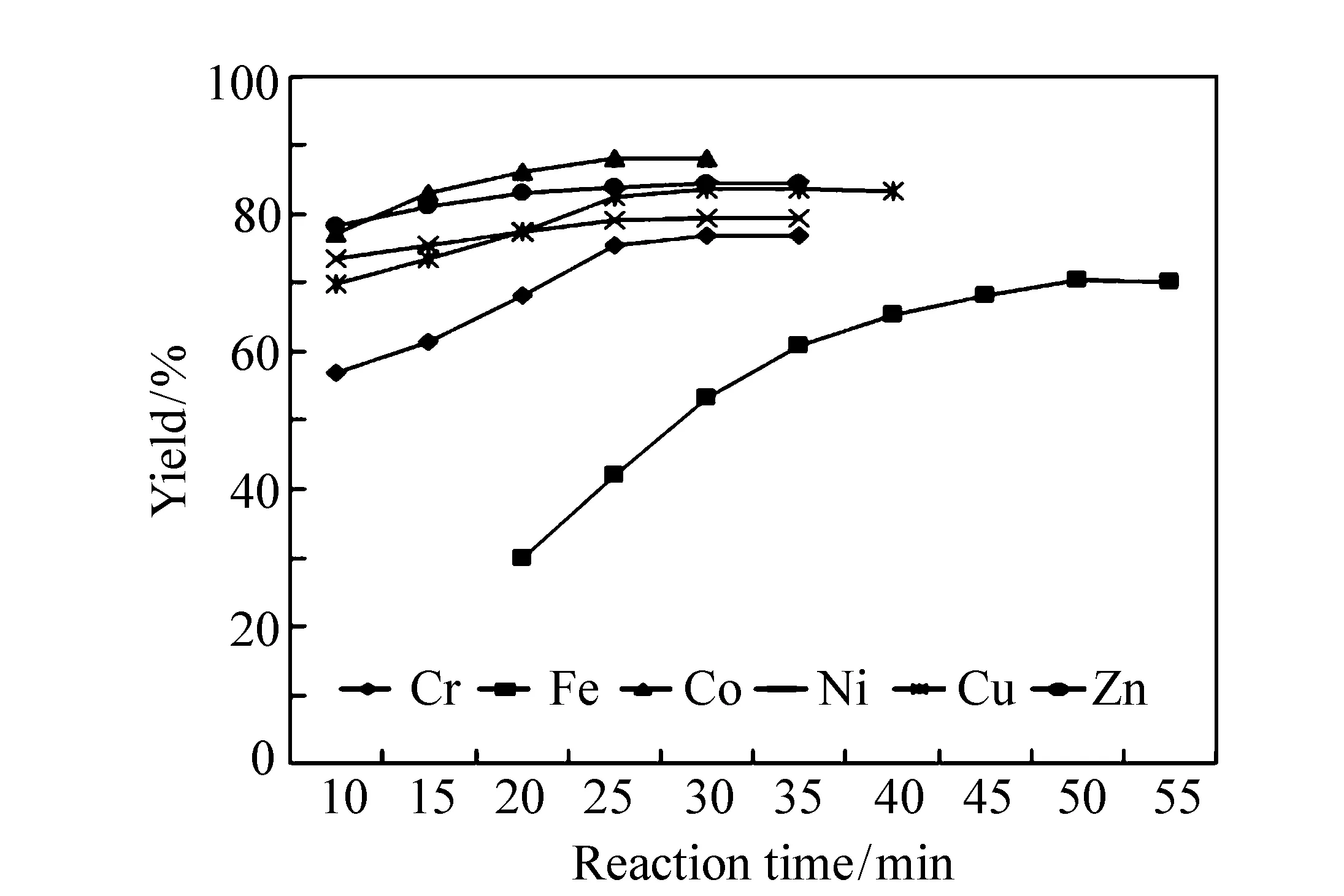
图5 不同中心金属的反应时间与产率 Fig.5 Rreaction time and yield of different central metals
各金属酞菁最佳合成条件见表2。

表2 金属酞菁最佳合成条件Tab.2 Optimum synthesis conditions of metal phthalocyanine
3.2 中心金属离子对酞菁化合物光谱性能影响
酞菁分子的4个异吲哚单元通过N桥联形成大环结构,直径约2.7×10-10m,中心金属离子的化合价、离子半径和配位数不同,可形成不同结构的金属酞菁化合物。半径较小的金属离子(Fe2+、Co2+、Ni2+等)形成的单层平面酞菁结构共轭体系小,Q带峰值波长有利于往短波移动。本文研究了Fe2+、Co2+、Zn2+、Cu2+4种金属酞菁化合物的光谱性能,其吸收光谱和反射光谱曲线如图6所示。从图中吸收光谱曲线可看出,钴、铜、铁金属酞菁的Q吸收峰值波长均在670 nm附近,锌酞菁在700 nm附近,均符合酞菁化合物Q带(600~800 nm)吸收峰特征,证明合成产物为实验预期的金属酞菁。金属离子对吸收峰的位移影响较小,差异(1~10) nm之间, Zn2+内层电子全满与其他过渡金属光谱差异较大,但也不超过30 nm;金属离子对吸收峰上升的陡峭程度影响较大,本文中钴酞菁的吸收峰最尖锐,在反射光谱曲线中表现反射率上升最陡。

图6 酞菁吸收峰曲线(上)与光谱反射曲线(下) Fig.6 Phthalocyanine absorption peak curve(top) and spectral reflection curve(below)
理论上吸收曲线峰值点对应于反射曲线的谷值点,但图6酞菁反射光谱与吸收光谱峰值波长差了100 nm左右,且吸收带展宽,造成光谱性能差异的主要因素是分子的聚集方式,不同的聚集方式会使吸收带拓宽、光谱移动。原因是反射光谱的酞菁不再如溶液中以单分子或多分子分散存在,而是互相叠加聚集。分子间不同排列方式产生的聚集形态造成光谱变化[18],如“面对面”的H聚集会使光谱产生蓝移。
3.3 聚集方式对酞菁化合物光谱性能的影响
酞菁化合物的光谱性能不仅依赖于单个酞菁分子的结构和性质,在很大程度上还取决于分子的聚集形式。以分子间弱相互作用聚集而成的多分子聚集体,由于分子间的激发转移作用,单分子受激发后的激子态会扩展到更多其他分子,形成聚集体整体的光响应[19],光谱展现出单分子所不具备的性质,如吸收谱线的交换变窄,吸收峰相对于单体的红移效应或蓝移效应。酞菁化合物的结构以及所处环境对聚集方式产生影响,并最终导致聚集体光谱性能的改变。本文从产物纯度、分散度、温度等环境因素对酞菁光谱性能的影响进行研究。
3.3.1 纯度对酞菁化合物光谱性能的影响
本文研究了合成酞菁产物经过多种方法提纯后的反射光谱。图7为柱层析后的铁酞菁样品(高纯度)与以水作为提纯剂的铁酞菁样品(存在较多有机物杂质)反射光谱测试结果,从图中可看出,去除杂质的高纯度铁酞菁由于分子间聚集作用,Q带吸收峰被大幅拓宽,整体反射率降低而呈紫黑色,而掺杂有机杂质的低纯度铁酞菁,由于掺杂的有机分子阻碍了酞菁分子间的聚集,在680 nm波长处的反射低谷与吸收峰相吻合,光谱反射率整体提升,与植物光谱较好拟合。
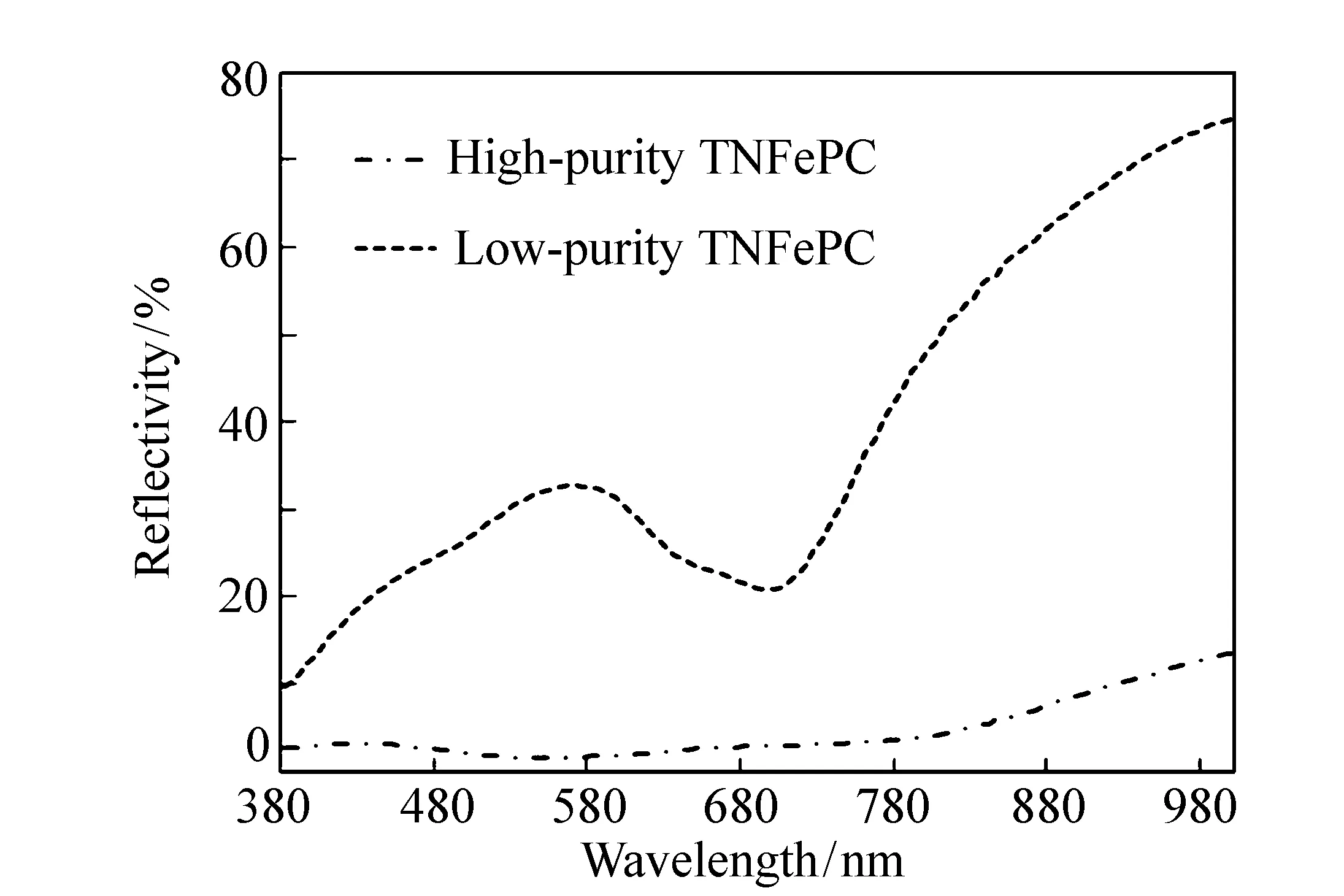
图7 不同纯度四硝基酞菁铁的光谱反射曲线 Fig.7 Spectral reflectance curves of different purity tetral phthalocyanine iron metals
图8为钴酞菁在未提纯(存在有机、无机杂质)、水提纯(存在少量有机参杂质)、酒精提纯(高纯度)的反射光谱。从图中可看出,提纯方法对钴酞菁光谱曲线的影响没有铁酞菁明显,因钴酞菁纯度高,杂质少。钴酞菁反射光谱的陡升效果与植物最接近,纯度越高,陡升效果越好,但反射谷与钴酞菁自身吸收峰相比,整体产生了红移,纯度提高,加聚分子间聚集程度,Q带吸收峰展宽,反射曲线红移。
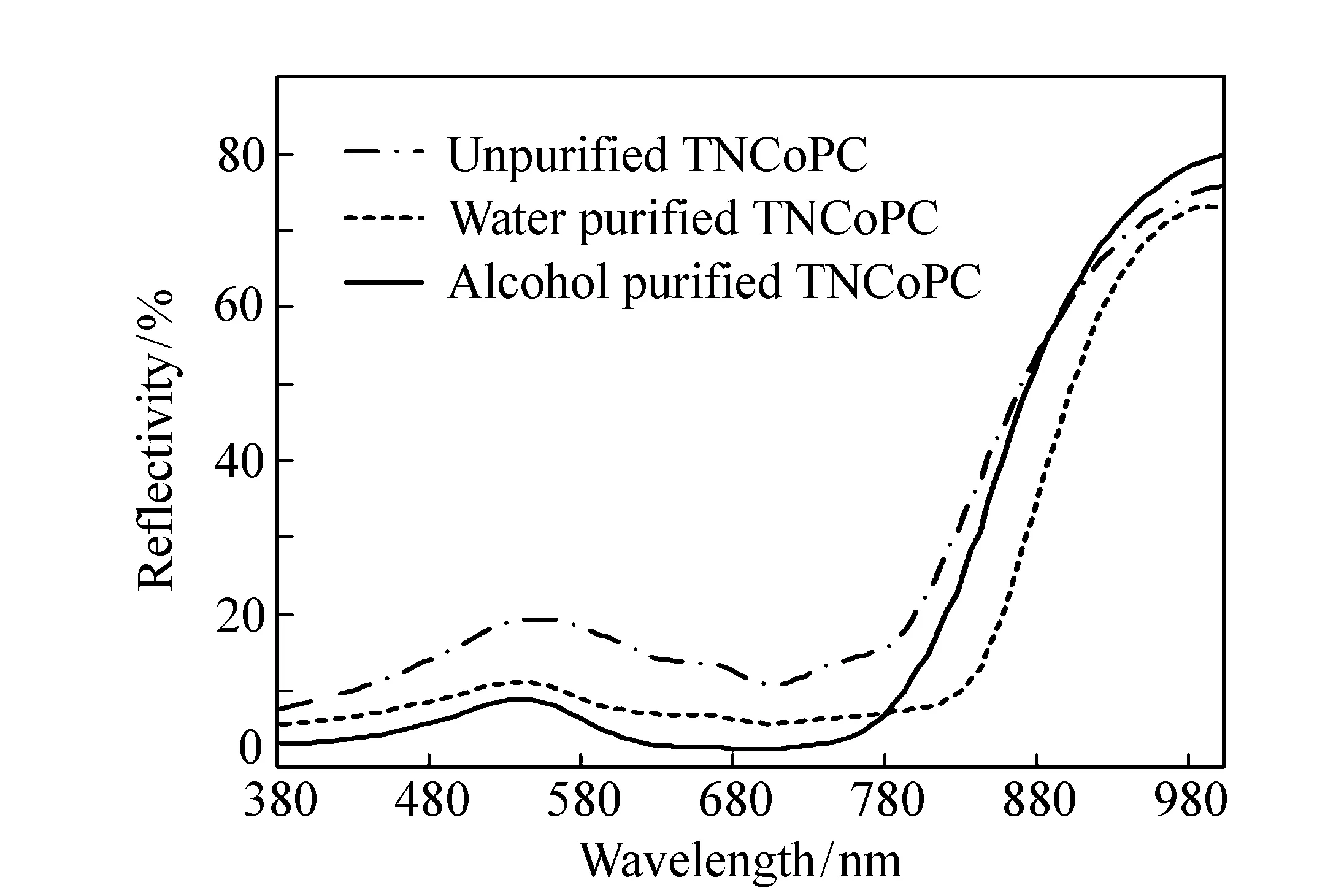
图8 不同纯度四硝基酞菁钴的光谱反射曲线 Fig.8 Spectral reflectance curves of different purity tetra-nitrophthalocyanine cobalt metals
3.3.2 分散度对酞菁化合物光谱性能的影响
本文研究了四硝基酞菁钴样品分别在不同溶剂、不同浓度、不同分散条件下的反射光谱,结果如图9、10、11所示。图9为酒精和二氯甲烷为溶剂进行分散的样品光谱曲线,二氯甲烷为溶剂分散的样品吸收峰红移更多,陡升明显,这可能是由于二氯甲烷能完全溶解四硝基酞菁钴,分散后的样品分布均匀粒度小,分子间的聚集作用加强,吸收峰展宽,反射曲线红移。

图9 不同溶剂分散的样品反射光谱曲线 Fig.9 Sample reflectance spectra of different solvents
图10为不同浓度和干燥条件下分散的样品的反射光谱曲线,从图中可看出,浓度和干燥条件对样品反射光谱曲线影响较小,主要是反射率上存在一定差异,未对其聚集方式产生明显改变,相对来说浓度小、湿度大的样品由于分子间距大,分子间聚集作用小,吸收峰展宽略小,陡升加剧。
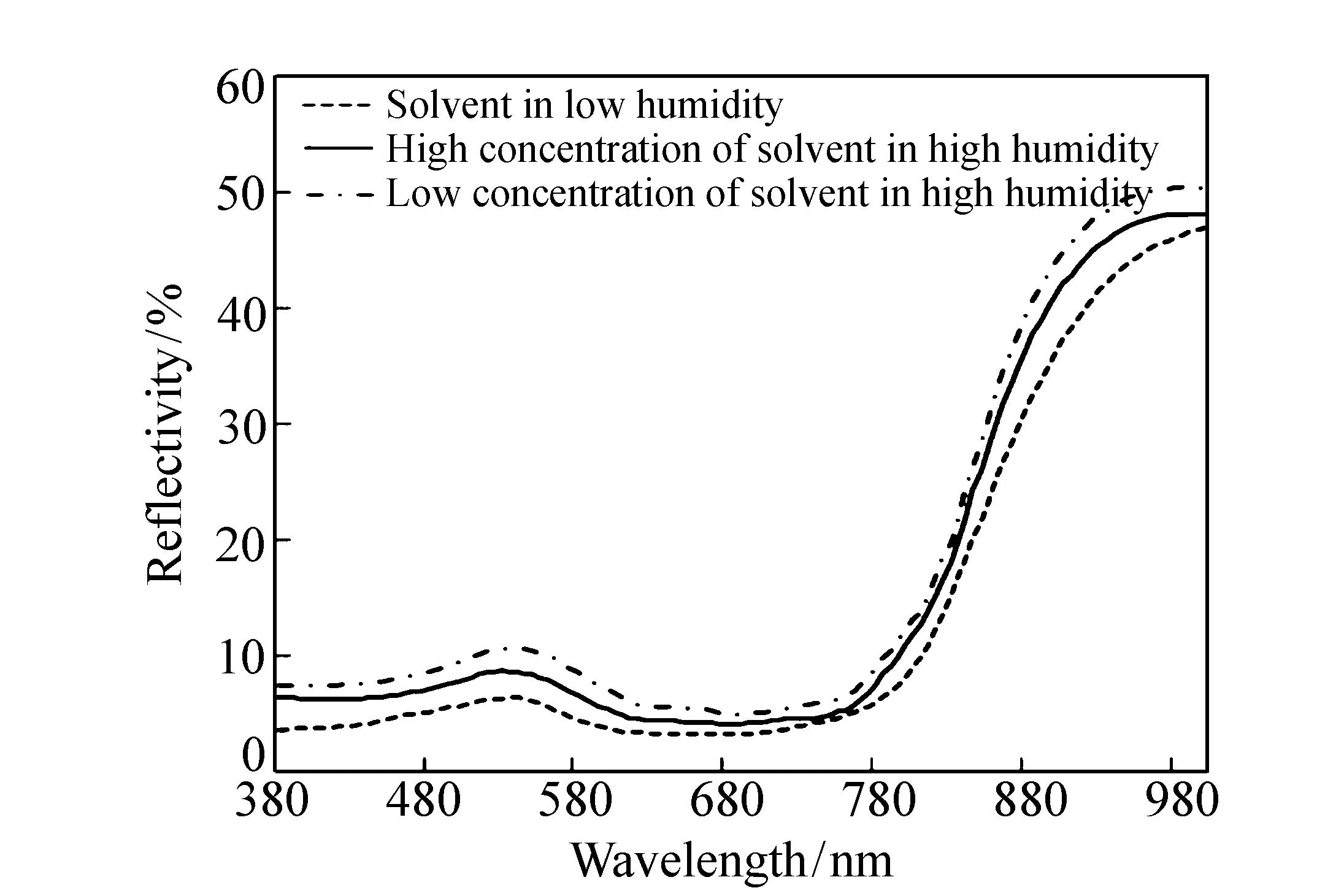
图10 不同浓度、湿度的样品反射光谱曲线 Fig.10 Sample reflectance spectra of different concentrations and humidity
图11为在25和60 ℃时用酒精分散样品的反射光谱曲线,60 ℃下样品的反射陡升明显增强,Q带发生收缩,温度的提升破坏了分子的有序排列,无序度提高,分子的聚集方式改变,聚集程度减弱,有利于Q带蓝移。

图11 不同温度分散的样品反射光谱曲线 Fig.11 Sample reflectance spectra of different temperature dispersion
4 结 论
本文利用自主设计合成装置合成了Fe2+、Co2+、Zn2+、Cu2+金属酞菁,探究了酞菁化合物最佳合成条件和提纯方法,针对反射光谱相对吸收光谱与植物光谱的红移,从影响酞菁聚集态的外界因素(产物纯度、分散程度和温度)研究光谱变化规律,得到以下结论:
(1)采用DBU催化合成法,利用自制装置合成的金属酞菁,在220~240 ℃下反应20~30 min,产物产率可达到80%,产物的吸收光谱符合酞菁化合物Q带(600~800 nm)吸收特征;
(2)合成的α-四硝基酞菁钴(CoPC(NO2)4)反射峰波长较无金属酞菁产生较大蓝移,峰形与植物光谱相拟合,近红外陡升最强;
(3)产物纯度、分散状态、温度影响酞菁分子聚集状态,导致反射光谱较吸收光谱产生变化。产物纯度高,分子间聚集明显,Q带峰值展宽,光谱红移;温度升高,分散程度高,阻碍分子间聚集,有利于光谱蓝移。

