鼻咽癌调强放射治疗设置头颈前部淋巴引流保护区的剂量学可行性研究
黄 娟,陈晓慧,翟瑞萍,孔芳芳,应红梅
复旦大学附属肿瘤医院放疗科,复旦大学上海医学院肿瘤学系,上海 200032
头颈部淋巴水肿(head and neck lymphedema,HNL)是鼻咽癌(nasopharyngeal carcinoma,NPC)调强放射治疗(intensitymodulated radiotherapy,IMRT)后一种常见的不良反应,而相关的研究和报道则较少。相比于肢体水肿,头颈部明显的水肿更容易影响外貌,可对患者的心理产生负面影响,如自尊心下降和社会适应不良等[1]。淋巴水肿的脸部、颈部还会影响患者的咀嚼、呼吸及头颈部活动等功能,在极端情况下,甚至会导致患者视力模糊、呼吸困难[2]。生理功能的下降反过来又可增加患者的心理压力,引发焦虑、抑郁等精神问题[3]。可见,HNL对患者的生活质量有着较大的影响,应引起更多的关注。本研究旨在探索一种预防或减轻NPC患者放疗后HNL的计划设计方法,研究其剂量学可行性。
1 资料和方法
1.1 临床资料
随机选取2017年6—10月在复旦大学附属肿瘤医院进行放射治疗的NPC患者共20例,其中男性12例,女性8例,中位年龄为46岁,T1期患者5例,T2期患者7例,T3期患者7例,T4期患者1例。
1.2 CT模拟定位和图像融合
患者仰卧位于平板体架上,以头颈肩热塑面罩进行体位固定扫描定位CT,图像经网络传输至飞利浦Pinnacle3 8.0治疗计划系统,与鼻咽部T1增强磁共振图像进行融合。
1.3 靶区与危及器官(organ at risk,OAR)的勾画
根据ICRU50和62号报告,进行靶区的勾画。大体肿瘤靶区(gross tumor volume,GTV)分为原发灶GTV(GTV_P)和淋巴结GTV(GTV_N),GTV_P包括鼻咽部原发肿瘤及咽后淋巴结;GTV_N为颈部阳性淋巴结,GTV均匀外放5 mm形成计划靶区(planning target volume,PTV)。临床靶区(clinical target volume,CTV)分为CTV1和CTV2,CTV1为鼻咽部亚临床区域和颈部高危淋巴引流区,CTV2为颈部低危淋巴引流区,一般包括Ⅳ区和Ⅴb区,各均匀外放3 mm形成PTV1和PTV2。勾画脑干、脊髓、视神经、视交叉、腮腺、口腔和喉等OAR。
1.4 靶区处方剂量及OAR的限量
T1、T2期患者,原发灶给予66 Gy的照射,T3、T4期患者,原发灶给予70.4 Gy的照射,颈部阳性淋巴结均给予66 Gy的照射。PTV1和PTV2的处方剂量分别为60和54 Gy,分30或32次照射。靶区的剂量要求如下:100%处方剂量线至少包绕95%的靶区体积,95%的处方剂量线至少包绕99%的靶区体积,大于110%处方剂量的体积不超过1%或1 cm3。OAR限量如下:脑干、视神经及视交叉最大剂量(Dmax)小于54 Gy或1%体积的受照剂量不超过60 Gy;脊髓Dmax小于45 Gy或l cm3体积的受照剂量不超过50 Gy;至少1侧腮腺50%体积的受照剂量不超过30 Gy;晶体控制在8 Gy以下;在保证靶区覆盖的前提下,眼球、颞叶、口腔和喉等的OAR受量越低越好。
1.5 计划设计
所有病例均在飞利浦Pinnacle3 8.0计划系统设计计划,采用同步加量的9野均分共面照射的简单调强放射治疗(simplified intensity-modulated radiotherapy,sIMRT)技术,总的子野数不超过45个,最小子野面积为10 cm2,最小子野跳数为10 MU[4]。计划A:常规sIMRT计划,按照上述的靶区剂量和OAR限量设计治疗计划,同时按照本中心的习惯,使用头颈后部淋巴引流保护区设计;计划B:在计划A的基础上,加用头颈前部淋巴引流保护区设计的sIMRT计划,鼻部开始往下,靶区中部靠近头颈前部皮肤处勾画一个直径为1~2 cm大小的辅助结构,大小与限量视与靶区距离的远近而定,剂量通常限制在15~20 Gy以下,其余计划设计的参数同计划A保持一致。
1.6 计划评估
通过剂量体积直方图来评估靶区的剂量分布和OAR受量,采用D98%、D2%、V95%(%)、V100%(%)、平均剂量(Dmean),适形性指数(conformity index,CI)及均匀性指数(homogeneity index,HI)来评估靶区的剂量分布。其中,Dx%代表x%的靶区体积所受到的剂量,Vx%(%)代表受到x%处方剂量照射的靶区体积占靶区总体积的百分比,CI和HI的定义见参考文献[5]。考虑到是否加用头颈前部淋巴引流保护区,对原发灶、阳性淋巴结及鼻部以上正常组织剂量的影响很小,为了统计方便,靶区主要比较PTV1和PTV2的剂量分布,正常组织主要比较以下参数:脊髓或脑干的Dmax,1 cm3脊髓或脑干所受到的剂量(D1cc),腮腺Dmean和受到30 Gy照射的体积百分比(V30),内耳Dmean,口腔和喉的Dmean、V50。
1.7 统计学处理
采用SPSS 22.0软件进行统计学分析,计量资料以x±s的形式表示,对两组计划的靶区剂量分布、OAR受量及机器跳数进行配对t检验分析,P<0.05(双侧检验)为差异有统计学意义。
2 结果
2.1 头颈前部淋巴引流保护区的形成
图1显示了1例T2N1M0患者两种计划设计在CT横断面上的剂量分布,可以清晰地看到计划B中前颈正中部有1个低剂量照射(<20 Gy)的淋巴引流保护区。
2.2 两组计划靶区剂量分布的比较
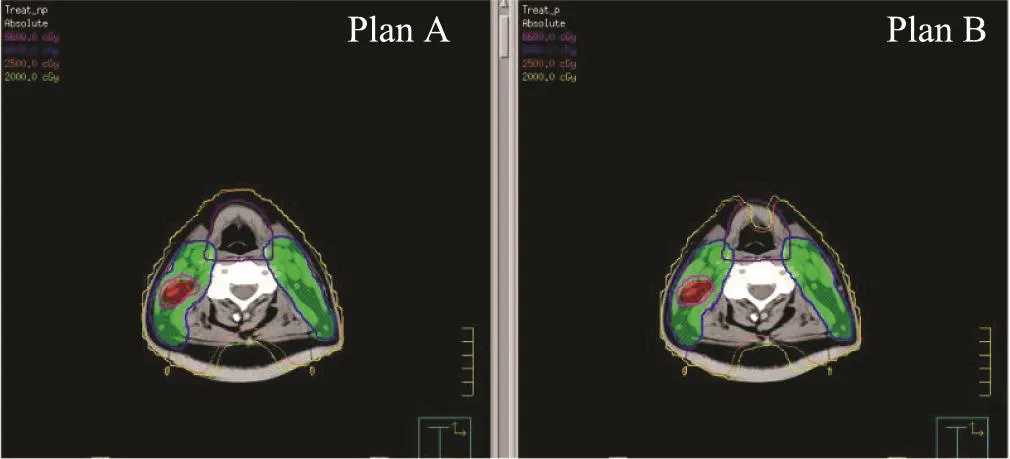
图 1 1例T2N1M0期NPC患者计划A和计划B在CT横断面上的剂量分布图Fig. 1 The dose distributions of plan A and plan B on CT images for a T2N1M0 patient with NPC
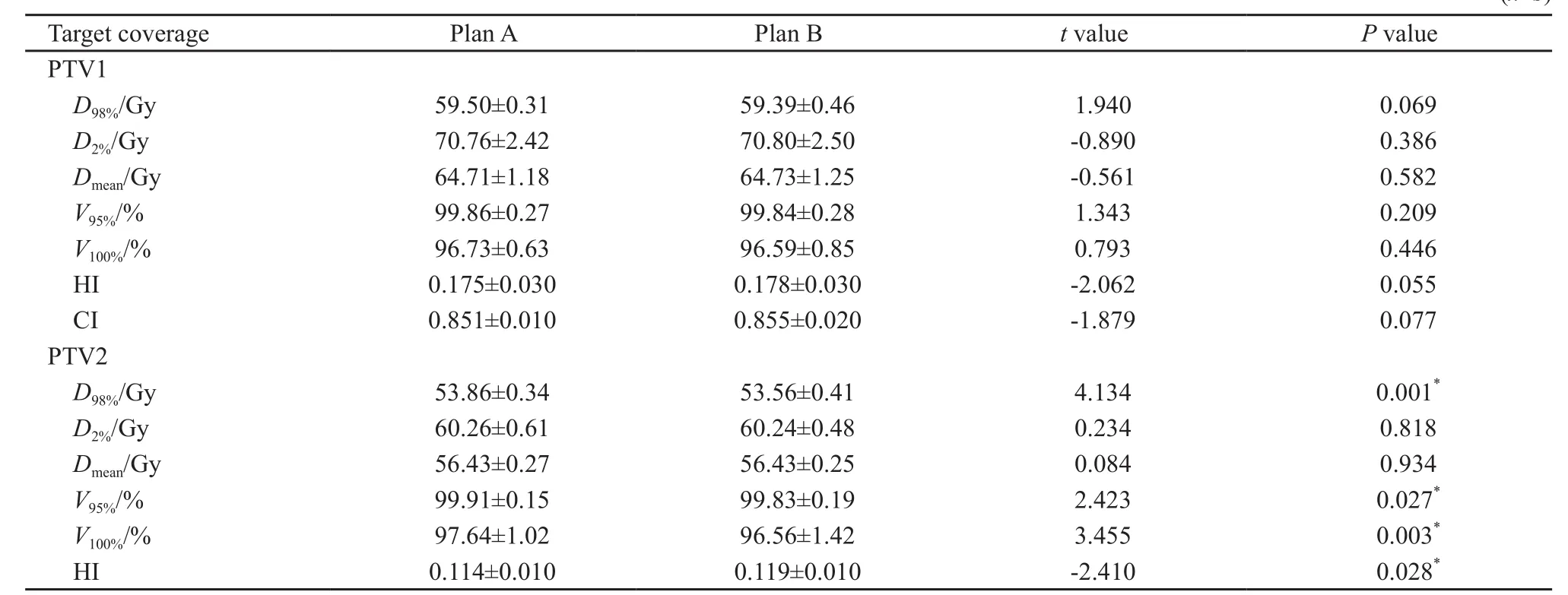
表 1 20例NPC患者计划A和计划B靶区剂量分布的比较Tab. 1 Comparison of target dose distributions for twenty patients with NPC between plan A and plan B(x±s)
由表1可见两组计划均满足临床靶区覆盖的要求,PTV1的D98%、D2%、V100%(%)、V95%(%)、Dmean、HI和CI均比较接近,差异无统计学意义(P>0.05)。PTV2的D98%、V100%(%)、V95%(%)和HI差异有统计学意义(P<0.05),但PTV2的靶区覆盖仍满足临床要求,D2%、Dmean的差异则无统计学意义(P>0.05)。
2.3 两组计划OAR受量的比较
左、右腮腺的Dmean、左侧腮腺的V30、口腔和喉的Dmean和V50差异均有统计学意义(P<0.05),其余正常组织包括左、右中耳,脊髓,脑干的受量差异均无统计学意义(P>0.05)。具体受量和统计结果见表2。
2.4 两组计划总的机器跳数的比较
与计划A相比,计划B的机器跳数略有增加,计划A和计划B的跳数均数分别为800.65和827.30,但差异无统计学意义(t=2.026,P=0.057)。
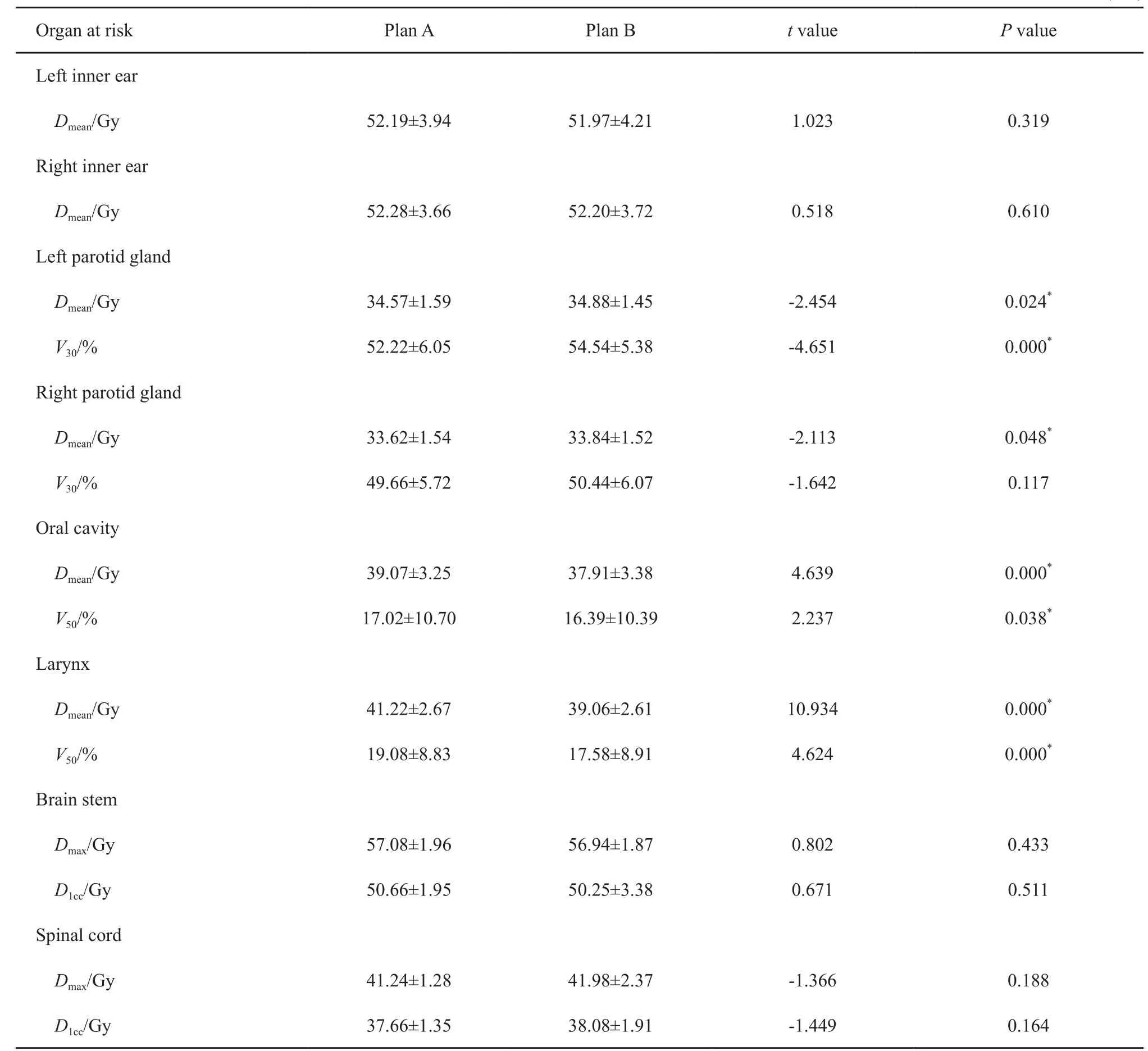
表 2 20例NPC患者计划A和计划B危及器官受量的比较Tab. 2 Comparison of dose-volume parameters of the organs at risk for twenty patients with NPC between plan A and plan B(x±s)
3 讨论
NPC放疗后发生的HNL属继发性淋巴水肿,可涉及机体外部结构,如面颈部的软组织,也可涉及内部解剖部位,如口腔、咽喉部[2]。外淋巴水肿的患者,颈部肿胀和纤维化可导致颈部活动范围减少;内淋巴水肿的患者,上呼吸道、咽喉部组织肿胀影响气道通气或导致吞咽困难[6-7]。体内淋巴液的正常流动对体液稳态、机体免疫和脂质再吸收起着至关重要的作用。放疗是NPC的主要治疗方式,射线可导致颈部淋巴管道闭塞、破坏,周围软组织受损,淋巴液回流受阻,组织间隙内淋巴液潴留,形成水肿,进一步激活炎性反应和免疫反应后可导致皮肤和皮下软组织纤维化和脂肪沉积[8]。此外,下颌、面颈部的活动性通常在治疗后有所下降,影响咀嚼和吞咽功能,区域肌肉活动的减少可能会进一步损害淋巴系统。IMRT虽然大大提高了靶区的剂量覆盖和OAR的保护,但是也存在一定的缺陷,为了满足肿瘤组织高剂量的覆盖和OAR尽可能低剂量的要求,周围未被关注的正常组织可能会受到更多的照射[9]。有动物实验显示,当小鼠尾巴接受15和30 Gy照射后,体积分别增加15%和25%[10],提示辐射对水肿的发生有剂量依赖性。本中心常规在头颈后部设置淋巴引流保护区(15 Gy以下的剂量限值)以利于淋巴回流,由于最常见的淋巴水肿部位是颈部和颏下区域,我们假设在头颈前部设置类似的淋巴引流保护区,是否会有助于缓解NPC患者放疗后的HNL,考虑到在头颈前部设置淋巴引流保护区离靶区较近,15 Gy的限量可能会影响靶区的覆盖,在离靶区较近的部位(如下颈双侧淋巴引流区)设置20 Gy的限值,从上至下留出一条低剂量照射的区域,用于淋巴回流。
当给予头颈前部淋巴引流保护区限量之后,在相同参数条件下优化两组计划,结果显示,上颈部靶区的覆盖、适形性及均匀性几乎没有变化。下颈部由于两侧靶区相距较近,靶区的覆盖和均匀性差异有统计学意义,但两者的差异并不大,且都符合临床要求。本研究中,使用头颈前部淋巴引流保护区的设计,腮腺Dmean略有增加,但是均值增加较少,只有0.2~0.3 Gy,而口腔Dmean却有较大的下降(均值下降1.1 Gy)。有研究报道,除了腮腺Dmean,口腔Dmean也与患者口腔干燥症的发生、生活质量有较大的关系,降低口腔Dmean,使得口腔内的小涎腺得到一定的保护,能有效地减少口腔干燥症的发生[11]。本研究中,口腔Dmean的降低弥补了腮腺受量增加所引起的唾液分泌减少对口干的影响。另有研究发现,大于39.0 Gy的照射与较长时间的口腔黏膜炎有关[12],加用头颈前部淋巴引流保护区后,口腔的Dmean从39.0 Gy降到了37.9 Gy,能更好地保护口腔黏膜,而口腔黏膜与内淋巴水肿有一定的联系[13]。同时,喉的平均剂量也有较大的下降(均值下降2 Gy),有研究报道,喉的平均剂量是最能预测喉水肿的独立影响因素,为了减少喉水肿的发生,喉的平均剂量应尽可能的低[14]。而喉的V50是预测喉水肿的另一个重要因素,V50的降低也有助于减少喉水肿的发生,计划B中,喉的V50均值降低了1.5%,而咽喉部的肿胀则与内淋巴水肿息息相关[13]。提示设置头颈前部淋巴引流保护区,既可在体表留出低剂量照射的区域以利于淋巴回流,有望减少外淋巴水肿的发生,还可以降低口腔、咽喉部的受量,一定程度上减少内淋巴水肿的发生。
综上所述,NPC患者给予头颈前部淋巴引流保护区的计划设计在剂量学上是可行的,且有一定的优势,在满足临床靶区覆盖的前提下,于头颈前部留出了低剂量(<20 Gy)照射的区域利于淋巴回流,且更好地保护了口腔、喉等可导致淋巴水肿的正常组织。但剂量学上的优势是否能转化为临床获益,还有待于临床随访进一步验证。

