非限域R-缬氨酸体系前线分子轨道的原子贡献
祝 颖, 杨雪磊, 曹殿钧
(吉林医药学院 生物医学工程学院, 吉林 吉林 132013)
缬氨酸(Val)是组成生命体蛋白质的重要氨基酸之一. 文献[1-2]研究表明,R-Val在生化领域应用广泛, 可模拟肺动脉内皮细胞的形态功能, 如纤维细胞生长繁殖被阻止及子宫内膜纤维细胞变厚增生被抑制等; 文献[3-4]研究了单体缬氨酸分子手性转变机理及水分子和羟基自由基对氢迁移反应的催化作用; 文献[5]研究了分子体系中以某些方法还原原子轨道, 并计算了分子轨道中基函数的贡献问题. 目前, 非限域条件下R-Val分子体系前线分子轨道成分原子贡献的理论研究尚未见文献报道, 基于此, 本文对非限域条件下R-Val分子体系前线分子轨道成分的原子贡献进行理论计算, 为揭示非限域条件下R-Val分子体系成键本质提供理论依据. 先用密度泛函理论中的B3LYP方法, 在6-31G(d)基组上优化R-Val基态几何构型[6], 再在相同理论方法下计算非限域条件下R-Val分子体系分子轨道的波函数, 并分析分子轨道成分的原子贡献情况.
1 理论和计算方法
根据分子轨道波函数的线性展开式
(1)
计算轨道成分, 用于讨论电子结构, 分析电荷转移, 并根据前线轨道理论分析反应位点等. 在实空间下对分子轨道进行划分即可计算分子轨道中的原子成分, 具有形式直观、 对基组依赖性小等优点. 用Hirshfeld和Cecke方法[5]计算原子贡献. 所有计算均在Gaussian 09[7]软件包内进行, 波函数分析由wfn程序[8-11]完成.
2 结果与讨论
2.1 基于Hirshfeld方法计算分子轨道的原子贡献
R-Val分子体系占据分子轨道32条, 用Hirshfeld方法基于程序内置的原子密度计算5条较高占据轨道和1条虚轨道, 即最高占据分子轨道(HOMO),HOMO-1,HOMO-2,HOMO-3,HOMO-4和最低未占分子轨道(LUMO)的原子贡献. 其中x轴与5C和10O原子的连线方向一致, 略有偏离, 由5C指向10O. 计算结果列于表1. 由表1可见, LUMO中的6C和10O原子贡献较大, 分别为40.350%和27.500%; HOMO中1N原子的贡献最大, 为66.348%; HOMO-1中的10O原子贡献最大, 为60.689%; HOMO-2中的10O和17O原子贡献较大, 分别为32.791%和25.640%; HOMO-3中的5C,8C,9C和10O的原子贡献接近, 均约为15%; HOMO-4中的5C和9C原子贡献较大, 分别为21.010%和22.763%.

表1 5条较高占据轨道和1条虚轨道的原子贡献(%)
2.2 R-Val分子体系中手性C原子在指定分子轨道内的贡献
在R-Val分子中, 以手性C原子为例, 考察3C原子在1~32前线分子占据轨道内的贡献, 计算结果列于表2(仅列出大于12.0%的贡献). 由表2可见, 用原子对轨道的贡献值乘以轨道的占据数即可得布居数值, 并给出各轨道的布居数加和值. 由于1~32为全部占据轨道, 因此甲基碳原子在R-Val分子中的总电子数为5.977 8, 其Hirshfeld电荷为6-5.977 8=0.022 2.
2.3 R-Val分子中C,O,N原子在指定分子轨道内的贡献
在R-Val分子中, 以氨基上的N原子为例, 考察1N原子在指定前线分子占据轨道内的贡献, 计算结果列于表3(仅列出大于12.0%的贡献). 由表3可见: 在全部占据轨道中, 氨基上1N原子在R-Val分子中的总电子数为7.212 5, 其Hirshfeld电荷为7-7.212 5=-0.212 5; 1N在3号和32号占据轨道贡献较大, 分别为99.427%和66.346%.

表2 3C原子在指定前线分子占据轨道内的贡献
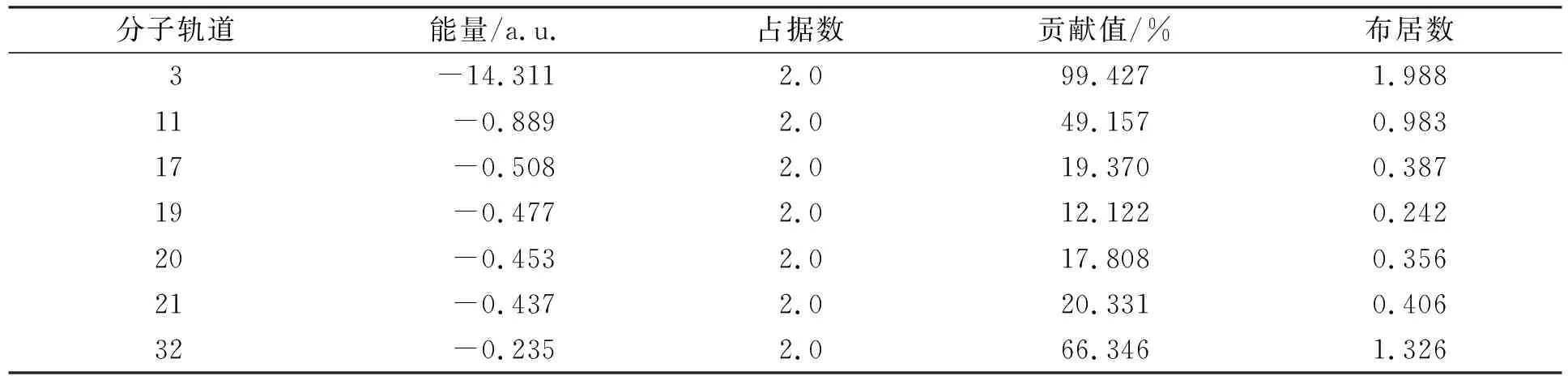
表3 1N原子在指定前线分子占据轨道内的贡献
在R-Val分子中, 以羰基上O原子为例, 考察10O原子在指定前线分子占据轨道内的贡献, 计算结果列于表4(仅列出大于12.0%的贡献). 由表4可见: 在全部占据轨道中, 10O原子在R-Val分子中的总电子数为8.269 5, 其Hirshfeld电荷为8-8.269 5=-0.269 5; 10O在2号和31号占据轨道贡献较大, 分别为99.709%和60.689%.

表4 10O原子在指定前线分子占据轨道内的贡献
在R-Val分子中, 以甲基上C原子为例, 考察5C原子在指定前线分子占据轨道内的贡献, 计算结果列于表5(仅列出大于12.0%的贡献).

表5 5C原子在指定前线分子占据轨道内的贡献
由表5可见: 在全部占据轨道中, 甲基上5C原子在R-Val分子中的总电子数为6.013 5, 其Hirshfeld电荷为6-6.013 5=-0.013 5; 5C在6号占据轨道贡献最大, 为98.969%.
2.4 R-Val分子体系分子轨道官能团片段的贡献
在R-Val分子中, 以氨基片段为例, 考察氨基官能团片段在占据轨道内的贡献, 计算结果列于表6(仅列出大于20.0%的贡献). 由于1~32为全部占据轨道, 因此氨基在R-Val分子中的总电子数为9.013 5, 其Hirshfeld电荷为9-9.013 5=-0.013 5; 氨基官能团片段在3号占据轨道贡献最大, 为99.796%.

表6 氨基官能团片段在指定前线分子占据轨道内的贡献
在R-Val分子中, 以羰基片段为例, 考察羰基官能团片段在占据轨道内的贡献, 计算结果列于表7(仅列出大于20.0%的贡献). 羰基在R-Val分子中的总电子数为14.052 7, 其Hirshfeld电荷为14-14.052 7=-0.052 7; 羰基官能团片段在4号占据轨道贡献最大, 为99.369%.
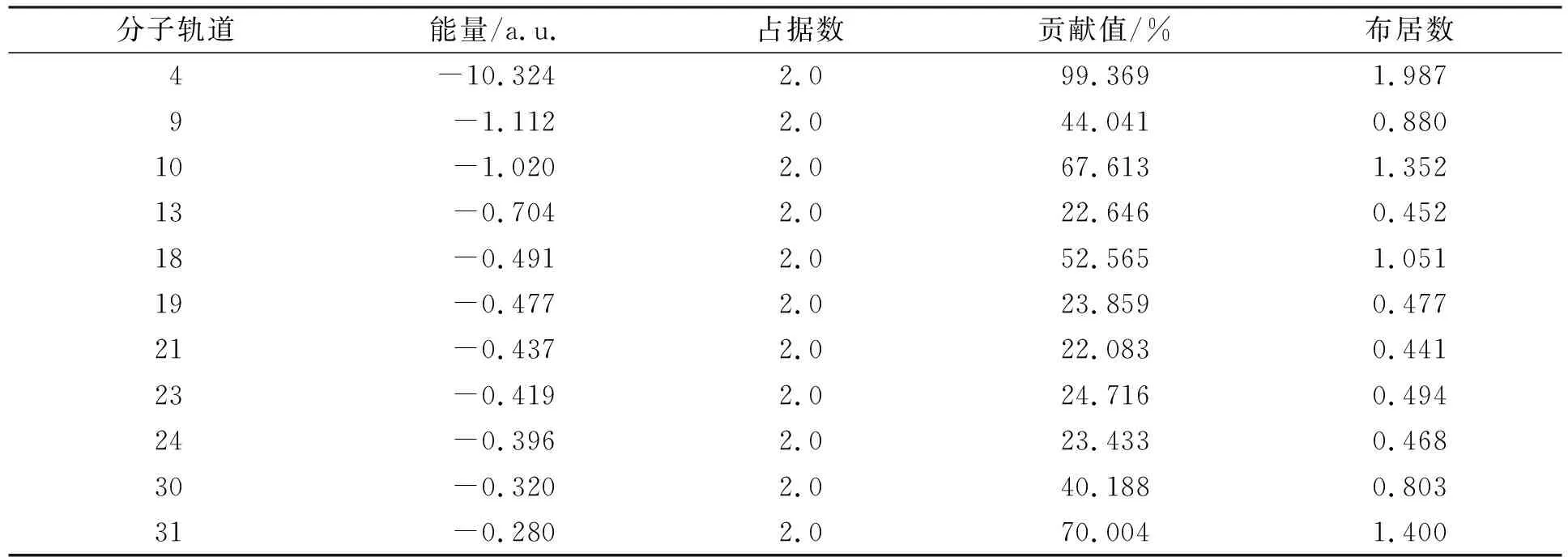
表7 羰基官能团片段在指定前线分子占据轨道内的贡献
在R-Val分子中, 以羟基片段为例, 考察羟基官能团片段在占据轨道内的贡献, 计算结果列于表8(仅列出大于20.0%的贡献). 羟基在R-Val分子中的总电子数为8.972 7, 其Hirshfeld电荷为9-8.972 7=0.027 3; 羟基官能团片段在1号占据轨道贡献最大, 为99.813%.

表8 羟基官能团片段在指定前线分子占据轨道内的贡献
由表7和表8可见, 羰基和羟基官能团片段对第9和第10号占据轨道贡献非常明显. 气相环境下R-Val第9和第10号占据轨道的前线分子轨道如图1所示.
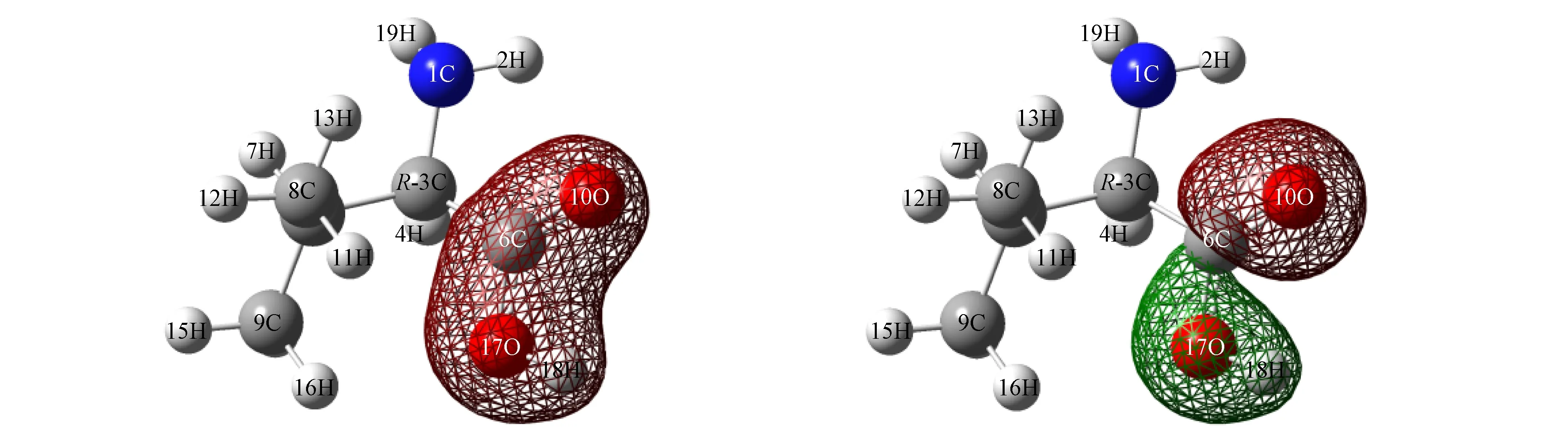
图1 气相环境下R-Val第9和第10号占据轨道的前线分子轨道Fig.1 Frontier molecular orbit of the ninth and tenth occupied orbit for gas phase R-Val
2.5 Becke方法分析分子轨道的原子贡献
R-Val分子体系占据分子轨道32条, 用Becke方法基于原子半径分析4条高占据轨道和1条虚轨道的原子贡献, 计算结果列于表9.

表9 4条较高占据轨道和1条虚轨道的原子贡献(%)
由表9可见, 在分析分子轨道的原子贡献时, Becke方法和Hirshfeld方法对占据轨道分析的定性结果基本一致; 定量结果略有差别, 如在HOMO-1中, 10O原子贡献偏大, 偏差值为3.88%; 在HOMO-2中, 10O和17O原子贡献偏大, 偏差值分别为1.40%和1.82%; 在HOMO-3中, 9C和10O原子贡献偏差较大, 偏差值约为10%. Becke方法和Hirshfeld方法对虚轨道分析的定性结果不一致, 定量结果差别明显, 如在LUMO中, 6C原子贡献较小, 偏差值为37.22%; 5C原子贡献最大, 偏差值为16.45%; 同时8C,9C和10O的贡献值均向相反方向变化, 偏差值均约为10%.
综上, 本文可得如下结论: 在分析分子轨道的原子贡献时, Becke和Hirshfeld方法对高占据轨道分析的定性结果基本一致, 定量结果略有差别; 对虚轨道分析的定性结果不一致, 定量结果差别明显, 如在LUMO中6C原子贡献较小, 偏差值为37.22%; 5C原子贡献最大, 同时8C,9C,10O的贡献值均向相反方向变化, 偏差值均约为10%.

