主动干预对肝硬化高危食管胃静脉曲张患者首次出血率和死亡率的影响
刘 楚,马丽黎,曾晓清,王 剑,李 锋,陈世耀,,3
复旦大学附属中山医院 1.消化科;2.内镜中心;3.复旦大学循证医学中心,上海 200032
食管胃静脉曲张(gastroesophageal varices,GOV)是肝硬化最常见的门静脉高压表现之一。肝硬化患者中存在GOV的约50%,较小直径的曲张静脉以每年8%的速度发展为较大直径的曲张静脉;食管胃静脉曲张破裂出血(eophagogastric variceal bleeding,EVB)的年发生率为5%~15%,6周病死率在20%左右[1],5年死亡率可达20%[2]。Baveno Ⅵ[3]推荐对小食管静脉曲张伴出血高危因素(红色征或Child-Pugh C级)或中-大食管静脉曲张(伴或不伴高危因素)进行非选择性β受体阻滞剂(non-selective betablockers,NSBB)或内镜下皮圈套扎(endoscopic band ligation,EBL),对胃静脉曲张可行NSBB或内镜下组织粘合剂治疗,不推荐药物和内镜联合、介入或手术治疗;欧洲指南[4]与中国指南[1]对高危因素的定义稍有出入,但对中-大静脉曲张的干预无争议。然而在中国的临床实践中一级预防存在很多问题,包括:药物不适合(存在难治性腹水、门脉系统广泛血栓、合并肝癌等),药物不耐受,内镜治疗技术的开展,患者对内镜治疗的顾虑,合并胃静脉曲张的治疗争议等。且国内对一级预防的探索和研究少见报道。本研究旨在描述临床实践中肝硬化高危出血患者一级预防现状,比较主动干预对患者首次出血率和死亡率的影响。
1 资料与方法
1.1一般资料回顾性收集2012年1月至2015年12月、前瞻性收集2016年1月至2016年12月我院消化科病房的肝硬化患者进行研究。纳入标准:(1)病史、影像学、病理诊断肝硬化;(2)入院前后3个月我院行胃镜检查;(3)既往无EVB史。排除标准:(1)既往有门脉高压相关的药物、内镜、介入或外科手术治疗史;(2)既往有食管或胃的外科手术史;(3)存在非肝癌的恶性肿瘤;(4)存在严重脏器疾病如心功能Ⅲ~Ⅳ级、CKD 4~5期、肝癌终末期、肝衰竭等;(5)胃镜阅片确认为无食管静脉曲张或小食管静脉曲张。本研究符合人体试验伦理学标准,经医院论文伦理委员会审核批准(批件号:B2015-149R)。
1.2分组和定义GOV的严重程度分级依据2016年《肝硬化门静脉高压食管胃静脉曲张出血的防治指南》进行[1];食管静脉曲张<5 mm定义为小静脉曲张,>5 mm为中-大静脉曲张。结果由2名10年以上经验医师进行独立判断;存在分歧的由第3名医师再次进行独立判断,根据3人中2人一致的结果进行分析。将肝硬化伴中-大食管静脉曲张患者按有无进行首次出血预防分为干预组与对照组。
干预组:入院后3个月内开始EVB的一级预防,至少接受一种预防措施,包括药物、内镜、介入或外科手术。(1)药物干预:连续服用NSBB(普奈洛尔或卡维地洛)至少1个月,普奈洛尔最小剂量10 mg/d,卡维地洛最小剂量5 mg/d;(2)内镜干预:至少接收1次内镜下食管曲张静脉套扎或硬化剂注射治疗;(3)介入干预:任何形式的门体分流或断流介入手术,如经颈静脉肝内门体分流术、脾动脉栓塞术或胃冠状静脉栓塞术等;(4)手术干预:任何形式的门体分流或断流外科手术,如脾切除术、贲门周围血管离断术、门-奇静脉断流术、门-腔静脉分流术等。
对照组:入院后3个月内未接受任何预防EVB的干预措施,或接受药物干预但因各种原因(如药物不耐受、自行停药等)连续用药时间不足1个月。
1.3观察指标通过检索患者历次就诊或入院信息,结合电话随访进行随访。主要观察指标为EVB;次要观察指标包括死亡(全因死亡、出血相关死亡、肝病相关死亡、肝癌死亡),肝硬化相关并发症(新发肝癌、肝性脑病、自发性腹膜炎、肝肺综合征、肝肾综合征),治疗相关不良事件。随访终点为出血、死亡、接受肝移植、转换治疗或研究截至日期。
1.4统计学分析采用Microsoft Excel 2016进行数据录入和管理,采用SPSS 24.0软件对研究数据进行统计分析。连续变量采用K-S检验对其进行正态性检验,符合正态分布的连续变量采用均数±标准差进行描述,不符合正态分布的连续变量采用中位数(25%位数~75%位数)进行描述,分类变量采用例数/%进行描述。符合正态分布的连续变量组间比较采用单因素ANOVA分析,不符合正态分布的连续变量和有序分类变量的组间比较采用非参数检验进行,无序分类变量的组间比较采用χ2检验进行;双侧P<0.05为差异有统计学意义。运用Kaplan-Meier法进行组间出血率和死亡率的比较,双侧P<0.05为差异有统计学意义。Cox等比例风险回归模型对影响出血的危险因素进行单因素分析,纳入P<0.2的单因素运用Cox回归后退法进行多因素分析。
2 结果
2.1病例入组情况2012年1月1日至2016年12月31日入住我院消化科诊断为肝硬化、无食管胃静脉曲张破裂出血史的患者共1 556例,前后3个月内本院未行胃镜检查1 132例,符合入选标准424例。排除既往门脉高压相关治疗史68例,非肝癌的恶性肿瘤64例,严重脏器疾病28例。剩下264例患者调阅胃镜报告,由2名10年以上经验消化内镜医师独立判断,进行Kappa分析;2名医师判定食管静脉曲张大小、严重程度、红色征和胃静脉曲张的Kappa值分别为0.842±0.029、0.718±0.032、0.666±0.049和0.796±0.039(P均<0.001)。最终确定存在静脉曲张175例(66.3%),包括孤立胃静脉曲张4例(1.5%),小食管静脉曲张61例(23.1%),中-大食管静脉曲张110例(41.7%)。110例中-大食管静脉曲张患者中15例出院后即失访(13.6%),由于无法判断患者的治疗和转归,不纳入分析;最终纳入95例行进一步随访和分析。
入组人群中男60例(63.2%),中位年龄57岁(47~62岁),肝硬化病因以乙肝后肝硬化为主59例(62.1%),Child分级以A级(50.0%)和B级(45.7%)为主,合并肝癌和门脉系统血栓分别为15例(15.8%)和16例(16.8%)(见表1)。
2.2分组与随访干预组和对照组各有50例(52.6%)和45例(47.4%)患者,中位随访时间分别为15.97个月(10.45~44.39个月)和15.49个月(6.51~33.61个月)。干预组Child A级例数比例更高,食管静脉曲张G3所占比例更多(见表1)。

表1 干预组与对照组基线情况比较Tab 1 Comparison of baseline between intervention group and control group
注:*:对照组50例患者中,1例未检测白蛋白,无法进行Child评分及分级,故Child分级中对照组例数为49。
干预组以内镜和药物干预为主。单独内镜干预29例(64.4%);单独药物干预9例(20.0%),药物联合内镜干预2例(4.4%),脾切除+贲门周围血管离断术和脾动脉栓塞术分别为4例(8.9%)和1例(2.2%)。初始单独药物干预15例,其中卡维地络14例;7例因用药时间未超过1周归为对照组。停药原因包括:普奈洛尔1例,用药后出现低血压表现;卡维地洛6例,2例未遵医嘱自行停药,2例腹泻,1例皮疹,1例低血压。余9例卡维地络预防患者用药至结局事件或研究截至日期未出现药物相关不良事件,维持剂量为(10±2.17)mg(5~12.5 mg)。29例内镜干预均行食管静脉曲张套扎治疗,次数为(1.93±1.16)次(1~5次);4例在随访中行1次硬化剂治疗。合并胃静脉曲张25例,18例行组织黏合剂治疗,次数为(1.56±0.78)次(1~3次)。内镜治疗患者均未出现治疗后急性感染、急性出血、异位栓塞等内镜治疗相关不良事件。药物联合内镜治疗的2例,1例为单纯食管静脉曲张,普奈洛尔维持剂量为10 mg/d,联合1次套扎和2次硬化剂注射治疗;1例为GOV,普奈洛尔维持剂量为30 mg/d,联合3次套扎治疗,均未出现治疗相关不良事件。4例脾切除联合贲门周围血管离断术和1例脾动脉栓塞术的患者随访至研究终点未出现治疗相关不良事件。
对照组的50例患者,在入院时合并肝癌、肝性脑病、广泛门静脉系统血栓和其他需转科治疗的疾病17例(34.0%);存在NSBB禁忌证、出现用药后不良事件,且内镜评估认为暂不适宜内镜治疗7例(14.0%);药物不适宜且拒绝内镜预防3例(6.0%);医师至少未提及一种预防措施21例(42.0%)。我们通过电话随访告知对照组患者未干预的风险、干预的必要性,而随访至结局事件或研究截至日期,未有患者进行治疗转换。
2.3主要结局:静脉曲张破裂出血对照组15例(30.0%)出血,出血6周内死亡3例(20.0%);干预组2例(4.4%)出血,无出血死亡;两组的出血率用Log-Rank检验比较,差异有统计学意义(P=0.001)。干预组较对照组6个月、12个月、18个月和24个月的未出血率依次增加3.7%、11.1%、23.1%和30.2%(见图1)。由于Child分级、食管静脉曲张严重程度在两组间存在差异,我们进一步对影响出血的因素进行了Cox回归单因素分析,将P<0.2的因素应用Cox回归后退法进行多因素分析。最终得出,干预是出血的保护因素(HR=0.105,95%CI:0.024~0.464,P=0.003),合并胃静脉曲张(HR=4.282,95%CI:0.971~18.891,P=0.055)是出血的独立危险因素(见表2)。
2.4次要结局对照组和干预组分别死亡11例(22.0%)和2例(4.4%),Log-Rank检验两组差异有统计学意义(P=0.011),干预组较对照组6个月、12个月、18个月和24个月死亡率依次减少8.8%、8.4%、11.5%和19.4%。其中对照组出血死亡3例,肝癌死亡4例,其他肝病相关死亡2例,肾衰死亡1例,原因不详1例;干预组2例均因肝癌死亡。按Child分级或静脉曲张严重程度分层分析后,各层的干预组与对照组死亡率差异无统计学意义。对照组和干预组的出血死亡率Log-Rank检验差异有统计学意义(P=0.043),对照组6个月、12个月、18个月和24个月的出血死亡率依次为2.2%、2.2%、6.2%和10.7%。
干预组新发肝癌2例,均未出血,其中1例因肝癌死亡;对照组1例新发肝性脑病,未出血,最终因肝衰竭、肝昏迷死亡。
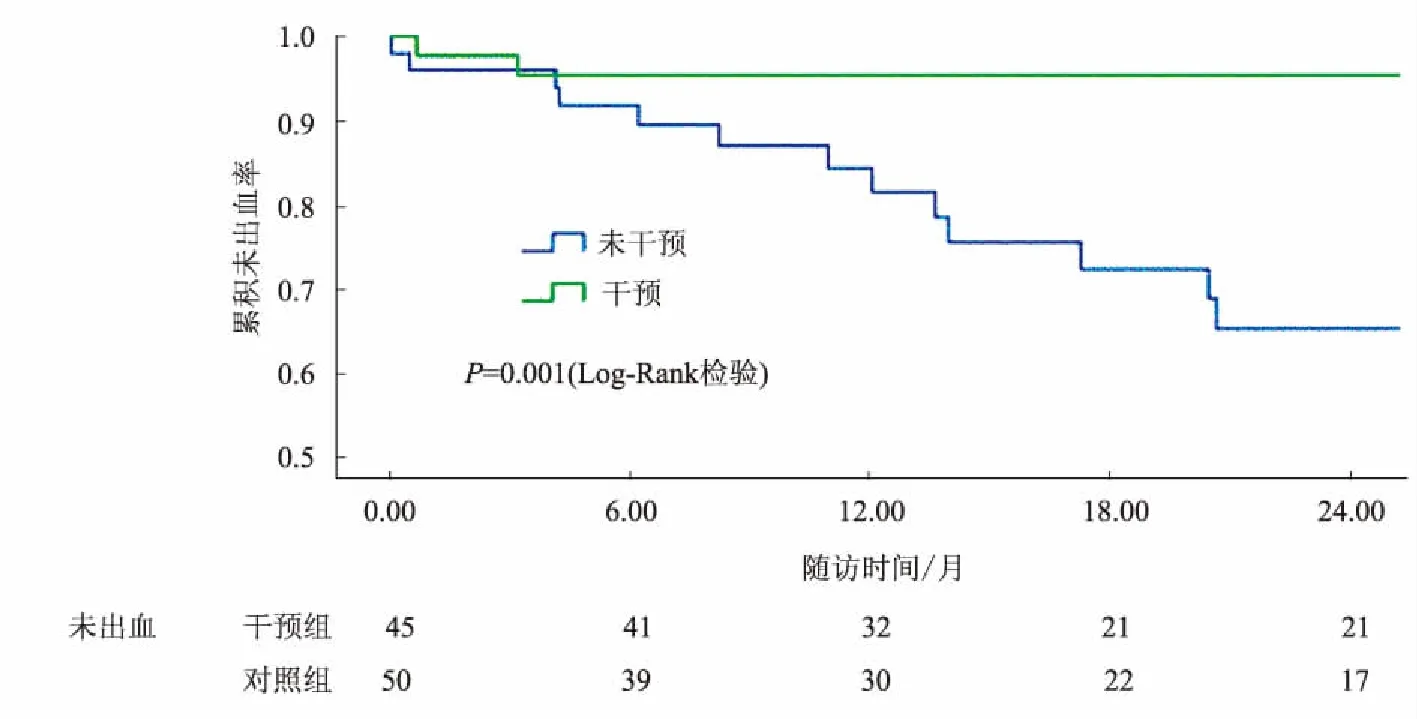
图1 干预组与对照组出血率比较

表2 中-大食管静脉曲张首次出血单因素和多因素分析Tab 2 Univariate and multivariate analysis of first bleeding in patients with large esophageal varices
注:运用Cox回归分析进行出血危险因素分析。单因素分析中P<0.2的干预、门脉血栓、胃静脉曲张、Child分级和HGB纳入多因素分析,应用Cox回归后退法,门脉血栓、Child分级和HGB失去统计学意义,最后留在方程中的为干预和胃静脉曲张。
3 讨论
药物/内镜干预较未干预在小静脉曲张、大静脉曲张和不分大小的食管静脉曲张中的2年出血率分别减少5%、16%和10%[5]。指南推荐对高危食管静脉曲张进行一级预防已有多年。2015年Baveno Ⅵ[3]推荐对小食管静脉曲张伴出血高危因素(红色征或Child-Pugh C级)或中-大食管静脉曲张(伴或不伴高危因素)进行NSBB或EBL治疗。NSBB通过阻断β1受体减少心脏输出和阻断β2受体增加血管收缩,从而减少门静脉血流、降低门静脉压力;卡维地洛同时作用于β受体和α1受体,较传统的NSBB(普奈洛尔或纳多洛尔)在降低门静脉压力方面可能有更好的效果[6-7]。基础血压低、支气管哮喘、难治性腹水[8]、自发性腹膜炎[9]等限制了NSBB的使用。对于无法耐受NSBB的中-大食管静脉曲张推荐EBL。EBL通过阻断曲张静脉血流从而达到减少出血风险的目的。一篇关注大静脉曲张伴高危出血风险因素人群的Meta分析[10]表明,EBL在降低出血率方面可能优于NSBB(HR=0.69,95%CI:0.52~0.91,P<0.01)。EBL的严重不良反应如溃疡、疼痛、食管狭窄或穿孔等,可能限制了其在临床的开展。同时,经济因素和地区医疗水平差异也是限制患者内镜预防的重要因素。国内外指南[1,3-4]均不推荐外科或介入断流/分流手术进行一级预防,因其增加了不良事件的发生反而降低了生存率;不推荐药物联合内镜治疗,因其无更好的获益反而增加了不良反应的发生[11]。
本研究描述了我院临床实践中的一级预防现状。2012年至2015年入组患者57例,共干预22例;2016年前瞻性收集38例,共干预23例;干预率从38.6%上升至60.5%,但肝硬化高危食管静脉曲张患者中实际出血预防率仍然较低。同期有72.8%的肝硬化患者并未进行静脉曲张评估,实际的未干预率和出血率将远远高于本研究的结果。对照组中,34%的患者合并新发肝癌、肝性脑病、广泛血栓或其他需转科治疗的疾病,14%的患者对NSBB和内镜治疗均存在顾虑,6%的患者存在NSBB禁忌证,同时拒绝内镜治疗,42%的患者在初次入院时并未接受全面的一级预防宣教。在此后的电话随访中,即便告知了对照组患者未干预的风险、一级预防的必要性,仍无患者进行一级预防。我们认为,临床医师对肝硬化伴高危食管静脉曲张患者的一级预防宣教不到位,患者对一级预防的重视程度低和治疗顾虑是影响一级预防的主要因素。而对合并肝癌、肝性脑病、门脉广泛血栓等疾病,NSBB和内镜治疗均不适宜的静脉曲张,首次出血预防的时机和方法值得进一步思考和探讨。
干预组中,以NSBB和内镜治疗为主。而在初始NSBB治疗的15例中,40%的患者因低血压(2例)、腹泻(2例)、皮疹(1例)和依从性差(2例)在1周内停药。内镜治疗的29例患者,食管静脉曲张以套扎为主,13.8%的患者在随访中曾行硬化剂治疗。尽管指南不推荐,本研究中仍有2例进行了NSBB和内镜联合治疗;4例进行了脾切除联合贲门周围血管离断术,1例进行了脾动脉栓塞术。
干预可降低中-大食管静脉曲张患者出血风险。积极干预较未干预患者的6个月、12个月、18个月和24个月的出血率分别减少3.7%、11.1%、23.1%和30.2%;而1999年D’AMICO等的研究[5]表明,NSBB组较未干预组的24个月出血率减少16%。本研究中出血患者6周死亡率为20%,与STOKKELAND等[12]的研究相符。而在干预患者中24个月出血率为4.5%,低于国外报道的单独药物或内镜预防的出血率(10%~30%)[6,13],这可能和随访时间较短、干预组纳入了外科/介入/内镜联合药物治疗的患者有关。
对出血的多因素分析时,合并胃静脉曲张是中-大食管静脉曲张出血的独立危险因素。本研究由于病例数和出血事件较少,未进一步分析不同干预措施对出血和死亡的影响。目前对胃静脉曲张出血是否进行一级预防、如何进行一级预防的临床研究较少。MISHRA等的研究[14]表明,对大的胃静脉曲张(直径>5 cm)的出血预防,组织黏合剂治疗可能较NSBB有效。
本研究首次描述了在中国临床实践中肝硬化高危食管静脉曲张患者一级预防现状,肝硬化高危食管静脉曲张的一级预防比例较低,合并胃静脉曲张是首次出血的独立风险因素之一,主动干预明显减少高危食管静脉曲张患者首次出血风险和死亡率。再次重申了干预对预防静脉曲张出血的重要性和必要性,为今后一级预防的健康教育和卫生决策提供了依据。

