小剂量沙利度胺预防宫颈癌放疗所致急性放射性肠炎的临床观察
程奇乐 王年飞 孙 彤 张明军 轩 菡 陈振东
放射性肠炎(radiation enteritis,RE)是腹盆腔及腹膜后恶性肿瘤接受放疗引起的常见肠道并发症。根据发病时间、病情缓急不同,放射性肠炎分为急性和慢性,急性放射性肠炎(acute radiation enteritis,ARE)常出现在放疗期间或放疗后2个月内,主要表现为腹泻、腹痛、黏液便、脓血便、里急后重感等。长期腹泻不仅导致患者电解质紊乱、体液丢失,还常迫使放疗中断、化疗药物减量,最终影响抗肿瘤效果。然而目前临床上针对ARE尚无统一的治疗方案,一般在患者出现症状后给予对症处理,如中药灌肠[1],虽有一定疗效,但ARE的出现对患者仍有较大影响,因此预防ARE的发生尤为重要。沙利度胺是一种消旋体谷氨酸衍生物,起初广泛用于治疗妊娠期呕吐,后因严重的致畸事件被禁用。近年来发现了其抗血管生成、免疫调节和抗炎等作用[2]。沙利度胺能够改善放疗辐射引起的炎性损伤[3],但目前国内外相关临床研究报道甚少。为探索沙利度胺能否预防宫颈癌放疗所致ARE,安徽医科大学第二附属医院肿瘤中心设计了本试验,观察其有效性及安全性,现报道如下。
1 资料与方法
1.1 一般资料 选择2016年1月至2017年8月在安徽医科大学第二附属医院肿瘤中心行同步放化疗的宫颈癌患者,共纳入71例,完成标准治疗69例。按照入院顺序,将患者随机分为试验组(34例)与对照组(35例)。两组患者年龄、分期、KPS评分、外照射CTV剂量等参数比较,差异无统计学意义(P>0.05)。见表1。

表1 两组患者一般资料比较
1.2 纳入标准与排除标准 纳入标准:①经病理证实为宫颈鳞癌;②临床分期为IIB~IVA期,采用FIGO 2009分期标准[4];③年龄为18~80岁;④预计生存时间>3个月者;⑤KPS评分≥70分;⑥治疗前血常规、肝肾功能、心电图等检查无明显异常;⑦依从性好,能够完成放化疗;⑧知情同意并签署知情同意书。排除标准:①存在胃肠道疾病患者;②沙利度胺过敏者;③神经精神系统异常者;④妊娠及哺乳期妇女;⑤新近发生血栓事件的患者。
1.3 治疗方法
1.3.1 放射治疗 放疗定位:所有患者定位前1 h排空直肠和膀胱,然后饮水憋尿充盈膀胱,取仰卧位,体膜固定后行CT扫描,范围从L1水平至坐骨结节下缘,扫描后图像传输至XIO计划系统进行靶区勾画。靶区勾画:临床靶区(clinical target volume,CTV)由同一医师勾画,CTV包括子宫、宫颈、肿瘤、阴道上1/3~1/2以及盆腔淋巴引流区,包括左右髂总血管、宫旁、骶前、闭孔的淋巴结区域,无腹主动脉旁淋巴结转移者,上界到L4之间,下界到闭孔下缘。计划靶区(planning target volume,PTV)根据安徽医科大学第二附属医院肿瘤中心实测摆位及系统误差在CTV的基础上外放5 mm。周围危及器官包括直肠、膀胱、股骨头和小肠,直肠勾画包括直肠壁和内腔,膀胱勾画包括整个膀胱壁和内腔,小肠勾画包括PTV 最上层面上10 mm范围内的所有小肠袢和肠系膜。由同一物理师采用XIO计划系统对患者设计逆向IMRT计划,处方剂量95% PTV 4 500~5 000 cGy/25 f/5 w,IMRT计划剂量约束条件相同,均采用6 MV-X线9野静态IMRT方式照射,入射方向为:0、40、80、120、160、200、 240、280和320°,准直器角度均为0°,根据射野强度分别进行剂量优化。外照射剂量达到3 000 cGy后开始后装治疗。外照射危及器官的限制:直肠V50<40%或V40<50%,膀胱V50<50%,股骨头V50<5%,小肠V50<10%。腔内照射:两组患均采用192Ir后装治疗机,根据患者的宫腔深度、两侧阴道深度及宫颈口外肿瘤的具体情况设计个性化的施源器大小,所有患者采用纱布条填塞前后阴道,X线模拟定位机摄取正交X线定位,腔内后装治疗每周1次,治疗当日不进行外照射,A点剂量为3 000 cGy/5f。
1.3.2 化学治疗 放疗期间两组患者均同步给予含顺铂方案化疗,具体为:顺铂 20 mg/m2,加入生理盐水250 mL,静脉滴注,第1~5天;亚叶酸钙 200 mg/m2,加入250 mL,静脉滴注2 h,第1~5天;5-氟尿嘧啶 375 mg/m2,加入生理盐水500 mL,静脉滴注3 h,第1~5天。每4周为1疗程。
1.3.3 沙利度胺治疗 试验组患者于放疗第1天开始,每晚睡前顿服沙利度胺(常州制药厂有限公司) 50 mg,直至放疗结束。
1.3.4 对症治疗及需要中断治疗的情况 两组患者均在出现II级ARE时接受洛哌丁胺(初始剂量4 mg,随后每隔4 h给药2 mg)+地塞米松(地塞米松5 mg加入盐水100 mL,静脉滴注,每天1次)直至腹泻缓解,必要时使用镇痛药,同时行大便常规检查,如提示白细胞阳性,则给予抗感染治疗;出现III级及以上ARE,则中断放疗并给予挽救治疗,包括止泻、静脉补液等。同步化疗期间两组患者均给予相应止吐处理(昂丹司琼 8 mg加入100 mL生理盐水中,每天1次;胃复安 10 mg,口服,每天3次)。两组患者放疗期间出现下列任意情况即中断治疗:①KPS评分≤60分;②III~IV级血液毒性(中性粒细胞计数<1.0×109/L或血小板计数<50.0×109/L);③III~IV级ARE。
1.4 观察指标 观察两组患者放疗期间及放疗后2个月内ARE的发生率及严重程度、ARE的发生时间、放疗中断情况、化疗期间恶心呕吐情况以及不良反应,包括骨髓抑制、便秘、皮疹、乏力、嗜睡、头晕头痛、厌食、周围神经炎等。
1.5 评价标准 根据美国肿瘤放射治疗协作组织急性放射损伤分级标准对急性肠道反应进行分级[5]:①0级无变化;②I级排便次数增多或排便习惯改变或直肠不适,无需用药;③II级腹泻,需用抗副交感神经药,直肠或腹部疼痛需镇痛药;④III级腹泻,需肠胃外支持,重度黏液或血性分泌物增多;⑤IV级急性或亚急性肠梗阻,瘘或穿孔,胃肠道出血需输血,腹痛或里急后重需置管减压,肠扭转。按照美国国立癌症研究所常见不良反应术语标准V3.0 对各种不良反应进行分级[6]。
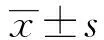
2 结果
2.1 两组患者放疗期间及放疗结束后ARE比较 放疗期间,试验组患者I~II级ARE的发生率(29.41%)低于对照组(62.86%),差异有统计学意义(P<0.05)。放疗结束后2个月内,试验组与对照组I~II级ARE的发生率分别为8.82%和14.29%,差异无统计学意义(P>0.05)。两组患者均未发生III、IV级ARE,未见放疗中断。见表2。
2.2 两组患者ARE发生时间比较 试验组患者发生ARE的平均时间为(24.00±4.16)d,对照组为(16.59±5.34)d,两组差异有统计学意义(t=3.872,P=0.001)。
2.3 两组患者化疗期间恶心呕吐发生情况的比较 化疗第3、4、5天试验组患者恶心发生率低于对照组,呕吐发生率低于对照组,差异均有统计学意义(P<0.05);而化疗第1、2天,两组患者的恶心、呕吐发生率差异无统计学意义(P>0.05)。见表3。

表2 两组患者放疗期间及放疗后ARE分级比较[例(%)]

表3 两组患者化疗期间恶心呕吐发生情况比较[例(%)]
2.4 两组患者不良反应情况比较 两组患者主要不良反应有白细胞减少、便秘、皮疹、乏力、头晕头痛,均无因严重不良反应而终止放疗。试验组患者嗜睡发生率为50.00%,厌食发生率为14.71%,试验组睡眠、食欲优于对照组,差异有统计学意义(P<0.05)。见表4。
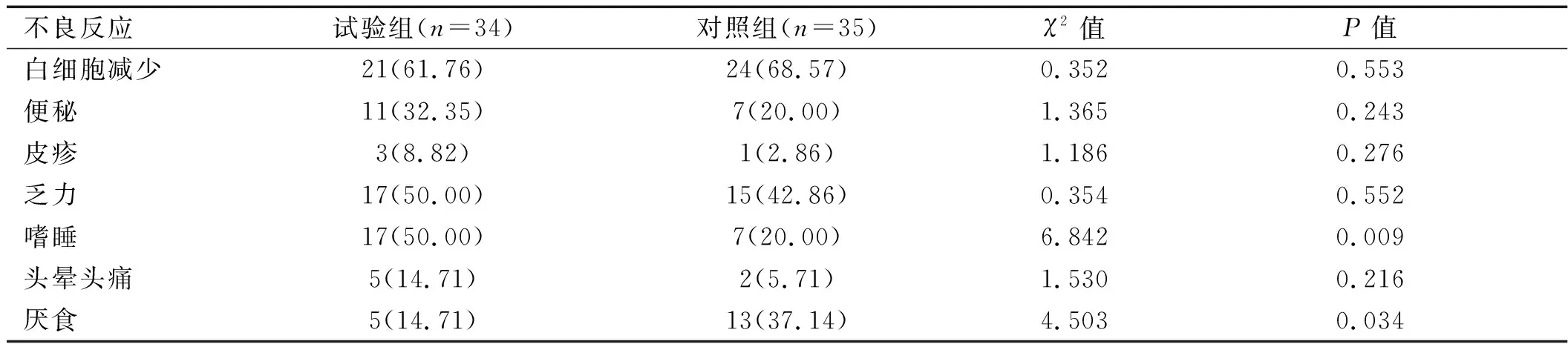
表4 两组患者不良反应发生情况比较[例(%)]
3 讨论
宫颈癌是女性生殖系统最常见的恶性肿瘤。2012年全球宫颈癌发病人数为528 000,死亡人数为266 000[7],其中85%在发展中国家。2015年中国宫颈癌发病率达到98.9/10万,病死率达30.5/10万[8]。一般情况下,早期宫颈癌的治疗以手术切除为主,局部晚期(IIB~IVA期)推荐同步放化疗作为其标准治疗方案。
盆腔放疗引起ARE的发生率可达40%~80%,各研究结果不一[9-10]。Hafiz等[11]研究发现ARE的发生率为55.56%,其中I级52.52%,II级3.03%。本研究中,对照组患者放疗期间I~II级ARE的发生率为62.86%,无III、IV级ARE的发生,与上述报道大致相仿。Krusun等[12]发现在放疗中断的患者中,15%的患者与ARE有关。随着放疗技术的发展,调强放疗技术(intensity modulated radiation therapy,IMRT)逐渐取代了传统的外照射技术,其在给予病灶较高照射量的同时可明显减少小肠、直肠等正常组织的受照射体积,降低不良反应的发生率。在本研究中,未出现与ARE有关的放疗中断,原因可能为IMRT的应用减轻了肠道的放射损伤。ARE的发生与放射线对肠道微血管及肠壁细胞的损伤有关[13]。肠道微血管损伤导致正常肠黏膜上皮面积减少,引起胆盐、脂肪代谢障碍及碳水化合物、蛋白质和维生素等吸收障碍。肠壁细胞的损伤引起促炎性因子如肿瘤坏死因子(tumor necrosis factor,TNF-α)等的释放,炎性反应的瀑布效应进一步加重肠壁细胞的损伤[14]。因此,TNF-α等炎症因子在ARE的发生发展中起着重要作用。研究[15]发现沙利度胺能够抑制TNF-α的生成,临床上已将沙利度胺用于治疗炎性肠病。基于上述研究,本试验在宫颈癌放疗期间应用小剂量沙利度胺来预防ARE的发生,结果发现其能够降低放疗期间I~II级ARE的发生率,与于娇等[16]研究结果相似。另外,本研究发现沙利度胺能够推迟ARE的发生时间,这对于提高患者的治疗耐受性有积极作用。
化疗引起的恶心呕吐是高致吐药物(顺铂)化疗引起的最常见副作用,通常认为化疗当天出现的恶心呕吐为急性恶心呕吐,化疗第2天开始出现的恶心呕吐为延迟性恶心呕吐。沙利度胺能够预防化疗引起的延迟性恶心、呕吐[17],本研究中,试验组化疗第3、4、5天沙利度胺组恶心、呕吐发生率低于对照组,提示沙利度胺能够减轻化疗引起的延迟性恶心、呕吐。沙利度胺的常见副作用有便秘、乏力、头晕头痛、嗜睡、周围神经病变、皮疹以及深静脉血栓形成等,其不良反应与剂量有关。在本研究中,沙利度胺的剂量为50 mg/d,观察到的主要不良反应有白细胞减少、便秘、乏力、嗜睡,均为轻度,对治疗未造成影响,提示小剂量沙利度胺相对安全。本研究发现试验组患者食欲、睡眠均得到改善,原因可能为沙利度胺可通过降低TNF-α、IL-6的产生而改善食欲,增加体质量[18]。
综上所述,沙利度胺能够降低患者放疗过程中ARE的发生率,推迟ARE的发生时间,并能改善肿瘤患者的食欲、睡眠状况,对化疗引起的胃肠道反应也有积极作用,在一定程度上提高了患者的治疗耐受性和依从性,但本研究样本量较小、随访时间短,最佳剂量和对患者的长期影响尚不确定,值得临床进一步推广及更深入地研究。

