单侧肺动脉缺如影像学7例分析
陈国良 靳永强 张福强 吴清玉
单侧肺动脉缺如(unilateral absence of pulmonary artery,UAPA)是极为罕见的先天性心脏病,单纯性UAPA在成年人发生率为200 000至300 000之一[1-2]。截止至2011年,文献报道的UAPA患者共有352例,约60%的UAPA可合并其他先天性畸形,法洛四联症为最常见的先天畸形[3-5]。临床表现为患侧心包内肺动脉完全缺失,对侧肺动脉连接主肺动脉,患侧肺的血供多来源于支气管动脉的代偿性扩张,但来源于肋间动脉、膈下动脉、锁骨下动脉甚至冠状动脉来源的侧枝血管均有报道[6-7]。
本研究总结UAPA患者的影像学特点,结合胚胎学发育理论,探讨UAPA形成原因。
资料与方法
1.临床资料 2011年6月 至2016年12月,我院共收治的UAPA患者共7例,男性6例,女性1例,年龄在3个月~16岁。经超声心动图、CT或心导管造影检查确诊,所有病例均有X线平片、心电图、超声心动图及详细临床资料。
2.心导管造影术 心导管造影采用Philip公司双C臂X线诊断仪,常规穿刺股动、静脉行右心室坐观位及升主动脉正侧位造影。心室及主动脉造影采用高压注射器注入造影剂,婴幼儿和儿童1.0~1.5mL/kg,1.2~1.5s内注入;14 岁以上患者心室造影25~35 mL/次,主动脉造影20~25mL/次,流速14~15mL/s。选择性侧支血管造影以手推方式注入造影剂。
3.心脏CT CT检查采用Philip 64排螺旋CT机,使用造影剂增强横断面扫描(1~2mL/kg),具体扫描参数:管电压 80~120kV,管电流 120~200mA,层厚0.625 mm。心血管扫描图像在GE AW 4.2工作站上作最大密度投影(MIP)、多平面重建(MPR)及容积重建(VR)。
结 果
1.合并畸形 在7个研究对象中,合并动脉导管未闭(patent ductus arteriosus,PDA)患者 2例,合并室间隔缺损1例,合并房间隔缺损、PDA 1例,合并法洛氏四联症1例,合并右心室双出口、肺动脉狭窄1例,合并肺动脉闭锁、室间隔缺损、PDA 1例。其中合并PDA患者动脉导管均连接正常侧肺动脉(表1)。
2.主动脉弓 左位主动脉弓4例,其中2例为左侧肺动脉缺如,2例为右侧肺动脉缺如;右位主动脉弓3例,均为左肺动脉缺如。
3.患侧肺组织血供 病例5纵膈无明显偏移,患侧肺血轻度增加,其余病例纵膈均向患侧偏移,患侧胸廓较对侧略小,透亮度稍减低,肺纹理模糊。
病例5患侧肺血供由2条粗大体肺侧枝供应,由降主动脉发出,分别供应左上肺及下肺,左上肺及下肺动脉在肺门部无交通。2条侧枝均无明显狭窄,直径分别为4mm及7mm,肺动脉压力与主动脉压力一致。肺内动脉分支正常无明显器质性肺动脉高压表现。其余病例均由支气管动脉、肋间动脉及胸廓内动脉发出细小体肺侧枝供应部分肺组织。

表1 7例UAPA患者的临床资料
讨 论
肺动脉系统的不同部位其胚胎学来源不同。主肺动脉来源于主肺间隔的形成将动脉干的分隔为主动脉及肺动脉,肺内动脉分支起源于肺芽(肺血管团),左、右肺动脉则由第六对动脉弓近端发育而来,其中第6对动脉弓的近端发育为左右肺动脉连接主肺动脉及肺门部肺动脉,第6对动脉弓的远端形成动脉导管连接主动脉及同侧肺动脉[8-9]。UAPA被认为是一侧第六对动脉近端未发育或异常退化使同侧肺动脉未发育,导致第六对动脉弓远端与肺门部肺动脉直接相连,即动脉导管与肺门部肺动脉相连供应同侧肺组织血供。对侧第六对动脉弓近端及远端发育正常,即主肺动脉延续为对侧肺动脉并与动脉导管相连[6](图 1)。
出生后,若动脉导管功能或解剖闭合,同侧肺动脉失去血液供应,肺动脉逐渐萎缩,甚至肺血管床数量减少,临床表现为患侧肺发育不良,肺容积减少,纵膈偏移。文献中报道的UAPA病例,在满意的血管造影、手术探查或尸检的情况下均能发现动脉导管或动脉韧带与患侧肺门部肺动脉相连[8,10]。患侧肺组织血供由细小体肺侧枝供应,这些细小侧枝作为滋养血管供应远端肺动脉(图2)。与胚胎期形成的粗大体肺侧枝不同,细小体肺侧枝为后天获得性的,主要因局部肺组织血供减少或严重发绀导致的[11]。
胚胎早期第六对动脉弓远端分别发育为双侧的动脉导管,其中与主动脉弓同侧的导管起源于主动脉弓降部,与主动脉弓对侧的导管起源于无名动脉或锁骨下动脉根部。多数情况下均为主动脉弓对侧导管退化,表现为动脉导管自主动脉弓降部发出,但某些情况也可出现主动脉弓同侧导管退化,对侧导管发育表现为动脉导管起自无名动脉或锁骨下动脉根部[12]。本组7例患者中有5例均表现为主动脉弓对侧肺动脉缺如,同侧肺动脉发育正常,但缺如侧肺动脉是否与主动脉位置相关还需进一步扩大样本量来验证。

图1 右心室造影示左肺动脉缺如;
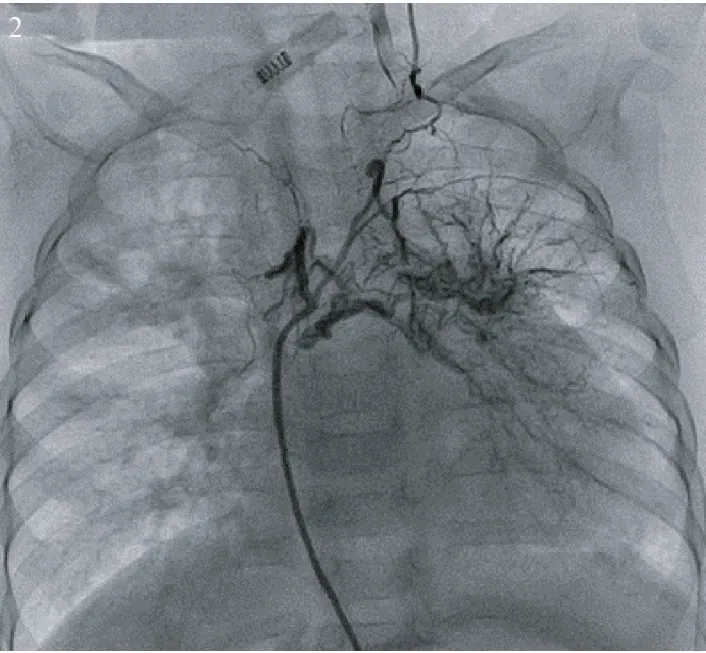
图2 降主动脉发出细小体肺侧枝,发出多支分支供应部分左肺

图3 心脏CT示左肺动脉缺如,动脉导管连接右肺动脉,两条粗大体肺侧枝起源于降主动脉,供应整个左肺血供;
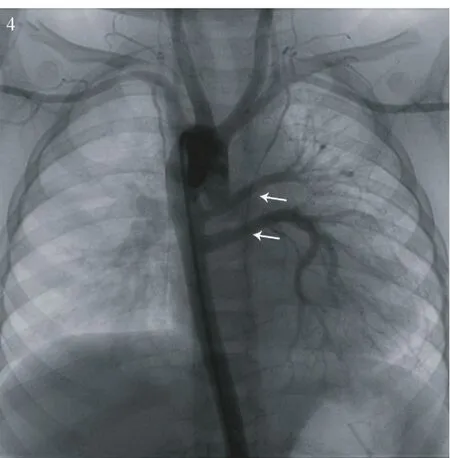
图4 降主动脉造影示2条粗大体肺侧枝起源于降主动脉,分别供应左上及左下肺,远端肺动脉分支正常,无明显器质性肺动脉高压表现。“△”示动脉导管未闭,“←”示粗大体肺侧枝
病例5(图3~4)与文献报道的UAPA主要有以下不同:①患侧肺组织无明显减小,纵膈并无明显移位,肺血轻度增多。②患儿肺血由两条粗大体肺侧枝供应,肺门部肺动脉分支异常,③锁骨下动脉根部未见动脉导管残端。④无细小体肺侧枝形成。从胚胎学角度来讲,此例UAPA患者与文献报道的病例的胚胎学机制不同。在胚胎发育早期,在第六对血管弓发育之前,原始的肺血管团通过节间动脉与降主动脉相连,保证原始肺组织的血供,当第六对动脉弓远端即动脉导管发育后,节间动脉退化、消失。当第六对动脉弓远端未能发育时,节间动脉保留连接体循环和肺循环,即体肺侧枝形成[13-14]。我们认为此患者的胚胎学机制为:右侧第六对动脉弓近端及远端发育均正常,形成动脉导管连接右肺动脉,而左侧第六对动脉弓近端及远端均未发育或早期退化,左肺保留与节间动脉的连接。因此,粗大体肺侧枝形成供应左肺血供,无左肺动脉及动脉导管形成。
总之,第六对动脉弓病变的范围决定了UAPA的临床表现形式。当一侧第六对动脉弓的近端及远端均未发育,临床表现为粗大体肺侧枝形成供应患侧肺血供。此类UAPA极为罕见,本病例是国内外文献的首次报道。当一侧第六对动脉弓的近端未发育或早期退化,动脉导管与肺门部肺动脉直接相连,出生后动脉导管一旦闭合,患侧肺失去血供临床上即表现为UAPA,细小体肺侧枝逐渐形成,供应部分患侧肺血供。

