622型三元正极材料的制备及其电化学性能
夏志美,陈 浩,肖 利,刘鹏程
622型三元正极材料的制备及其电化学性能
夏志美,陈 浩,肖 利,刘鹏程
(湖南工业大学冶金与材料工程学院,湖南 株洲 412007)
将622型前驱体与0.24 Li2CO3-0.76 LiOH锂盐体系、氯化钾熔盐混合,在通空气气氛中采用熔盐法制备了622型三元电池正极材料(LNCM),采用XRD和SEM表征考察了锂源和钾盐的比例及焙烧温度和时间对LNCM晶体结构的影响,得出最佳制备条件为:锂源与钾盐1∶5,前驱体和锂源1∶1.1,焙烧温度为750 ℃,焙烧时间为15 h。将LNCM作为正极材料组装成扣式电池,对其进行了多项电化学性能指标测试,结果表明该材料在2.7~4.3 V内,0.1 C放电倍率下,具有182.5 mA·h/g首次放电容量,库仑效率为89.1%;在2.7~4.5 V,0.1 C条件下循环100圈后容量仍有183.2 mA·h/g,容量保持率为91.5%。
622型前驱体;LNCM;熔盐法;晶体结构;电化学性能
目前电池的正极材料多以LiNiO2、LiCoO2、LiMn2O4等材料组成,因这些材料的实际比容量和热稳定性都很难满足大功率动力电池的需要,人们对高容量、高电压的正极材料的寻找变得更加迫 切[1]。镍钴锰三元材料Li[NiCoMn]O2是近年来开发的一类锂离子电池正极材料,较好地结合了LiCoO2、LiNiO2和LiMnO2三种材料的优点,具有循环性能好、生产成本较低、容量较高等优势,且与钴酸锂材料的放电平台十分接近,可以应用于市场上的很多电子产品中,已经成为市场上应用最广泛的正极材料[2]。按照过渡金属离子相对含量的不同,分为111、424、523、622、811型。
镍钴锰三元正极材料的制备工艺与材料的结构、形貌和电化学性能有很大的关系,学者们研究出了多种合成方法,DENG等[3]以NaOH为沉淀剂、氨水为络合剂在0 ℃下搅拌9 h得到前驱体,然后与LiOH混合焙烧得到LiNi1/3Co1/3Mn1/3O2材料,其首次放电容量可达到172 mA·h/g。YANG等[4]用碳酸盐共沉淀法制备了层状111三元材料,并探讨了4种不同锂源对材料的物理和电化学性能的影响。TAN等[5]使MnO2纳米棒为原料,与NiO、Co2O3、Li2CO3混合研磨,在900 ℃下焙烧得到大倍率充放电性能优异的 LiNi1/3Co1/3Mn1/3O2正极材料。GANGULIBABU等[6]采用玉米粉为凝胶剂和助燃剂通过溶胶-凝胶法制备出了 LiNi1/3Co1/3Mn1/3O2电极材料。GAO等[7]首先以镍钴锰的乙酸盐为原料、柠檬酸为螯合剂,在乙醇溶液中制成凝胶烘干得到前驱体,然后将前驱体与锂源在900 ℃下焙烧24 h 得到性能优异的LiNi1/3Co1/3Mn1/3O2电极材料。SHUI等[8]将乙酸锂和镍钴锰的乙酸盐溶于去离子水中,然后进行喷雾干燥,850 ℃焙烧后得到三元材料,在2.0~4.5 V内,电流密度为0.1 C时其首次放电容量为159.3 mA·h/g。
本文采用熔盐法,将622型前驱体与0.24 Li2CO3-0.76 LiOH锂盐体系混合(二者在此比例下具有最低的共融点,共融点温度是423 ℃),在高温下以熔融盐KCl为助熔剂制备锂电池用三元复合正极材料(LNCM)。相比传统的固相烧结法,熔盐法合成无机粉体材料过程中,低熔点的熔盐能为化学反应提供液相环境,具有较高的离子扩散系数和溶解能力,促使化学反应加速进行,因此较传统固相法合成温度低,产物的结晶度和形貌更好。
1 实 验
1.1 实验材料
实验所用主要材料有622型三元前驱体,由广东佳纳能源科技有限公司提供;碳酸锂(Li2CO3,分析纯,天津市福晨化学试剂厂);氢氧化锂(LiOH·H2O,分析纯,天津市科密欧化学试剂有限公司);氯化钾(KCl,分析纯,湖南汇虹试剂有限公司)。
1.2 正极材料的制备
取622前驱体(100 ℃下干燥3 h)与0.24 Li2CO3-0.76 LiOH锂盐体系、氯化钾熔盐混合,球磨干磨3 h;然后用两段温度焙烧,冷却到室温后,取出样品溶解并用去离子水和乙醇洗涤,直至最后一次滤液中检测不到Cl-为止,再将抽滤后的样品放入100 ℃干燥箱中干燥12 h得到正极材料,将干燥后的样品进行XRD和SEM检测。
将洗净烘干后的铝片正极集流体(铝箔)放在涂布机上,蘸取适量的浆料(正极材料,乙炔黑,黏结剂配比为8∶1∶1)涂布在铝片集流体上,用刮刀刮过得到涂布均匀的三元复合电极,100 ℃真空干燥24 h,然后用切片机获得直径为14 mm的极片后放入手套箱中备用。
1.3 电池的制作
以制备的三元复合电极为正极、锂片为负极(参比电极)、商业用1 mol/L LiPF6/EC+DMC溶液为电解液,在充满氩气的手套箱内,将负极壳、锂片、隔膜片、正极片、垫片、正极壳按顺序装配成扣式电池,进行电化学性能分析。
2 实验结果与分析
2.1 熔盐与锂源的比例对产物结构的影响
取锂源与前驱体的配比为1∶1.1,混合物料先在500 ℃焙烧4 h,再在750 ℃焙烧8 h,研究了熔盐与锂源配比分别为3∶1、4∶1、5∶1对制备的正极材料结构的影响。图1和表1分别是不同熔盐与锂源配比下制备的LNCM的XRD图和(003)及(104)峰的相对强度及比值。

图1 焙烧8 h得到的622型三元正极材料XRD图

表1 不同熔盐比例下焙烧8 h得到的622型三元正极材料(003)和(104)峰强度及比值
从图1可以看出,熔盐与锂源配比对622型三元正极材料的衍射峰强度影响明显。从表中的分析数据可知(003)/(104)峰强的比值大约为1,其峰强比值小于1.2说明三元正极材料中锂镍混排明显[9]。另外(006)/(102)以及(108)/(110)的分峰不明显,所以材料不具有完整的层状结构。从图中无法确定KCl和混合锂盐的最优比例,原因可能是第二阶段的保温时间太短,晶体结构还未完整形成。
为了改善材料的结构,将第二段焙烧时间延长到12 h,此时制备得到的LNCM的XRD如图2所示,(003)及(104)峰的相对强度及比值列于表2。

表2 不同熔盐比例下焙烧12 h得到的622型三元正极材料(003)和(104)的峰强度及比值
结合图2和表2的数据可知第二段焙烧时间从8 h升高到12 h,(104)的峰强度降低,说明锂镍混排程度降低,但是(006)/(102)以及(108)/(110)的分峰还未达到预期目标,再次延长第二段焙烧时间到15 h,不同熔盐与锂源比例下制备的LNCM的XRD如图3所示,(003)及(104)峰的相对强度及比值列于表3。
由表3可知,此时(003)/(104)的峰值比远大于1.2,说明此时三元正极材料中的锂镍混排现象已经完全消失,晶体的结构完整,且熔盐的配比为5∶1时(003)/(104)的峰值比最大,说明其结晶程度最好。

图3 焙烧15 h得到的622型三元正极材料XRD图

表3 不同熔盐比例下焙烧15 h得到的622型三元正极材料(003)和(104)的峰强度及比值
2.2 产物形貌分析
图4是熔盐配比为5∶1,第二阶段焙烧时间为15 h条件下制备的正极材料的不同放大倍率SEM形貌图。
从图4可以看出,熔盐法制备得到的正极材料为类球形的小颗粒,分散性很好,平均粒径约5 μm,其形貌特征明显优于传统固相法制备得到的622型正极材料[10]。

图4 622型正极材料的不同倍数扫描电镜图
2.3 电化学性能分析
2.3.1 充放电测试
为了研究制备得到的正极材料的充放电性能,进行了充放电容量测试,图5是电池在0.1 C倍率下电压区间为2.7~4.3 V的两次充放电曲线图。由图5可知,首次充电容量为充电204.9 mA·h/g,放电容量为182.5 mA·h/g,库仑效率为89.1%;第2次充电容量为198.4 mA·h/g,放电容量为181.3 mA·h/g,库仑效率为91.5%。首次库仑效率较高,不可逆容量较少,说明制备的三元材料结构稳定,嵌脱锂过程可逆性高。
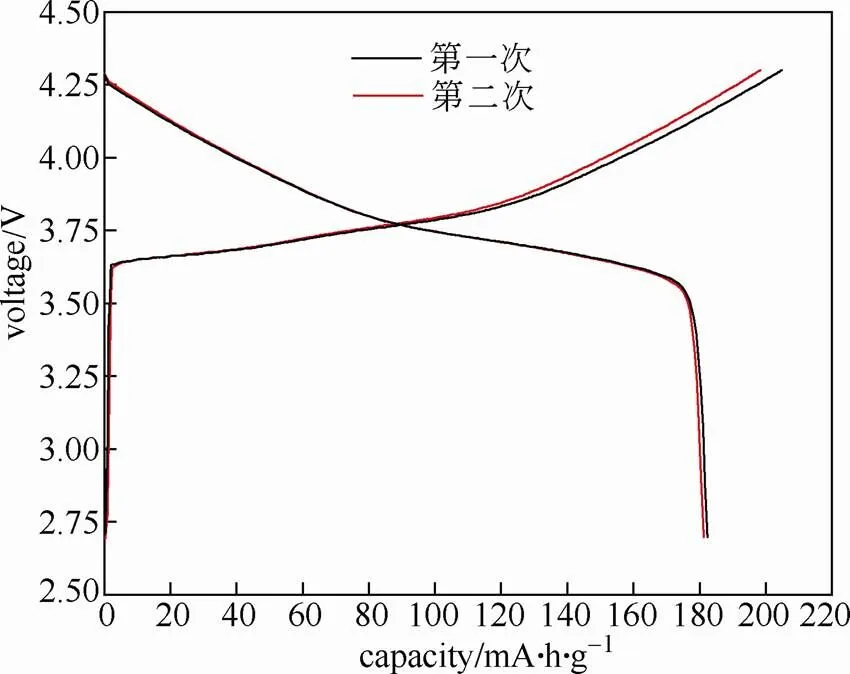
图5 首次、第二次充放电曲线
2.3.2 交流阻抗测试
为了分析制备的622型三元材料的阻抗大小,进行了交流阻抗测试并进行了等效电路模拟,结果如图6所示。
交流阻抗谱包含两部分,高频区的半圆和低频区直线。高频区域是一个与电解液中锂离子通过活性材料颗粒表面SEI 膜扩散迁移相关的半圆;低频区域是锂离子在活性材料颗粒内部的固体扩散过程相关的一条斜线。而半圆于电解质和电极表面的电荷转移电阻有关。图中的第3次循环后电荷转移电阻仅为160 Ω,说明LNCM有较低的电荷转移阻抗,有利于Li+在充放电过程中的嵌入与迁出,随着循环次数的增加,三元材料层状结构坍塌,锂捏混排加剧,阻抗增加。
2.3.3 循环伏安测试
为了判断发生的充放电过程中电极反应的可逆性和极化程度,确定氧化还原反应的数目,在2.5~4.6 V,扫速为0.1 mV/s条件下进行了2次充放电的循环伏安特性测试,结果如图7所示。
从图7可以看出,两次循环在3.9 V和3.8 V左右存在氧化峰,对应着Ni2+氧化成Ni4+和Co3+氧化成Co4+,并伴随着锂离子的脱出反应,在3.7 V左右是还原峰,是锂离子的嵌入反应;从图中还可以看出,两次循环的氧化还原峰之间的电压差分别为0.247 V和0.112 V,说明极化较小,该电池的可逆性和循环性能都比较好。
2.3.4 倍率性能测试
图8为不同电压下的倍率性能曲线。从图中可以看出,2.7~4.5 V的性能最好,在0.1 C、0.2 C、0.5 C、1.0 C、2.0 C倍率下的容量分别为201.1 mA·h/g、185.3 mA·h/g、168.8 mA·h/g、142.7 mA·h/g、116.2 mA·h/g,倍率衰减程度2 C/0.1 C为57.7%。在随着倍率增加,不同电压范围下的比容量都会衰减,这是电极材料的极化作用造成的,极化作用越大其衰减的比例就会越大;不同电压下各循环5次都比较平稳,而高电压下,电池容量最高,且损失比较小,可逆程度高,说明在高电压下充放电有利于获得更高的容量。

图8 倍率性能测试图
2.3.5 循环性能测试
图9是组装的电池在不同电压窗口下0.1 C时循环100次的循环性能测试图。
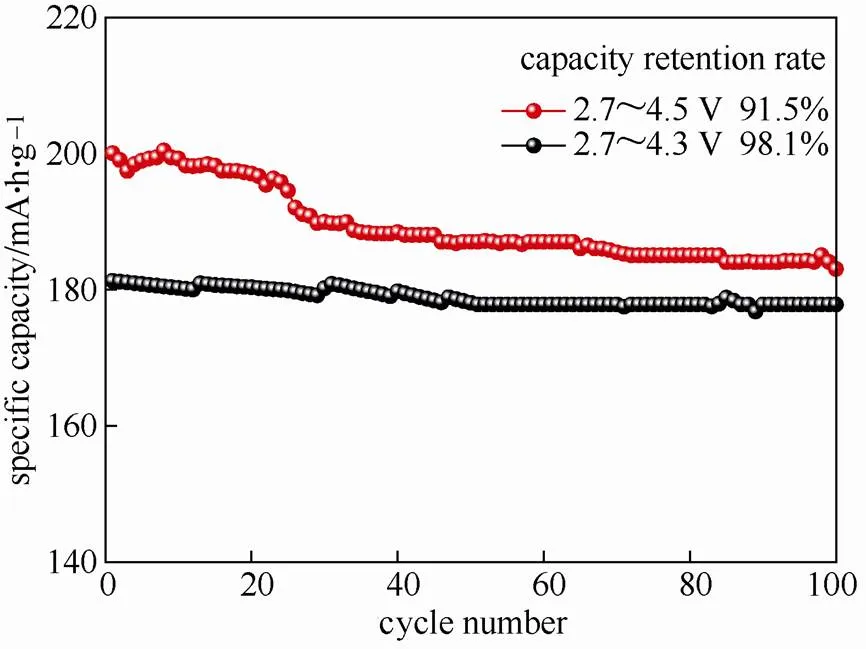
图9 不同电压下循环性能图
从图9可以看出当电压在2.7~4.5 V之间时具有更高的初始放电比容量,循环100次后,电池容量仍有183 mA·h/g,容量保持率为91.5%,但是在循环初期(0~30圈)时,容量衰减很快,这可能是由于在高截至电压(4.5 V)下,材料内部的锂离子脱出量大,导致了结构的不稳定和过渡金属的还原,产生了大量的不可逆容量;在过充条件下,三元材料容易在表面发生层状结构向岩盐结构和尖晶石结构的转变,同时释放氧气,这也是锂离子电池发生热失控的一个重要原因[11]。而在2.7~4.3 V之间时,虽然初始容量只有181.3 mA·h/g,但是循环100次后,电池容量仍然有177.8 mA·h/g,容量保持率有98.1%,说明其结构稳定,锂离子脱嵌的可逆性强。因此,电压范围在2.7~4.3 V时循环性能更佳。
3 结 论
本论文以622型三元电池材料前驱体为原料,采用单一变量的实验方法,考察了熔盐比例、焙烧时间等因素对LNCM晶体结构的影响,获得了最佳制备工艺条件;表征了622型LNCM的物理和电化学性能,得到的结论如下。
(1)LNCM的最佳制备条件为:熔盐比例为5∶1,第二阶段焙烧时间为15 h,温度为750 ℃。此条件下制备的622型LNCM为类球型,平均粒径约5 μm,且具有最佳的物理性能。
(2)材料界面反应阻抗为160 Ω,有利于Li+在充放电过程中的嵌入与迁出;在2.7~4.5 V,0.1 C条件下循环100圈后容量仍有183 mA·h/g,容量保持率为91.5%;在2.7~4.5 V之间时倍率性能最好;LNCM在高截至电压下有较高的电容量,但是低截至电压下循环性能较好。
[1] 周恒辉, 慈云祥, 刘昌炎. 锂离子电池电极材料研究进展[J]. 化学进展, 1998, 10(1): 85-94.
ZHOU H H, CI Y X, LIU C Y. Progress in studies of the electrode materials for Li-ion batteries[J]. Progress in Chemistry, 1998, 10(1): 85-94.
[2] 瞿波, 张冰, 郑胜男, 等. 四大类锂离子电池正极材料进展[J]. 电源技术, 2016, 40(7): 1515-1518.
ZHAI B, ZHANG B, ZHENG S N, et al. Progress of four types of cathode materials for lithium-ion batteries[J]. Chinese Journal of Power Sources, 2016, 40(7): 1515-1518.
[3] DENG C, ZHANG S, FU B L, et al. Synthetic optimization of nanostructured LiNi1/3Co1/3Mn1/3O2cathode material prepared by hydroxide coprecipitation at 273K[J]. Journal of Alloys and Compounds, 2010, 496(1/2): 521-527.
[4] YANG S Y, WANG X Y, YANG X K, et al. Influence of Li source on tap density and high rate cycling performance of spherical LiNi1/3Co1/3Mn1/3O2for advanced lithium-ion batteries[J].Journal Solid State Electrochemistry, 2012, 16(3): 1229-1237.
[5] TAN L, LIU H W. High rate charge-discharge properties of LiNi1/3Co1/3Mn1/3O2synthesized via a low temperature solid-state method[J]. Solid State Ion, 2010, 181(33/34): 1530-1533.
[6] GANGULIBABU, BHUVANESWARI D, KALAISELVI N. Comparison of corn starch-assisted sol-gel and combustion methods to prepare LiMnCoNiO2compounds[J]. Journal Solid State Electrochemistry, 2013, 17(1): 9-17.
[7] GAO P, YANG G, LIU H D, et al. Lithium diffusion behavior and improved high rate capacity of LiNi1/3Co1/3Mn1/3O2as cathode material for lithium batteries[J]. Solid State Ionics, 2012, 207: 50-56.
[8] SHUI M, GAO S, SHU J, et al. LiNi1/3Co1/3Mn1/3O2cathode materials for LIB prepared by spray pyrolysis I: The spectral, structural, and electro-chemical properties[J]. Ionics, 2013, 19(1): 41-46.
[9] CHANG Z R, YU X, TANG H W, et al. Synthesis of LiNi1/3Co1/3Al1/3O2cathode material with eutectic molten salt LiOH-LiNO3[J]. Powder Technology, 2011, 207(1/3): 396-400.
[10] LIANG L W, DU K, PENG ZH D, et al. Co-precipitation synthesis of Ni0.6Co0.2Mn0.2(OH)2precursor and characterization of LiNi0.6Co0.2Mn0.2O2cathode material for secondarylithium batteries[J]. Electrochimica Acta, 2014, 130: 82-89.
[11] HWANG S, CHANG W Y, KIM S M, et al. Investigation of changes in the surface structure of LiNi0.8Co0.15Al0.05O2cathode materials induced by the initial charge[J]. Chemistry of Materials, 2014, 26(2): 1084-1092.
Preparation and electrochemical performance of a type 622 ternary cathode materials
XIA Zhimei, CHEN Hao, XIAO Li, LIU Pengcheng
(College of Metallurgy and Material Engineering, Hunan University of Technology, Zhuzhou 412007, Hunan, China)
A 622-type ternary cathode materials (LNCM) was prepared by using molten salt made from a lithium salt based type-622 precursor, 0.24 Li2CO3-0.76 LiOH and potassium chloride in an air atmosphere.The effects of the ratio of lithium and potash, reaction time and reaction temperature on the crystal structure of the LNCM were investigated by XRD and SEM.The optimum preparation conditions were found to be from a lithium source to potassium salt ration of 1∶5, a precursor to lithium source ratio of 1∶1.1, a reaction temperature of 750 ℃, and a calcination time of 15 hours.LNCM as a cathode material was assembled into a button battery, and a number of electrochemical performance indexes were obtained, e.g. over the 2.7—4.3 V voltage range at 0.1 C rate, the specific capacity of the first discharge cycle was 182.5 mA·h/g, the Coulomb efficiency was 89.1%; over the 2.7—4.5 V voltage range at 0.1 C rate, the discharge specific capacity was 183.2 mA·h/g after 100 cycles, the capacity retention rate was found to be 91.5%.
622 type precursor;LNCM; molten salt method;crystalstructure; electrochemical performance
10.12028/j.issn.2095-4239.2018.0112
TM 911
A
2095-4239(2018)05-921-05
2018-07-02;
2018-08-02。
国家自然科学基金(51774127,51704107),湖南省自然科学基金(2018JJ2091,2018JJ3124)及湖南省重点实验室开放基金(MMA201705)项目。
夏志美(1980—),女,讲师,研究方向为湿法冶金和电化学冶金,E-mail:zhimei_x@163.com;
肖利,教授,研究方向为电化学冶金,E-mail:xiaoli_csu@163.com。

