锂离子电池二氧化锡负极材料研究进展
刘旭燕, 孙 超, 韩艳林, 潘 登
(1. 上海理工大学 机械工程学院,上海 200093;2. 上海理工大学 材料科学与工程学院,上海 200093)
锂离子电池作为一种新型清洁的可充电电源,具有质量轻、污染小、工作电压高、能量密度大、循环寿命长等优点,在国防、电动车和电子领域展示了广阔的应用前景,被誉为21世纪的理想电源,在过去的几十年里引起了越来越多的关注[1]。
负极材料是影响锂离子电池比容量和使用寿命的重要因素之一。目前商品化的锂离子电池主要以石墨或改性石墨作为负极材料,其优点是循环性能和倍率性能较好,但其理论比容量仅为372 mAh/g,很难在电动汽车等高能量密度要求的领域里得到广泛使用。尤其是在能源极其匮乏的时期,研究出一种高能量密度的负极材料来替换碳材料,使锂离子电池得到更加广泛的应用,这也是现代能源需求发展的趋势。近年来,硅基材料、锡基材料、碳材料、过渡族金属等材料,已经成为国内外研究的热点[2-4]。而二氧化锡(SnO2)以其高的理论比容量(782 mAh/g)、储量丰富、成本低、无污染、相对较低的充放电平台等优点,被认为是最理想的用来替换已商业化的石墨材料的负极材料[5]。
1 二氧化锡负极材料丞待解决的问题
自从1997年Fuji公司的研究人员发现无定形锡基复合氧化物(简称TCO)具有较好的循环寿命和较高的可逆比容量以来,氧化锡基材料逐渐引起了人们的广泛关注[6]。虽然SnO2负极材料有很多优点使得它成为有潜力替代石墨的负极材料之一,但是它同时也存在以下3大致命缺陷:a. 充放电时,在锂离子的脱出嵌入过程中体积变化较大,高达300%,这导致了电极在循环过程中会被严重破坏,进而导致比容量快速衰减;b. SnO2本身低电导率降低了电子传递速度,因此限制了锂离子电池的倍率性能;c. 由于首次嵌锂过程中不可逆反应的发生,使得首次库仑效率较低及额外消耗了正极材料。针对以上3大问题,许多研究人员致力于通过设计不同形貌的SnO2纳米材料,或者通过掺杂(碳类材料等)、修饰等方法,来缓解以SnO2为锂离子电池负极材料产生的缺陷。其中不同形貌包括:零维纳米材料,纳米颗粒[7];一维纳米材料,纳米线、纳米棒、纳米管[8];二维纳米材料,纳米片、纳米带[9];三维纳米材料,纳米空心结构等[10]。例如: Kim等[11]合成SnO2粒径约为3 nm的纳米颗粒,首次放电比容量达到740 mAh/g,并且在60次循环后仍保持97%的比容量。Um等[12]将SnO2纳米材料嵌入到泡沫铜中,以此形成三维无定型纳米多孔材料。通过此方法在以0.5 C倍率充放电的条件下循环50次以后仍然获得了可逆比容量为750 mAh/g。另一方面,富碳材料由于其拥有较好的体积变化缓冲能力和导电性能,已经被广泛应用于提高SnO2复合氧化物材料的电化学性能。Paek等[13]利用石墨烯薄片和纳米SnO2纳米颗粒合成纳米多孔电极材料。由于石墨烯薄片不仅能够降低体积的变化,同时也提高了其导电率,从而获得了高达810 mAh/g的可逆比容量[14]。此外,石墨烯纳米片还能在充放电过程中阻止SnO2纳米颗粒的团聚。然而,不管是改变材料的形貌还是掺杂石墨类材料都不能很好地解决锂离子电池首次库仑效率低的问题。因为从Li/SnO2半电池的电化学过程可知:
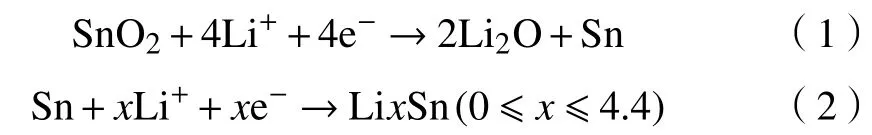
首次库仑效率低是由于首次放电过程中不可逆反应造成的。从反应式(1)可知,1 mol SnO2与4 mol Li+反应生成1 mol Sn原子和2 mol的Li2O。随后1 mol的Sn原子就会与x mol的Li+反应,生成LixSn的合金。在合金化的反应中1 mol的Sn原子最多会消耗掉4.4 mol的Li+,即在首次嵌锂过程中单次最多会消耗掉8.4 mol的Li+。然而由于不可逆反应,至少有4 mol的Li+将不能被利用,这就导致了首次库仑效率低(40%)。因此,要提高首次库仑效率就必须要降低首次充放电过程中不可逆反应的发生。
当然,仅仅提高首次库仑效率也只能在一定程度上改善SnO2为负极材料的缺陷,如果想要整体改善这一缺陷,还需要能够有效缓解体积效应和粉化现象。因此提高电极的循环稳定性和首次库仑效率已成为SnO2负极材料研究的关键,这对于研发新型高性能锂离子电池具有重要意义。目前,研究人员主要通过制备纳米结构SnO2和构建复合材料来解决上述问题。
2 纳米结构材料
2.1 零维纳米材料(0D Nanomaterials)
SnO2纳米颗粒是最早直接应用到锂离子电池的锡基负极材料。后来越来越多的人开始研究更多的方法来更加有效地合成粒径更小、尺寸更均匀的SnO2纳米颗粒材料。例如:热解金属有机前驱体[15]、溶胶凝胶法[16]、氧化SnCl2[17]、超声合成法[18]、水热法[19]等。
SnO2纳米颗粒材料不仅具有较大的比表面积,使其拥有较高的表面能,还能很大程度上缓解SnO2负极材料在充放电过程中的体积变化。因此,许多研究人员利用氧化锡纳米颗粒在相同体积变化率条件下体积变化较小的特点,进行了大量的研究。Shen等[20]以SnCl4·5H2O作为锡源,采用水热法来合成二氧化锡纳米颗粒。在实验过程中,通过调节水热温度和时间来控制合成氧化锡的粒径。水热温度为110 ℃时所合成的粒径为3 nm的SnO2,其纳米颗粒的循环稳定性最佳,并且其比容量也最高。这也很好地证明了当纳米颗粒的粒径足够小时能够有效缓解SnO2负极材料在循环过程中的体积效应。虽然当颗粒尺寸足够小时能够提高锂离子电池的稳定性能,有效缓解体积效应,减少粉化现象,3 nm的SnO2颗粒首次库仑效率仍然较低,这主要是由于纳米SnO2与电解液的副反应造成的不可逆反应。减少不可逆副反应的途径较多,对SnO2纳米材料作表面镀层处理、加添加剂或者对纳米SnO2作掺杂处理(SiO2,Li2O,TiO2等),都可以有效减少副反应的发生。例如,Xu 等[21]以 SnCl2·5H2O 和 Si(OMe)4为原料,通过尿素控制反应的pH值,采用水热法制备出了细小的SnO2·SiO2复合物,使活性物质SnO2很好地分散于非活性物质SiO2中,保持活性成分在原子或纳米尺寸上均匀地分散在非活性成分中。 颗粒尺寸均匀(约30 nm)且分散情况较好,无定型的SiO2的网络结构可以很好地缓解SnO2在充放电过程中粉化脱落的问题。这主要是由于活性材料为纳米SnO2·SiO2颗粒,可以有效改善循环过程中活性粒子间以及活性粒子与电解液之间的电接触,大大缩短了锂离子在电极中的扩散路程,加快了锂离子的扩散速度,使得纳米活性材料具有优良的循环性能。而且材料中的SiO2是惰性的,呈无定型态,没有明显的微粒边界存在,可以更好地容纳活性中心SnO2嵌脱锂时产生的体积变化,从而避免电极产生大的应力和疲劳,延缓和抑制电极的崩裂和粉化,有效抑制电极的比容量衰减。由SnO2·SiO2放电比容量与循环次数的关系曲线可知,其首次放电比容量达到1 208 mAh/g,首次可逆比容量为756 mAh/g,首次库仑效率达到62.6%,而且,随后的库仑效率都保持在90%以上,比容量衰减率只有0.9%。对较纯的SnO2负极材料而言,SnO2·SiO2复合物作为锂离子电池负极材料的首次库仑效率已有一定程度的提高,同时纳米SnO2·SiO2复合物电极具有较好的循环嵌脱锂性能,并且其反应原理与纯的SnO2一样。这也很好地证明了SiO2的无定型结构能够提高SnO2负极材料的性能,说明了掺杂无定型结构的SiO2如何缓解SnO2充放电过程中的体积效应。因此经过掺杂或者修饰的SnO2是很有潜力的锂离子电池负极材料。
2.2 一维材料 (1D Nanomaterials)
许多一维纳米结构的SnO2负极材料已经被广泛地应用和研究,不仅在锂离子电池领域[22],在传感器领域也应用广泛[23]。一维纳米材料通常是指拥有大的长径比结构的纳米材料,例如纳米棒[24]、纳米线[25]、纳米带[26]、纳米管。
2.2.1 纳米棒
2004年,Vayssieres等[27]采用熔融盐法合成了SnO2纳米棒,这是在800 ℃条件下烧结SnCl4,NaCl,NaBH4的混合溶液,最终得到了纯度和结晶度较高的纳米棒。另外,他们还进一步研究了煅烧温度和时间对纳米棒的影响。虽然此方法通过缩短煅烧时间到15 min就能形成纳米棒结构,但煅烧温度太高,其电化学性能并不良好。对此,许多研究团队在这种方法的基础上,结合退火方法获得更优性能的SnO2纳米棒。Wang等[28]利用上述方法合成了SnO2纳米棒,这种纳米棒表现出了较好的电化学性能,其比容量达到了1 100 mAh/g。从图1(a)和(b)可知,虽然用熔融盐法合成的纳米棒尺寸均匀,分散性非常好,但是水热法合成的纳米棒应用更加广泛。通常以SnCl4为锡源、NaOH为沉淀剂、CH3CH2OH为溶剂,通过控制水热反应温度和时间合成形状规整的SnO2纳米棒[29]。由图 1(c)和(d)可知,当用尿素作为 OH-源时,SnO2纳米棒能够在更低温度(90 ℃)的条件下得到。由于晶体的各向异性,SnO2金红石结构在[001]晶向的表面能最大,最终SnO2纳米棒将会沿着[001]方向生长[30],因此利用水热法以及SnO2的生长机理可以在基底上生长有序的SnO2纳米棒。在金属基底上生长出来有序的SnO2纳米棒,并且可以通过控制基底或者前驱体的浓度控制长径比。水热法合成的有序SnO2可以在不需要黏结剂和导电剂而直接作为锂离子电池的负极。有序的SnO2纳米棒在循环100次之后仍然能够保持580 mAh/g的可逆比容量,更重要的是,这种特殊的结构在循环50次之后仍然能够保持完整,这展现出了比无序SnO2纳米棒或者SnO2纳米颗粒更好的性能。当然,除了水热法之外还有模板法也得到了广泛应用,例如Du等[31]运用模板法合成了ZnO/SnO2复合氧化物纳米棒。他们首先利用原位生长法在钛基底上生长一层有序的ZnO纳米棒,随后对ZnO表面用聚合物电解质进行改性,最后在长有ZnO的纳米棒上滴加SnCl4溶液,在常温下静置2 h,最终形成如图2(a)所示(见下页)的ZnO/SnO2复合氧化物纳米棒。从图2(b)可知(见下页),ZnO/SnO2复合氧化物纳米棒在循环了20次后,可逆比容量仍然高达790 mAh/g。这种方法合成的有序结构能够非常牢固地与钛基底黏结在一起,直接被用作锂离子电池的负极,不仅能够降低锂电池的成本,而且还可以进一步降低电池的内阻。因此,这种结构不仅能够有效降低锂离子传输的阻力,还可以缩短锂离子的传输路径。 由图2(c)(见下页)可知,利用模板法得到的复合氧化物纳米棒芯部主要成分是ZnO,外部包覆着20 nm左右的由粒径为5 nm的SnO2纳米颗粒组成的SnO2层。并且,每个纳米棒之间均匀的间距不但给锂离子的传输提供足够的空间,也可以有效缓解体积效应导致的粉化现象。所以有序的结构能够有效缓解充放电过程中的体积效应,同时也为锂离子和电子的传输提供了更多的空间和便捷的路径。
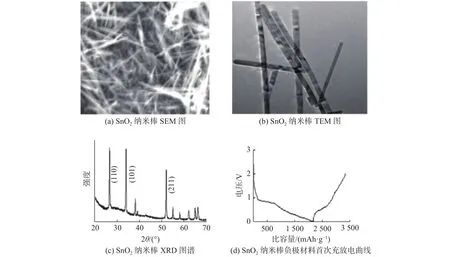
图 1 SnO2纳米棒的形貌及特性图Fig.1 Morphology images and performance of SnO2 nanotubes
2.2.2 纳米线
自2001年Wang等[32]用热蒸发法制备出了纳米线以来,许多研究人员利用这种方法也合成了SnO2纳米线。除此之外,Xi等[33]利用微波等离子体喷射反应器,以Sn颗粒为锡源,在一定距离的表面上形成纳米线。实验表明,通过这种方法形成的SnO2纳米线能够很好地适应锂离子电池在充放电过程中的体积变化。通过用Sn修饰的SnO2纳米线可以在循环100个周期之后仍然达到814 mAh/g的可逆比容量。这种特殊的结构表现出了比Sn/SnO2混合纳米线以及纯的SnO2纳米线更好的性能。当然,运用其他方法也能获得优质性能的SnO2纳米线结构,如静电纺丝[34]和化学气相沉积法。
2.2.3 纳米管
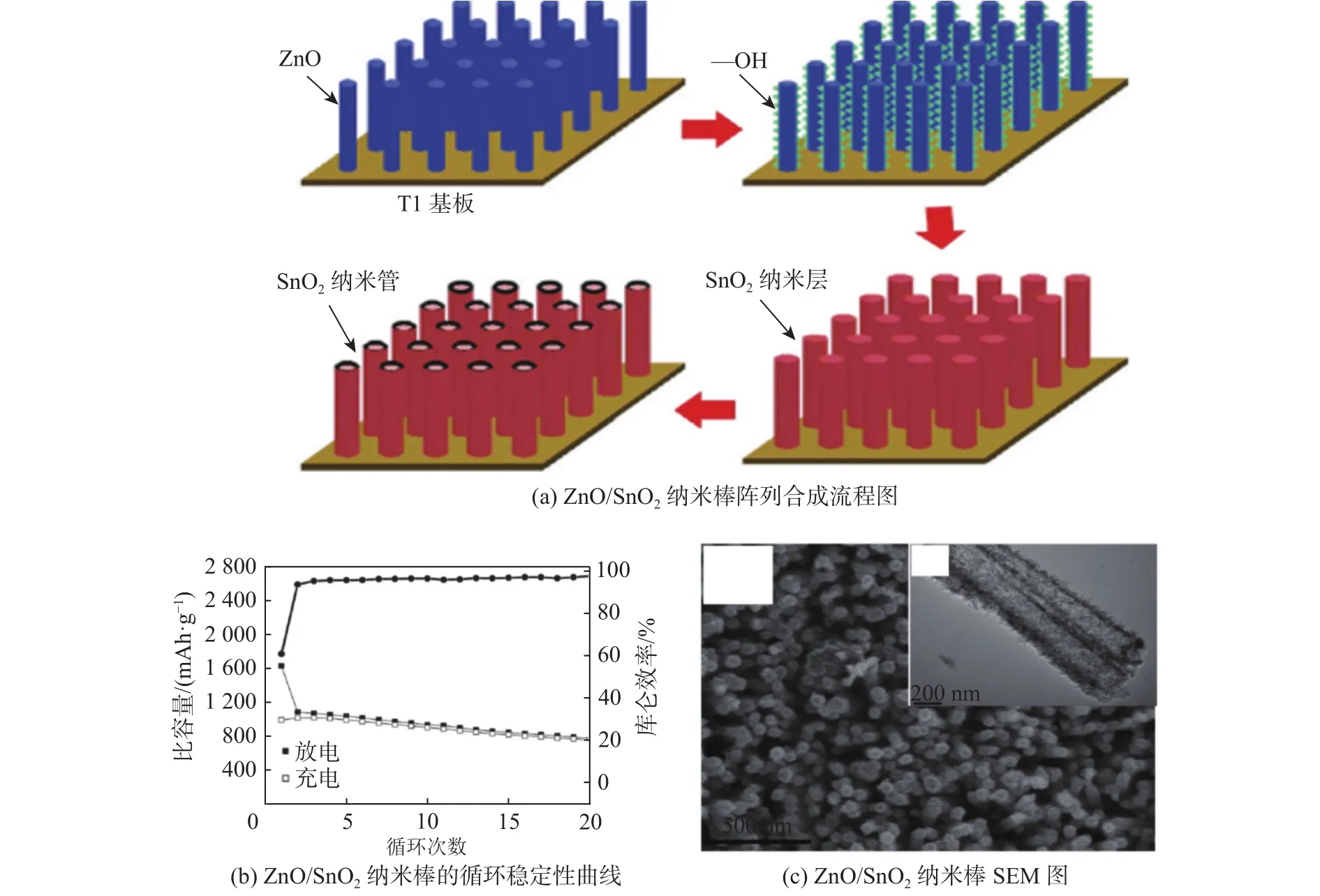
图 2 ZnO/SnO2纳米棒阵列的示意图及特性图Fig.2 Morphology images and performance of ZnO/SnO2 nanotube arrays
由文献可知,阳极氧化铝早已被应用为模板来合成纳米管[35]。这一过程通常分为3步:前驱体渗透至模板里;形成目标结构;移除模板。Wang等[36]运用这种方法合成了分散均匀的纳米管。他们发现,多次重复第一步可以有效调节纳米管的厚度;而且用高浓度的NaOH作为腐蚀剂来移除模板时,只需要超声清洗就可得到分散均匀的纳米管。SnO2纳米管具有良好的储锂性能,即使在循环80次后可逆比容量仍然达到了525 mAh/g。这主要是因为较短的贯通纳米管能够提供更多的锂离子活性位点及更大的比表面积,同时合适孔径的纳米管状结构也可以有效缓解锂离子电池充放电过程中的体积效应。但是,对于合成SnO2纳米管的模板来说要求较高,这就需要用来合成的模板材料易于控制。因为这种类型的多孔膜模板的孔径对衍生材料结构的形成也有重要影响。虽然大孔径的模板能形成管状结构,但是如果模板的孔径太小可能会形成纳米线而不是纳米管。通过不断实验,最终有人发现可在金属基底上形成SiO2模板,然后再将模板静置在SnO2的前驱体溶液中,随后通过水热反应形成SnO2的核壳结构,最终通过NaOH腐蚀的方法移除SiO2模板,得到SnO2纳米管。Kumar等[37]利用SiO2形成各种不同形状的模板,合成了各种类型的纳米管结构。纳米管的尺寸对锂离子电池的性能导致了很明显的影响,其中短纳米管的性能较好,这主要是由短纳米管本身所决定的。另外,Zeng等[38]合成了SnO2/α-Fe2O3纳米管。首先是ZnO-SnO2纳米管的形成,然后在ZnO-SnO2上包覆α-Fe2O3层,最后移除ZnO模板得到SnO2/α-Fe2O3复合氧化物纳米管。通过上述方法合成的纳米管结构清晰,壁厚大约30 nm,而且将这种纳米管用于做锂离子电池的负极材料时,也表现出了非常好的稳定性。在SnO2参与充放电反应时,α-Fe2O3还处于非活性状态,仍然保持着最初的结构形貌。这种结构能够缓解锂离子在充放电时合金化导致的体积膨胀,从而很好地保护负极材料的结构不受破坏。除此之外,在LixSn完全附着在α-Fe2O3内壁之后,这时形成的Fe会包覆在LixSn外面,这又保护了负极材料结构的完整性。SnO2这种特殊结构材料可以高倍率放电,具有高比容量和高库仑效率。它的综合性能比前面提到的纳米棒、纳米颗粒都要好,这可能是由于SnO2和α-Fe2O3之间的相互协调作用,以及其规整的排列为反应提供了更加合适的环境。而且,这种方法也可以应用于其他金属氧化物材料来合成类似的结构,从而进一步提高SnO2作为锂离子电池负极材料的性能。
2.3 二维材料
SnO2纳米片结构并不像一维结构那样被广大研究人员所关注,最主要的原因是目前仍然没有合适的方法合成形状均匀的SnO2纳米片。通过研究发现用来合成SnO2纳米片的锡源材料主要有锡盐类材料,包括当用这些前驱体来合成SnO2纳米片时,需要在Sn2+氧化成Sn4+的同时必须能很好地控制SnO2原子的各向异性,才能够合成纯度较高和形状规则的SnO2纳米片。正是由于这种复杂性,通常在已经合成的SnO2纳米片中会含有SnO的成分。利用水热法,以SnCl2作为前驱体,合成了相对纯度较高、形状合适的SnO2纳米片。研究发现加入少量的聚吡咯烷酮(PVP)可以控制SnO2的形貌[42]。从图3(a)和(b)可知,加入的聚吡咯烷酮可以有效控制纳米片的尺寸,合成的SnO2纳米片更加均匀也更小。由图3(c)的XRD扫描图谱可知,加入的聚吡咯烷酮并不影响SnO2纳米片的生长沿着110晶面生长。而且从图3(d)可知,加了PVP的SnO2表现出了更好的电化学性能。这说明SnO2纳米片也可以应用于锂离子电池的负极材料。
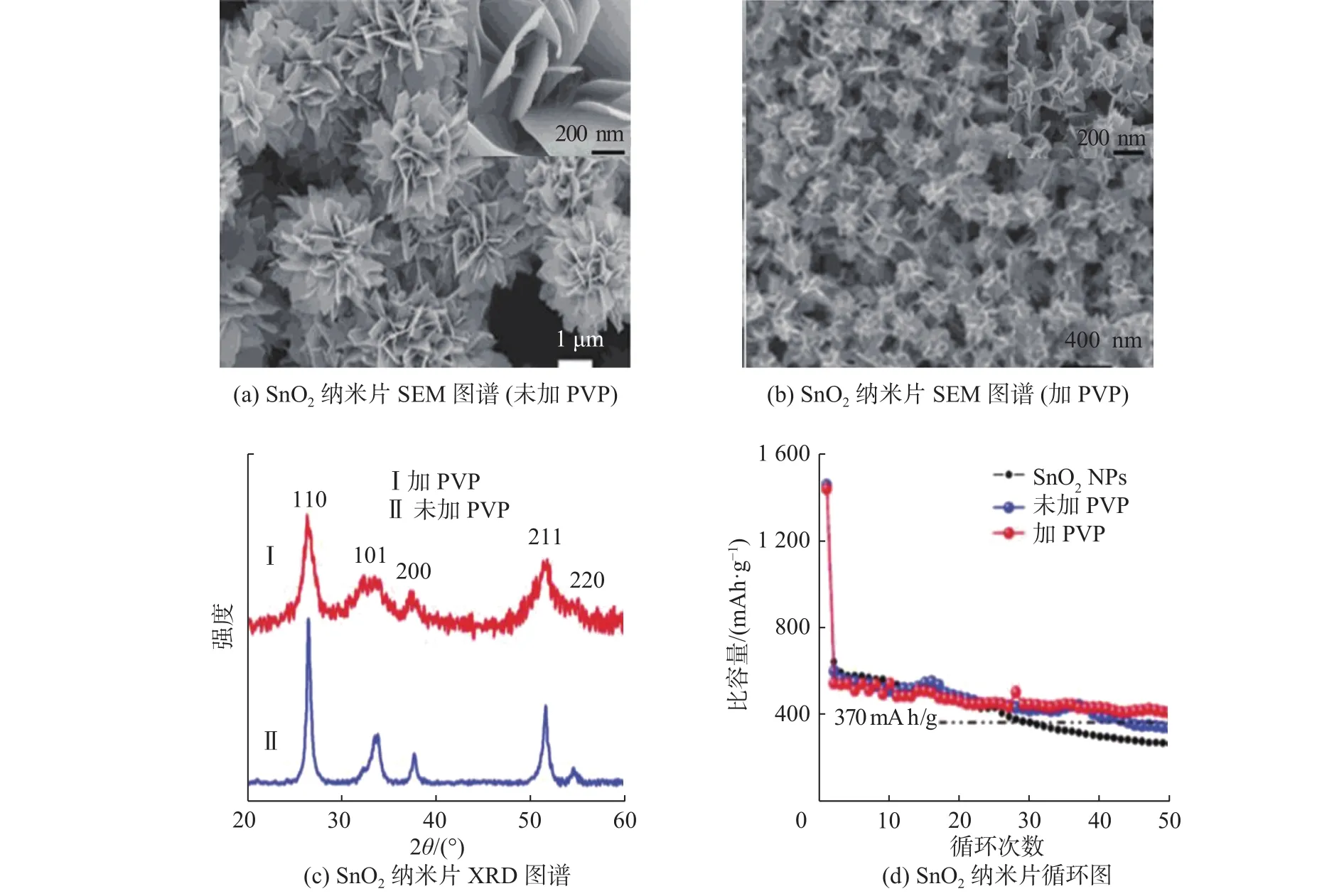
图 3 SnO2纳米片的形貌及特性图Fig.3 Morphology images and performance of SnO2 nanosheets
2.4 三维材料 (3D Nanomaterials)
三维纳米结构是指由零维、一维、二维中的一种或多种基本结构单元组成的复合材料。合成SnO2三维纳米结构材料的方法主要分为两种:模板法和非模板法。SnO2纳米材料不仅可以应用于锂离子电池负极材料方面[43],而且在传感器和水处理方面有着广泛的应用[44]。
虽然模板法制备过程较为复杂,但由于它可以控制产品的形貌、尺寸、均一性等优点,因此被广泛应用。其实验过程主要分为3步:制备模板;将沉积液滴到模板上;移除模板。模板法主要分为硬模板法与软模板法。其中由于硬模板合成容易,形貌尺寸均匀,所以硬模板法应用更为广泛。被作为硬模板的材料有很多种,最常用的有SiO2,PS等。
Du等[45]以SiO2微球作为硬模板,成功地获得SnO2的核壳结构。实验中,他们以四氯化锡(SnCl4)为前驱体,SiO2作为模板,利用水热法合成了SnO2核壳结构,实验过程如图4(a)所示(见下页)。由图4(b)可知(见下页),最终合成的SnO2纳米核壳结构形貌尺寸均一。从图4(c)可知(见下页),硬模板法合成的SnO2首次放电比容量高达1 701 mAh/g,而且稳定性比纳米颗粒要高。这种结构表现出比纳米颗粒更好的性能,主要是因为SnO2核壳结构比纳米颗粒结构的比表面积更大,并且结构也比较稳定。当然,除了用SiO2作为模板外,PS也经常用来做模板,实验过程如图5所示(见下页)。图中,D0,D分别为干燥前、干燥后相邻两PS球的间距。例如,Zhong等[46]利用PS微球作为模板,合成了均一的SnO2核壳结构。另外,还有以五水合氯化锡和叔丁醇为前驱体,在PS模板上合成类似贝壳形状的SnO2核壳结构,这种结构的SnO2表现出了较好的循环稳定性,在循环20次以后比容量达到了870 mAh/g。还有碳微球也经常被作为硬模板来合成核壳结构,但在最终移除模板的过程中可能会由于产生的CO2气体破坏核壳结构,从而限制了碳微球作为合成SnO2核壳结构的模板。
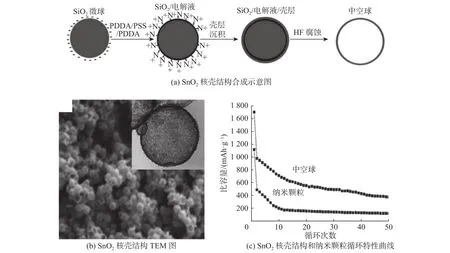
图 4 SnO2核壳结构的示意图及特性图Fig.4 Morphology images and performance of SnO2 hollow spheres
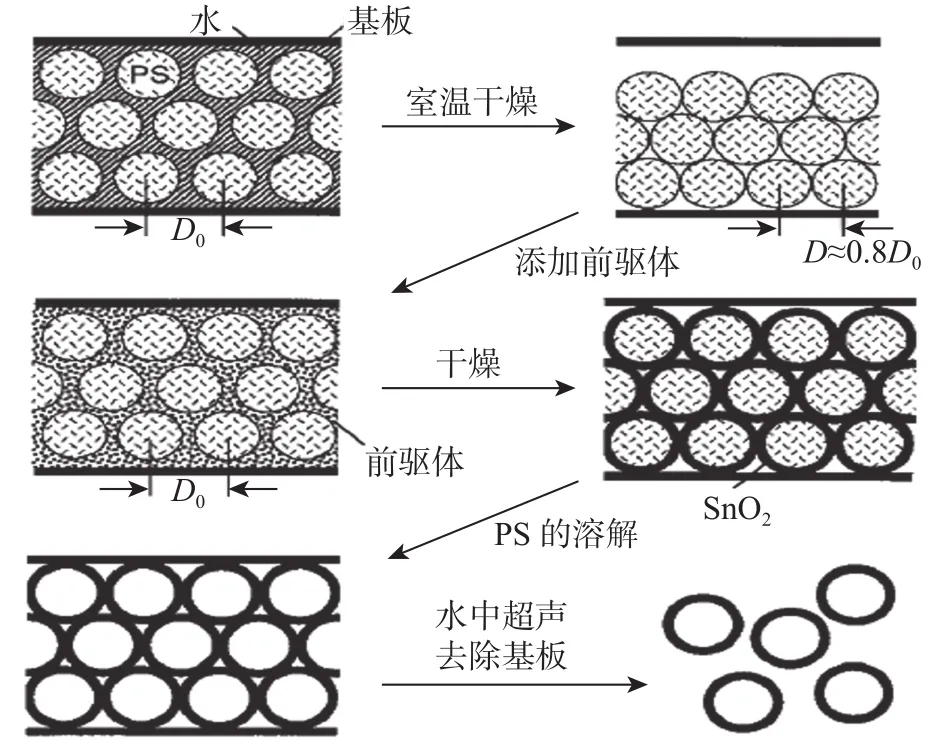
图 5 以PS微球为模板合成SnO2纳米核壳结构示意图Fig. 5 Schematic outline of the experimental procedure for SnO2 hollow spheres with PS
除传统的硬模板法外,一些研究者还应用许多软模板法来合成三维结构的SnO2负极材料。例如:Wang等[47]将十二烷基苯磺酸钠溶于水中形成均一的溶液,然后Sn2+会在表面活性剂的作用下形成胶团,随后慢慢地形成SnO2核壳结构。这种软模板法也适用于合成其他金属氧化物的核壳结构。
还有一种是利用奥斯特瓦尔德熟化机制形成SnO2三维纳米结构的非模板法。这种方法合成各种结构包括核壳结构,也可以是类似花瓣状的结构。但是,这种方法的合成过程较难控制,所以很难合成核壳结构清晰、尺寸均一的SnO2。通过将锡酸钾溶于去离子水和无水乙醇中,利用水热法最终合成了SnO2核壳结构材料,这种核壳结构首次比容量高达1 140 mAh/g,循环40次以后还能保持659 mAh/g的比容量。虽然首次比容量较高,但是稳定性能并不是很好,对实验条件的要求也比较高。尽管研究发现这种多孔独特的核壳结构在锂离子电池充放电过程中起到了很好的疏散作用,能够缩短锂离子和电子的扩散路径以及提供更多的储锂位点[48],但是实验不可控的因素较多,因此这种方法还有待进一步优化。
3 结 论
全面总结了SnO2基材料的锂离子电池负极材料的研究进展。首先概述了SnO2的不同形貌如纳米颗粒、纳米棒、纳米片、纳米微球等在锂离子电池方面的特性,例如SnO2纳米颗粒粒径小于3 nm时,作为锂离子电池负极材料表现出了非常好的循环稳定性能。然后阐述了通过掺杂或修饰改善其结构及电化学性能。
近年来,对SnO2基纳米结构的研究已经取得了进展,纳米结构材料可以一定程度上缓解锂离子电池在充放电过程中的体积效应,而且通过合成具有特殊结构的SnO2复合氧化物材料也可以进一步提高循环性能。但是,现阶段所研究的SnO2基负极材料的各项性能指标,还未能达到商业化的使用标准,仍然有很长一段路要走。不管是零维纳米结构还是三维纳米结构的SnO2材料都存在很好的研发潜力,所以在今后的研究中我们更应该致力于研究更加复杂、更适合锂离子电池的纳米结构负极材料。参考文献:
[1]丁翔, 黄丽华, 纪敏, 等. 氮化碳自组装包裹对SnO2-TiO2复合锂离子电池负极材料电化学性能的影响[J]. 有色金属材料与工程, 2016, 37(2): 1-7.
[2]WINTER M, BESENHARD J O. Electrochemical lithiation of tin and tin-based intermetallics and composites[J]. Electrochimica Acta, 1999, 45(1/2): 31-50.
[3]KASAVAJJULA U, WANG C S, APPLEBY A J. Nanoand bulk-silicon-based insertion anodes for lithium-ion secondary cells[J]. Journal of Power Sources, 2007, 163(2):1003-1039.
[4]POIZOT P, LARUELLE S, GRUGEON S, et al. Nanosized transition-metal oxides as negative-electrode materials for lithium-ion batteries[J]. Nature, 2000,407(6803): 496-499.
[5]CHEN J S, LOU X W. SnO2-based nanomaterials:synthesis and application in lithium-ion batteries[J]. Small,2013, 9(11): 1877-1893.
[6]ZHAO Q Q, MA L S, ZHANG Q, et al. SnO2-based nanomaterials: synthesis and application in lithium-ion batteries and supercapacitors[J]. Journal of Nanomaterials,2015, 2015: 850147.
[7]LI J X, ZHAO Y, WANG N, et al. A high performance carrier for SnO2nanoparticles used in lithium ion battery[J]. Chemical Communications, 2011, 47(18):5238-5240.
[8]GUO C X, CAO M H, HU C W. A novel and lowtemperature hydrothermal synthesis of SnO2nanorods[J].Inorganic Chemistry Communications, 2004, 7(7):929-931.
[9]ZHAO L, XU C F, SU H F, et al. Single-crystalline rhodium nanosheets with atomic thickness[J]. Advanced Science, 2015, 2(6): 1500100.
[10]ZHAO K, DU G F, QIN G H, et al. Facile synthesis of boscage-like SnO2nanorods by hydrothermal method[J].Materials Letters, 2015, 141: 351-354.
[11]KIM C, NOH M, CHOI M, et al. Critical size of a Nano SnO2electrode for Li-Secondary battery[J]. Chemistry of Materials, 2005, 17(12): 3297-3301.
[12]UM J H, CHOI M, PARK H, et al. 3D macroporous electrode and high-performance in lithium-ion batteries using SnO2coated on Cu foam[J]. Scientific Reports, 2016,6: 18626.
[13]PAEK S M, YOO E, HONMA I. Enhanced cyclic performance and lithium storage capacity of SnO2/Graphene nanoporous electrodes with three-dimensionally delaminated flexible structure[J]. Nano Letters, 2009, 9(1):72-75.
[14]LIAN P C, ZHU X F, LIANG S Z, et al. High reversible capacity of SnO2/Graphene nanocomposite as an anode material for lithium-ion batteries[J]. Electrochimica Acta,2011, 56(12): 4532-4539.
[15]虞祯君, 王艳莉, 邓洪贵, 等. SnO2/石墨烯锂离子电池负极材料的制备及其电化学行为研究[J]. 无机材料学报,2013, 28(5): 515-520.
[16]MANORAMA S V, BASAK P, RANA R K, et al.Nanostructured metal oxides: low temperature synthesis and biomimetic approaches[J]. Proceedings of the National Academy of Sciences, India Section B: Biological Sciences, 2012, 82(4): 573.
[17]SINGH V, SINGH D, KUMAR S, et al. Structural and morphological study of nickel doped tin oxide nanoparticles synthesized via sol-gel technique[J].Nanomaterials: Applications and Properties, 2015, 4(1):01PCSI04.
[18]JIANG L H, SUN G Q, ZHOU Z H, et al. Size-controllable synthesis of monodispersed SnO2nanoparticles and application in electrocatalysts[J]. The Journal of Physical Chemistry B, 2005, 109(18): 8774-8778.
[19]CHANNU V S R, HOLZE R, WICKER S A, et al.Synthesis and characterization of (Ru-Sn)O2nanoparticles for supercapacitors[J]. Materials Sciences and Applications, 2011, 2(9): 1175-1179.
[20]SHEN E H, WANG C L, WANG E B, et al. PEG-assisted synthesis of SnO2nanoparticles[J]. Materials Letters, 2004,58(29): 3761-3764.
[21]XU X F, ZHANG H Y, CHEN Y M, et al. SiO2@SnO2/Graphene composite with a coating and hierarchical structure as high performance anode material for lithium ion battery[J]. Journal of Alloys and Compounds, 2016,677: 237-244.
[22]梁英, 张勇, 田志高, 等. 纳米SnO2-SiO2复合氧化物的制备与电化学性能[J]. 电源技术, 2008, 32(12): 841-844.
[23]PARK M S, WANG G X, KANG Y M, et al. Preparation and electrochemical properties of SnO2nanowires for application in lithium-Ion batteries[J]. Angewandte Chemie International Edition, 2007, 46(5): 750-753.
[24]HUANG H T, TIAN S Q, XU J, et al. Needle-like Zndoped SnO2nanorods with enhanced photocatalytic and gas sensing properties[J]. Nanotechnology, 2012, 23(10):105502.
[25]CHENG B, RUSSELL J M, SHI W S, et al. Large-scale,solution-phase growth of single-crystalline SnO2nanorods[J]. Journal of the American Chemical Society,2004, 126(19): 5972-5973.
[26]LIU L Z, LI X X, WU X L, et al. Growth of tin oxide nanorods induced by nanocube-oriented coalescence mechanism[J]. Applied Physics Letters, 2011, 98(13):133102.
[27]VAYSSIERES L, GRAETZEL M. Highly ordered SnO2nanorod arrays from controlled aqueous growth[J].Angewandte Chemie International Edition, 2004, 43(28):3666-3670.
[28]WANG J S, SUN J Q, ZHANG G S, et al. Preparation of SnO2nanorods via oriented aggregation of nanoparticles[J]. Vacuum, 2007, 82(1): 5-8.
[29]SONG H C, WANG H X, LIN Z X, et al. Hierarchical Nano-branched c-Si/SnO2nanowires for high areal capacity and stable lithium-ion battery[J]. Nano Energy,2016, 19: 511-521.
[30]XUE X Y, CHEN Z H, XING L L, et al. SnO2/α-MoO3core-shell nanobelts and their extraordinarily high reversible capacity as lithium-ion battery anodes[J].Chemical Communications, 2011, 47(18): 5205-5207.
[31]DU N, ZHANG H, CHEN B D, et al. One-pot, large-scale synthesis of SnO2nanotubes at room temperature[J].Chemical Communications, 2008, 14(26): 3028-3030.
[32]WANG Y, LEE J Y. Molten salt synthesis of tin oxide nanorods: morphological and electrochemical features[J].The Journal of Physical Chemistry B, 2004, 108(46):17832-17837.
[33]XI G C, YE J H. Ultrathin SnO2nanorods: template- and surfactant-free solution phase synthesis, growth mechanism, optical, gas-sensing, and surface adsorption properties[J]. Inorganic Chemistry, 2010, 49(5):2302-2309.
[34]WANG J Z, DU N, ZHANG H, et al. Large-scale synthesis of SnO2nanotube arrays as high-performance anode materials of Li-Ion batteries[J]. The Journal of Physical Chemistry C, 2011, 115(22): 11302-11305.
[35]DAI Z R, PAN Z W, WANG Z L. Novel nanostructures of functional oxides synthesized by thermal evaporation[J].Advanced Functional Materials, 2003, 13(1): 9-24.
[36]WANG Y, LEE J Y, ZENG H C. Polycrystalline SnO2nanotubes prepared via infiltration casting of nanocrystallites and their electrochemical application[J].Chemistry of Materials, 2005, 17(15): 3899-3903.
[37]KUMAR V, KIM J H, PENDYALA C, et al. Gas-phase,bulk production of metal oxide nanowires and nanoparticles using a microwave plasma jet reactor[J]. The Journal of Physical Chemistry C, 2008, 112(46):17750-17754.
[38]ZENG W Q, ZHENG F P, LI R Z, et al. Template synthesis of SnO2/α-Fe2O3nanotube array for 3D lithium ion battery anode with large areal capacity[J]. Nanoscale, 2012, 4(8):2760-2765.
[39]THOMAS R, MOHAN RAO G. SnO2nanowire anchored Graphene nanosheet matrix for the superior performance of Li-ion thin film battery anode[J]. Journal of Materials Chemistry A, 2015, 3(1): 274-280.
[40]WANG Y, WU M H, JIAO Z, et al. One-dimensional SnO2nanostructures: facile morphology tuning and lithium storage properties[J]. Nanotechnology, 2009, 20(34):345704.
[41]BRINA P, GIULIANO G, MIGLIARESE M C, et al.Deposition and diffusion of plasma sputtered platinum nanoparticles in porous anodic alumina oxide[J]. Canadian Anaesthetists’ Society Journal, 2010, 23(5): 505-517.
[42]YANG H M, YU G G, LIU H W. Synthesis of 3D flowerlike SnO2with hierarchical nanostructure and high reversible capacity as lithium-Ion battery anode[J]. Journal of Electronic Materials, 2015, 44(10): 3744-3751.
[43]WANG H K, FU F, ZHANG F H, et al. Hydrothermal synthesis of hierarchical SnO2microspheres for gas sensing and lithium-ion batteries applications: fluoride-mediated formation of solid and hollow structures[J]. Journal of Material Chemistry, 2012, 22(5): 2140-2148.
[44]LIU S Q, XIE M J, LI Y X, et al. Novel sea urchin-like hollow core-shell SnO2superstructures: facile synthesis and excellent ethanol sensing performance[J]. Sensors and Actuators B: Chemical, 2010, 151(1): 229-235.
[45]DU N, ZHANG H, CHEN J E, et al. Metal oxide and sulfide hollow spheres: layer-by-layer synthesis and their application in lithium-ion battery[J]. The Journal of Physical Chemistry B, 2008, 112(47): 14836-14842.
[46]ZHONG Z Y, YIN Y D, GATES B, et al. Preparation of mesoscale hollow spheres of TiO2and SnO2by templating against crystalline arrays of polystyrene beads[J].Advanced Materials, 2000, 12(3): 206-209.
[47]WANG Y, HUANG Z X, SHI Y M, et al. Designed hybrid nanostructure with catalytic effect: beyond the theoretical capacity of SnO2anode material for lithium ion batteries[J]. Scientific Report, 2015, 5: 9164.
[48]LOU X W, WANG Y, YUAN C, et al. Template-free synthesis of SnO2hollow nanostructures with high lithium storage capacity[J]. Advanced Materials, 2006, 18(17):2325-2329.

