NZVI@mSiO2合成调控及有机质对其去除地下水中氯代烃影响研究
陈 帅, 李 辉, 周礼洋, 刘勇弟, 任路遥
(华东理工大学 资源与环境工程学院,上海 200237)
氯代烃作为重要的化工原料和有机溶剂目前已被广泛应用于制药、脱脂、皮革、电子、干洗及农药等行业[1]。氯代烃化学性质较稳定、生物降解性差,属持久性污染物,渗漏及不当使用已使其成为地下水中最常检测出污染物[2]。大部分氯代烃都有致癌或潜在三致(致突变、致癌、致畸)危害,对人体健康与生态环境安全造成严重影响[3]。例如,1,1,1-三氯乙烷(1,1,1-TCA)在《蒙特利尔破坏臭氧层物质管制议定书》签署(1987年)前已被广泛使用[4],目前已被确定为潜在致癌物质并被美国环保署(USEPA)列入优先控制污染物清单。地下水中氯代烃污染治理已成为全世界地下水污染研究领域的热点问题,研发出经济有效的地下水中氯代烃去除技术十分必要。
零价铁(ZVI)在近年来已成为地下水中氯代烃污染治理的重要材料[5-7]。目前,国内外的研究者在使用ZVI去除地下水中氯代烃的机理及应用基础方面都已开展了系统研究[8-9]。提高ZVI去除氯代烃的效率一直是关注的热点。纳米零价铁(NZVI)因其高比表面积、高表面及化学反应活性,已被广泛用于氯代烃去除[10]。然而,NZVI颗粒会彼此吸附而形成大的、微米到毫米尺度颗粒而降低其迁移能力与有效表面积[1],从而降低去除氯代烃的能力。在NZVI上合成氧化硅(SiO2)壳层可阻止NZVI颗粒的团聚和氧化[1,11]。作者的前期研究[1]采用化学还原和改进的Stöber法制备了纳米零价铁@介孔氧化硅(NZVI@mSiO2)核-壳结构材料,由于mSiO2壳上的介孔孔道,其比表面积高于NZVI与已报道的NZVI@SiO2核-壳结构材料[12-13],有利于其对氯代烃的吸附与降解。mSiO2壳层优异的表面和结构性能使NZVI@mSiO2具有比NZVI更好的分散性、迁移性及去除氯代烃的性能,具有较好的应用前景。NZVI@mSiO2或其他负载型NZVI材料对污染物的去除主要依靠壳层或载体对污染物的吸附和NZVI对污染物的降解的协同作用[14]。前人的研究将两者合并讨论,不能准确阐明材料去除氯代烃的机理[9]。有机质(NOM)在地下水中普遍存在,其含量通常在数mg/L到数百mg/L之间[15],可改变颗粒悬浮液的的稳定性[16]和颗粒的聚合动力学[17],它与壳层或载体之间复杂的相互作用对材料吸附和降解污染物的行为非常重要。文献[9]概括了一些前人得出的NOM对ZVI去除污染物的影响规律,NOM对ZVI去除污染物可能有促进、抑制或不影响的作用。 NZVI@mSiO2作为NZVI的改进材料,研究NOM对其吸附去除和吸附-降解去除氯代烃行为的影响很有意义。
本研究旨在考察不同硅源前驱体添加量及添加硅源前驱体后的反应时间对NZVI@mSiO2结构的影响,分析NOM对其去除地下水中氯代烃行为的影响,为该材料的应用提供理论基础。
1 实 验
1.1 实验药品
三氯化铁(FeCl3·6H2O,纯度99%)、硼氢化钠(NaBH4,纯度 96%)、乙醇(C2H5OH,纯度99.7%)、氨水(NH4OH,28%)、十六烷基三甲基溴化铵(CTAB,纯度99%)、正硅酸乙酯(TEOS,28%)、盐酸溶液(1 mol/L)、有机质(灰分10%,水分8%,含铁量3%)、去离子水。
1.2 材料制备
将0.483 g的FeCl3·6H2O溶解在有50 mL水和45 mL乙醇的有N2保护的三口烧瓶中,并用JJ-1型机械搅拌器以600 r/min的转速搅拌10 min。将0.3 g的NaBH4溶解在25 mL去离子水中,并用BQ50-1J-A型蠕动泵将溶液以1.5 mL/min的速度加入三口烧瓶中30 min后便可制备出NZVI。
要制备NZVI@mSiO2,需在制备出NZVI后继续将4 mL氨水和0.6 g CTAB加入三口烧瓶中,继续以600 r/min的搅拌速度搅拌30 min。然后,将一定量的TEOS快速加入三口烧瓶。之后体系以300 r/min的搅拌速度搅拌一定时间,即可制备出NZVI@mSiO2。将制备出的NZVI@mSiO2使用盐酸溶液将NZVI核消解后,可制备出mSiO2。将制备出的NZVI@mSiO2和mSiO2用ScanSpeed 1236R型离心机在3 000 r/min的离心速度下离心1 min后,用乙醇清洗并离心,重复3次。然后用真空干燥箱干燥16 h备用。
1.3 材料表征
用JSM-6360LV型扫描电子显微镜(SEM)观察NZVI@mSiO2的表面形貌,测试前对样品进行喷金处理,工作电压为15 kV。用JEM-1400型透射电镜(TEM)观察NZVI@mSiO2结构,样品分散在乙醇中后用铜网收集,工作电压为120 kV。采用纳米测量软件Nano Measurer 1.2统计计算图像中粒子的粒径。
1.4 吸附去除与吸附-降解去除氯代烃实验
在室温下,mSiO2或NZVI@mSiO2吸附去除或吸附-降解去除 1,1,1-TCA(60 mg·L-1)的实验在100 mL血清瓶中进行,每个血清瓶中加入0.29 g的mSiO2或0.39 g(含0.1 g 的NZVI)的NZVI@mSiO2。将血清瓶放入自制转鼓中,以15 r/min的速度转动,以模拟地下水流动。在确定的取样时间(0,10,20,40,60,90,120 min),取 2 mL 混合溶液,采用GC-2014C气相色谱仪测定1,1,1-TCA的浓度,并据此评价mSiO2或NZVI@mSiO2吸附去除(Q为每克材料在规定时间吸附污染物的量)或吸附-降解去除氯代烃的能力。在每次取样的同时将2 mL去离子水注射到血清瓶中,避免在取样过程中引入空气。
使用NZVI@mSiO2去除1,1,1-TCA过程可采用伪二级反应动力学模型拟合[1]。
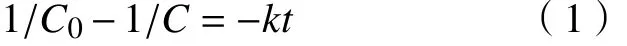
式中:C为在t时刻溶液中1,1,1-TCA的浓度;C0为溶液中1,1,1-TCA的初始浓度;k为二级反应动力学速率常数。
实验中均采用3次实验的平均值进行绘图和分析,图中显示的数据为平均值及标准差。所采用的分析仪器在测量之前均进行了校准,并定期通过分析一组标准样品进行校准。校准结果与最近的初始校准曲线相比,满足标准(决定系数R2≥0.99)。
1.5 悬浮稳定实验
将0.29 g的mSiO2和100 mL去离子水放入容积为250 mL的烧杯中,采用JJ-1型机械搅拌器以100 r/min的速度搅拌1 min,然后将悬浮液倒入容积为100 mL的量筒中进行沉降测试。在沉降测试 0,5,10,20,30,45,60 min 时收集上清液样品(3 mL),用UV-1800紫外分光光度计测定上清液透光率,所采用波长为420 nm。上清液的低透光率表明悬浮液稳定性高,而高透光率则表明悬浮液稳定性低。
2 结果与讨论
2.1 反应条件对NZVI@mSiO2结构的影响
1000μL TEOS 添加后不同反应时间(1,2,4,7 h)所得的NZVI@mSiO2形貌如图1所示。随着反应时间的延长,氧化硅不断在NZVI表面吸附、聚合并生成mSiO2层。1 h时,材料主要以裸露的NZVI为主,但也已经有一些mSiO2在NZVI表面生成。不过,此时mSiO2壳层在NZVI核表面上的生长并不均匀,所制备的NZVI@mSiO2的粒度分布范围较大,20~50 nm的粒度区间内均有颗粒分布。2 h时,mSiO2持续在NZVI的表面生成,同样地,此时mSiO2壳层在NZVI核表面上的生长仍然不均匀,所制备的NZVI@mSiO2的粒度分布范围仍然较大。4 h时,已经在NZVI外形成了稳定mSiO2壳层,所合成的NZVI@mSiO2粒径已基本均匀。4 h以后,NZVI@mSiO2的颗粒大小已无明显变化,表明在4 h时NZVI@mSiO2的制备可被认为已经完成。

图 1 不同反应时间制备NZVI@mSiO2的SEM图Fig.1 SEM images of NZVI@msiO2 prepared with different reaction time
添 加 不 同 量 的 TEOS( 600, 1 000, 1 400,1 800 μL)所得的 NZVI@mSiO2的 SEM和 TEM图像如图2和3所示。mSiO2的厚度随着TEOS添加量的增加而增大。随着TEOS的添加量从600 μL升高到 1 400 μL,再到 1 800 μL,mSiO2壳层的厚度从13 nm升高到25 nm,并最终形成块状复合物。高TEOS添加量可能会破坏NZVI@mSiO2的颗粒结构,从而形成NZVI@mSiO2块状聚体。

图 2 不同TEOS添加量制备NZVI@mSiO2的SEM图Fig.2 SEM images of NZVI@msiO2 prepared with different TEOS dosages

图 3 不同TEOS添加量制备NZVI@mSiO2的TEM图Fig.3 TEM images of NZVI@msiO2 prepared with different TEOS dosages
mSiO2的厚度影响其在空气中的稳定性。随着厚度的增加,NZVI核在空气中可保存的时间变长,但也使其不易与污染物发生反应。前期探索性实验结果表明:TEOS添加量为1 000 μL,反应4 h可获得结构稳定、反应活性较高的NZVI@mSiO2。后续的吸附与吸附-降解去除氯代烃实验均采用该反应条件所获得的NZVI@mSiO2。
2.2 铁剂量对NZVI@mSiO2吸附-降解去除氯代烃的影响
通过改变NZVI@mSiO2的添加量控制体系中的铁剂量。铁剂量对NZVI@mSiO2吸附-降解去除1,1,1-TCA性能的影响结果及伪二级反应动力学拟合结果如图4和表1所示(见下页)。随着时间的延续,在各铁剂量条件下,NZVI@mSiO2对1,1,1-TCA去除率均逐渐增加。铁剂量为0.5 g/L时,NZVI@mSiO2对1,1,1-TCA的去除效果最差,仅有46%的1,1,1-TCA在2 h后被NZVI@mSiO2去除,其反应速率常数为0.001 3 L/(mmol·min)。而在铁剂量为4 g/L时,NZVI@mSiO2对1,1,1-TCA的去除效果最好,有将近99%的1,1,1-TCA在2 h后被NZVI@mSiO2去除,其反应速率常数为 0.028 0 L/(mmol·min)。该结果表明,铁剂量的升高促进了NZVI@mSiO2对氯代烃的吸附-降解去除行为。
Matheson等[18]的研究证实了四氯化碳(CT)的去除速率常数与铁剂量呈现很好的线性关系(R2=0.96)。Deng等[19]在用 ZVI还原一氯乙烯(VC)的研究中也发现产物乙烯的浓度随铁剂量的增加而增加。类似地,使用NZVI还原1,1,1-TCA,铁剂量大于0.32 g/L时,相关的伪一级速率常数随铁剂量的增加而增大[20]。因此, 铁剂量的升高将会提供更多的反应活性位点,有更多的NZVI参与反应,从而有利于对氯代烃的吸附-降解去除。
2.3 NOM对mSiO2吸附去除氯代烃的影响
不同NOM添加量条件下,mSiO2吸附去除1,1,1-TCA的结果如图5所示(见下页)。随着时间的延续,在不同NOM添加量时mSiO2对1,1,1-TCA的吸附量逐渐增加。体系对1,1,1-TCA的吸附效果随着NOM添加量的增加而变好。当NOM添加量为0 g/L时,体系对氯代烃的吸附效果最差,在2 h后吸附去除量达到3.16 mg/g;当NOM添加量达到2.5 g/L时,体系对氯代烃的吸附效果最好,在2 h后吸附去除量达到6.45 mg/g。

图 4 铁剂量对NZVI@mSiO2去除1,1,1−TCA的影响及动力学拟合Fig.4 Removal of 1,1,1−TCA by NZVI@mSiO2 at different NZVI dosages

表 1 不同铁剂量去除1,1,1−TCA过程的反应速率常数Tab.1 Removal rate constant of 1,1,1−TCA by NZVI@mSiO2 at different NZVI dosages
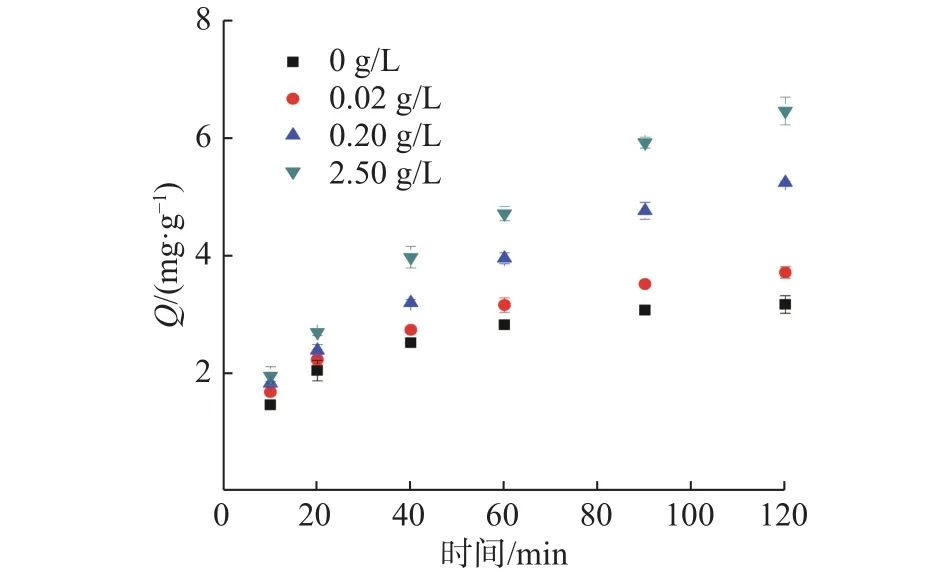
图 5 不同NOM添加量时mSiO2对水溶液中1,1,1−TCA的吸附Fig.5 Adsorption of 1,1,1−TCA by mSiO2 at different NOM concentrations
NOM是一种含有生物聚合物和降解产物的非均质大分子[21]。通常包含烷烃骨架以及芳香烃类官能团(包括羧酸、酚类、羟基和醌类等)[22]。由于其高的羧酸和酚类成分,以及其中弱有机酸的自动分解作用[23],pH=3~10时,NOM表面通常荷负电。前人研究了NOM与纳米材料的相互作用及其对纳米材料悬浮稳定性的影响。NOM可以显著降低碳基纳米材料的沉降,提高其悬浮稳定性[24]。由于纳米颗粒吸附腐殖酸大分子后的的立体排斥作用[25],NOM也可影响非碳基纳米颗粒的稳定性[26]。例如,NOM可增加赤铁矿[27]、金纳米颗粒[28]、 Si纳 米 颗 粒[29]、 Ti纳 米 颗 粒[30]的 分 形 维数,从而提高其悬浮稳定性。粘土经常将NOM吸附在表面,可增强静电稳定以及由吸附的NOM引起的立体稳定,有助于粘土胶体的稳定[31]。
然而,随着NOM添加量的增加,mSiO2的悬浮稳定性却有所降低。不同NOM添加量条件下的悬浮液上清液透光率如图6所示。随着时间的延续,在各NOM添加量时mSiO2与水的悬浮液上清液的透光率均逐渐增加。未添加NOM时,mSiO2与水的悬浮液上清液的透光率最低,显示出较好的悬浮稳定性。然而,NOM添加量达到2.5 g/L时,mSiO2与水的悬浮液上清液的透光率最高,沉降1 h后达到了18.1%,显示出较差的悬浮稳定性。在将NOM添加到水环境中后,将会引入新的成分,这些新的成分会对纳米颗粒吸附污染物的行为起到一定作用。Afrooz等[32]研究发现,加入NOM后,增强了颗粒同质和异质的团聚,这些增加的成分及团聚体,可作为相互作用的额外表面。此外,NOM还可以在mSiO2表面添加高亲和力的吸附点[31,33-34]。NOM的SEM结果如图7所示,可以发现,NOM中包含大量片状或絮状不溶物,这些不溶物会通过吸附桥连或网捕卷扫等作用而使部分mSiO2颗粒聚沉,从而减弱mSiO2与水的悬浮稳定性[1]。同时,这些不溶物也会增加体系新的吸附位点,从而促进体系对氯代烃的吸附去除。
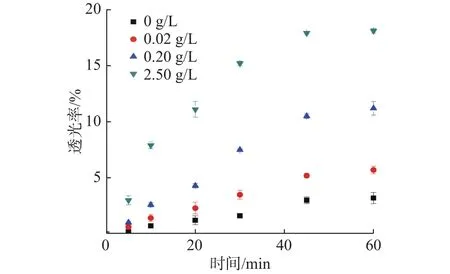
图 6 不同NOM添加量时mSiO2与水的悬浮液上清液透光率随时间的变化Fig.6 Light transmittance varying with time of the supernatant of mSiO2 in deionized water at different NOM concentrations

图 7 NOM的SEM图Fig.7 SEM images of NOM
2.4 NOM对NZVI@mSiO2吸附-降解去除氯代烃的影响
通常,NOM可吸附在ZVI表面的铁(氢)氧化物上[35]。这些吸附的有机质即便含量很少,也可能占据ZVI表面的活性位点,从而降低ZVI对污染物的去除率。
有机质对NZVI@mSiO2吸附-降解去除水溶液中1,1,1-TCA的性能的影响及反应动力学方程拟合结果如图8和表2所示。随着时间的延续,在各NOM添加量条件下NZVI@mSiO2对1,1,1-TCA去除均逐渐增加。NOM添加量为0 g/L时,NZVI@mSiO2对1,1,1-TCA的去除效果最差,有72%的1,1,1-TCA在2 h后被NZVI@mSiO2去除,其反应速率常数为 0.004 1 L/(mmol·min)。而在NOM添加量为2.5 g/L时,NZVI@mSiO2对1,1,1-TCA的去除效果最好,有将近99%的1,1,1-TCA在2 h后被NZVI@mSiO2去除,其反应速率常数为0.035 1 L/(mmol·min)。该结果表明,随着 NOM添加量的增加,体系对1,1,1-TCA的去除效果变好。
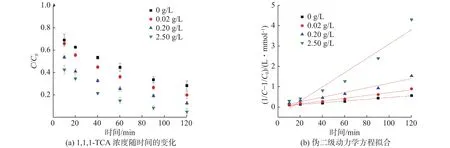
图 8 不同NOM添加量对NZVI@mSiO2去除1,1,1−TCA的影响及动力学模拟结果Fig.8 Degredation of 1,1,1−TCA by NZVI@mSiO2 at different NOM dosages and the dynamic simulation results
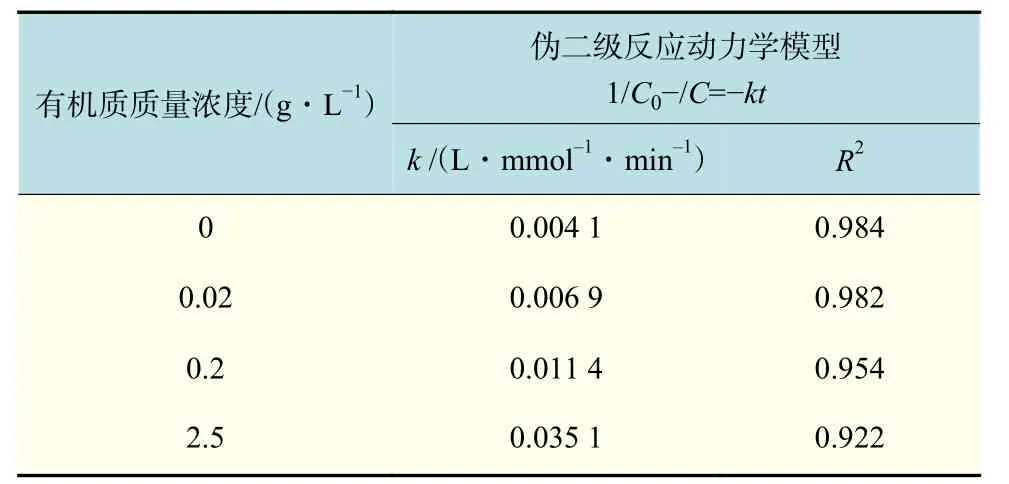
表 2 不同NOM添加量去除1,1,1−TCA过程的反应速率常数Tab.2 Removal rate constant of 1,1,1−TCA by NZVI@mSiO2 at different NOM dosages
添加NOM后可以改变溶液pH。NOM添加量对NZVI@mSiO2去除水溶液中1,1,1-TCA体系的pH变化的影响如图9所示(见下页)。随着NOM添加量的增加,溶液pH逐渐降低,当NOM的添加量达到2.5 g/L时,溶液pH降低到5.3。由于NOM的加入所导致的溶液pH降低加速了NZVI@mSiO2中NZVI核的腐蚀与NZVI上形成的钝化层的剥除,从而提高了NZVI@mSiO2的去除效率。
另外,NOM具有较强的与阳离子结合而形成稳定化合物的能力,这也可能影响ZVI对污染物的去除[36]。ZVI腐蚀产生的离子也会与NOM复合,导致反应体系中生成沉淀,这些沉淀物同样增加了吸附表面,促进ZVI对污染物的去除。Liu等[37-38]报道,在用ZVI处理Cr6+时,Fe-腐植酸(HA)复合物的形成加速了ZVI的溶解。随着ZVI的溶解,在Ca2+和Mg2+离子存在的情况下甚至形成直径为0.45 μm的金属-HA复合物[39]。这些复合物可能会影响ZVI体系污染物的吸附或降解。例如,由于NOM增加了两种醌类的电子传导介质(羟萘醌和蒽醌-2,6-二磺酸),硝基苯(NB)和CT的还原速率有所增加,HA被观测到可以从内部的ZVI核传递电子到外层的Fe3+,从而使外层的Fe3+-HA复合物中的Fe3+转变为Fe2+,用以还原溴酸盐[40]。Liu等[37]也发现,HA的存在可提高ZVI对三氯乙烯(TCE)的去除,原因是 HA在ZVI表面的吸附重新分割了ZVI表面形成的沉积物,从而使其能够继续与TCE反应。
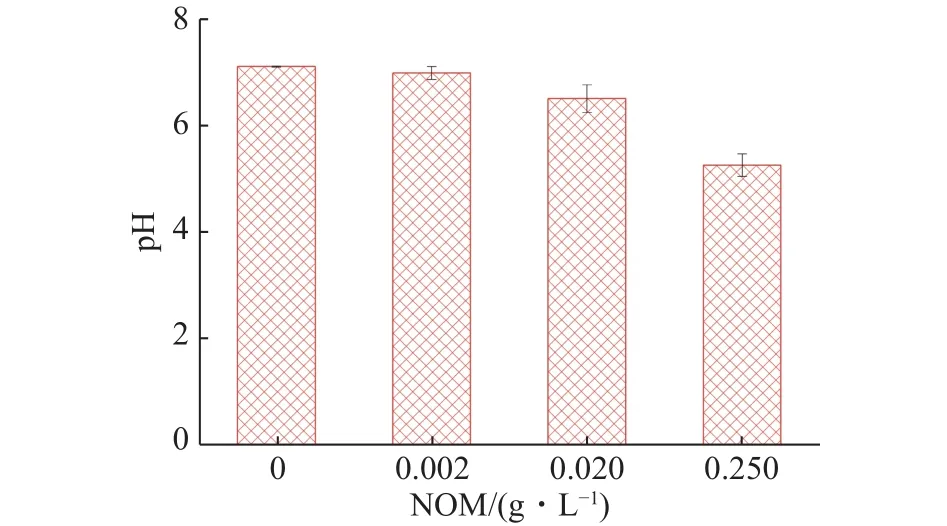
图 9 不同NOM添加量时 NZVI@mSiO2去除1,1,1−TCA体系的pH Fig.9 Solution pH value at different NOM dosages
前面讨论了NOM添加量对mSiO2吸附去除氯代烃的影响。NOM将会引入新的成分,这些新的成分可能会增加新的吸附位点,促进对污染物的吸附去除。可见,NOM添加量对NZVI@mSiO2去除氯代烃的影响包括:增加吸附表面而导致1,1,1-TCA的吸附去除;降低了体系pH而提高NZVI核的反应活性并促进1,1,1-TCA 的吸附-降解去除。
3 结 论
a. 在加入TEOS后4 h便可获得结构稳定的NZVI@mSiO2。
b. mSiO2壳层厚度随着TEOS添加量的增加而增大。
c. 高的铁剂量提供更多可供反应的活性位点,有利于对氯代烃的去除。
d. NOM降低了NZVI@mSiO2与水悬浮液的稳定性,但由于其增加的吸附位点及部分溶解后降低了溶液pH而促进了对氯代烃的吸附去除与吸附-降解去除。

