流动注射法测定海水中的活性硅酸盐
鲍静姣,尤炬炬,郭远明,王 姮
(1.浙江省海洋水产研究所,浙江 舟山 316021;2.浙江省海洋渔业资源可持续利用技术研究重点实验室,浙江 舟山 316021)
海水中的硅酸盐是生物生长所必需的营养盐之一,是构成硅藻、放射虫和有孔虫等海洋生物有机体的重要组分[1],在海洋生态系统中起着至关重要的作用。海水中的硅酸盐若低于一定浓度水平,硅藻等浮游生物的生长便会受抑制,从而导致海洋初级生产力降低;而浓度太高时,则易引发赤潮等灾害性现象[2]。因此,监测海水中的硅酸盐对海洋生物资源的开发利用和赤潮预报具有重要的意义[3]。目前海水中的活性硅酸盐的分析方法以传统的分光光度法为主,这个方法基本上都存在分析速度慢和稳定性等缺点。近年来,不少学者运用流动注射分析仪进行活性硅酸盐的测定。流动注射法是由丹麦技术大学的RUZICKA和HAMNSEN提出的一门易于实现实时、在线分析的新型自动分析技术[4]。在此技术之上不断完善海水中活性硅酸盐的流动注射分析法,使样品基体稳定,精密度好,操作简便、快捷,利于在线分析,非常适合大批量的海水样品测定。
1 材料与方法
1.1 原理
酸性条件下,硅酸盐和钼酸盐、抗坏血酸反应生成一种蓝色化合物在820 nm下检测。在加入抗坏血酸前加入草酸的目的是为了减少磷酸盐的干扰。
1.2 仪器
德国SEAL Analytical AA3流动注射分析仪(流动注射分析仪硅酸盐分析模块流路如图1所示)、37℃加热池(5.37mL)、泵管(6+2空气+1进样器冲洗)、实验室常用仪器和器皿。
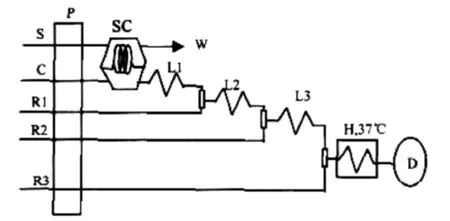
P:蠕动泵; S:样品; C:载流; R1:显色剂; R2:草酸; R3:抗坏血酸;SC:采样环; L1-L3:混合圈; H:加热装置; W:排废; D:检测器
图1 可溶性硅酸盐测定流路
Fig.1 Flow diagram of soluble silicates determination
1.3 试剂
硅酸盐标准溶液:300.0mg/L(国家标准物质);
硅酸盐标准使用液:用硅酸盐标准溶液配制成15.0 mg/L的硅酸盐标准使用液;
钼酸铵:将4.2 mL浓硫酸边搅拌边加入800 mL纯水中,再加入15 g钼酸铵和5 gSDS并稀释至1L,混合均匀后储存于棕色聚乙烯瓶中,每两周更新。溶液必须是澄清无色的;
抗坏血酸:50 g抗坏血酸溶于700 mL纯水,稀释至1000 mL。溶液混均匀,储存于棕色聚乙烯瓶中,每周更新;
草酸溶液:95 g草酸溶于800 mL纯水,稀释至1000 mL。溶液混均匀,储存于棕色聚乙烯瓶中。
1.4 实验方法
1.4.1 标准系列配置
取6个50 mL容量瓶分别移取:0.00、1.00、2.00、4.00、6.00、8.00 mL硅酸盐标准使用液加纯水稀释至标线,混匀,使标准系列浓度分别为:0.000、0.300、0.600、1.20、1.80、2.40 mg/L。
1.4.2 仪器测定
按图1连接试剂、纯水和试样。打开AA3流动注射分析仪和工作软件,键入实验参数:选通道、杯续杯数、样品数;进样/冲洗:3.0;平滑:10;基线校正:自动基线参比(%)10,运行延迟时间(min):6.0。为了使样品不受环境等污染,在进样器外安装了有机玻璃罩。
启动AA3流动注射分析仪,37℃加热池(5.37 mL),泵入纯水至基线稳定后,再泵入试剂到进样通道,达到试剂基线稳定。测定标准曲线,要先测一下标准曲线浓度的最高点,最佳峰高75%~95%之间,设定它的增益点,然后开始自动分析。
2 结果与讨论
2.1 条件试验和优化
通过试验表明,当S 泵管内径为1.85 mm,C 泵管内径为1.52 mm,R1 泵管内径0.89 mm,R2 泵管内径为0.64 mm,R3 泵管内径为0.89 mm,L1 混合圈长75 cm,L2和L3 混合圈长均为135 cm,SC 毛细管长为250 cm,泵速为35 r /min 时,试验基线平稳,可获得较高且稳定的吸光度值。
2.1.1 选择泵管
通过试验表明,对于流量≤0.6 mL/min 使用管116-0536-07,即草酸泵管和抗坏血酸泵管;对于流量≥0.6 mL/min 使用管116-0536-11,即钼酸铵泵管。通过实验,泵管的粗细,使试剂和样品的流速加入有精确的测量过程,每2 s 注入1 个气泡,一个样品包括20~30 个片断,每一个片段被测量100 次,即每一个样品会被测量2 000~3 000 次。反应过程中产生的小气泡能轻易溶入大气泡中,不会产生乱峰,并降低流速和减少试剂消耗,可以反应完全,不用担心扩散和带过,因此以上的泵管选择为最佳。
2.1.2 基体效应
样品本身的颜色,一些物质的荧光特性等造成测量不准称之为基体效应。将试验中的显色剂溶液用去离子水代替,其他试剂及实验条件完全不变,对样品进行测定,如有响应,则存在基体效应,通过实验发现,测定基线平稳,说明本方法无基体效应。
2.1.3 盐度干扰
由于海水中由于海水含有大量的Cl-、Na+等,对反应有一定的影响,试验配制不同盐度的1.00 mg /L 硅标准溶液,对其进行测定,测定结果表1 所示:结果可以发现,海水的盐度不同,对于含有相同SiO32-浓度的样品,测定结果差异较大,需要对结果进行校正。
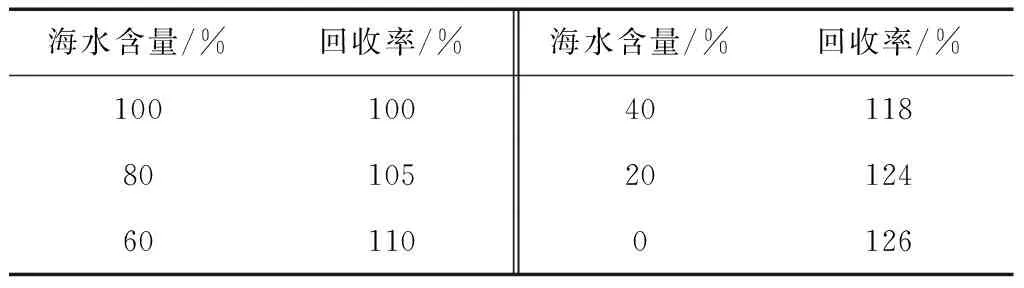
表1 盐分变化影响
2.2 方法的线性、最低检出限
在上述已优化好的测量条件下,设定检测范围内0.00~2.40 mg/L进行测定标准曲线,线性关系良好,相关系数均为0.9999左右,能满足检测要求。SiO32-标准曲线测定结果如图2所示。
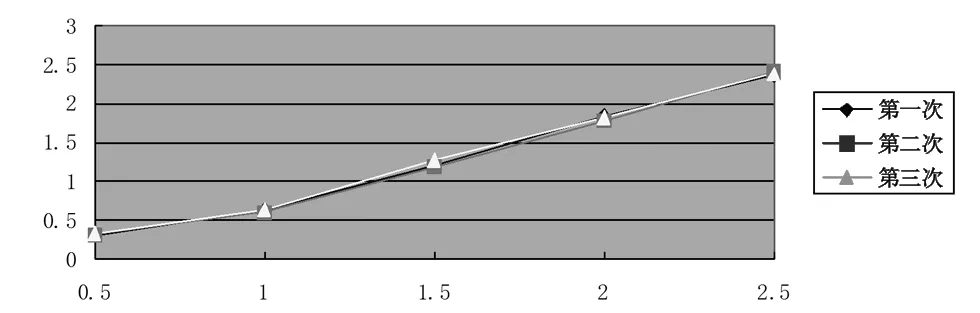
图2 SiO32-标准曲线
检出限:用统计测量法对空白溶液连续测定15次,得出方法检出限0.050 mg/L。
2.3 精密度和准确度
平行测定不同浓度的标准样品 6 次,求得不同浓度的相对标准偏差见表 2。
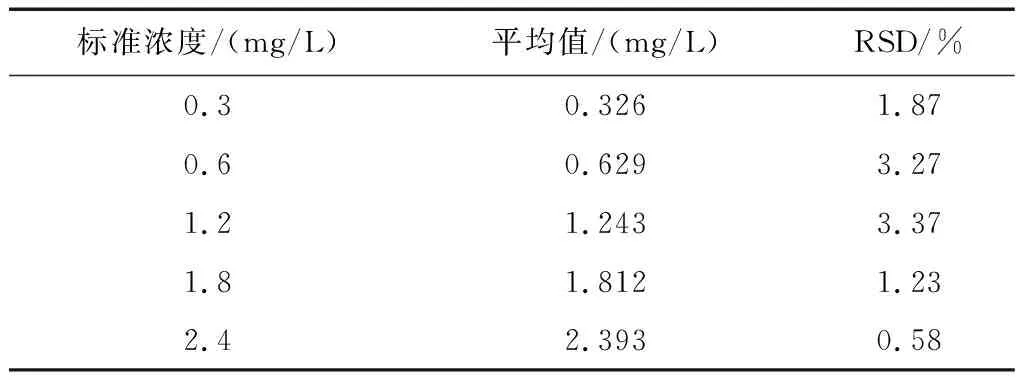
表2 不同浓度标液的相对标准偏差
从表2可以看出当样品浓度在 0.300~2.40 mg/L 时,测定的相对标准偏差均≤5.0%,《海洋监测规范》要求 RSD≤10%[5]。结果表明,该方法有较好的精密度,符合国标的检测要求。
2.4 实际海水样品检测结果及加标回收率实验
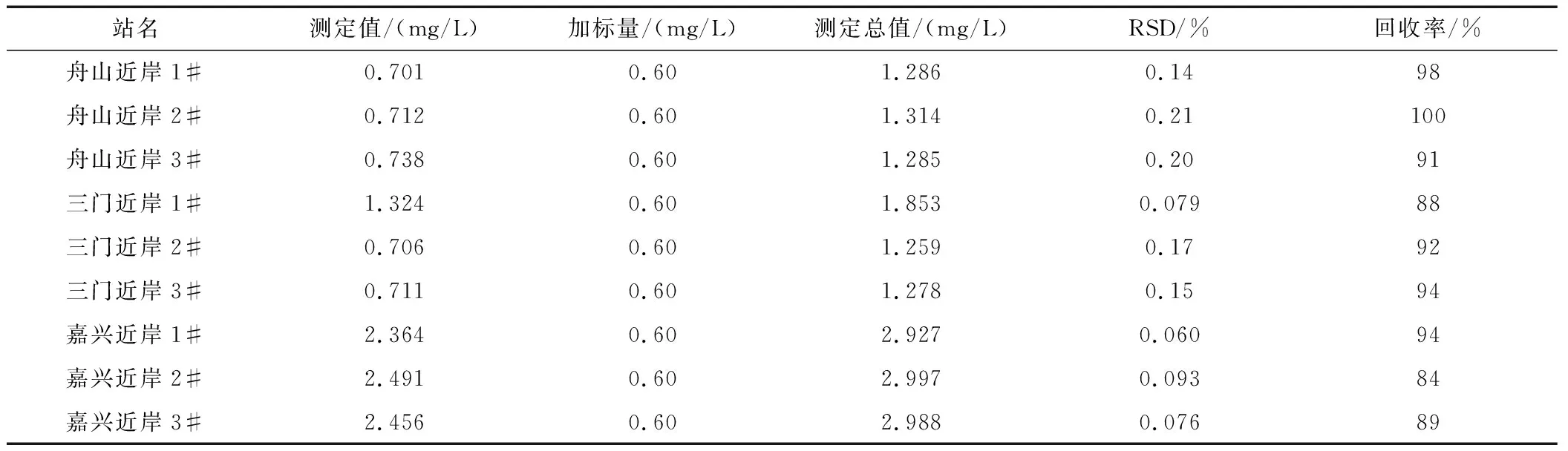
表3 样品分析结果
本文对舟山、三门和嘉兴附近海域采集样品,将水样过滤后直接进样分析,平行测定 6 次,同时采用标准加入法,检验方法的回收率。分析结果与方法的回收率见表3。
从表 3 可以看出,方法的 RSD 完全能满足《海洋监测规范》的要求,RSD 分别为 0.060%~0.21%,加标回收率为 84%~100%。
3 小结
本文讨论了运用AA3流动注射分析仪测定海水中的活性硅酸盐,选择最佳优化条件,建立最佳测定方法。标准曲线的相关系数均在0.9999左右,水样经过滤无需处理,在浓度范围内直接检测,得出结果。该方法操作简单,测定速度快,每小时测定的样品高达35个,具有快速、省时、方便、基体干扰小,精密度、准确性好等优点,适用于批量样品的测定。

