有机胺溶液吸收二氧化硫解析再生与工艺条件的相关性研究
杨学彦,张立忠,李国明,杨晓丽
(宁夏宝塔石化科技实业发展有限公司,宁夏 银川 750001)
1 材料与方法
1.1 材料与试剂
见表1。

表1 实验药品
1.2 实验仪器
见表2。

表2 实验仪器
1.3 连续试验装置及流程

1-二氧化硫钢瓶,2-空气压缩机,3-转子流量计,4-吸收塔,5-蠕动泵,6-储液罐,7-解吸塔,8-即热式电加热套,9-蛇形冷凝管,10-真空泵,11-冷却水浴锅
图1 乙二胺/磷酸溶液脱硫流程图

1-真空泵,2-U型压差计,3-转子流量计,4-阀门,5-解吸塔出口混合气体
实验装置分为四个部分:一是模拟烟道气供气装置,二是吸收塔,三是解吸塔,四是液相液体加热和冷却循环装置。从图1可以看出模拟烟气由空气压缩机和二氧化硫钢瓶通过流量计控制,排放出一定比例的SO2气体和空气的混合气体进入吸收塔下部,与自上而下的吸收液逆流接触。来自吸收塔的冷富液在进入解吸塔之前需要加热,要加热到一定的解吸温度才能进解吸塔,在这里用的加热的装置为圆筒柱状的即热式加热器,解吸塔内的热富液(富含SO2的吸收液)被闪蒸后,热富液中的蒸汽从解吸塔顶通过玻璃蛇形冷凝管冷却,热贫液通过自制冷却水浴锅冷却,然后进入储液罐,在这过程用的冷却介质为恒量自来水。在整个循环过程的流程具体有:(一)模拟烟道气经过缓冲罐用玻璃转子流量计(3-1,3-2)控制一定的流量,再输送到吸收塔底部(4),在吸收塔内没有完全吸收的SO2就从吸收塔(4)顶部的分流管排出。(二)吸收液从储液罐(6-2)通过泵(5-1)抽取到吸收塔(4)顶部自上而下用于吸收,然后回到储液罐(6-1),此过程中用流量计(3-3)控制吸收液流量,(三)富液通过泵(5-2)输送到解吸塔顶部,然后在解析塔内自上而下进行解吸,再回到储液罐(6-2),在此过程中富液要先经过圆筒柱状的即热式加热器(8)才进入解析塔。(四)解析出来的SO2蒸汽被蛇形冷凝管冷凝(9),SO2气体通过真空泵(10)抽到进气口位置继续吸收,冷却后的液体就顺着管路流到储液罐(6-2),解吸后的高贫液从塔底侧端流入贫液罐,后将高温贫液放于水浴锅内(11),再次通过水浴锅内恒量的自来水冷却贫液,使温度降低至25~30℃左右。然后继续做循环吸收,以上就是整个气液走向流程。相关用的设备及材料,混合气体从底部经过用不锈钢钢管自制的吸收和解吸塔,其填料是用陶瓷拉西环散装填装。通过用型号为KPPC75DC24CTRL蠕动泵输送吸收液在吸收塔和解吸塔间循环,实验所用的管道是耐高温的硅胶管内径为8 mm。整个实验温度是通过热电偶控制加热液体的温度,使得整个过程液体的温度能控制在所需的温度范围,自制冷却水浴锅的材料为不锈钢材质。
1.4 实验操作
前期的单变量间歇实验得到了吸收和解吸过程中的最佳脱硫率和解吸率操作工艺参数,在连续性试验中采用的最佳操作工艺参数和设备几何尺寸:吸收温度为室温,解吸温度在95~105℃,乙二胺+磷酸溶液中乙二胺浓度为0.3mol/L,模拟烟道气体积流量70 m3/h,在吸收液浓度为0.3 mol/L时烟道气中SO2摩尔分数分别定格为0.1%和0.2%,气液两相的体积流量比G/L=0.8~1.0,溶液初始pH值6.5~7.0,吸收液和解吸液的循环流量为100 L/h。以上就是在间歇性试验中得到的最佳试验参数。符合上述工艺参数的设备几何尺寸。吸收塔的塔径为41 mm,填料层的高度为2.2 m;解吸塔的塔径为41 mm,填料层的高度为2.2 m,填料塔加工材质为不锈钢,填料为散堆填装的拉西环尺寸为10×10×1.5 mm。本论文在此基础上按照图1进行吸收和解吸的连续性试验。
(1)在实验之前,将自来水灌入贮液灌中,按照实验的步骤正常先运行一次,需检查的项目要包括整套系统各个接口处是否有漏水现象,流量计是否能正常显示出读数,加热器实验装置是否有堵塞现象,是否能稳定供热等,每个风机与高低温循环泵是否可以进行正常的运转;
(2)若装置没有异常后,将按要求配制的0.3 mol/L乙二胺含量和52 L pH值=7.5的乙二胺-磷酸吸收液平均灌入吸收塔和解吸塔的贮液罐中;
(3)打开低高温循环泵,使循环泵的流量均要达到100 L/h;
(4)打开主风机,使空气流量达到100 m3/h;
(5)打开抽风机,观察U型管和转子流量计是否正常;
(6)打开SO2钢瓶的阀门,调节阀门和转子流量计使SO2流量达到所需值;
(7)用规格为50mL的注射器隔十五分钟在吸收塔进气口、出气口和排气口取气40mL,碘量法测定所取得气体SO2含量,并在贮液槽出口处放约10mL的液,用pH计测定吸收液pH值;
(8)当吸收率低于90%或者pH值低于6.0则开始解吸:开自来水开关,再打开两个加热器,调节变频器使它稳定在预定温度;
(9)每隔15min,用规格为50 mL注射器在吸收塔进气口处、吸收塔出气口处和排气口处取气40 mL,用规格为20 mL注射器在解吸气体风机出口处抽20 mL气,并在贮液槽出口处放约10 mL液,用pH计测吸收液的pH值;
(10)当实验数据均达到稳定,解析率、吸收率和pH值都能基本维持不变的情况下,说明实验结束,关闭系统。
1.5 实验测定方法
1.5.1 SO2浓度测定
根据实验室的条件和课题研究要求,再加上碘量法操作简单,本实验采用碘液法[1-2]测定烟道气中SO2浓度和烟道气中SO2含量。
在做实验中采用的是抽取的方式抽取SO2,从而测定烟道气中SO2含量,在试验前必须要做空白滴定实验提供参数,滴定吸收溶液所消耗的碘液量为V0。在实验过程中用规格为50 mL注射器在模拟烟气中取体积为V1mL的混合气,将混合气体慢慢注入8mL装有氨基磺酸铵和硫酸铵配制的混合吸收溶液中。在滴定实验开始时在吸收溶液中滴两三滴的淀粉溶液作指示剂,再用碘液滴定混合吸收液,当溶液颜色变化是从无色变为蓝色,说明滴定实验操作已经到了终点,结束操作,记录下碘液消耗量V。则烟道气中SO2的浓度计算公式为:
(1)
C-烟道气中二氧化硫浓度,mg/m3;
V-滴定烟道气消耗的碘液量,mL;
V0-空白滴定消耗碘液量,mL;
V1-取样烟气的体积,mL。
C0-碘液浓度,mol/L;
1.5.2 吸收率计算方法
试验中每隔15min用注射器在吸收塔气体进出口处抽取烟道气40 mL,慢慢注入到8 mL氨基磺酸铵+硫酸铵溶液中,让SO2被充分吸收后,用碘量法滴定的方法测定计算烟道气中SO2的浓度,如下所示就是计算吸收率的计算公式:

(2)
C0-吸收塔进气口处烟道气中SO2浓度,mg/m3;
C1-吸收塔出气口处烟道气中SO2浓度,mg/m3。
1.5.3 解吸率计算方法
隔15min,用规格为50mL注射器在气体入口和出口处取4 mL气,用规格为20 mL注射器在解吸气体风机出口处抽气20 mL,碘量法分别滴定测定和计算烟道气中SO2的浓度和解吸气体抽风机出口处的SO2的浓度,吸收塔进出口的体积流量为Q1,解吸出口的体积流量为Q解,并用如下计算式计算解吸过程的解吸率。

(3)
C0-吸收塔进气口处烟道气中SO2浓度,mg/m3;
C1-吸收塔出气口处烟道气中SO2浓度,mg/m3;
C解-解吸气体抽风机出口处的SO2的浓度,mg/m3;
Q解-解吸出口的体积流量,m3/h;
Q1-吸收塔进出口的体积流量,m3/h。
2 结果与讨论
2.1 SO2浓度对吸收率和解吸率的影响
在实验研究中分别测试了不同解吸温度(95℃和98℃)下不同烟道气(SO2浓度分别是0.1%和0.2%)SO2起始浓度对吸收率和解吸率的影响。其中初始吸收液pH值 为7.5,初始乙二胺浓度为0.3 mol/L,液气比为1.0 L/m3。得到的吸收率和解析率随时间的变化曲线图,如图3~6所示。
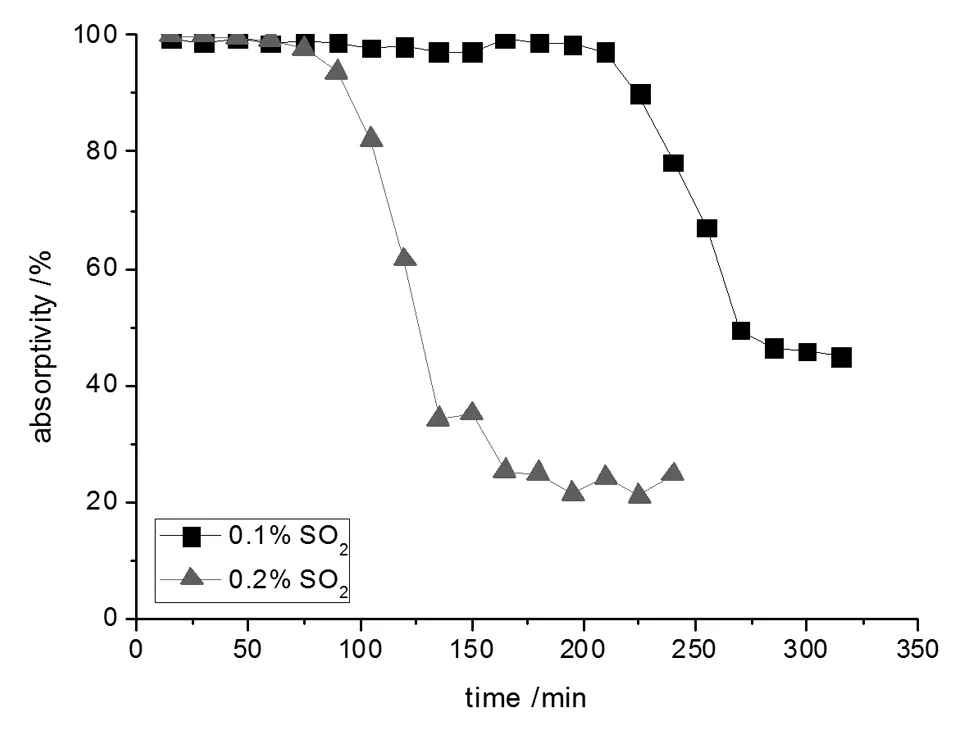
图3 不同SO2浓度对吸收率的影响(解吸温度95℃)

图4 不同SO2浓度对吸收率的影响(解吸温度98℃)
从图3和图4中可以知道,吸收率曲线在初始一段时间内保持一定值且基本不变,而过了一段时间后随着吸收时间的延长SO2的吸收率明显降低,再经过一定时间后吸收率又趋向一个较低数值的稳态。
在上述曲线图中可以得出结论就是烟道气SO2浓度高会提高乙二胺的吸收率,但实验的进行后期在其他条件(如热稳态盐)的影响下,吸收液对低浓度的SO2的吸收率要高。

图5 不同SO2浓度对解吸率的影响(解吸温度95℃)

图6 不同SO2浓度对解吸率的影响(解吸温度98℃)
在图5和图6可以看出实验解吸数据有一段都是零,是因为在反应开始时,解析反应还没开始,等吸收率下降到95%或者pH值达到6的时候才开始解吸操作,所以从这里我们也知道,SO2浓度高的吸收速率快,易达到解析过程,在解析过程开始的一段时间,解析率是随着时间的推移缓慢上升,但到了一定时间之后解析速率猛升,几乎成斜率为1,但又过一段时间解析率开始下降。在一定程度上解析率对烟气SO2浓度也有一定的依赖性,烟气SO2浓度越高解吸速率就越快,对于0.1%的SO2和0.2%的烟气SO2对比来说浓度高的解析率就高,从数据分析的图中也可以知道烟气SO2浓度高的其在图中的斜率就大,从上述四个图的分析中得出的结论:在反应的一定时间内烟道气中SO2浓度越高越促进乙二胺的吸收和解吸,在解吸反应进行两小时后乙二胺吸收液对吸收低浓度SO2更有优势。
3 结论
本论文在连续性试验得出如下主要结论:
(1)在连续性试验操作中一定的反应时间内烟道气中SO2浓度越高越促进乙二胺对SO2的吸收和解吸,但反应足够长时对吸收低浓度SO2更有优势。
(2)在试验研究中随着解吸温度的升高溶液的解吸能力越强。在相同二氧化硫浓度不同解吸温度95℃和98℃相比下,解吸温度高的,解吸率高。
(3)在相同二氧化硫浓度不同解吸温度95℃和98℃相比下,解吸温度高的,循环对应的吸收率低。

