高效液相色谱法测定冬凌草甲素脂质体的含量
王知平
(山西卫生健康职业学院,山西太原030012)
冬凌草甲素(oridonin)属于贝壳杉烯二萜类化合物,是从唇形科(Labiatae)香茶菜属(Isodon)植物冬凌草中提取出的主要成分,该物质具有抗癌活性[1-2]。由于冬凌草甲素味苦,水溶性、脂溶性较差,不适合直接制备成注射液或者乳剂,且制备片剂的生物利用度较低。有文献报道,采用加入有机溶剂和表面活性剂的方法可增加冬凌草甲素的溶解度制备成静脉注射剂,但此种方法改进容易引起不良反应[3]。通过对冬凌草甲素的性质进行分析,决定将其制为脂质体,增加溶解度,提高药物的生物利用度。文献报道,多采用薄层色谱法、反相高效液相色谱法、高效毛细管电泳法等方法测定冬凌草甲素的含量。本文采用高效液相色谱法(HPLC)测定冬凌草甲素及其自制脂质体的含量,方法简便,结果准确,为其脂质体的质量控制提供参考。
1 仪器与试药
1260系列高效液相色谱系统(美国Agilent公司,G1314B DAD检测器,G1311C四元泵,G1329B标准型自动进样器,G1316A柱温箱)。冬凌草甲素原料药(南京邦诺生物科技有限公司,纯度>98.0%);冬凌草甲素对照品(中国药品生物制品检定所,批号:111721-200501,纯度>98.5%);乙腈、甲醇均为色谱纯(山东禹王实业有限公司),其余试剂为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Agilent Zorbax C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水(55∶45);柱温:30 ℃;检测波长:241 nm;流速:1 mL/min;进样量:20 μL。理论板数按冬凌草甲素峰计不低于2 000,冬凌草甲素与杂质峰之间的分离度应符合要求R>1.5,冬凌草甲素峰的拖尾因子小于 1.5。
在此色谱条件下,冬凌甲素对照品及冬凌甲素钠脂质体色谱图见图1。
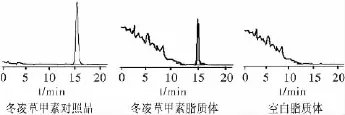
图1 冬凌甲素对照品、冬凌甲素钠脂质体和空白脂质体色谱图
2.2 线性试验
对照品贮备液的配制:精密称取冬凌草甲素对照品10 mg,置于50 mL的容量瓶中,加甲醇溶解,稀释至50 mL刻度线,摇匀,即得。
对照品溶液的配制:取6个洗净的10 mL容量瓶,分别精密移取对照品贮备液0.5 mL、1.0 mL、2.0 mL、3.0 mL、4.0 mL、5.0 mL 于容量瓶中,加流动相稀释至10 mL刻度线,摇匀,得到浓度分别为10 μg/mL,20 μg/mL,40 μg/mL,60 μg/mL,80 μg/mL,100 μg/mL 的系列对照品溶液,按照“2.1”项下条件进样,记录色谱图。横坐标为冬凌草甲素的量(μg),纵坐标为冬凌草甲素的峰面积(A),绘制标准曲线进行回归,回归方程为:A=22.18C+6.15,r=0.999 5。结果表明,冬凌草甲素在10~100 μg/mL浓度范围内,峰面积与浓度线性关系良好。
2.3 溶液稳定性试验
取6份浓度为40 μg/mL的对照品溶液,在室温下放置,分别于 0 h、1 h、2 h、3 h、4 h、6 h、8 h、10 h、12 h 进样 20 μL,得到色谱图,记录峰面积。结果表明:冬凌草甲素峰面积的RSD为0.72%,表明样品溶液在12 h之内稳定。
2.4 精密度试验
精密配制浓度为 10 μg/mL,40 μg/mL,80 μg/mL的对照品溶液各3份,同一天内早、中、晚各进样分析两次,记录色谱图,代入标准曲线中计算药物浓度,计算日间精密度、日内精密度和准确度。结果表明,日内、日间精密度的RSD分别为0.8%和1.2%,准确度在90%~110%之间(测定的平均药物浓度与实际浓度的比值)。
2.5 重复性实验
精密量取冬凌草甲素脂质体6份,加入甲醇溶解超声10 min破乳,使溶液澄清,流动相定容,并摇匀,配制成一定浓度的溶液,取20 μL进样,并记录色谱图,将峰面积带入标准曲线中计算得到冬凌草甲素脂质体中药物的含量。结果显示,冬凌草甲素的含量RSD为1.92%,表明此方法重复性良好。
2.6 回收率试验
精密量取空白脂质体1.0 mL共9份,置于10 mL的容量瓶中,分别加入冬凌草甲素对照品,配成相当于样品含量的80%,100%,120%低、中、高浓度的样品溶液各三份。将上述溶液,加入适量甲醇溶解超声破乳,进样,得到色谱图,记录峰面积,代入回归方程,得到冬凌草甲素脂质体中药物的含量。再将测得量与加入量相比得到冬凌草甲素的加样回收率,结果显示低、中、高三个浓度的平均回收率分别为100.3%,99.9%,99.5%,RSD分别为1.2%,0.58%,0.56%。平均回收率为99.9%,平均RSD为0.77%。
2.7 冬凌草甲素脂质体包封率的测定
包封率是指包封于脂质体内的药物量占脂质体混悬液药物总量的比例。
洗脱液用PBS水溶液,配制方法:取磷酸二氢钾6.8 g,纯净水稀释至1 000 mL,采用NaOH溶液调节pH至6.5。
取自制冬凌草甲素脂质体样品3批(批号为20170504,20170511,20170515),每批取 3 份,分别上样于已预先用生理盐水平衡好的Sephadex-G50凝胶柱,洗脱液以0.5 mL/min的流速洗脱,将药物洗脱液分别收集在10 mL的容量瓶中,加甲醇超声破乳,流动相定容,取20 μL进样,得到色谱图,记录峰面积,代入回归方程,计算得到溶液中冬凌草甲素的质量m1。
精密吸取同样量未过柱的冬凌草甲素脂质体三批(批号为 20170504,20170511,20170515),每批取3份,置于10 mL量瓶中,甲醇溶解超声破乳,流动相定容,进样,得到色谱图,记录峰面积,代入回归方程,计算药物质量,取平均值,得总药物质量m1。计算包封率,其包封率分别为95.82%、94.39%、94.75%,平均包封率为94.99%。
3 讨论
本研究中,破乳影响药物的释放,影响药物包封率的测定,进而影响脂质体质量的好坏,而破乳选择的方法是超声,因此需要通过选择合适的超声时间进行破乳[2]。利用紫外可见分光光度计对冬凌草甲素和脂质体中辅料在200~400 nm波长下扫描,发现冬凌草甲素在241 nm附近有最大吸收,因此选择241 nm作为检测波长。
有关包封率的测定大多采用离心超滤法、凝胶过滤法、透析法、葡聚糖凝胶柱层析法等。在前期研究中,将这几种方法都做了比较,4种方法测得结果葡聚糖凝胶柱层析法的结果最好,因此选择了比较经典的葡聚糖凝胶柱层析法测定[4]。
本文建立高效液相色谱法测定自制冬凌草甲素脂质体中冬凌草甲素的含量,方法简便,容易操作,测定结果准确,包封率测定也符合要求。

