高通量测序在罗氏沼虾抗病力比较中的应用
明 磊,戴习林*,江宗冰,丁福江
(1.上海海洋大学/农业部淡水水产种质资源重点实验室,上海 201306; 2.上海申漕特种水产开发公司,上海 201516)
罗氏沼虾(Macrobrachiumrosenbergii)属节肢动物门(Arthropoda)、甲壳纲(Crustacea)、十足目(Decaplda)、游泳亚目(Natqntin)、长臂虾科(Palaemonidae)、沼虾属(Macrobrachium),自然分布于东南亚各国,印度、斯里兰卡、泰国、马来西亚、柬埔寨、越南、菲律宾等国的淡水、半咸水环境中均有分布,被不少国家和地区移养繁殖,成为移养地的主要淡水养殖品种[1]。近年来,由于养殖模式集约化以及养殖水环境恶化等问题,罗氏沼虾病害日趋严重,其中由弧菌引起的细菌性疾病可发生于罗氏沼虾的亲虾培育和育苗阶段,临床表现为肌肉白浊、红体等,病虾常浮于水面,给罗氏沼虾的苗种业和养殖业带来巨大危害。
溶藻弧菌(Vibrioalginolyticus)属于弧菌科(Vibrionaceae)、弧菌属(Vibrio),为革兰氏阴性短杆菌[2],广泛分布于世界各地海水及河口区[3],数量在海水类弧菌中居于首位[4],对鱼、虾、蟹等水产动物均具有较强的致病性。为了提高罗氏沼虾的抗病性能,笔者所在实验室自2011年通过自然选择和人工感染溶藻弧菌开展了罗氏沼虾的抗病选育工作。为了进一步了解罗氏沼虾抗病子3代群体的抗病性能,本研究通过对罗氏沼虾进行溶藻弧菌肌肉注射感染,借助高通量测序首先分析了注射溶藻弧菌后罗氏沼虾体内菌群的变化,然后对感染成活率最高和最低的抗病选育群体以及非选育群体的养殖池水及肠道组织进行菌群多样性分析,以期为罗氏沼虾的免疫机制研究以及进一步选育提供理论依据。
1 材料和方法
1.1 试验材料
试验亲虾的基础群体来源于上海申漕特种水产开发公司的人工养殖繁殖群体(已连续 15 a闭锁选育),采取肌肉注射方法感染溶藻弧菌,存活的健康罗氏沼虾群体作为抗病专门化品系选择系的基础群体[5]。试验用虾是经人工选择配对和育苗并自然交尾建立的4个罗氏沼虾抗病专门化品系中选择系子3代群体(A、B、C、D)和1个上海申漕特种水产开发公司繁育养殖的非选育群体(E)。5个群体试验用虾规格一致,体长(8.25±0.73)cm,体质量(16.76±4.76)g,于水泥池(8 m×3 m×1.2 m)中养殖。试验用溶藻弧菌为从上海申漕特种水产开发公司的罗氏沼虾亲虾培育池养殖水体中分离,经鉴定传代保种的溶藻弧菌菌种,对罗氏沼虾具有很强致病性[5]。试验用水为24 h曝气后经检测无余氯残留的自来水。
1.2 试验方法
1.2.1 菌悬液的制备 将菌种在牛肉膏蛋白胨液体培养基中活化,然后在TCBS固体培养基中进行划线分离,37 ℃培养24 h;挑选长势良好的菌落接种于牛肉膏蛋白胨液体培养基,于28 ℃、200 r/min恒温振荡培养箱富集培养18 h;收集菌液,4 ℃、4 000 r/min离心10 min后弃上清液,无菌生理盐水洗涤沉淀2次后按要求稀释成1×108cfu/mL(采用平板活菌计数法)的菌悬液,4 ℃保存备用。
1.2.2 注射感染试验及肌肉组织的取样 做试验前将试验水槽(70 cm×50 cm×40 cm)冲洗干净,用5‰高锰酸钾水溶液浸泡30~60 min进行消毒,最后用自来水冲洗干净。向水槽中注入占水槽体积2/3的自来水,充分曝气24 h后放虾。
对4个抗病选育群体(A、B、C、D)和1个非选育群体(E)进行弧菌注射感染试验,各罗氏沼虾群体的对照组(a、b、c、d、e)注射生理盐水,每个试验组均设2个平行。感染方法为肌肉注射法,在第二、三腹节间注射1×108cfu/mL的溶藻弧菌悬液(此剂量经预试验确定),注射剂量为3×106cfu/g。
每个平行组感染20只虾(1 min内感染完成),分别在感染后5、30、60、90、120 min取样,每个平行组在不同取样时间点各随机选取1只存活的罗氏沼虾,于无菌条件下取感染部位(第二、三腹节间)的肌肉放入灭菌离心管中(同一试验组的2个平行肌肉样品放1个离心管),标记后-80 ℃冷冻保存。样品编号:A群体感染组编号依次为A1、A2、A3、A4、A5,其生理盐水对照组为a1、a2、a3、a4、a5;以此类推,共50个样品。
取完虾样后,每个平行组感染30只虾用来统计不同群体的感染成活率,试验周期为15 d,每天定时统计各组的死亡只数。试验虾的日常管理工作参照文献[5]的方法进行。
1.2.3 罗氏沼虾肠道和养殖水环境的取样 对感染成活率最低、最高的罗氏沼虾抗病选育群体以及非抗病选育群体进行取样,取样样品包括罗氏沼虾的水泥池(8 m×3 m×1.2 m)养殖水体及肠道组织。养殖水体样品的编号依次为F、G、H,肠道组织的编号分别为Ⅰ、Ⅱ、Ⅲ。取样方法为每个养殖水泥池的四角和中间分别取500 mL水体,混合后用0.22 μm孔径的无菌纤维素滤膜进行抽滤,无菌滤膜-80 ℃保存备用。同时每个池挑选规格一致的10只虾(每个取样点2只),于冰上无菌操作获取肠道组织,将10只虾的肠道混合成一个样品。
1.2.4 高通量测序 用 OMEGA 公司的 Soil DNA试剂盒提取罗氏沼虾组织样本和养殖水体中的细菌总DNA,用1%琼脂糖凝胶电泳检测DNA完整性。PCR扩增的引物序列为338F:5′-ACTCCTACGGGAGGCAGCA-3′,806R:5′-GGACTACHVGGGTWTCTAAT-3′。PCR扩增采用20 μL反应体系:5×Fast Pfu Buffer 4 μL,2.5 mmol/L dNTPs 2 μL,引物(5 μmol/L)各0.8 μL,BSA 0.2 μL,Fast Pfu Polymerase 0.4 μL,Template DNA 10 ng,补 ddH2O 至20 μL。PCR反应条件:95 ℃变性180 s;95 ℃ 30 s,55 ℃ 30 s,72 ℃ 45 s,28 个循环;72 ℃延伸10 min。使用上海美吉生物公司16s-338F-806R MiSeq测序平台进行测序。
1.2.5 测序数据的分析
1.2.5.1 数据分析流程 数据分析流程主要包括:数据处理→聚类(Operational taxonomic unit,OTU)→分类学分析。其具体分析方法为:使用Trimmomatic和FLASH软件对数据进行优化和统计;采用Usearch(Version 7.1,http://drive5.com/uparse/)软件平台进行OTU聚类,采用RDP classifier贝叶斯算法对97%相似水平的OTU代表序列进行分类学分析,并分别在各个分类水平统计各样本的群落组成;计算统计学分析指数(Chao、Ace、Shannon、Simpson),估计环境群落的物种丰度和多样性;使用97%相似度的OTU,利用mothur进行稀释性分析,利用R语言工具制作稀释性曲线图;使用97%相似度的OTU,利用mothur计算不同随机抽样下的多样性指数Shannon值,利用R语言工具制作曲线图;OTU分布Venn图利用R语言工具统计并作图;利用R语言进行主成分分析(PCA)并作图;利用R语言或Excel制作群落结构组分图。
1.2.5.2 统计学分析指数(Chao、Ace、Shannon、Simpson)的计算公式 Chao:用Chao1算法估计样本中所含OTU数目的指数,Chao1在生态学中常用来估计物种总数。计算公式如下:
式中,SChao1=估计的OTU数;Sobs=实际观测到的OTU数;n1=只含有1条序列的OTU数目(如“singletons”);n2=只含有2条序列的OTU数目(如“doubletons”)。
Ace:用来估计群落中OTU数目的指数,是生态学中估计物种总数的常用指数之一,与Chao1的算法不同。计算公式如下:
式中,ni=含有i条序列的OTU数目;Srare=含有“abund”条序列或者少于“abund”的OTU数目;Sabund=多于“abund”条序列的OTU数目;abund=“优势”OTU的阈值,默认为“10”。
Simpson:用来估算样本中微生物多样性的指数之一,在生态学中常用来定量描述一个区域的生物多样性。Simpson指数值越大,说明群落多样性越低。
式中,Sobs=实际观测到的OTU数目;ni=第i个OTU所含的序列数;N=所有的序列数。
Shannon:用来估算样本中微生物多样性的指数之一。它与Simpson多样性指数常用于反映alpha多样性指数。Shannon值越大,说明群落多样性越高。
式中,Sobs=实际测量出的OTU数目;ni=第i个OTU所含的序列数;N=所有的序列数。
Coverage :是指各样本文库的覆盖率,其数值越高,则样本中序列被测出的概率越高,而没有被测出的概率越低。该指数反映本次测序结果是否代表了样本中微生物的真实情况。
式中,n1=只含有1条序列的OTU数目;N=抽样中出现的总序列数目。
2 结果与分析
2.1 基于16S rRNA 基因测序的细菌多样性
由图1和图2可知,56个样品(50个肌肉组织、3个水样和3个肠道组织)曲线逐渐趋向平坦,表明测序数据量合理,有效测序数量已经能够很好地覆盖测序样品的菌群组成。由表1可知,A群体感染组的Ace指数最高,E群体对照组的Ace最低;C群体感染组的Shannon多样性指数(3.30)最高,Simpson指数最低(0.080 0);D群体对照组的Shannon多样性指数(2.54)最低,Simpson指数最高(0.243 1)。观察发现,各群体感染组的Simpson指数均低于对照组,说明感染溶藻弧菌会导致罗氏沼虾组织的菌群多样性升高。由表2可知,水样F的Simpson指数最低(0.094),菌群多样性最高;水样H的Simpson指数最高(0.131),菌群多样性最低。肠道组织样品Ⅰ的Simpson指数最高(0.321),菌群多样性最低;肠道组织样品Ⅲ的Simpson指数最低(0.087),菌群多样性最高。
2.2 基于弧菌含量的抗病力分析
由表3可知,4个罗氏沼虾抗病选育群体的注射生理盐水对照组均未检测出弧菌,而非选育群体的对照组于60 min检测出0.008 13%的弧菌,表明罗氏沼虾的抗病选育取得了一定效果。注射感染组中,A群体的虾5个时间段中体内弧菌含量都为0,表明A群体有较强的抗弧菌感染能力,选育效果明显;C群体的虾体内平均弧菌含量高达2.718 40%,抗弧菌感染能力在5个群体中最低,选育效果不明显;B群体的虾体内平均弧菌含量为0.002 83%,抗弧菌感染能力仅次于A群体;D、E群体的体内平均弧菌含量相差不大。根据5个时间段中不同群体虾肌肉组织的平均弧菌含量,得到5个群体的抗弧菌感染能力为A>B>E>D>C。
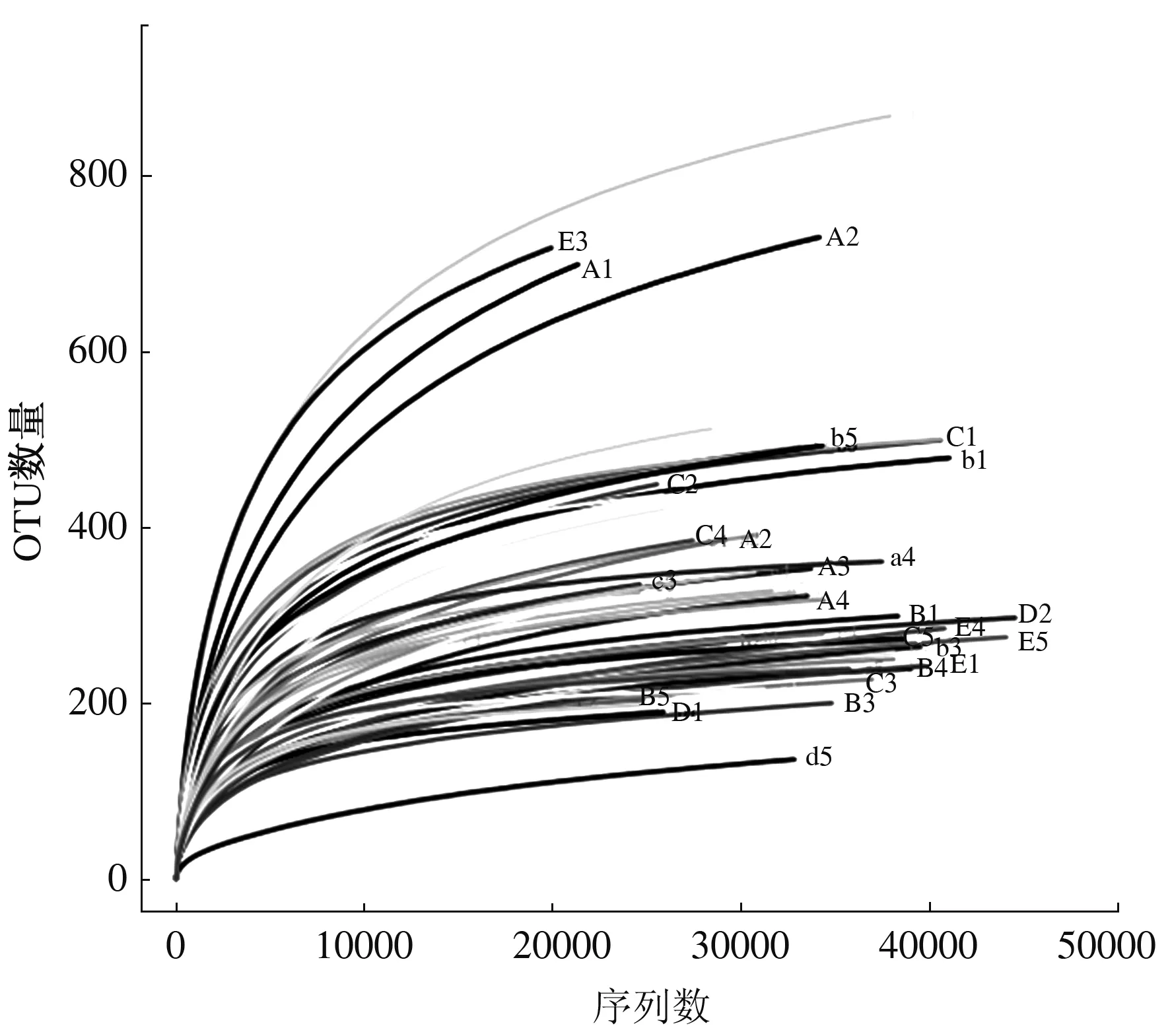
图1 罗氏沼虾肌肉组织样品高通量测序结果的稀释性曲线
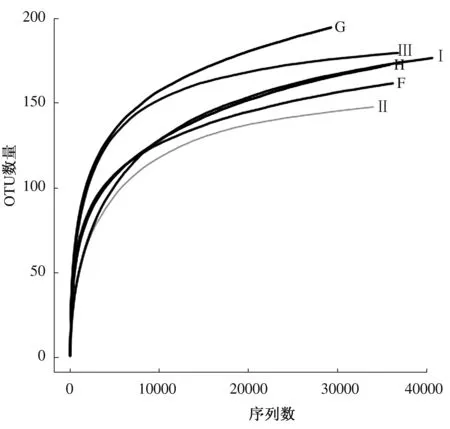
图2 罗氏沼虾养殖水体及肠道组织高通量测序结果的稀释性曲线
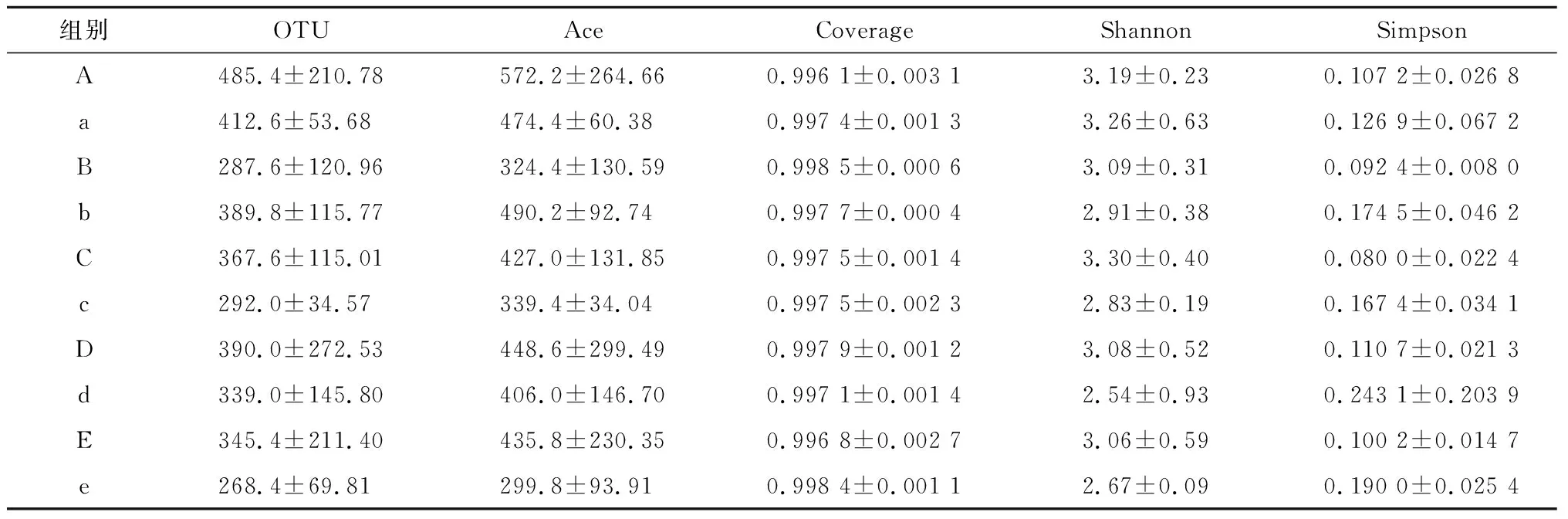
组别OTUAceCoverageShannonSimpsonA485.4±210.78572.2±264.660.996 1±0.003 13.19±0.230.107 2±0.026 8a412.6±53.68 474.4±60.38 0.997 4±0.001 33.26±0.630.126 9±0.067 2B287.6±120.96324.4±130.590.998 5±0.000 63.09±0.310.092 4±0.008 0b389.8±115.77490.2±92.74 0.997 7±0.000 42.91±0.380.174 5±0.046 2C367.6±115.01427.0±131.850.997 5±0.001 43.30±0.400.080 0±0.022 4c292.0±34.57 339.4±34.04 0.997 5±0.002 32.83±0.190.167 4±0.034 1D390.0±272.53448.6±299.490.997 9±0.001 23.08±0.520.110 7±0.021 3d339.0±145.80406.0±146.700.997 1±0.001 42.54±0.930.243 1±0.203 9E345.4±211.40435.8±230.350.996 8±0.002 73.06±0.590.100 2±0.014 7e268.4±69.81 299.8±93.91 0.998 4±0.001 12.67±0.090.190 0±0.025 4
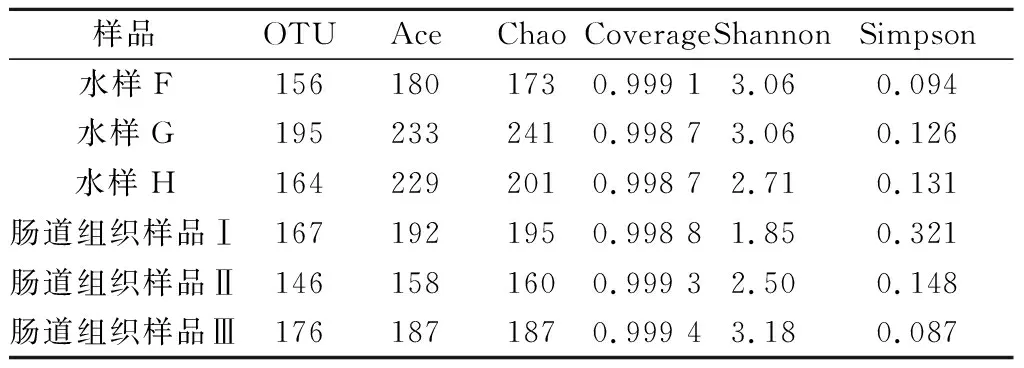
表2 基于16S rRNA基因序列的罗氏沼虾肠道组织和养殖水环境细菌多样性指数

表3 注射感染后不同时间段抗病选育群体与非选育群体罗氏沼虾体内的弧菌含量 %
2.3 罗氏沼虾抗病选育与非选育群体的感染成活率比较
本研究对4个罗氏沼虾抗病选育群体和非选育群体进行人工注射溶藻弧菌感染,测试不同选育群体之间的抗弧菌感染能力差异。感染15 d后统计2个平行组的平均成活率,结果表明,不同群体间的抗病能力存在一定差异(图3)。其中A群体的平均感染成活率最高,为83.33%,C群体的平均感染成活率最低,为58.33%,B、D、E群体的平均感染成活率分别为66.67%、61.67%、63.33%。A群体的抗病能力与C群体差异显著(P<0.05),B、C、D、E群体间差异均不显著。
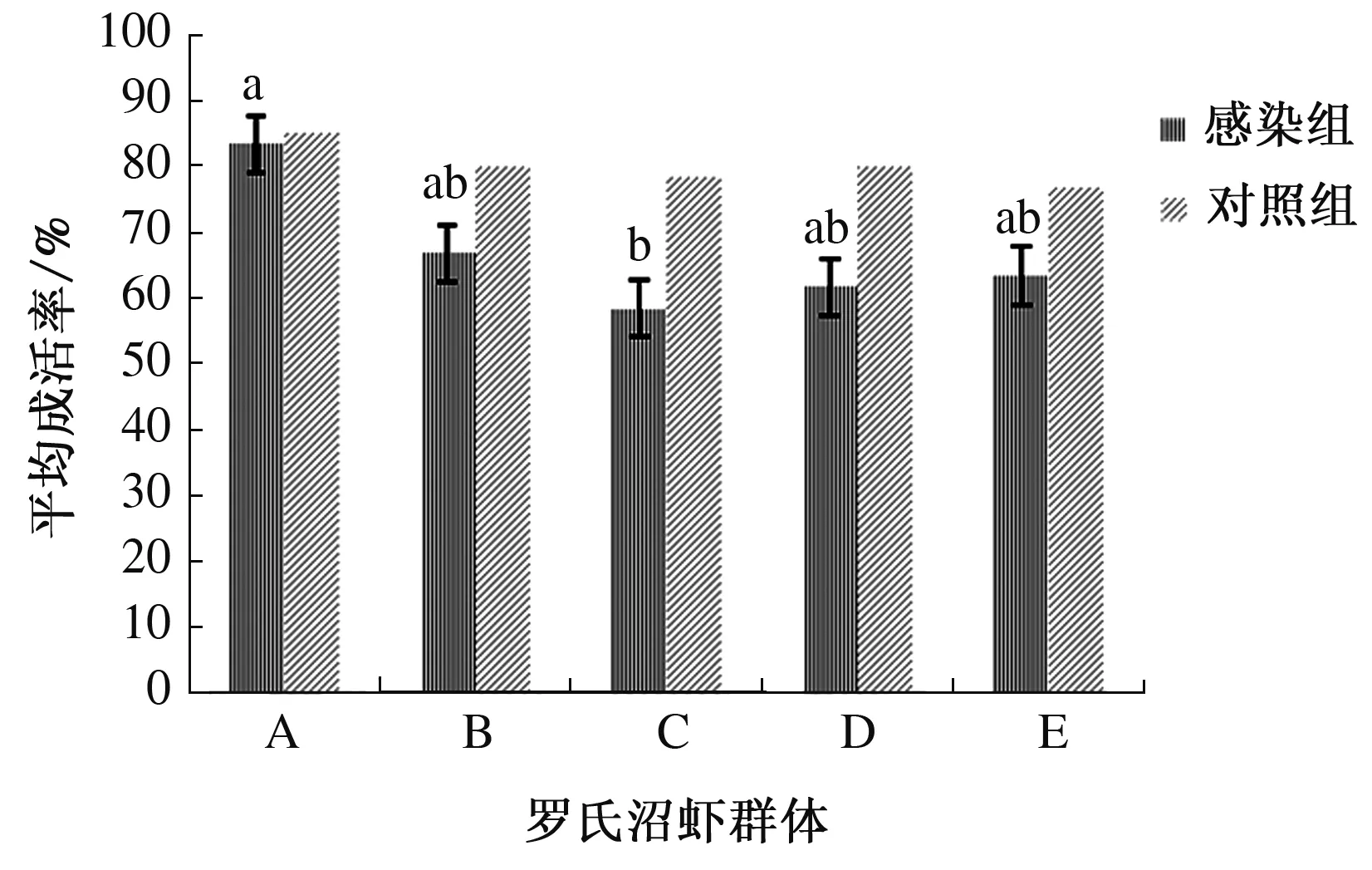
不同小写字母表示处理间差异显著(P<0.05)
2.4 罗氏沼虾抗病选育与非选育群体感染组和对照组肌肉组织样品微生物菌群分析
如表4所示,感染组和对照组的罗氏沼虾样品中微生物主要分为6个门,分别是厚壁菌门、变形菌门、拟杆菌门、放线菌门、软壁菌门、酸杆菌门。各组样品中厚壁菌门都占绝对优势,C群体对照组最高为71.63%;次优势类群为变形菌门,含量最高的为D群体对照组的41.90%,含量最低的为C群体对照组的21.08%;软壁菌门和酸杆菌门在各组群体中含量相对较低。
从属的分类水平进行分析发现(表5),各感染组芽孢杆菌属、假单胞菌属、嗜冷杆菌属的含量都高于对照组,而乳球菌属、丛毛单胞菌属(除了C群体)、乳酸杆菌属的含量则明显低于对照组。
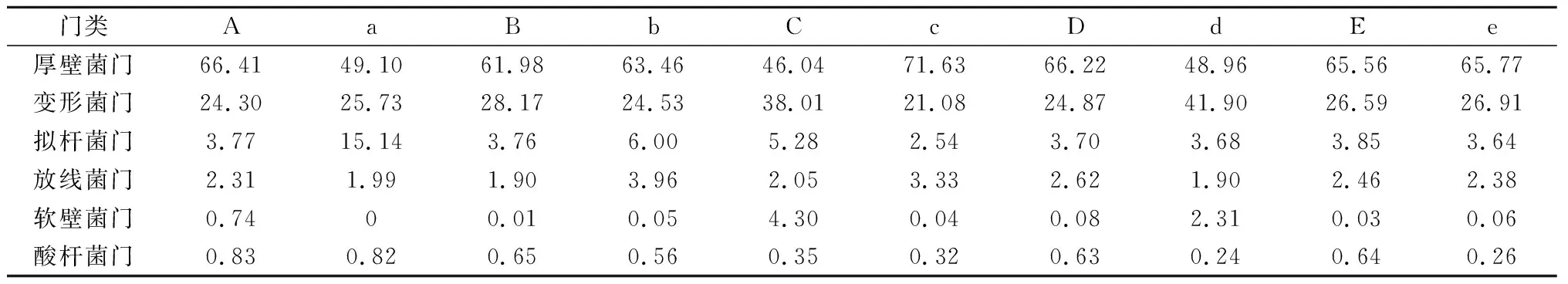
表4 罗氏沼虾抗病选育与非选育群体各组别肌肉组织样品优势细菌门类及相对丰度 %
2.5 罗氏沼虾抗病选育与非选育群体肠道组织和养殖水体微生物菌群分析
如表6所示,6个样品中微生物主要分为3个门,分别是变形菌门、拟杆菌门和厚壁菌门。对感染成活率最低、最高的罗氏沼虾抗病选育群体以及非抗病选育群体进行取样,其中肠道组织样品Ⅲ(非选育群体E)的变形菌门含量最高(69.48%),拟杆菌门含量最低(6.44%);水样H(非选育群体E)的变形菌门含量最低(23.90%),拟杆菌门含量最高(67.56%);肠道组织样品Ⅱ(选育群体A)的厚壁菌门含量最高(33.54%),水样F(选育群体C)的厚壁菌门含量最低(3.03%)。
从属的分类水平进行分析可发现(表7),水样F(选育群体C)的优势菌群主要有黄杆菌属(20.85%)、Aquibacter(21.75%)、赤杆菌属(5.84%)、Perlucidibaca(8.60%)和Alishewanella(8.06%);肠道组织样品Ⅰ(选育群体E)的优势菌群主要有黄杆菌属(52.60%)、肠杆菌属(18.78%)和芽孢杆菌属(4.00%);水样G(选育群体A)的优势菌群主要有黏着杆菌属(31.54%)、Leisingera(10.22%)、Algoriphagus(6.79%)、假交替单胞菌属(8.52%)和Ruegeria(6.33%);肠道组织样品Ⅱ(选育群体A)的优势菌群主要有黄杆菌属(11.21%)、肠杆菌属(30.87%)、芽孢杆菌属(15.17%)、类芽孢杆菌属(10.19%)和Carboxylicivirga(5.25%);水样H(非选育群体E)的优势菌群主要有黏着杆菌属(10.37%)、Flavobacteriaceae unclassified(26.44%)、Leisingera(8.52%)、NS3a marine group(19.07%)和Algoriphagus(8.01%);肠道组织样品Ⅲ(非选育群体E)的优势菌群主要有肠杆菌属(22.54%)、芽孢杆菌属(10.37%)、类芽孢杆菌属(6.97%)和Aquabacterium(7.45%)。可以看出,养殖水体和肠道组织中的细菌相对丰度不同,但也共有一些优势菌属。
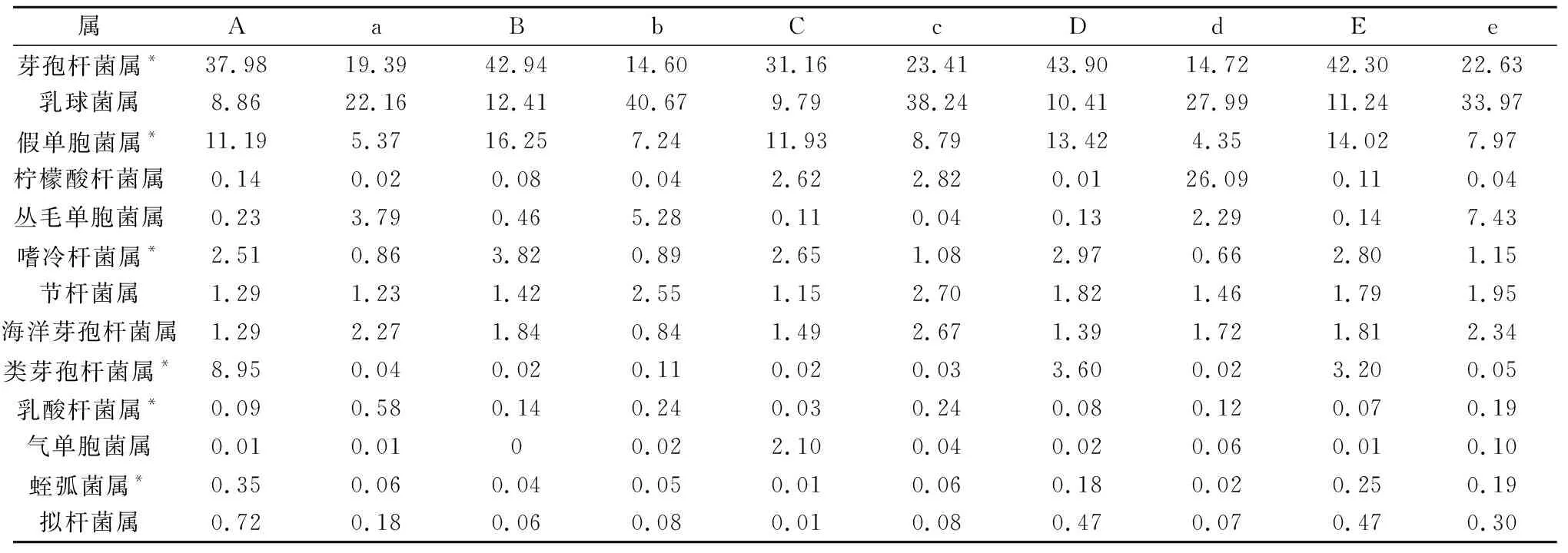
表5 罗氏沼虾抗病选育与非选育群体各组别肌肉组织样品优势细菌属类及相对丰度 %
注:其中*为常见益生菌。

表6 罗氏沼虾选育与非选育群体肠道组织和养殖水环境优势细菌门类及相对丰度 %
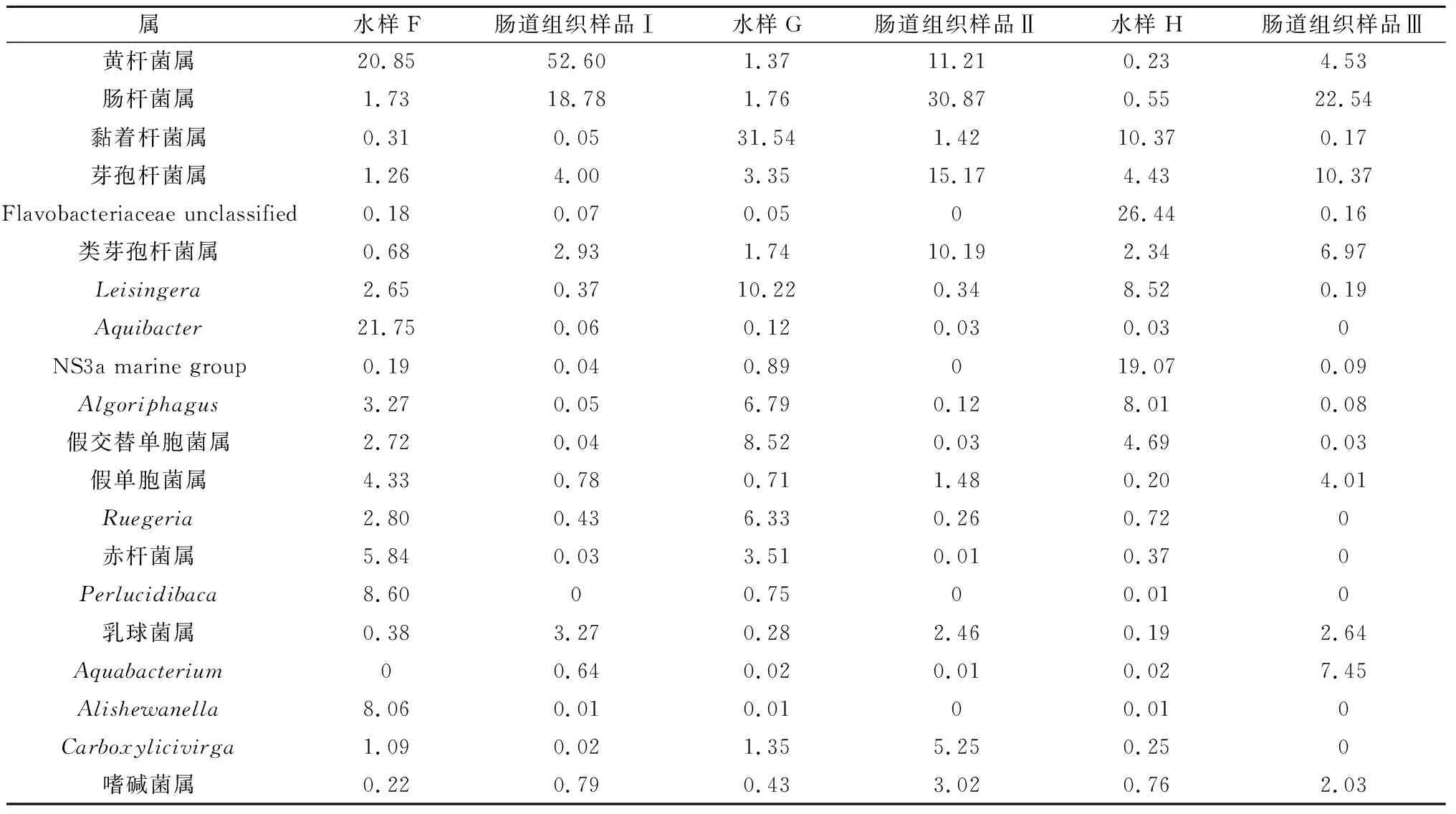
表7 罗氏沼虾选育与非选育群体肠道组织和养殖水环境优势细菌属类及相对丰度 %
3 结论与讨论
3.1 微生物多样性分析
高通量测序技术是相对于第一代测序(Sanger法)技术,又称新一代或第二代测序技术,具有测序通量高、准确度高、性价比高等优点[6],为研究大规模环境样品的菌群多样性提供了强有力的工具。目前该技术已广泛应用于淡水、海洋、土壤、动物消化系统等环境微生态结构的研究[7-10]。
有学者研究发现,水产动物消化道和养殖水环境相通,养殖水环境会直接影响水产动物肠道组织的菌群结构[11-12]。也有很多研究者认为水产动物消化道的菌群结构具有相对独立性,并不完全受养殖水环境的影响。张正等[7]研究发现,池塘养殖半滑舌鳎消化道菌群的细菌种类多样性和菌群组成结构都和池水中的细菌存在着明显的不同,几乎没有相关性。王贤丰等[13]对拟穴青蟹的养殖水环境和肠道组织进行了菌群多样性分析,结果表明,拟穴青蟹肠道与其池塘养殖环境中菌群结构密切相关,但肠道菌群相对独立,其优势细菌种类与养殖环境中优势细菌种类无关。本研究对感染成活率最高的抗病选育群体A、感染成活率最低的抗病选育群体C和非抗病选育群体E的肠道组织和养殖水体进行了菌群多样性比较,分析养殖水体是否会影响罗氏沼虾肠道组织的菌群结构,从而探讨对其感染成活率产生的影响。研究结果表明,罗氏沼虾肠道和养殖水环境中的菌群密切相关,但肠道菌群相对独立,并不完全受养殖水环境的影响。本研究水环境中黏着杆菌属、Aquibacter等含量相对较高,而在肠道组织中含量相对较低;水环境中肠杆菌属、芽孢杆菌属、乳球菌属等的含量相对较低,而在肠道组织中相对较高。
随着养殖过程中各种疾病的频繁暴发,罗氏沼虾的抗病选育工作显得尤为重要,这其中益生菌是当前的研究热点。已有研究结果表明,在斑节对虾饲料中添加芽孢杆菌能有效提高对虾的生长率和成活率,降低哈维氏弧菌对斑节对虾的感染率[14]。张盛静等[15]研究表明,在凡纳滨对虾饲料中添加芽孢杆菌能显著提高对虾抗哈维氏弧菌感染的能力,显著降低对虾肠道内弧菌数量。孟霄鹏等[16]以类芽孢杆菌作为益生菌投喂到凡纳滨对虾的饲料中,结果表明,类芽孢杆菌明显改善对虾肠道的菌群组成,提高对虾的抗病能力。本研究结果显示,抗病选育群体A的感染成活率显著高于抗病选育群体C,而B、C、D、E群体间则差异不显著。比较各群体感染组肌肉组织中细菌的相对丰度可以发现,A组中类芽孢杆菌的含量最高,为8.95%,而C组中含量仅为0.02%;除此之外,C组中芽孢杆菌的含量最低,为31.16%,而A、B、D和E组中芽孢杆菌的含量则差异不显著。研究表明,芽孢杆菌和类芽孢杆菌可能是造成A群体和C群体感染成活率差异显著的原因。为了进一步分析产生显著差异的原因,本研究对A群体和C群体的养殖池水和肠道组织进行菌群多样性分析。结果表明,A群体肠道组织中芽孢杆菌和类芽孢杆菌的相对丰度均显著高于C群体,和分析肌肉组织得出的结论一致。比较A群体和C群体的养殖池水,芽孢杆菌和类芽孢杆菌的含量差异不显著。关于芽孢杆菌和类芽孢杆菌能否提高罗氏沼虾抗弧菌感染的能力,还需进一步研究。
3.2 抗病选育及抗病力评价
近年来,随着养殖技术的不断提高,罗氏沼虾开始由粗放养殖向集约化养殖发展,由此也带来一系列问题:养殖环境恶化,多种疾病暴发等等,给我国罗氏沼虾养殖业的健康可持续发展造成了极大困扰。为了从根源上预防或解决病害问题,需尽快培育出罗氏沼虾抗病新品种。水产动物抗病选育的常见方法有选择育种、杂交育种、基因和分子标记辅助选择育种及转基因育种等。无论何种选育方法,其最终目标都是为了显著提高水产动物在经历病害暴发后的成活率,然而现实中很难模拟养殖环境下的病害暴发,一般采用测定感染或养殖成活率来直接反映抗病能力,也可以测定与疾病相关的免疫指标来间接反映[17-21]。此外,随着分子标记技术的发展,一些抗病基因(如MHC基因Cyca-DAB1等位基因)的多态性往往也用来作为评价抗病性能的重要指标[22-23]。目前的抗病选育工作更注重成活率的高低,但某些细菌性疾病并不会造成动物的患病死亡,只会导致动物食欲减退,影响其生长性能。与常规抗病选育方法相比,本研究采用的高通量测序技术,一方面可以通过测定不同时间段罗氏沼虾体内弧菌的含量直观地反映各罗氏沼虾群体的抗病能力,并辅助分析造成抗病能力产生显著差异的原因;另一方面可以帮助淘汰体内有病原菌的个体,同时结合各种性状的表型值,为尽快选育出优良品种提供保障。
综上,通过分析罗氏沼虾感染溶藻弧菌后体内弧菌的含量,结合感染成活率结果,得出各群体的抗病性能为A>B>E>D>C。A群体的抗病能力与C群体差异显著,B、C、D、E群体间差异均不显著。罗氏沼虾体内的菌群结构和养殖水环境密切相关,但又相对独立;体内芽孢杆菌和类芽孢杆菌的相对含量可能是造成A群体和C群体感染成活率差异显著的原因。

