日立7100生化分析仪BUN、CK指标的性能验证
王永梅
方法学评价不仅是实验室认可的必需条件,更是实验室质量管理的基本要求。临床医学实验室在检测项目开展之前,首先核实和验证性能参数是否与厂家声明的性能相符,或者是否满足临床的需要。同时可以利用检测系统的性能参数,正确解读报告结果及合理解释检测结果。实验室应对方法学进行评价,包括准确度、精密度、线性范围、稳定性、参考范围等。
竞技体育运动员在长期运动训练过程中对运动刺激已经适应,相对于正常人群,他们的各种生化指标对运动反应产生的变化就显得没有那么敏感,此时数据的准确性和可信度对科研人员进行机能评定就显得极其重要,而且对于运动员和教练员执行及调整训练计划也能提供可靠的科学依据。因此运动训练监控检测需要更高的灵敏度、稳定性和准确性。
本文参照CLSI指南有关文件,借鉴临床医学实验室性能验证方法,选择常规生化测试项目血尿素氮(BUN)、肌酸激酶(CK),从精密度、正确度、参考区间等[1],验证7100全自动生化分析仪的分析系统。建立符合本实验室质量管理要求的评价体系,确保检测质量。最终通过室间质评考核为全运会奥运会备战积累个体化数据,从而更好地服务于体育科研。
1 研究对象与方法
1.1 研究对象
1.1.1 样本
上海东方绿舟体育训练基地女足、男排、女排、游泳等项目一线运动员共40名,其中男子20名,女子 20 名,平均年龄为(23.4±2.1)岁。
1.1.2 仪器及试剂
日立7100全自动生化分析仪,采用日本和光株式会社BUN、CK试剂及配套校准品。
1.1.3 质控品
上海市临床检验中心下发的Beckman质控品,水平 1(407081)、水平 2(407082)、水平 3(407083)。
1.2 .方法
实验过程均按实验室标准操作规范相关要求,定期维护保养、校准,所有数据测试前均进行室内质控操作,确保质控数据在控时,再进行样本测试。
1.2.1 精密度验证
按照EP5-A2文件,使用Beckman低、中、高值3个水平的质控血清作为精密度评估样本。每天进行常规质量控制,剔除失控数据[2]。1.2.1.1批内精密度
Beckman高、中、低3个水平质控品重复测试20次,计算标准差和变异系数(CV)。1.2.1.2批间精密度
3个水平质控品每天重复测试2次,取平均值,连续测试20 d,计算标准差和CV。1.2.1.3判定标准
批内精密度<1/4TEa(总允许误差)、批间精密度 <1/3TEa。
1.2.2 正确度验证
本实验室采用2016年5月和2016年9月两次上海市临床检验中心室间质评回报结果作为评价指标,对回报数据进行分析。计算本参评实验室每个项目的测定结果与靶值的偏倚(bias),偏倚%计算公式为:偏倚%(bias%)=(各实验室测量结果 -靶值)/靶值×100%。偏倚%在允许误差范围内的结果为可接受结果,以每个项目5个数据中最大偏倚作为该项目的正确度,以不超过1/2TEa(CLIA’88)为判断标准。
1.2.3 参考区间验证
根据NCCLS C28-A2文件进行参考区间验证,在检验总体中随机抽取20个参考样本,20个参考个体样本应合理地代表实验室选择的健康总体,并且满足其分组标准。每个样本重复测试两次取平均值。如果20例参考个体中不超过2例的检测值在参考范围之外,那么供应商提供的实验室报告的95%参考区间是可以接受的[3]。
2 结果
2.1 精密度验证
由表1可见,两个项目3个水平的批内精密度CV均小于1/4TEa;由表2可见,3个水平批间精密度的CV均小于1/3TEa。

表1 批内精密度检测结果(%)Table I Test Result of the Within-run Precision(%)
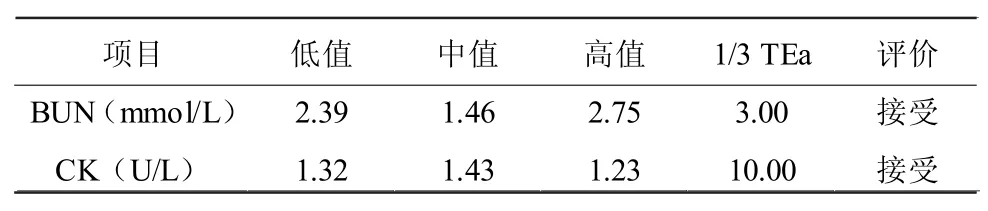
表2 批间精密度检测结果(%)Table II Test Result of the Between-run Precision(%)
2.2 正确度验证
由表3和表4可见,2016年两次上海市临床检验中心室间质评结果,正确度均不超过1/2TEa。
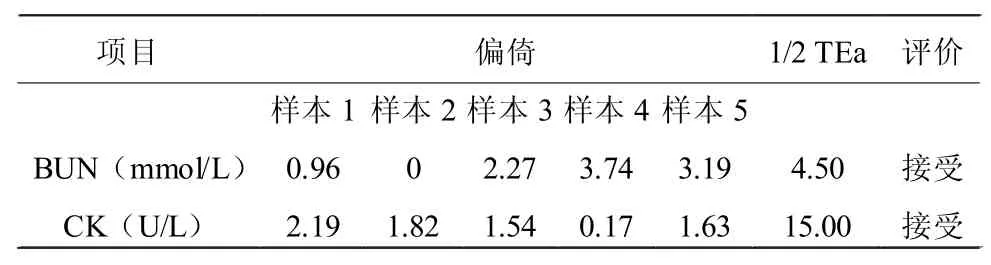
表3 2016年度第一次正确度验证结果(%)Table III First Accuracy Verification Result in 2016(%)
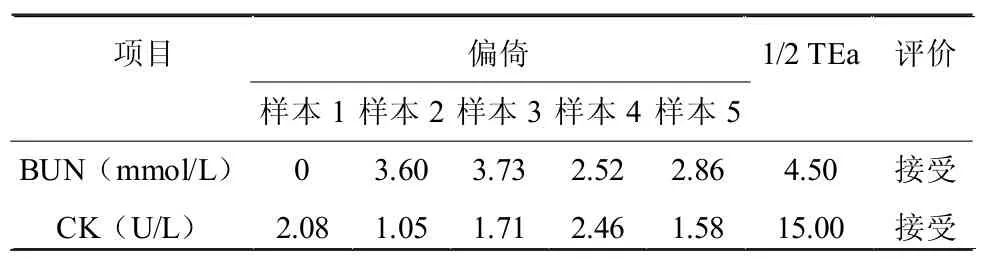
表4 2016年度第二次正确度验证结果(%)TableIVSecondAccuracyVerificationResultin2016(%)
2.3 参考区间验证
由表5可见,本实验室可以直接使用厂商说明书提供的参考区间。
3 讨论
在实验室实际工作过程中,由于仪器设备部件的老化和磨损进行重大维护保养或者试剂在运输和储存条件等状况发生变化时,就需要对检测系统进行验证并记录确认结果,将确认过的程序文件化,完善本实验室的标准操作规范文件。
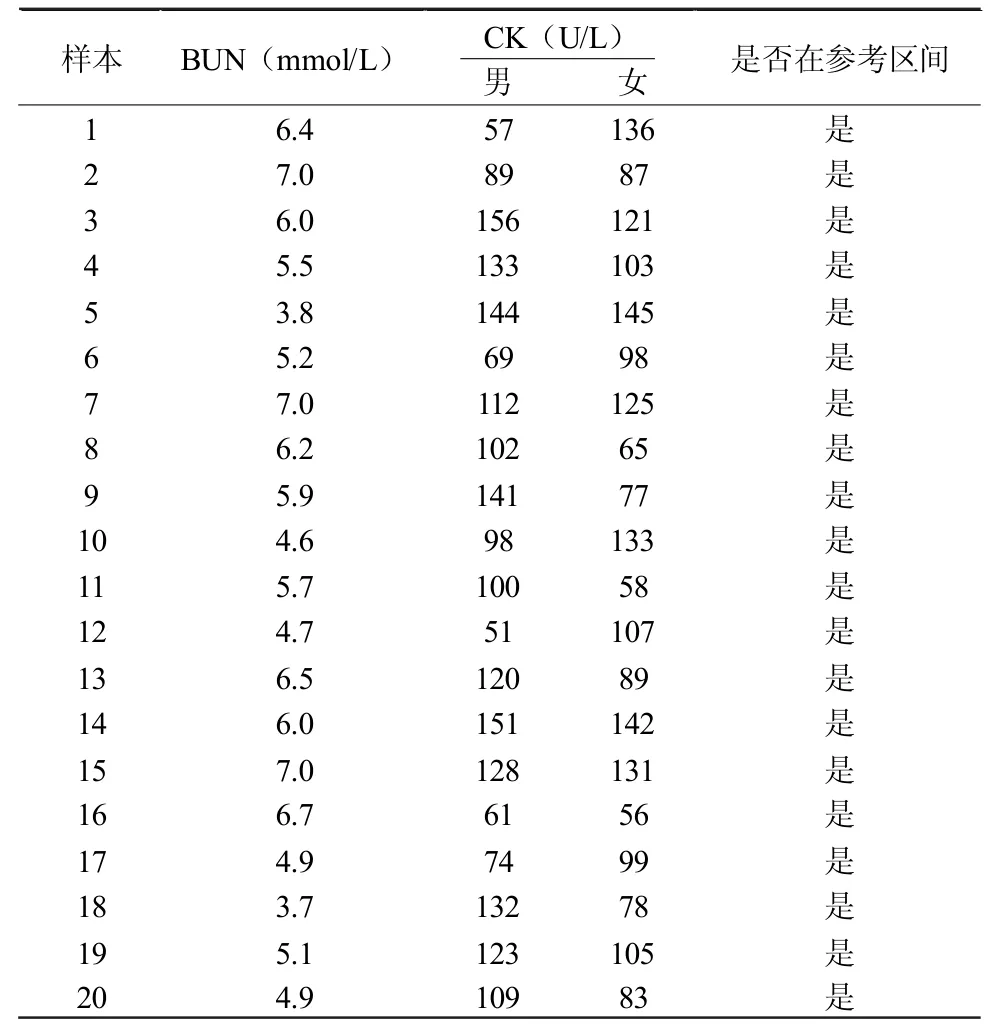
表5 参考区间验证结果Table V Verification Result of the Reference Range
精密度是检测系统方法学评价的基础,而且本实验室对样品只作单次测量便发出报告,这种情况下精密度性能验证显得极其重要。考虑到本实验室的具体情况,采用EP5-A2文件作为精密度评估方案依据,采用CLIA’88要求或生物变异度要求或厂家所声明的CV作为可接受标准[4],验证日立7100全自动生化分析仪批内精密度和批间精密度。从表1可见,BUN和CK高、中、低值3个水平的批内精密度CV均小于1/4TEa;BUN和CK高、中、低值3个水平批间精密度的CV均小于1/3TEa。两个项目的批内精密度和批间精密度检测结果均满足实际误差要求。
正确度是大量测定的均值与真值的接近程度,是表示测量结果中系统误差大小的程度。本次验证是以2016年两次参加上海临检中心室间质评结果计算,偏倚%在允许误差范围内的结果为可接受结果。从表3和表4看出,两次室间质评中十个样本BUN和CK两个项目的正确度均小于1/2TEa,表明正确度验证均在允许范围内。
参考区间验证是判断厂商提供的实验室报告的参考区间是否可以接受,比较小样本参考值和原始参考值之间的可比性。实验室在日常生化测试中,根据分组和健康标准,抽选出20个运动员样本,使用当天新鲜血清标本进行测定分析。若3例以上超出区间界限,重新选择20个样本进行验证。结果判断:R=测定的结果在参考范围例数/总测定例数,若R>90%,即验证满足要求。从抽取的参考样本检测结果表 5可见,BUN结果范围为[3.7~7.0]mmol/L,厂家给出的BUN的参考区间为[2.82~7.06]mmol/L,20个参考样本的测定结果R>90%;CK结果范围,女性为[56~145]U/L,男性为[51~156]U/L,厂家给出的 CK的参考区间女性为[34~145]值 U/L,男性为[46~171]U/L,20个参考样本的测定结果R>90%。由此判断本实验室可以直接使用厂商提供的参考区间。
综上验证,7100生化分析仪检测系统所选用的验证方案可操作性和实用性较强,探讨了一套较标准的性能验证方案,对建立标准化和规范化的实验室具有重要意义。在提高实验室质量控制的同时,不断提高实验室操作人员的水平,各指标达到厂家声称的范围,保证了检验结果的准确可靠。并且进一步完善了本实验室的标准操作规范(SOP)文件。

