三氟甲基吡啶在作物保护中的重要性
曹晓峰,张瑞峰 编译
(华东理工大学 药学院,上海200237)
为了初步了解三氟甲基吡啶在作物保护中的应用,统计了1990年至2017年9月间公布的具有ISO通用名的农用化学品。对含有三氟甲基吡啶的化合物进行了分类(杀虫剂与杀线虫剂一起计数)。此外,还统计了含有三氟甲基苯环的化合物的数目,结果如表1所示。

表1 含有芳基或吡啶基三氟甲基(CF3)取代基的具有ISO通用名的农用化学品
表1数据表明,与1990-1999年相比,2000-2017年(9月)具有ISO通用名的化合物数量有所减少,这可能涉及许多与本综述所述内容无关的原因。其次,在1990-1999年,只有4个(2%)有ISO通用名的化合物含有三氟甲基吡啶,而含有三氟甲基苯基环的化合物为9个(4.5%)。在2000-2017年期间,共有166个有ISO通用名称的化合物,其中10个(6%)含有三氟甲基吡啶,20个(12%)含有三氟甲基苯基环。显然三氟甲基取代基在农用化学品中起着重要作用。Adam Burriss等认为含三氟甲基吡啶化合物的数量从2% (10年期间)上升到6% (18年期间)的一个重要原因是可以进一步修饰的三氟甲基吡啶的合成方法的增加,导致潜在产品的化学多样性增加。
已有人对氟在生命科学行业的重要性进行了综述,最近对包含吡啶环的作物保护产品的发现进行了调研。此外,已报道了生物活性分子中所含的特定三氟甲基吡啶的合成方法。第一次报道三氟甲基吡啶合成方法是在1947年,通过用氟交换氯制备三氟甲基吡啶,如图1所示。

图1 第1个报道的三氟甲基吡啶环的合成路线
在该例子中,三氟甲基取代基连接到吡啶环的2-和 4-位。为了方便本综述是基于这个编号顺序命名化合物的;早期杀菌剂、除草剂和杀虫剂的发现和之后杀菌剂、除草剂、杀虫剂和杀线虫剂的发现是以含3-和5-三氟甲基吡啶为特征。以下部分介绍了含有4-和6-三氟甲基吡啶的产品,以更好地反映所用的不同合成方法(图2)。

图2 命名法:箭头表示三氟甲基吡啶环与分子的连接点
1 氯氟交换技术产物:3-和 5-三氟甲基吡啶衍生物
早期含有三氟甲基吡啶的植物保护产品包括杀菌剂、除草剂和杀虫剂。在这些农药的发现中关键因素是基于首次报道的合成方法的化学工艺的发展提供了可以大规模生产的三氟甲基吡啶原料。3种关键的三氟甲基吡啶中间体如图3所示。

图3 早期的三氟甲基吡啶中间体
许多专利详细描述了如何大规模制备这些中间体。例如,2-氯-5-三氟甲基吡啶2是由2-氯-5-三氯甲基吡啶在430 ℃氟化铬III/氧化铝混合催化剂下与氟化氢反应制得。该专利申请的实施例 4报道了以86%的产率生产287 kg的2。进一步的研究利用β-甲基吡啶作为起始材料,在各种金属氟化物催化下与氯气和氟气的混合物发生反应。温度变化导致生成 2与 2-氯-3-三氟甲基-吡啶 1,2,6-二氯-3-三氟甲基吡啶和 3-三氟甲基吡啶的混合物。这种混合物可以通过蒸馏分离。据报道,2也可由2,6-二氯-3-三氟甲基吡啶发生电化学脱氯生成。此外还报道了 2发生气相氯化反应生成了2,3-二氯-5-三氟甲基吡啶3。尽管这项技术是在20世纪70年代后期和80年代初开发的,但这些中间体仍在近期专利申请中频繁出现。例如,1可以由3-三氟甲基吡啶N-氧化物制备。

图4 含有3-或5-三氟甲基吡啶环的早期作物保护产品
三氟甲基与吡啶上氮共同的吸电子效应使得中间体1、2和3中邻近氮的氯易于被亲核试剂取代,从而允许下一步化学反应容易进行。Haga等人对这些中间体的应用以及除草剂精吡氟禾草灵和啶嘧磺隆,杀菌剂氟啶胺和杀虫剂氟啶脲的发现进行了综述,如图4所示。
除上述产品外,另4个上市的植物保护产品的发现中也使用了中间体3,如图5所示。
啶蜱脲是在 1983年专利申请中首次被报道的主要用于控制蜱和螨等动物健康有害生物的几丁质合成抑制剂,其结构与氟氯脲十分接近。
于2006年上市的氟吡菌胺由中间体3制备,用于防控卵菌病。
随后又在2012年推出了第2种杀菌剂氟吡菌酰胺。氟吡菌酰胺是呼吸链的复合体II的抑制剂,用于防治葡萄和蔬菜的灰霉病和白粉病以及防治线虫等。
另一个含有 5-三氟甲基吡啶的农用化学品的例子是杀线虫剂fluazaindolizine。
另一个含有 5-三氟甲基吡啶结构的商品化杀虫剂是三氟甲吡醚。该化合物具有新颖的作用机制,可能与代谢活化有关,被用于防控棉花和蔬菜的鳞翅目和缨翅目害虫。它是由中间体 2合成,如图 6所示。
三氟甲基吡啶中间体1、2和尤其是3的出现,已经导致许多用于防治病害、杂草、害虫和线虫的作物保护产品的发现与上市。Adam Burriss等认为以上发现中的一些关键因素是:⑴ 可大规模生产关键中间体的化学工艺;⑵ 这些中间体的生产材料成本低;⑶ 这些中间体易用于研究;⑷ 这些中间体易于转化成最终的活性成分。

图5 含有5-三氟甲基吡啶环的作物保护产品的其他例子

图6 三氟甲吡醚——含有5-三氟甲基吡啶环的杀虫剂的另一个例子
2 含三氟甲基吡啶环的产品:4-和 6-三氟甲基吡啶衍生物
含有4-三氟甲基吡啶或6-三氟甲基吡啶环的几种农作物保护产品已被发现并上市。使用不同于以上的化学方法来制备这些化合物;三氟甲基吡啶环由三氟甲基酮4而来。
使用这种小的,高度反应性的三碳三氟甲基结构单元,制备4-或6-三氟甲基吡啶环。然后将这些化合物进一步加工成最终产品。例如,氟啶虫酰胺,最终吡啶上的氮是以1,4方式引入酮4;然后形成的烯胺与乙烯基醚丙烯酸酯(acrylate vinyl ether)反应,然后进行分子内环化和水解产生4-三氟甲基吡啶中间体。啶氧菌酯的合成中,酮4首先与丙二酰胺反应,然后产物经历分子内闭环,最后脱羧生成 6-三氟甲基吡啶中间体(图7)。
使用这种化学方法发现并上市的产品见图8和表2。
除草剂氟硫草定和噻草定也含有 6-三氟甲基吡啶环。现在吡啶环是用三氟甲基酮酸酯构建(图9)。
2017年公布了2个含有三氟甲基吡啶的最新农药的通用名称;acynonapyr (或 pyrinonafen)是杀螨剂,fluopimomide是杀细菌和真菌剂(图 10)。中间体2和3再次在这些产品的合成中起到了重要作用,这说明化学家们仍使用此方法开发新作物保护剂。
从上面的许多例子可以看出,三氟甲基吡啶结构片段在作物保护中发挥了重要作用。很有意思的是,只有2个带有 4-三氟甲基吡啶环的产品上市,同时发现了6个带有6-三氟甲基吡啶环的产品。促成这一成功的关键因素之一是化学,使得任一位置含有三氟甲基的吡啶环可以容易被制备,并且易于被进一步的修饰,并通过化学转化合成最终活性分子

图7 制备4-或6-三氟甲基吡啶环的化学方法

图8 衍生自化合物4的含有4-或6-三氟甲基吡啶环的产品

表2 衍生自化合物4的含有4-或6-三氟甲基吡啶环的产品
3 物理化学性质的影响
除草剂精吡氟禾草灵比将其吡啶N改为CH的苯基类似物有更好的生物利用度(图11)。
有文献对药物化学中在芳香环中引入氮原子的影响进行了综述。列举了许多不同的例子,介绍了N引入前后化合物的活体活性、生物利用度、功能活性或安全性等特性的差异。正如该综述所述,将芳香环上的1个C-H用N取代,可以导致化合物物理化学性质发生重大改变,例如亲脂性的改变。氮原子的引入会产生相应苯环所没有的偶极矩和碱性中心。

图9 除草剂氟硫草定和噻草定由三氟甲基酮酸酯制备

图10 最近提出的2个具有三氟甲基吡啶的分子
引入三氟甲基可以使化合物的 logP增大约1.1。除了对亲脂性的影响外,三氟甲基对化合物的碱性也有显著的影响,这是由于该取代基具有吸电子的特性。因此在化合物中引入吡啶氮和三氟甲基时应该共同考虑2种基团对化合物性质的影响。
接着笔者研究了这种叠加作用是否与三氟甲基在吡啶环上的取代位置有关。使用软件(ACD/Percepta,Build 2726, Advanced Chemistry Development, Inc.,Toronto, ON, Canada, www.acdlabs.com; Schrödinger Release 2017-1:Jaguar, Schrödinger, New York,USA),计算表明与3(或5)和4位相比,三氟甲基取代基位于2(或6)位时,对吡啶氮碱性的影响显著增大(图 12)。
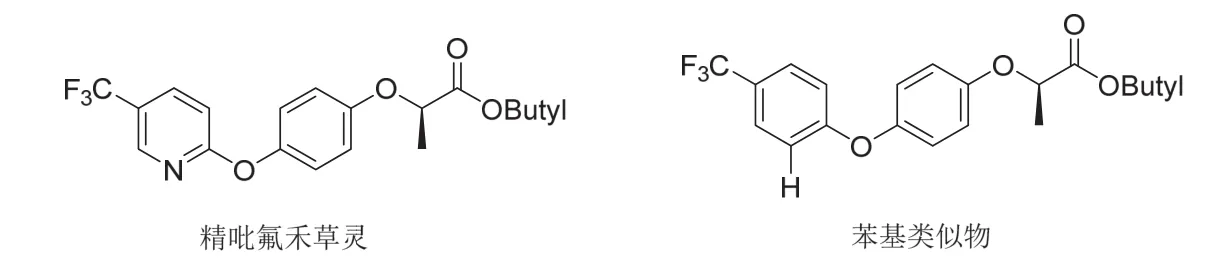
图11 精吡氟禾草灵和分子匹配的苯基类似物的结构

图12 用2个独立的软件程序计算不同位置的三氟甲基取代基对吡啶上氮的pKa值的影响
4 分子匹配分析
分子匹配分析经常被用来比较仅一处不同的一对分子的一组测量值,研究分子中一个基团或原子变化的影响。氟吡草酮是抑制对羟苯基丙酮酸双氧化酶(HPPD)的除草剂。通过与苯基类似物5的分子匹配分析,可以发现二者在物理化学性质和离体活性方面存在一些差异(图13)。
苯基类似物5还没有被报道过,但是可以通过文献中描述的方法来合成。氟吡草酮和它的苯基类似物5的物理性质很相近。2种化合物都具有适宜除草剂吸收和迁移的 logP和酸性 pKa。从测定的logP和pKa的差异中可以看出氟吡草酮中的吡啶氮具有降低其疏水性和增加酸度的作用。然而与苯基类似物5相比,氟吡草酮的水溶性要高。这些差异单独影响可能非常小;然而这些因素与离体结合的增加共同有助于解释2种化合物活体除草活性的差异性。

图13 选择性测量除草剂氟吡草酮与分子匹配的苯基类似物5的物理化学性质和与HPPD结合后的解离速率
用之前所描述的方法,用从拟南芥中获得的HPPD酶测定离体解离率。就HPPD而言,氟吡草酮以31.4 h的解离率与之结合,大约是用苯基类似物5所测得的3倍。这意味着,与化合物5相比氟吡草酮与目标酶的结合时间更长,因此在喷洒后可以更好地抑制杂草的生长。虽然氟吡草酮的物理化学性质更有利于生物利用度,但笔者认为氟吡草酮使离体酶的失活作用是苯基类似物5的3倍,这是因为缺电子的吡啶环与活性位点中芳族残基的 π-π相互作用更强导致。有文献已经报道了通过引入氮等杂原子提高与芳香残基的π-π相互作用。
与苯基类似物5相比,氟吡草酮的离体活性增加也体现在活体活性上。图14为氟吡草酮与苯基类似物在芽前和芽后对一系列单子叶和双子叶杂草的活性。

图 14 氟吡草酮和苯基类似物5芽前和芽后除草活性(剂量为125 g/hm2)
如图 14所示,氟吡草酮对多种重要单子叶(SETFA, PANDI, DIGSA, ECHCG)和双子叶杂草(ABUTH, XANST, IPOSS, CHEAL)有很好的芽后防除作用,氟吡草酮的用量为125 g/hm2。和对苯环上进行取代的预期一样,化合物5具有类似的芽后活性,但对SETFA活性较低。在施用量为125 g/hm2时,氟吡草酮显然比化合物5对相同的一组杂草的芽前施用活性更好,特别是对SETFA和IPOSS。这些结果支持这样的假设:与苯基类似物5相比,氟吡草酮中的吡啶环提高了对杂草的芽前应用生物利用度。
很明显,氮原子在氟吡草酮的吡啶环中的不同位置,也可能影响化合物的性质和除草活性。已有文献报道了这种三氟甲基吡啶HPPD除草剂中氮原子位置对与氟吡草酮很相关的类似物化合物6的(图15)重要性。化合物6和氟吡草酮一样,浓度为125 g/hm2时对相同的单子叶和双子叶杂草有优异的芽前和芽后除草活性。相比之下,位置异构体7和8的芽前除草活性显著降低(图15a)。与化合物6相比,化合物7,8芽后应用(图15b)的除草活性相似。
尚未完全了解氮原子在三氟甲基吡啶环中不同位置对活体活性影响的原因。只能说当考虑在活性成分研究中使用三氟甲基吡啶时,应该注意研究三氟甲基吡啶环所有可能的位置异构体。
另一个实例为一类具有杀虫活性的氧化磷酸化解偶联剂,来进一步对含有三氟甲基吡啶化合物和与其分子匹配的苯基类似物进行比较。这些亚肼基-苯基-乙腈衍生物(图16)是报道过的最有效的氧化磷酸化解偶联剂。据报道,分子的logP和pKa这2个参数对于这种作用机制很重要,因为这种分子需要穿过线粒体膜来接受和给出质子。据报道,大多数有效的解偶联剂具有亲脂性,其logP为6~6.5,pKa约为7.5。图16列出了分子匹配分析预测的logP、计算出的pKa以及测量的氧化磷酸化的解偶联活性(uncoupling of oxidative phosphorylation activity) (EC50)。

图 15 3个三氟甲基吡啶HPPD除草剂的芽前和芽后除草活性(剂量为125 g/hm2)

图16 用分子匹配分析得到的试验杀虫解偶联剂的logP、pKa以及在新陆原伏蝇成虫线粒体上的解偶联活性(EC50)
已经使用内部软件预测logP,该软件是基于23 000多个内部和公共数据开发的非线性模型。在95%的置信区间内预测误差为0.9个log。使用Epik程序3.4版本计算了pKa。
比较9和10两个分子,发现三氟甲基吡啶和三氟甲基苯基类似物在预测的物理化学性质和测量的解偶联效力方面存在差异。作为氧化磷酸化的解偶联剂三氟甲基吡啶9的潜在活性是苯基类似物的5倍(5 nM vs 25 nM),这可以由其较低的pKa来解释(8.78 vs 9.2),虽然化合物9的logP也较低(4.68 vs 6.04)。在这种情况下,似乎pKa具有更重要的影响,且4.68的logP高到足以使化合物渗入线粒体和运输。虽然腙氮原子的去质子化位点与吡啶氮的距离较远,但通过计算仍然观察到pKa降低大约0.5个单位。其结果与氟吡草酮的相似。
通过比较2种化合物11和12的活体杀虫活性,可以进一步进行分子匹配分析(图 17)。以有效成分mg/L进行试验,幼虫死亡率为80%或更高。

图17 化合物11和12对棉贪夜蛾和玉米根虫的杀虫活性的分子匹配分析
三氟甲基吡啶化合物11比苯基类似物12活性高,浓度为 12.5 mg/L (有效成分)对海灰翅夜蛾(Spodoptera litloralis)和Diabrotica baltealta幼虫致死率100%,而化合物12在100 mg/L (有效成分)没有杀虫活性。
通过比较氟啶胺和其苯基类似物化合物13来说明杀真菌剂的分子匹配分析。已有文章报道了一系列二芳基胺的解耦联活性以及物理化学性质。本文献中包含杀真菌剂氟啶胺,以及分子匹配的苯基类似物13。图18为它们的物理化学参数以及解偶联活性。
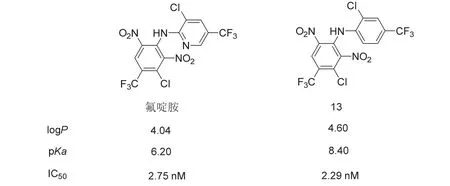
图18 氟啶胺和苯基类似物13的分子匹配分析
与化合物13 (8.40)相比,氟啶胺中的吡啶氮导致pKa降低(6.20);这是由于吡啶环有更强的吸电子性,并且推测失质子物质的负电荷更容易去离子化(稳定) ,即吡啶环比苯环更稳定。正如预期的那样,氟啶胺的亲脂性稍低于化合物13,如计算值所示(氟啶胺为4.40,13为4.60)。这些计算值与报道的数据非常接近。这些差异没有体现在它们作为解偶联剂上,如图18所示具有相似的离体解偶联活性。
5 总 结
三氟甲基取代的吡啶环在作物保护研究中发挥了重要作用,越来越多的带有这种结构片段的杀菌剂、除草剂、杀虫剂和杀线虫剂被发现并上市。在一些例子中,具有三氟甲基吡啶环的化合物比三氟甲基苯基类似物具有更好的生物利用度或离体活性。如果先前发现含有三氟甲基吡啶和5-三氟甲基吡啶的产品具有偶然性,受到原料的影响,那该如何看待含有4-或6-三氟甲基吡啶的新产品?显然,这些早期的成功鼓励研究人员继续以三氟甲基吡啶为植物保护产品的结构片段进行研究,并利用三氟甲基吡啶环的有用特性。三氟甲基吡啶合成方法的发展和应用的拓展已经证明了这点,并由此法开发的产品目前正在上市。基于以上几点,预计含有三氟甲基吡啶环的其他作物保护产品将会被设计与发现。问题是,“三氟甲基的取代基将会在吡啶环上的什么位置出现。”

