鲶鱼皮明胶的功能性质分析
李从虎,孙秀芳,王慧婷,张笑笑,周颖,吴彦*
1(安庆师范大学 生命科学学院,安徽 安庆,246133) 2(皖西南生物多样性研究与保护安徽省重点实验室,安徽 安庆, 246133) 3(水生生物保护与水生态修复安徽省高等学校工程技术研究中心,安徽 安庆,246133)
明胶是一种从动物的皮、骨、腱等含胶原蛋白的组织中经过一系列化学处理以后部分水解的高分子蛋白质[1]。因其具有优良的生物相容性、生物降解性和低免疫原性等特性,而广泛应用于生物医药、组织工程和食品等领域。明胶除了具有水合作用外,还具有其他两类重要的性质:(1)凝胶化作用,如组织化和水结合能力;(2)表面性质,如泡沫性、乳化性、吸附性和成膜性[2]。
目前,明胶产品多来源于猪皮和牛皮。由于受口蹄疫和疯牛病等人畜共患病以及一些宗教信仰的影响,这一原料来源的明胶产品饱受争议[3]。鱼类副产物2014年在世界范围内的产量高达5 000万t[4],因此,利用这类下脚料生产明胶成为哺乳动物明胶原料来源的有效替代者,且鱼类明胶的提取技术已日趋成熟。ABDELMALEK等[5]从乌贼皮中提取明胶,其提取率达到6.82 g/100g(湿重)。在食品领域,明胶的应用仍基于其优良的功能性质。例如,NHARI等[6]将明胶添加到酸奶酪中,用以增强酸奶酪的粘稠性而降低其脱水缩合作用。此外,明胶的泡沫性可用于冰激凌中,乳化性也可适用于肉类产品中[7]。可见,基于明胶功能性质的研究对于其应用具有重要的指导意义。
鲶鱼(Mystusmacropterus)是我国养殖的主要淡水鱼种类之一,广泛分布于我国江河湖泊,尤以长江、钱塘江流域居多。依据中国渔业统计年鉴数据显示,2015年鲶鱼产量达45万t。鲶鱼肉质鲜美,富含蛋白质、氨基酸、脂肪等营养物质,但其加工过程中会产生大量的鱼皮、鱼骨等副产物,约占鱼体总重的50%[8]。在鲶鱼加工副产物中,其皮肤组织富含大量胶原蛋白,可继续加工利用,不仅降低人畜共患病的风险,也促进了鲶鱼皮废弃物的资源化利用和人类的可持续发展。因此,本文以鲶鱼皮为原料,提取出明胶,研究其持水性、泡沫活性和稳定性以及不同条件下的乳化活性和稳定性,以期为其工业应用提供理论指导。
1 材料与方法
1.1 原料与试剂
新鲜鲶鱼(Mystusmacropterus),购于安庆本地农贸市场(2017年4~7月),原料获取后去除杂质,将鱼皮组织置于冰箱中冷冻保存;植物油由中粮集团提供;HCl、NaOH等试剂均为分析纯。
1.2 仪器与设备
SJIA-10N型冷冻干燥机(宁波双嘉仪器有限公司);PHS-3C型精密pH计(上海雷磁仪器厂);SC-3612型离心机(安徽中科中佳科学仪器有限公司);HHS-8S型电热恒温水浴锅(上海宜昌仪器纱筛厂); 78HW-1型磁力搅拌器(上海皓庄仪器有限公司); 752可见-紫外分光光度计(上海精科实验有限公司);组织捣碎机(金坛友联仪器研究所);BX51光学显微镜(日本OLYMPUS公司)。
1.3 实验方法
1.3.1 明胶提取
草鱼皮明胶提取参照文献[5]的方式进行。
1.3.2 明胶的持水性分析
明胶的持水性参照CHO等[9]介绍的方法来测定。取1只精确称重的离心管,放入1.0 g冻干的明胶和10.0 g去离子水。随后样品在20 ℃下每隔15 min剧烈搅拌5 s,总时间为1 h,然后将样品以5 000×g的速度离心20 min。弃去上清液,并将离心管倾斜45°放至于滤纸上30 min。最后称取总质量,得到结合水的质量,从而计算出明胶的持水性(以冷冻冻干的明胶计)。通过改变溶剂的离子强度(NaCl,0.1、0.2、0.4、0.6、0.8和1.0 mol/L)考察离子强度对明胶持水性的影响。
1.3.3 明胶的起泡性分析
明胶的起泡性分析参照文献[10]的方法进行。将明胶溶解于去离子水中得到质量浓度为10、20、30、40和50 g/L的溶液,静置20 min后,置于匀浆器中高速搅拌(10 000 r/min)10 min使其产生气泡。随后,迅速将样品移入100 mL量筒中,分别记录0、5、10、20、30 min后液体和气泡的总体积。泡沫活性(FE)和泡沫稳定性(FS)按以下公式计算:
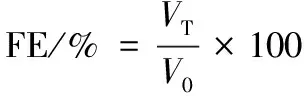
(1)
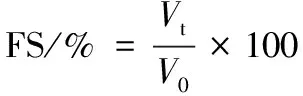
(2)
式中:FE,泡沫活性,%;FS,泡沫稳定性,%;VT和Vt分别为0和t min气泡总体积,mL;V0,产生气泡前的总体积,mL。
1.3.4 明胶乳液类型鉴别
参照文献[11],将冷冻干燥的明胶溶解于去离子水中得到10 g/L的明胶溶液,取50 mL溶液与5 mL植物油混合均匀并在匀浆器中高速搅拌(10 000 r/min)10 min,得到明胶乳液。取一滴亚甲基蓝溶液(1 g/L)于乳液(10 mL)样品中,置于漩涡振荡器中振荡10 s,静置3 min后观察乳状液的颜色,以鉴别乳液的类型。
1.3.5 明胶乳液的显微形态
参照文献[5],按上述方法制备明胶乳液,将其稀释后,取一滴于载玻片上,并盖上盖玻片,静置5 min后用光学显微镜观察样品的显微形态。
1.3.6 明胶的乳化力分析
乳化活性(EAI)和乳化稳定性(ESI)作为间接测定乳液粒子大小的指数,可以通过浊度法测定[10]。将样品乳液制备好后分别在0 min和10 min吸取乳液用1 g/L 十二烷基磺酸钠(SDS)稀释并用漩涡振荡器振荡10 s。最后用紫外-可见分光光度计在500 nm下测定稀释液的吸光度。EAI和ESI可由公式(3)和(4)计算得到:
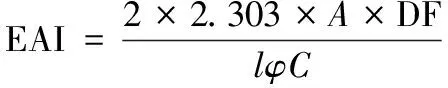
(3)

(4)
式中:EAI,乳化活性,m2/g;ESI,乳化稳定性,min;A,500 nm下的吸光度;l,比色皿直径,m;DF,稀释倍数;φ,植物油所占比例,%;C,明胶质量浓度,g/m3;A0,初始吸光度值;ΔA=A0-A10;Δt=10 min。
考察明胶乳化力时,基本条件设置为:明胶质量浓度10 g/L,pH 7.0,温度20 ℃,离子强度为0。改变其中一个条件,固定其它条件以确定不同环境条件对草鱼皮明胶乳化力的影响。其中,质量浓度:10、20、30、40、50 g/L;pH 3.0、4.0、5.0、6.0、7.0、8.0、9.0;离子强度:0.1、0.2、0.4、0.6、0.8、1.0 mol/L;温度:20、25、30、35、40、45、50 ℃。
1.3.7 数据分析与处理

2 结果与分析
2.1 明胶的持水性分析
蛋白质与水的相互作用通常包括3个方面,即蛋白质最内层紧密作用的结合水、依靠氢键等作用于蛋白质表面的不可冻结水和依靠物理溶胀截留的自由水[12]。将蛋白质与液态水直接作用,通过其自身的溶胀、黏度增加和形成凝胶等一系列物理化学反应所吸收的水分称为持水性。蛋白质的持水能力可以达到改善产品质量、提高产品得率的目的。图1所示为离子强度对明胶持水性的影响。由图1可知,当离子强度由0增加到0.2 mol/L时,持水性逐渐提高,0.2 mol/L时,明胶的持水性最大,达到6.5 g/g;当离子强度增加至0.8 mol/L,明胶持水性显著降低;继续增加离子强度,持水性降低逐渐趋于平缓。这是因为在低离子强度时,离子并未破坏明胶的水化层,反而增加了明胶的溶解性,促进了明胶与水分子的相互作用;而当离子强度超过0.2 mol/L时,盐离子与蛋白质竞争水分子,破坏了蛋白质的水化层和双电层,使得蛋白质脱水并降低其持水性;当离子强度大于0.8 mol/L,因盐离子竞争了大部分水分,导致明胶持水性降低缓慢[13]。
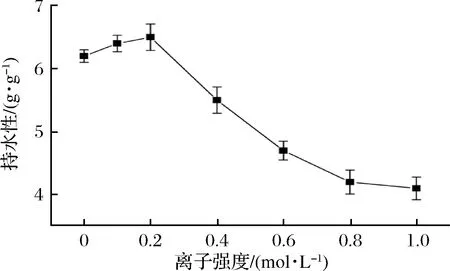
图1 离子强度对明胶持水性的影响Fig.1 Effect of ionic strength on the water binding capacity of gelatin
2.2 明胶的起泡性分析
图2为以吐温80为对照的鲶鱼皮明胶的泡沫活性和泡沫稳定性。

图2 鲶鱼皮明胶、吐温80的泡沫活性和泡沫稳定性Fig.2 Foam expansion (FE) and foam stability (FS) of catfish skin gelatin and tween 80
当鲶鱼皮明胶质量浓度由10 g/L增加到50 g/L,其泡沫活性由127.66%增加至151.23%,且随着时间的延长,明胶的泡沫活性和稳定性逐步降低。这一趋势与乌贼皮明胶[5]、星鲨明胶[14]和触须鱼明胶[15]相同。早在1983年,TOWNSEND和NAKKAI[16]就报道了增加蛋白质的疏水性可以增强食品蛋白质的泡沫活性和泡沫稳定性。随着明胶质量浓度的增加,明胶分子的疏水区域增多、黏度增大,从而促进了其在气液界面形成紧密结合的多层膜,并最终导致泡沫活性和稳定性的增强[5]。随着时间的延长,在重力作用下,气泡间易发生扩散并最终破裂,导致所测试浓度范围内,明胶的泡沫稳定性逐渐降低[10]。吐温80的泡沫活性和稳定性的趋势与鲶鱼皮明胶相同,但远远高于鲶鱼皮明胶。与传统的表面活性剂吐温80相比,鲶鱼皮明胶是一种亲水性蛋白质,且分子量较大导致分子面积的增大和泡沫表面的内聚力减少,从而使其泡沫活性和稳定性较差[17]。
2.3 明胶乳液类型的鉴别
乳液一般分为水包油型(O/W)和油包水型(W/O),可通过染色法进行鉴别。将极微量的水溶性染料滴入到乳液中,如果整个乳液带有染料颜色则为O/W型乳液,若用油溶性染料结果则恰好相反。常用的油溶性染料有红色的苏丹Ⅲ等,水溶性染料则有荧光红、亚甲基蓝等。以水溶性染料亚甲基蓝染色乳液的方法鉴别明胶和吐温80乳液的类型。根据外观可知,2种乳液都呈现水溶性染料亚甲基蓝的颜色,因此判断2种乳液均为O/W型乳液。
2.4 明胶乳液的显微形态
图3为明胶乳液在光学显微镜下的形态。对比吐温80发现,明胶乳液中仅有小部分液滴的直径较大,这是因为鲶鱼皮明胶的亲水性以及分子量较大,使其吸附于油滴界面的能力较弱且数量较少[18]。然而,绝大多数鲶鱼皮明胶乳液的数量和大小与吐温80乳液相当,表明了鲶鱼皮明胶在食品领域中可用作乳化剂的潜力。

a-吐温80;b-明胶图3 吐温80和明胶乳液在高倍镜下的显微形态Fig.3 Micro-morphology of emulsions for tween 80 and gelatin
2.5 明胶的乳化力分析
2.5.1 明胶浓度对其乳化力的影响
图4为不同浓度明胶溶液对其乳化活性(EAI)和乳化稳定性(ESI)的影响。由图可知,随着明胶溶液质量浓度的增加,乳化活性逐渐增大,而乳化稳定性却呈下降的趋势。虽然有文献[19]报道从金枪鱼鱼鳍提取出的明胶的乳化活性和稳定性随着明胶浓度的增加一直呈现增加的趋势,但也有报道乌贼皮明胶的乳化活性随浓度增加而增加,而乳化稳定性却逐渐下降[5]。随着鲶鱼皮明胶浓度的增加,其与油滴界面接触的数量增多,从而导致乳化活性增强;但浓度增加,明胶分子之间易聚集,使得乳液液滴粒子不断增大,而且明胶分子与油滴界面之间的疏水作用的平衡也会随其浓度的增大而破坏,导致鲶鱼皮明胶的乳化稳定性反而下降[20]。
2.5.2 pH值对明胶乳化力的影响
图5为鲶鱼皮明胶溶液在不同pH值下的乳化活性和乳化稳定性。由图5可见,随着pH值的升高,明胶的乳化活性和乳化稳定性降低,在pH 5.0时达到最低,随后乳化活性和乳化稳定性则随着pH值的升高而继续升高。pH 5.0时,明胶溶液的乳化活性和乳化稳定性最小,分别为27.45 m2/g和39.54 min。有文献报道当溶液的pH值远离蛋白质的等电点时,其溶解性和电子排斥力增大,因而能够促进蛋白质样品的乳化活性和乳化稳定性[21-22]。已经测定本方法提取的鲶鱼皮明胶的等电点为4.89,接近5.0,明胶在此时的溶解性和电子排斥力最低,聚集形成直径较大的聚集体,由此导致其乳化活性和乳化稳定性下降到最低值。

图5 pH值对明胶乳化活性和乳化稳定性的影响Fig.5 Effect of pH on the emulsion activity index and emulsion stability index of gelatin
2.5.3 离子强度对明胶乳化力的影响
离子强度对鲶鱼皮明胶乳化活性和乳化稳定性的影响如图6所示。从图6中可以很明显的看出,当NaCl浓度增加至0.2 mol/L时,明胶的乳化活性逐渐增加,继续增加离子强度时,明胶的乳化活性却显著下降;而在所测试的离子强度范围内,明胶的乳化稳定性却呈不断降低的趋势。这一现象与乌贼皮明胶[21]以及鹰嘴豆蛋白提取液[22]的乳化力相符合。低离子强度下(<0.2 mol/L),盐溶效应提升了明胶的溶解性,促进了明胶分子与油滴之间的相互作用,从而使明胶乳化活性增加,而Na+可能结合到明胶分子中,导致明胶的乳化稳定性呈下降趋势[22]。当离子强度大于0.2 mol/L时,盐析效应,使明胶乳液粒径不断增大,导致乳化活性和乳化稳定性逐渐降低[23]。此外,AEWSIRI等[21]研究NaCl对明胶乳化力的影响时,认为NaCl的存在使得乳液液滴之间的排斥力不能有效克服液滴之间的吸引力(如范德华力和疏水作用),这种电子筛选使得乳液的净电荷降低并最终导致明胶的乳化活性和乳化稳定性的降低。

图6 离子强度对明胶乳化活性和乳化稳定性的影响Fig.6 Effect of ionic strength on the emulsion activity index and emulsion stability index of gelatin
2.5.4 温度对明胶乳化力的影响
温度对鲶鱼皮明胶乳化活性和稳定性的影响如图7所示。当温度从20 ℃升高到30 ℃时,明胶的乳化活性和乳化稳定性缓慢上升,随着温度的继续升高,其乳化活性和乳化稳定性呈现降低的趋势。当温度低于30 ℃时,可以促进埋藏在明胶分子内部的疏水区域的展开[22],增强蛋白质分子与油滴之间的相互作用,从而导致明胶的乳化活性和乳化稳定性的升高。然而当温度高于30 ℃时,明胶分子从乳液液滴表面的解吸附作用使得乳液液滴破裂和不稳定[24]。此外,温度升高,乳液液滴的运动增强,容易相互碰撞形成颗粒较大的液滴,导致明胶的乳化活性和乳化稳定性降低。

图7 温度对明胶乳化活性和乳化稳定性的影响Fig.7 Effect of temperature on the emulsion activity index and emulsion stability index of gelatin
3 结论
明胶的持水性、起泡性和乳化性在食品领域中具有重要的应用。研究结果表明,鲶鱼皮明胶在低离子强度下具有良好的持水性;其乳液呈O/W型,乳化力与吐温80相当,但起泡性相对较差。当明胶质量浓度为50 g/L和离子强度为0.2 mol/L时,其乳化活性提升,但却在10 g/L明胶质量浓度和较低离子强度具有较强的稳定性。此外,在等电点附近和高温条件下,明胶的乳化活性和稳定性显著降低。实验结果表明鲶鱼皮明胶具有食品工业应用的潜力,今后可通过修饰提升其性能,进一步扩大应用范围。

