石灰软化-超滤技术在柠檬酸沼气双发酵耦联工艺中的应用
苏先峰,徐健,2,鲍家伟,张宏建*,毛忠贵*
1(江南大学 生物工程学院,工业生物技术教育部重点实验室,江苏 无锡,214122) 2(湖北工业大学 生物工程与食品学院,湖北 武汉,430000)
柠檬酸作为一种极其重要的有机酸,被广泛应用于食品、化工、医药等领域[1-2]。我国柠檬酸生产主要采用木薯和玉米淀粉作为发酵原料,每生产1 t柠檬酸会产生7.5~15 m3的发酵废水。发酵废水具有低pH、高COD浓度等特点[3-4]。我国柠檬酸产量和出口常年位居世界首位,大量发酵废水的有效处理给企业带来了巨大挑战。随着国家环保监测的越来越严格,柠檬酸废水治理问题日益突出。目前,柠檬酸行业普遍采用厌氧-好氧-深度处理工艺来处理发酵废水,虽然厌氧处理具有高效率、低能耗优势[4],但好氧单元具有纯消耗、零收益、占地面积广等问题[5],工艺的经济性尚不能让人满意。
为解决好氧单元弊端以及减少新鲜水用量,本实验室提出柠檬酸沼气双发酵耦联工艺,如图1所示。木薯和玉米淀粉作为原料,以黑曲霉作为生产菌株,生产柠檬酸。提取后的发酵废水进入厌氧反应器,在厌氧菌群的作用下,将大量有机物转为沼气。厌氧消化液经资源化处理后作为配料水,回用于下一批柠檬酸发酵,从而解决废水排放问题以及减少新鲜水用量[6]。
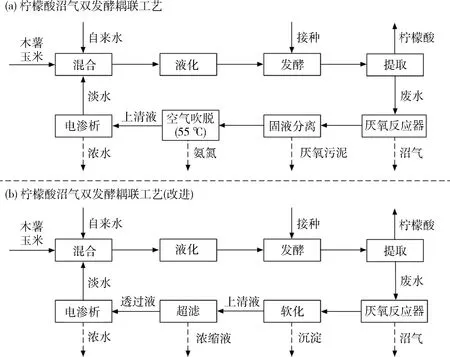
图1 柠檬酸沼气双发酵耦联工艺流程图Fig.1 Flow chart of integrated citric acid-methane production process
经研究发现,厌氧消化液中最主要的抑制因子为高浓度Na+和Na4+[7],故采用电渗析和空气吹脱以消除抑制作用[8]。但是,当前工艺还存在一些问题。电渗析在对厌氧消化液进行脱盐时,由于淡水中Ca2+、Mg2+以及在电场力作用下迁移至浓水,故浓水发生严重结垢现象。膜表面的结垢会导致电渗析离子交换膜脱盐性能下降、膜电阻增加以及能耗增加[9]。为评估电渗析进水水质类型和消除结垢现象,引入朗格利尔饱和指数(Langelier saturation index, LSI)。当LSI<0时,水体有腐蚀倾向,可以继续溶解碳酸钙;LSI=0,水体无腐蚀和结垢倾向;LSI>0,水体有结垢倾向,产生碳酸钙沉淀[10]。空气吹脱为了提高脱氨效率,将厌氧消化液升温并维持在55 ℃,这一过程需要消耗大量能源。另外,电渗析可以将从淡水室浓缩至浓水室[11],完全可以取代空气吹脱,从而实现脱氨的目的。超滤以压差作为推动力,通过膜孔的筛分作用将料液中大于膜孔的大分子溶质截留,实现大分子与溶剂以及小分子的分离[12]。超滤凭借其操作简单、条件温和,而被广泛应用为纳滤、反渗透以及电渗析等深度膜处理的预处理手段[13-14]。本文研究了石灰软化的投加量对硬度降低的效果,超滤的操作条件对透过液通量的影响,以及经电渗析处理后的厌氧消化液回用发酵情况,以期证明改进后的工艺可行性,为柠檬酸行业的清洁生产与持续发展提供新的角度。
1 材料与方法
1.1 材料
1.1.1 菌株与培养基
本文采用实验室保藏的黑曲霉(Aspergillusniger)MZ-11。土豆葡萄糖琼脂(PDA)培养基用于菌株的培养和保藏,其成分(g/L)为:200土豆、20葡萄糖、1.5 MgSO4、3 KH2PO4和20琼脂。
1.1.2 原料与试剂
木薯和玉米均由河南天冠企业集团有限公司提供。耐高温α-淀粉酶(酶活力为20 000 U/mL),由无锡杰能科生物工程公司提供。中温厌氧消化颗粒污泥由宜兴协联生物化学有限公司提供。其余均为市售分析纯化学试剂。
1.1.3 设备
组合摇床(HYL-C),太仓强乐实验设备有限公司;SBA-40B型葡萄糖生物传感器,山东省科学院生物研究所;电渗析器及离子交换膜,山东天维膜技术有限公司;超滤小型试验设备(PL-T2-500),安徽普朗膜技术有限公司;高效液相色谱仪(Ulti Mate 3000),美国 Dionex公司;分析柱为美国Bio-Rad公司HPX-87 H 型离子交换柱;示差折光检测器(R1-101),日本Shodex公司;分光光度计(UV-2100),上海尤尼柯仪器有限公司;5 L 上流式厌氧污泥床(UASB)反应器,上海大明教育仪器有限公司;磁力搅拌器(78-1),江苏金坛市荣华仪器制造有限公司。
1.2 实验方法
1.2.1 种子培养
木薯粉碎后过40目筛,按照料水质量比为1∶3.6,加入去离子水混合,配制种子培养基。30%的H2SO4或2 mol/L NaOH调节pH值至6.0,按照10 U/g添加淀粉酶,沸水浴保温2 h。液化结束后冷却至室温,去离子水补充液化过程中的蒸发水分,调节pH值至5.5并添加1 g/L (NH4)2SO4作为种子培养所需氮源。按照70 mL/L分装至1 L锥形瓶中,于115 ℃温度下灭菌20 min。无菌水配制浓度为6.0×106个的均匀孢子悬液,取10 mL接入装有70 mL无菌种子培养基的1 L锥形瓶中。在(36±1)℃、200 r/min条件下培养21 h。
1.2.2 柠檬酸发酵
木薯和玉米粉碎后过40目筛,按照质量比4∶1混合,并按照料水比体积1∶4.5,加入工艺用水混合,配制发酵培养基。发酵培养基液化过程同种子培养基,液化结束后pH值调至5.5,添加去离子水控制总糖浓度为160 g/L。按照34 mL装液量分装至500 mL锥形瓶中,于115℃温度下灭菌20 min。接种量为15%(v/v),在(37.5±1)℃、260 r/min条件下培养92 h。所有摇瓶实验重复3次。
1.2.3 上流式厌氧污泥床(UASB)消化条件
厌氧消化过程在5 L上流式厌氧污泥床中进行的。污泥接种量为30%(v/v),反应器温度控制在(35±1)℃,柠檬酸沸水进样体积为500 mL/d,COD平均去除率为(94.1±2.5)%。
1.2.4 Ca(OH)2处理厌氧消化液
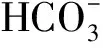
1.2.5 超滤处理
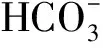

表1 柠檬酸厌氧消化液的化学性质Table 1 Chemical characterization of citric acid anaerobic digestion effluent
1.2.6 电渗析处理
电渗析器由3个独立的循环流道组成,分别为淡水、浓水和极水。每个流道含有1 个循环泵、1个转子流量计(0~100 mL/min)和1 个1.5 L 水槽。膜堆由2块钛度钌极板、21张均相阳离子交换膜和20张均相阴离子交换膜组成。极水为0.1 mol/L Na2SO4溶液。每次实验时,待脱盐的厌氧消化液体积为2 L,按照淡浓水体积比为8∶2(淡水1.6 L,浓水 0.4 L),分别置入淡水水槽和浓水水槽。电渗析操作电压为10 V,流量为60 mL/min。为确保厌氧水回用时钠离子质量浓度低于200 mg/L[17],故淡水电导率降低至600 μs/cm为电渗析脱盐实验结束的终点。
1.3 分析方法
总糖和残总糖测定:样品采用质量分数为4%的HCl于沸水浴中水解2 h,冷却后用NaOH调pH值至中性,通过SBA-40B型葡萄糖生物传感器测定[18]。
柠檬酸、葡萄糖和异麦芽糖含量测定:利用高效液相色谱仪进行检测。流动相为5 mmol/L H2SO4,流速为0.6 mL/min,进样量为20 μL,柱温为60 ℃。
碱度、硬度、浊度、电导率、氨氮、挥发性脂肪酸(VFAs)均采用标准方法[19]测定,并且碱度与硬度折合为CaCO3来计算。
(4)能力提高:淤试题讲评课中强化阅读微技能的使用,以此加强学生在做题中自觉运用所学阅读技巧和解题策略的意识和习惯,提高学生在语篇中准确、快速获取信息的能力。于加强阅读、提高学生的阅读兴趣。除了试题中的阅读材料,教师要帮助学生选择并鼓励学生阅读原汁原味的、贴近生活、题材新颖、富有时代气息的文章(和高考选材接轨,如:英文报纸杂志),以此提高学生的阅读理解能力、英语思维能力、综合认知能力;培养文化品格、思维品质;开阔视野、拓展知识面、与时俱进。
电渗析能耗根据文献所用方法[20]计算。
朗格利尔饱和指数(LSI)是1936年朗格利尔(Langelier)提出的关于水中碳酸氢盐溶解平衡的理论,描述的是碳酸钙固体与水中存在的二氧化碳之间的平衡关系表达式,其计算公式[21]如下:
LSI=pH-pHs
pHs=(9.3+A+B)-(C+D)
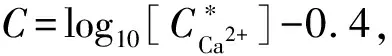
2 结果与讨论
2.1 未软化的厌氧消化液对电渗析影响
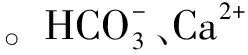
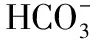
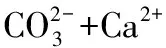
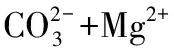
2.2 Ca(OH)2投加量的影响
Ca(OH)2投加量对厌氧消化液化学性质的影响如表3所示。由表3可知,Ca(OH)2投加量从1.5增加至3.0 g/L时,随着Ca(OH)2添加量的增加,静置后上清液中碱度、钙硬度和镁硬度均呈下降趋势。在2.5 g/L投加量下,钙硬度下降趋势变缓慢。在3.0 g/L投加量下,钙硬度降到最低值,镁硬度基本去除,这是因为溶液pH值远大于Mg(OH)2完全沉淀时pH值( pH=10.87)。在Ca(OH)2投加量为3.5 g/L时,碱度略微上升,而钙硬度急剧增加,说明有部分反应剩余的Ca(OH)2溶解。随着Ca(OH)2投加量的增加,上清液的电导率呈现先下降后升高趋势,这是因为投加Ca(OH)2软化过程中,、OH-、Ca2+和Mg2+相互反应的结果,尤其后期电导率的升高也来源于过量的Ca(OH)2溶解。
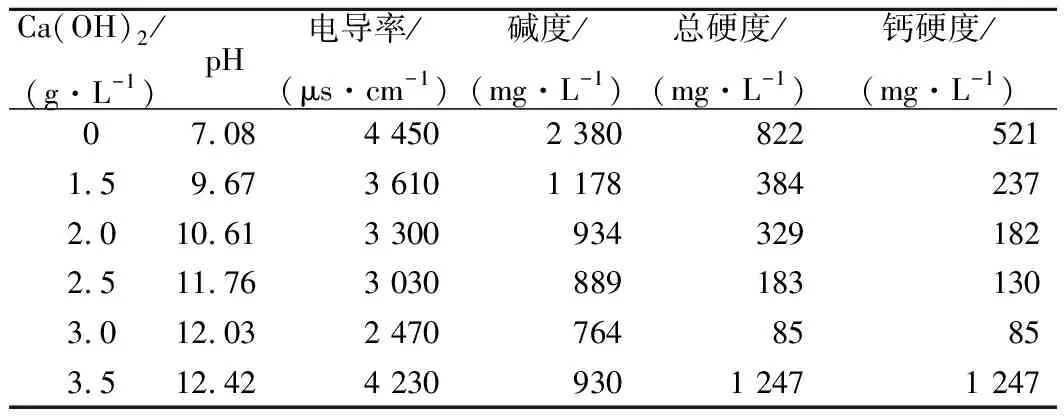
表3 Ca(OH)2投加量对厌氧消化液化学性质的影响Table 3 Effects of lime dosage on chemical characterization of anaerobic digestion effluent
实验得出的最佳Ca(OH)2投加量为2.5 g/L,这与理论计算值1.40 g/L差距很大。首先,厌氧消化液中含有未降解的有机物,可能会随着软化pH值的升高而部分沉降。沉降的有机物和软化生成的CaCO3、Mg(OH)2晶体会将部分Ca(OH)2固体粉末包裹在内,阻止其向水中溶解,从而影响软化效果,间接增加了Ca(OH)2软化用量[23]。其次,在软化效果受上述原因被削弱基础上,Ca(OH)2微溶于水的特性更是加剧了投加量的增加。综上所述,考虑到因被包裹在内而损失量和为推动软化反应进行,Ca(OH)2的投加量应远超过一般情况下的0.2~0.4 mmol/L[23]。根据实验结果,故将投加量定为2.5 g/L。
2.3 软化后静置时间对厌氧消化液余浊的影响
当Ca(OH)2投加量为2.5 g/L时,软化后余浊随时间变化的趋势如图2所示。由于Ca(OH)2溶解缓慢,并且其软化效果受到多方面因素影响,故厌氧消化液pH值上升速度很慢。当搅拌时间为100 min时,溶液pH值出现小幅度的增加,从11.74增加到12.01。这说明软化反应结束,剩余的Ca(OH)2开始溶解,可以停止搅拌静置沉淀。在静置过程中,pH值基本维持在12.05附近不变,这是因为Ca(OH)2随着CaCO3、Mg(OH)2晶体以及有机物松散絮体一起抱团沉降,溶解作用下降。当刚停止搅拌时,厌氧消化液上清液浊度最高。一方面,厌氧消化液含有未被降解的有机物以及少量夹带的絮状污泥,故水体本身初始浊度高。另一方面,由于软化过程中生成大量的CaCO3和Mg(OH)2晶体,使得浊度进一步增加[22]。余浊在静置前90 min内迅速下降至35.80 NTU,而在90~120 min内只下降了0.46 NTU。这说明静置90 min后,CaCO3、Mg(OH)2晶体和过量的Ca(OH)2基本沉降结束。当Ca(OH)2投加量为2.5 g/L时,软化后厌氧消化液理化性质如表3所示。钙硬度为104 mg/L,而镁硬度基本消除。故将软化后厌氧消化液静置时间定为90 min,以充分去除沉淀,减少pH值回调HCl用量。
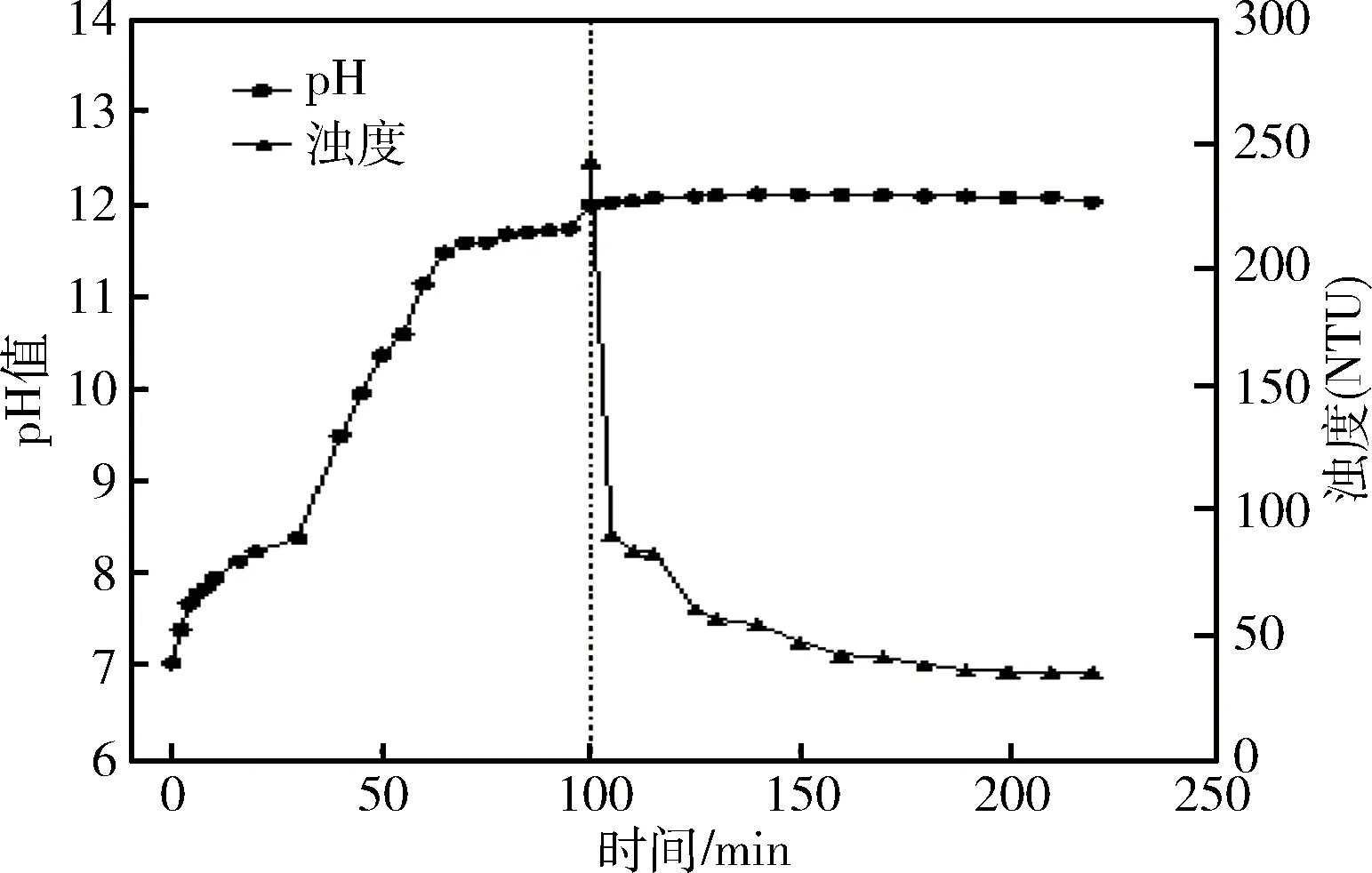
图2 厌氧消化液余浊和pH值随时间变化(Ca(OH)2投加量为2.5 g/L)Fig.2 Variations of residual turbidity and pH of anaerobic digestion effluent with time (lime dosage of 2.5 g/L)
2.4 超滤操作条件优化
超滤透过液通量是衡量超滤过程的重要指标,其受多因素影响,如温度、操作压强、膜面流速和料液pH值,其中最重要的是操作压强和膜面流速[24],故本文选择这两个因素并对其进行考察。
在恒定操作压强0.15 MPa下, 探究不同膜面流速对超滤通量的影响,结果如图3-a所示。膜面流速从3.095 m/s提高到5.014 m/s,通量随之增加;而从5.014 m/s提高到6.066 m/s时,通量却下降。通量大小反映了膜污染程度的轻重。膜面流速的适当提高,可以使得膜表面污染层厚度变薄,跨膜阻力得以减小,通量从而增加。过高流速则会导致膜表面污染层厚度太薄,使得分子量小于膜孔径的有机物截留率降低,膜孔内污染程度加深,膜通量从而下降。此外,过高的膜面流速会消耗更多的动能,故膜面流速选择4.023 m/s。
在恒定膜面流速 4.023 m/s下, 探究不同操作压强对超滤通量的影响,结果如图3-b所示。初始通量随着操作压力的增加而增加。这是因为实验初始时,超滤膜还未受到污染,故随着操作压力的增加,初始膜通量也随之增加。而前10 min内,超滤透过液通量迅速衰减,表明膜表面以及膜孔内部污染出现并且污染逐渐加深。而10 min之后,被截留的有机物在膜表面形成的污染层导致跨膜阻力增加,以及膜孔内的有机物阻塞,其综合污染效果在超滤中后期变化缓慢,从而导致膜通量下降趋势平缓。随着操作压力的升高,超滤过程相对平稳时,0.20 MPa 下的膜通量高于0.15 MPa和0.25 MPa,故最佳操作压强为0.20 MPa。
综上所述,超滤最佳操作压强和膜面流速为0.20 MPa和4.023 m/s。
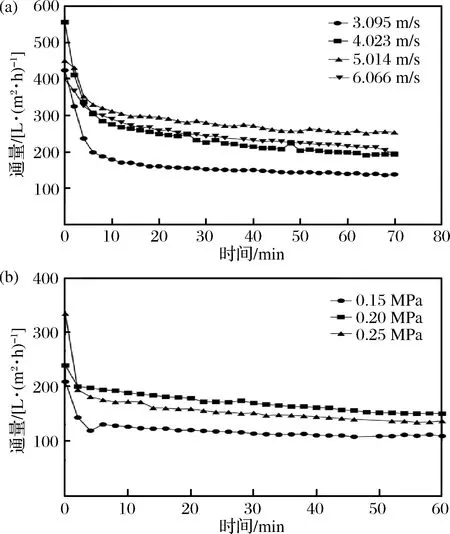
a-膜面流速;b-操作压强图3 操作条件对超滤透过液通量的影响Fig.3 Effect of operation pressure on the permeate flux of ultrafiltration
2.5 软化前后对电渗析操作影响
电渗析处理软化和未软化的厌氧消化液过程如图4所示。
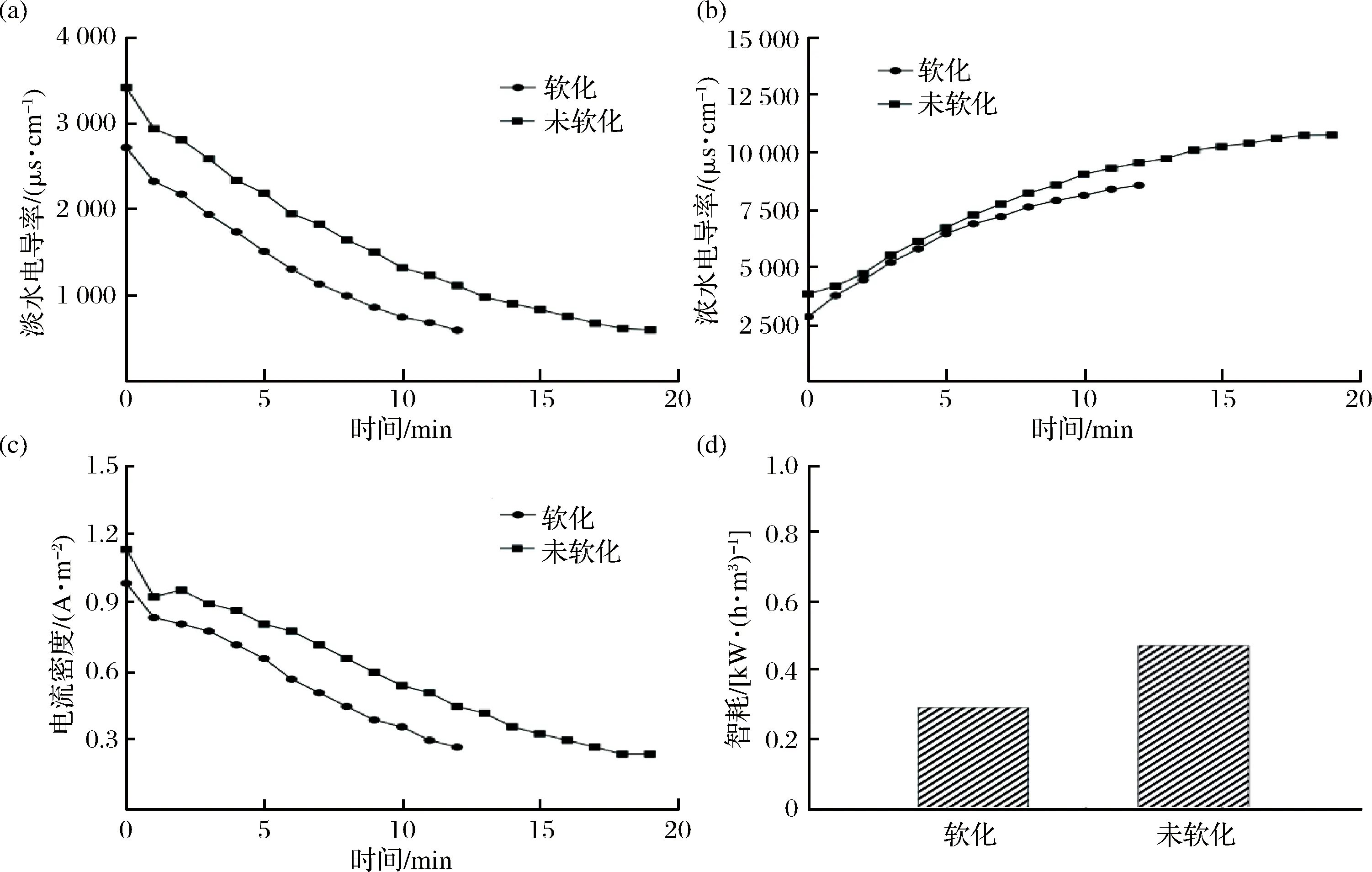
a-淡水电导率;b-浓水电导率;c-电流密度;d-能耗图4 电渗析处理软化和未软化的厌氧消化液Fig.4 Electrodialysis treatment of anaerobic digestion effluent with and without lime softening
图4-a、4-b分别展示了淡水电导率、浓水电导率随时间的变化。由于软化后的厌氧消化液采用HCl回调pH值至8,故初始电导率低于未软化处理的厌氧消化液。厌氧消化液中的阴阳离子在电场力的作用下,从淡水中迁移至浓水中,淡水电导率不断降低,而浓水电导率不断增加。因为未软化的厌氧消化液的初始电导率较高,所以其浓水电导率较高。图4-c展示的是电流密度随时间的变化趋势,其与淡水电导率变化趋势一致。在恒定操作电压10 V下,电渗析膜堆总电阻越高,则电流密度越低。电渗析淡水电导率不断降低,导电性能不断下降,故电渗析膜堆总电阻逐渐增加。此外,由于软化后的厌氧消化液电导率较低,故膜堆电阻较高,电流密度较未软化的要低。图4-d展示的是两种处理方式下的厌氧消化液经电渗析处理结束时的能耗。由于软化的厌氧消化液电导率较低,脱盐过程中的电流密度较低,并且在相同的脱盐终点下,耗时也相对缩短,故单位体积能耗较低。
软化和未软化的厌氧消化液经电渗析处理前后的理化性质如表4所示。软化后的厌氧消化液的碱度和钙硬度为161和134 mg/L,较未软化大幅度降低,故其LSI较未软化要低。电渗析脱盐结束后,软化和未软化的浓水LSI均小于临界结垢值(LSI=1),完全不会结垢[25]。
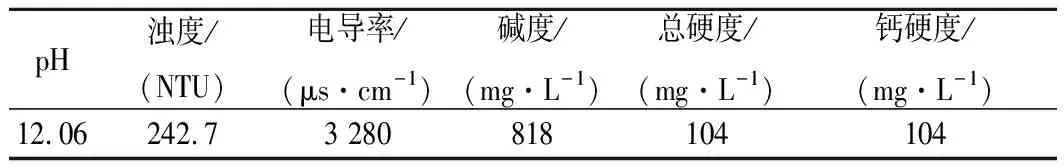
表4 厌氧消化液中投加2.5 g/L Ca(OH)2后的理化性质Table 4 Chemical characterization of anaerobic digestion effluent with the lime dosage of 2.5 g/L
2.6 处理后的厌氧消化液回用对柠檬酸发酵影响
厌氧消化液经不同处理手段处理后的金属离子浓度如表5所示。石灰软化操作显著降低了钙镁离子浓度,而超滤主要为去除大分子有机物,故对厌氧消化液金属离子浓度影响不大。电渗析处理后的厌氧消化液金属离子浓度大幅度下降,并且在脱盐终点时溶液中主要的金属离子是钠离子。
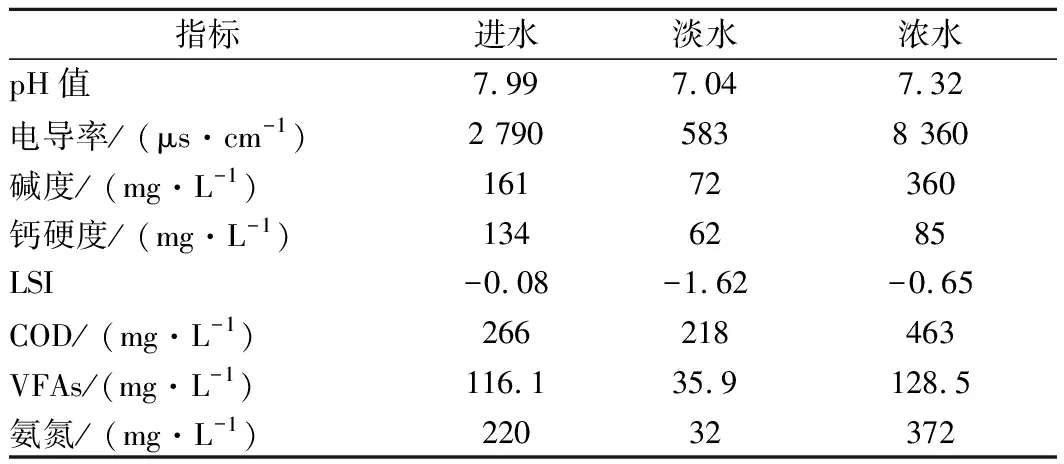
表5 厌氧消化液经电渗析处理后的理化性质Table 5 Chemical characterization of anaerobic digestion effluent with electrodialysis treatment
软化后的厌氧消化液经超滤和电渗析处理,作为配料水回用于柠檬酸发酵,其发酵结果如图5所示。处理后的厌氧消化液的柠檬酸、残总糖和残异麦芽糖质量浓度分别为(134.67±4.72)、(28.33±1.52)和(3.80±0.36) g/L,与采用去离子水配料发酵结果相近。柠檬酸发酵废水经UASB厌氧反应器处理后,溶液中Na+、氨氮是废水直接回用后导致柠檬酸产量下降的主要原因,其临界抑制浓度分别为200和100 mg/L;厌氧消化液中挥发性脂肪酸主要成分为乙酸和丙酸,其临界抑制浓度分别为480和296 mg/L[26]。厌氧消化液经软化、超滤和电渗析处理后,Na+、氨氮和VFAs的大幅度下降,并低于临界抑制浓度。电渗析淡水回用发酵,柠檬酸产量基本与去离子水发酵结果相当。这说明,厌氧消化液经该工艺处理后,可作为配料水回用于柠檬酸发酵。
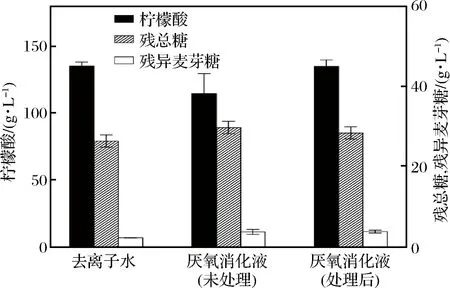
图5 不同处理后的厌氧消化液对柠檬酸发酵的影响Fig.5 Effects of anaerobic digestion effluent with different treatments on citric acid fermentation
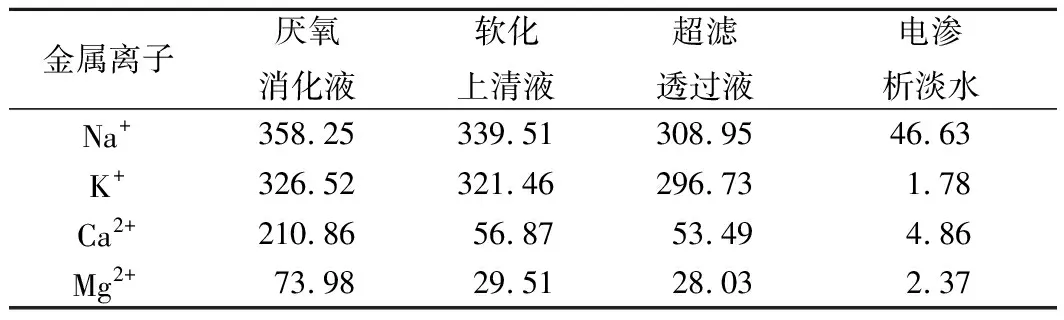
表6 厌氧消化液经不同手段处理后的金属离子质量浓度 单位:mg/LTable 6 The concentrations of metal ions in anaerobic digestion effluent with different treatment
3 结论
柠檬酸厌氧消化液采用石灰软化降低硬度,Ca(OH)2最优投加量为2.50 g/L,总硬度从1 376 mg CaCO3/L降至200 mg CaCO3/L以下,满足后续处理要求。超滤处理软化后的厌氧消化液的最优操作压强和膜面流速,分别为0.20 MPa和4.023 m/s。对软化后的厌氧消化液进行电渗析脱盐,生产的淡水作为配料水,回用至柠檬酸发酵,其柠檬酸产量为(134.67±4.72) g/L,基本与去离子水发酵水平持平。石灰软化-超滤技术在柠檬酸沼气双发酵耦联工艺中具有工业应用价值,革除高能耗的空气吹脱单元,解决了电渗析脱盐浓水结垢问题,对实现柠檬酸行业清洁生产具有重要意义。

