口服降糖药分别联合不同胰岛素类似物治疗血糖控制不佳2型糖尿病的临床研究
陆玉莲,钱铁镛,陈一丁,沈史伟,姚伟峰
本研究背景:
2型糖尿病作为临床高发慢性疾病,患者主要以持续性血糖水平异常升高为主要特征,并且伴随由于胰岛素分泌缺陷而引发的三大代谢紊乱,即蛋白质、脂肪及糖代谢紊乱。已有相关研究表明2型糖尿病的发生和发展与患者自身胰岛素分泌量较低以及胰岛素抵抗具有相关性,部分2型糖尿病患者在运动、饮食干预的基础上服用降糖药的效果并不佳,机体血糖指标难以得到稳定控制。而目前国内不同种类胰岛素治疗口服降糖药血糖控制不佳2型糖尿病的临床研究并不多见。二甲双胍作为口服降糖药是临床治疗2型糖尿病的首选药物,而地特胰岛素、双相门冬胰岛素30为两种胰岛素类似物。在本研究中将二甲双胍分别与两种胰岛素类似物联合治疗,旨在探究药物治疗2型糖尿病的有效方案。
2型糖尿病(type 2 diabetes mellitus,T2DM)是进行性恶化的代谢性疾病,基本病理机制是胰岛素抵抗和胰岛素分泌不足,疾病前期以胰岛素抵抗为主,口服降糖药效果明显,伴随胰岛β细胞功能的进行性衰退,部分患者即便增加口服降糖药剂量或联合两种以上降糖药,依然不能有效达到血糖控制目标。因此,启动胰岛素治疗就成为血糖达标的重要手段,对于病程较长的T2DM患者,胰岛素治疗甚至可能是最主要血糖控制措施[1]。随机对照试验证实,对于单纯口服降糖药或单纯注射胰岛素血糖无法达标的患者采用二者联合方案,有助于血糖达标[2-3]。胰岛素类似物因相对于人胰岛素具有耐受性好、低血糖事件少的优点,逐步受到临床医生和患者的青睐,但由于个体差异显著,目前对口服降糖药血糖控制不佳患者尚无统一的降糖方案,本研究采用随机对照试验对比了二甲双胍分别联合长效胰岛素类似物(地特胰岛素)和预混胰岛素类似物(双相门冬胰岛素30)的临床疗效与安全性,结果如下。
1 资料与方法
1.1 纳入与排除标准 本研究获得无锡市第二人民医院医学伦理委员会批准及患者知情同意。纳入标准:年龄<75岁;T2DM明确诊断1年以上;服用双胍类、磺脲类、格列奈类、α-糖苷酶抑制剂、二肽基肽酶Ⅳ抑制剂等药物>3个月且糖化血红蛋白(HbA1c)≥7.0%;签订随访协议书。排除标准:丙氨酸氨基转移酶水平高于参考范围(<40 U/L)上限2倍,男性血清 肌 酐(Scr)>133 μmol/L 或 女 性 Scr>124 μmol/L,既往接受胰岛素及胰岛素类似物或胰高血糖素样肽1受体激动剂类药物治疗,严重糖尿病慢性并发症,甲状腺等内分泌疾病,心肌梗死病史,近期使用糖皮质激素,对胰岛素过敏,运动障碍。
1.2 临床资料 选取2014年8月—2016年12月无锡市第二人民医院收治的符合上述纳入与排除标准的T2DM患者112例为研究对象。按照《医学统计学》(第6版)[4]附录随机数字表将患者分为A组57例、B组55例。A组中男32例、女25例,年龄42~73岁,T2DM病史3~11年,体质指数(BMI)19.5~29.2 kg/m2,腰臀比(WHR)0.83~0.89;B组中男 26例、女 29例, 年 龄 40~72岁,T2DM 病 史4~12年,BMI 20.1~31.2 kg/m2,WHR 0.84~0.90。两组患者性别、年龄、T2DM病史、BMI、WHR、入组时HbA1c、合并高血压、血脂异常、高尿酸血症比例比较,差异均无统计学意义(P>0.05,见表 1)。
1.3 治疗方案 所有患者行运动干预与饮食控制,停服除二甲双胍外所有降糖药,积极控制血压。在上述基础上,A组采用二甲双胍+地特胰岛素降糖方案。具体为:早、中、晚餐后口服盐酸二甲双胍缓释片(500 mg/片,成都恒瑞制药有限公司,国药准字H20030952)500 mg,每晚睡前10 min腹部皮下注射1次地特胰岛素(300 U/3 ml,诺和诺德制药有限公司,国药准字J20090101),起始剂量0.1~0.2 U/kg,每2 d根据空腹血糖(FPG)调整胰岛素用量,调整方案参照《中国2型糖尿病防治指南(2013年版)》[5]推荐标准,以达到并维持FPG<6.1 mmol/L且不引起明显低血糖为目标。B组采用二甲双胍+双相门冬胰岛素30降糖方案。二甲双胍口服方案同A组,每日早晚餐前5 min腹部皮下注射1次双相门冬胰岛素30(300 U/3 ml,诺和诺德制药有限公司,国药准字J20100037),胰岛素起始方案同A组,并监测晚餐前血糖,根据《中国2型糖尿病防治指南(2013年版)》[5]推荐方案优先调整晚餐前血糖。
1.4 评价指标 (1)血糖指标:治疗前与治疗12周后,采用日立7600全自动生化分析仪测定患者FPG、餐后2 h血糖(2 hPG)(葡萄糖氧化酶法),并采用美国BIO.RAD全自动血红蛋白检测仪测定HbA1c(高效液相色谱法),计算治疗后FPG(FPG<6.0 mmol/L)、2 hPG(2 hPG<8.0 mmol/L)及 HbA1c(HbA1c<7.00%)达标率。(2)胰岛功能指标:治疗前与治疗12周后,采用贝克曼库尔特Unicel DXI800全自动化学发光免疫分析仪测定血清胰岛素(FIns)(化学荧光法),通过稳态模型(HOMA)计算胰岛β细胞功能指数(HOMA-β)〔HOMA-β=20×FIns/(FPG-3.5) 〕与胰岛素抵抗指数(HOMA-IR)〔HOMA-IR=(FIns×FPG)/22.5〕[6]。(3)胰岛素类似物用量:记录两组患者每日胰岛素类似物用量。(4)BMI:治疗前与治疗12周后测量身高、体质量,计算BMI。(5)药物不良反应:重点记录低血糖事件发生情况,FPG<3.9 mmol/L或低血糖症状能通过进食自行缓解定义为低血糖事件,FPG<2.8 mmol/L或患者不能自行处理,需他人帮助给予碳水化合物、胰高血糖素或其他复苏措施定义为重度低血糖事件[7]。
1.5 统计学方法 采用SPSS 22.0软件进行统计学处理,计量资料以()表示,两组间比较采用独立样本t检验,组内比较采用配对t检验;计数资料比较采用χ2检验或Fisher's确切概率法。以p<0.05为差异有统计学意义。
2 结果
2.1 血糖与HbA1c变化比较 治疗期间,A、B组分别脱失2例、1例,两组实际纳入分析55例、54例。治疗前,两组患者FPG、2 hPG、HbA1c比较,差异均无统计学意义(P>0.05);治疗12周后,两组患者FPG、2 hPG、HbA1c比较,差异均无统计学意义(P>0.05);A组和B组治疗12周后FPG、2 hPG、HbA1c较治疗前降低,差异均有统计学意义(p<0.05,见表2)。
2.2 FPG、2 hPG、HbA1c达标率比较 治疗12周后,两组患者FPG、2 hPG、HbA1c达标率比较,差异均无统计学意义(P>0.05,见表3)。
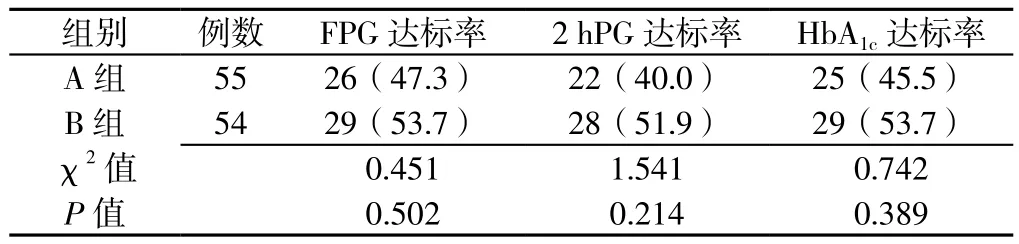
表3 两组患者治疗12周后FPG、2 hPG、HbA1c达标率比较〔n(%)〕Table 3 Comparison of FPG,2 hPG,and HbA1c compliance rates between the two groups after 12 weeks of treatment
2.3 HOMA-β、HOMA-IR变化比较 治疗前,两组患者HOMA-β、HOMA-IR比较,差异均无统计学意义(P>0.05);治疗12周后,两组患者HOMA-β、HOMA-IR比较,差异均无统计学意义(P>0.05)。A组和B组治疗12周后HOMA-β较治疗前升高,HOMA-IR较治疗前降低,差异均有统计学意义(p<0.05,见表4)。
2.4 胰岛素类似物用量比较 A组患者胰岛素类似物用量为(24.96±3.57)U/d,B组患者胰岛素类似物用量为(25.18±3.85)U/d,差异无统计学意义(t=0.309,P=0.758)。
2.5 BMI变化及药物不良反应发生率比较 治疗前及治疗12周后,两组患者BMI比较,差异均无统计学意义(P>0.05);两组患者治疗前与治疗12周后BMI比较,差异均无统计学意义(P>0.05,见表5)。两组患者治疗期间主要发生低血糖事件、转氨酶升高、头痛、胃肠功能紊乱等,两组低血糖事件均能自行处理解决,未出现重度低血糖事件。两组患者低血糖事件、转氨酶升高、头痛、胃肠功能紊乱发生率比较,差异均无统计学意义(P>0.05,见表6)。

表1 两组患者基线特征及合并症比较Table 1 Comparison of baseline characteristics and comorbidities between the two groups
表2 两组患者治疗前与治疗12周后血糖与HbA1c变化比较Table 2 Comparison of changes in blood glucose and HbA1c between the two groups before and after 12 weeks of treatment
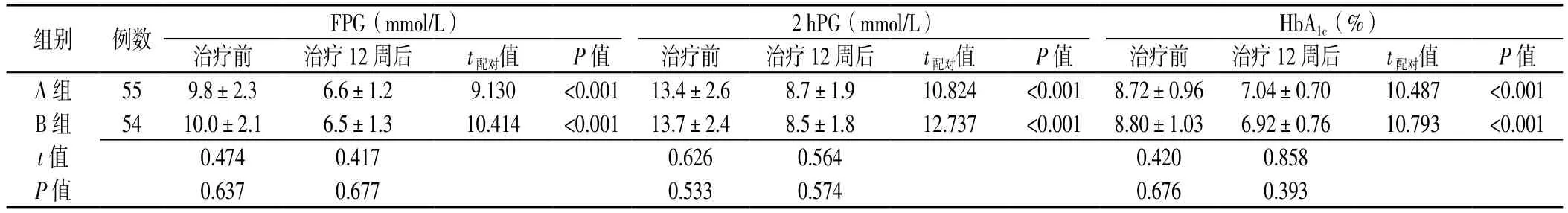
表2 两组患者治疗前与治疗12周后血糖与HbA1c变化比较Table 2 Comparison of changes in blood glucose and HbA1c between the two groups before and after 12 weeks of treatment
注:FPG=空腹血糖,2 hPG=餐后2 h血糖
组别 例数 FPG(mmol/L) 2 hPG(mmol/L) HbA1c(%)治疗前 治疗12周后 t配对值 P值 治疗前 治疗12周后 t配对值 P值 治疗前 治疗12周后 t配对值 P值A组 55 9.8±2.3 6.6±1.2 9.130 <0.001 13.4±2.6 8.7±1.9 10.824 <0.001 8.72±0.96 7.04±0.70 10.487 <0.001 B组 54 10.0±2.1 6.5±1.3 10.414 <0.001 13.7±2.4 8.5±1.8 12.737 <0.001 8.80±1.03 6.92±0.76 10.793 <0.001 t值 0.474 0.417 0.626 0.564 0.420 0.858 P值 0.637 0.677 0.533 0.574 0.676 0.393
表4 两组患者治疗前与治疗12周后HOMA-β、HOMA-IR变化比较Table 4 Comparison of HOMA-β and HOMA-IR changes between the two groups before and after 12 weeks of treatment

表4 两组患者治疗前与治疗12周后HOMA-β、HOMA-IR变化比较Table 4 Comparison of HOMA-β and HOMA-IR changes between the two groups before and after 12 weeks of treatment
注:HOMA-β=稳态模型胰岛β细胞功能指数,HOMA-IR=稳态模型胰岛素抵抗指数
组别 例数 lnHOMA-β lnHOMA-IR治疗前 治疗12周后 t配对值 P值 治疗前 治疗12周后 t配对值 P值A组 55 11.8±3.3 74.7±18.7 24.509 <0.001 6.26±1.84 2.16±1.02 14.453 <0.001 B组 54 11.6±3.5 78.5±21.7 22.409 <0.001 6.33±1.90 2.08±0.93 14.764 <0.001 t值 0.307 0.991 0.432 0.428 P值 0.759 0.324 0.667 0.670
3 讨论
胰岛素抵抗和胰岛β细胞功能的进行性衰退贯穿T2DM的发生、发展。在T2DM早期,糖尿病主要表现为外周组织对葡萄糖的利用障碍,口服降糖药能一定程度刺激胰岛β细胞的分泌,从而有助于血糖达标。伴随糖尿病病程的延长,胰岛对葡萄糖的反应敏感性下降,胰岛β细胞功能逐步降低,单纯的口服降糖药及运动疗法已无法达到血糖控制目标,此时在口服降糖药基础上补充胰岛素就成为促进血糖达标的重要手段。长效胰岛素类似物和预混胰岛素类似物因其降糖作用持久平稳,低血糖发生率低而在临床上备受推崇,本研究即通过随机对照方法观察并比较二甲双胍分别联合长效胰岛素类似物和预混胰岛素类似物的降糖效果。
二甲双胍是胰岛素增敏剂,一直是指南推荐的首选口服降糖药,主要通过增加外周组织对葡萄糖的摄取和利用来实现降糖目的。二甲双胍能减轻患者体质量,与胰岛素连用能抵消胰岛素引起的体质量增加的不良反应[8],但长时间大剂量服用二甲双胍有增加脂质代谢紊乱与降糖效果下降的风险[9]。地特胰岛素是一种经人工修饰以六聚体形式存在的长效胰岛素类似物,与人胰岛素高度同源,皮下注射后,释放缓慢,体内与清蛋白结合率高达99%,进而造成其与胰岛素受体的结合延迟,体内变异度小,0.4 U/kg的治疗剂量下作用时间长达20 h,且无明显峰值,每日注射1次便会产生持久的降糖效果,且地特胰岛素具有不明显增加体质量的优势[10]。双相门冬胰岛素30是一种预混胰岛素类似物,由30%可溶性门冬胰岛素和70%鱼精蛋白门冬胰岛素组成,其中可溶性门冬胰岛素注射后起效仅需5~15 min,能提供更快、更高的餐时胰岛素分泌峰值,与餐后血糖高峰几乎同步;鱼精蛋白门冬胰岛素则释放缓慢,则作为基础胰岛素的补充,有效降低FPG。二者合成曲线更接近生理条件下胰岛素的分泌模式,能为患者提供基础和餐时量胰岛素的供给[11],有效降低餐前低血糖风险和餐后血糖的过度漂移。
表5 两组患者治疗前与治疗12周后BMI变化比较(,kg/m2)Table 5 Comparison of changes in BMI between the two groups before and after 12 weeks of treatment

表5 两组患者治疗前与治疗12周后BMI变化比较(,kg/m2)Table 5 Comparison of changes in BMI between the two groups before and after 12 weeks of treatment
组别 例数 治疗前 治疗12周后 t配对值 P值A组 55 24.7±2.8 24.9±2.5 0.395 0.694 B组 54 25.2±3.1 25.1±2.8 0.176 0.861 t值 0.895 0.393 P值 0.373 0.695
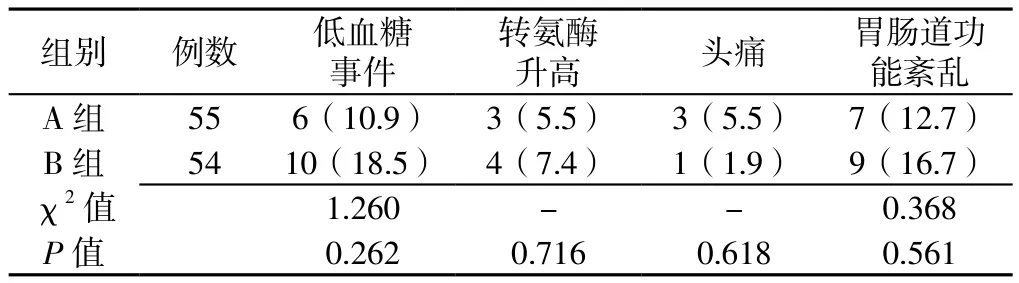
表6 两组患者药物不良反应发生率比较〔n(%)〕Table 6 Comparison of the incidence of adverse drug reactions between the two groups
本研究中,对口服降糖药血糖控制不佳的T2DM患者改用二甲双胍+特地胰岛素和二甲双胍+双相门冬胰岛素30治疗12周,两组治疗后FPG、2 hPG、HbA1c均较治疗前大幅下降,HOMA-β、HOMA-IR均较治疗前大幅改善,45.0%以上的患者实现了HbA1c达标,说明两种方案对单纯口服降糖药血糖控制不佳的T2DM患者均有效,患者胰岛素分泌与胰岛素抵抗水平均较治疗前改善;两组治疗后FPG、2 hPG、HbA1c下降幅度相近。
文献报道,基础胰岛素联合口服降糖药治疗血糖控制不佳的T2DM患者改用双时相门冬胰岛素30联合二甲双胍,16周后HbA1c达标率为60.0%[12],本研究治疗12周后B组HbA1c达标率为53.7%,结果与其相近。
体质量增加与药物性低血糖是启动胰岛素治疗中的两大障碍。通常意义上胰岛素剂量越大,体质量增加越明显,而体质量增加又不利于血糖控制,文献报道,T2DM患者胰岛素治疗1年内体质量增加了(0.98±0.71)kg,且HbA1c每降低1%体质量增加2 kg[13]。本研究中两种胰岛素类似物联合二甲双胍治疗12周后,体质量变化不明显,可能是二甲双胍的降体质量作用抵消了两种胰岛素的升体质量作用,因而二甲双胍联合胰岛素类似物可以在不明显增加体质量的同时实现血糖的控制。同时,更好的血糖控制常伴随着更高的低血糖风险,低血糖带来的头晕、心悸等症状又会对患者使用胰岛素带来阴影,影响胰岛素治疗依从性。本研究中B组低血糖事件发生率较A组偏高,可能与B组较A组增加了注射次数而造成胰岛素作用的叠加及药物本身的峰值有关;虽两组均为轻度低血糖事件,但也应警惕发生重度低血糖事件的风险。
综上所述,对单纯口服降糖药血糖控制不佳的T2DM患者,采用二甲双胍联合地特胰岛素或双相门冬胰岛素30均能在无明显体质量变化的基础上达到相似的降糖效果。但本研究所选样本量不多,且研究时间较短,今后将扩大样本量及研究时间,以进一步分析其远期效果。
作者贡献:陆玉莲、钱铁镛、陈一丁进行文章的构思与设计,撰写论文;陆玉莲、沈史伟进行研究的实施与可行性分析;陆玉莲、钱铁镛、姚伟峰进行数据收集;钱铁镛、陈一丁、姚伟峰进行数据整理;陈一丁、沈史伟进行统计学处理;钱铁镛、姚伟峰进行结果的分析与解释;陆玉莲进行论文的修订;陆玉莲、沈史伟、姚伟峰负责文章的质量控制及审校;陆玉莲、钱铁镛对文章整体负责,监督管理。
本文无利益冲突。

