乳胶增强免疫比浊法与电化学发光法检测降钙素原的对比分析
降钙素原(procalcitonin)是反映患者全身炎性反应活跃程度的一种蛋白质指标[1],在细菌感染、脓毒症、脏器功能衰竭等疾病时血浆中的水平与疾病程度呈正比例升高[2],因可以有效指导临床抗生素的使用安全而在临床中广泛应用[3-4]。目前以电化学发光-双抗体夹心法为主流检测方法,价格较贵,本研究对胶乳增强免疫比浊法与Roche电化学发光-双抗体夹心法检测降钙素原结果进行分析比较,评估检测成本相对较低的胶乳增强免疫比浊法在临床使用的可行性。
1 资料与方法
1.1 一般资料:采用无菌真空采血管采集住院患者新鲜血液标本2~3 ml,以3 000 r/min分离血清,依照CLSI EP9-A2用患者样本进行两种方法比对及偏倚评估,选择的比对样本在检测方法线性范围内呈低、中、高值均匀分布,并且>50%的标本浓度在正常参考区间外,两种检测方法均使用留取当天的样本2 h内测定完毕。
1.2 仪器与试剂:两种方法检测均在Roche Cobas8000全自动生化免疫分析流水线上进行检测,参比方法使用Roche原装进口的配套试剂及校准品,采用的检测方法为电化学发光-双抗体夹心法,检测范围是0.02~100 ng/ml,试验方法试剂为宁波美康生物科技有限公司的降钙素原检测试剂盒,检测方法为胶乳增强免疫比浊法,线性范围是0.05~60 ng/ml。
1.3 方法
1.3.1 方法的选择:乳胶增强免疫比浊法为试验方法(Y),电化学发光-双抗体夹心法为比较方法(X),依据EP9-A2文件要求进行方法间比对实验。
1.3.2 样本检测:操作者能够熟练掌握使用仪器设备,实验前认真做好仪器的保养、校准、维护等。做好室内质控并保证质控结果受控,然后进行标本的测定,比对方法与实验方法每个样本均重复进行2次检测。80例患者样本共得到320个血清样本测定数据结果。
1.3.3 数据结果离群值检查:以检测结果绝对差值和相对差值应小于4倍平均绝对差值和4倍相对差值平均值作为方法内离群点界限;以两种方法的绝对差值与相对差值,小于4倍的绝对差值平均值和4倍的相对差值平均值作为方法间离群点判断界限。
1.3.4 数据作图
1.3.4.1 重复检测均值的散点图:以试验法双份测定的均值对比较方法双份测定的均值的散点图,Y轴为试验方法即胶乳增强免疫比浊法检测的结果,X轴为比较方法(电化学发光-双抗体夹心法)的结果。
1.3.4.2 所有结果的散点图:以试验方法的每个检测结果Yij对比较方法结果均值作图。
1.3.4.3 均值差异偏倚图:以电化学发光法为X轴变量(-X)对(Y+X)/2作图。
1.3.4.4 单个结果差值偏倚图:(单个试验方法结果YIJ-单个比较方法结果Xi)对(试验方法均值比较方法均值2作图。
1.3.5 X取值范围合适宽度检验:用两种方法的直线相关系数(r)判断X的取值范围是否合适够宽,如果r≥0.975,则可用线性回归来统计斜率和截距[5],并计算试验方法线性回归方程Y=bX+a。
1.3.6 两种方法偏倚评价:选定PCT医学决定水平(Xc)的3个浓度水平0.5 ng/ml、2 ng/ml、10 ng/ml计算出相应的 Bc%和95%可信区间,按照美国CLIA'88允许误差10%为标准,判断两种方法偏倚是否可接受。
1.3.7 在PCT医学决定水平0.5 ng/ml、2 ng/ml、10 ng/ml处以比较方法为参考方法计算两种方法检测结果的阳性符合率,评估两种方法临床测定结果的一致性。
1.4 统计学处理:采用SPSS22统计软件进行数据分析,计数数据的比较采用χ2检验法,P<0.05为差异有统计学意义。试验方法(Y)和比较方法(X)测定数据在Excel 2007软件上按照NCCLS EP9-A2文件要求编制相关函数公式进行计算分析,软件自动进行数据统计并绘制图表。
2 结果
(4E)
2.2 数据作图:散点图1和散点图2可见,试验方法与比较方法检测结果线性关系良好,无明显离群点,数据分布均匀;在偏倚图3、4中可见,两种方法对同一份标本测定结果偏差较小,无明显离群值,分布合理。

图2 所有结果的散点图

图3 均值差异与二种方法的均值的偏倚图

图4 单个结果差值对两种方法的均值的偏倚图
2.3 研究数据取值合适范围的检验:比较方法的(X)的取值合适范围,可用相关系数γ做粗略的估计。依据EP9-A2文件给出的r计算公式得出本研究的r=0.990 92。大于文件要求的r≥0.975的要求,说明本研究数据取值范围合适,回归方程的斜率和截距可靠。
2.4 直线回归分析:依据EP9-A2文件相关计算公式,本研究数据求得截距(a)=0.037斜率(b)=0.99215,直线回归方程为Y=0.037+0.992 15X。
2.5 临床可接受评价:相对偏差Bc%=(Bc/Xc)×100%小于1/2CLIA'88相对允许总误差(TEa%)表明试验方法的检测结果与比较方法一致,具有可比性。见表1。
2.6 选定 PCT医学决定水平0.5 ng/ml、2 ng/ml、10 ng/ml以比较方法为参考方法计算两种方法检测值的阳性符合率为95%、96.25%、95.0%,差异无统计学意义(P >0.05),见表2。
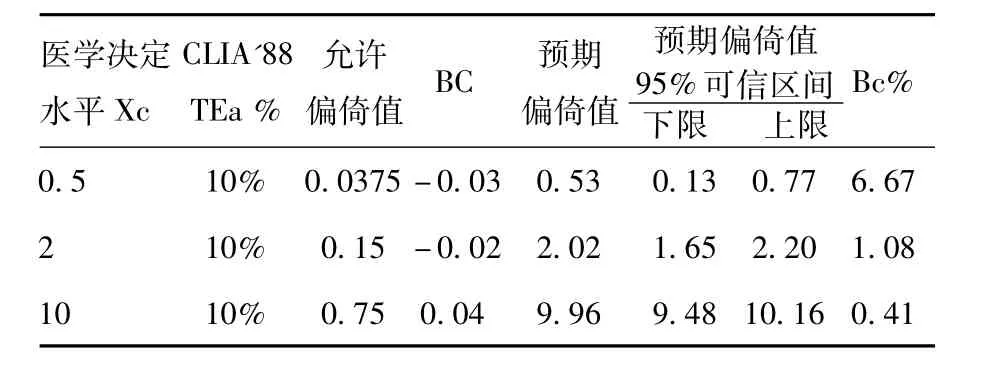
表1 医学决定水平(Xc)偏倚
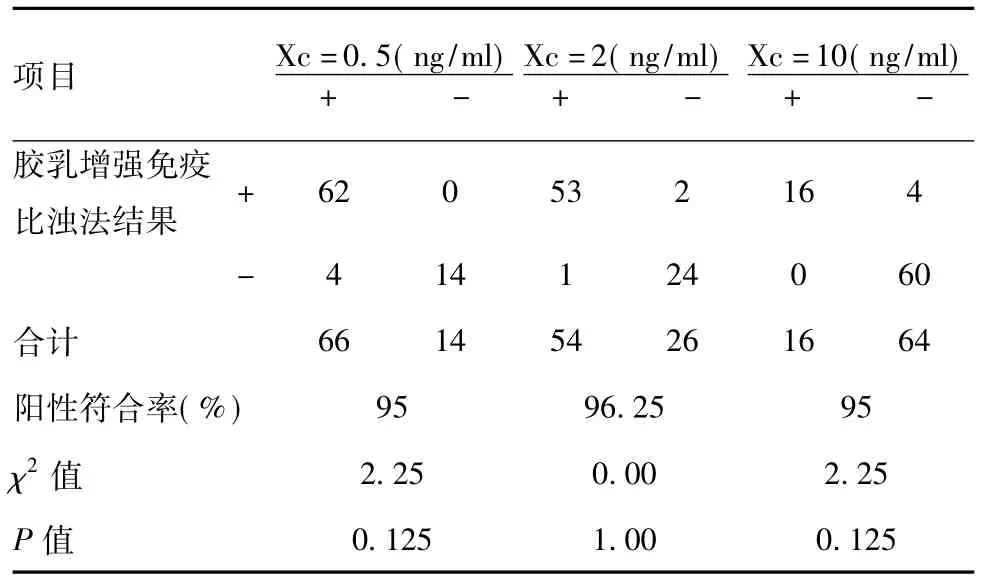
表2 两种方法结果阳性符合率分析
3 讨论
目前降钙素原已在临床上广泛的应用[6-7],该项目的检测方法有凝胶层析法、高效液相色谱分析法、化学发光法、放射免疫分析法、胶乳增强免疫比浊法等。而高效液相色谱分析法与凝胶层析法检测过程费时且不易自动化,难以在医院临床处理大量常规标本的检测,放射免疫分析法(RIA)对pH、离子强度、反应温度等要求较高,影响因素很多,虽然在操作过程中注意相关事项,该方法的检测结果的稳定性较好,但是不可回避的是它存在着放射污染问题,且试剂有效期短,影响了其发展。国内外应用广泛的PCT检测分析方法是化学发光法,该方法具有高灵敏度,检测下限≤0.02 ng/ml,有较宽的测定范围0.02~100 ng/ml,检测过程不需要任何额外辅助光源,免除了因辅助光源本身稳定性、光栅、光波选择器等的影响,使检测结果灵敏度高、稳定可靠、误差较小,同时试剂稳定期长。但是电化学发光不可避免的问题是试剂成本高,配套的仪器设备维护费用较高。胶乳增强免疫比浊法操作也是目前较常见的降钙素原的检测使用方法,该方法随着乳胶颗粒技术上的优化和发展,特别是纳米级粒子的推出解决了单克隆抗体结合力不强的问题,使该方法的检测线性范围窄、干扰因素多、实验室稳定差等问题有了显著的改进。本研究中该试验方法的检测线性范围是0.05~60 ng/ml,成本较电化学发光-双抗体夹心法试剂大幅降低,但由于在抗原抗体特异性反应时,生成结合物的量与反应物的浓度有关,该方法不可避免地会存在该现象。
不同检测系统结果不一致的情况是一个普遍存在的问题,也常见很多报道。引起的原因很多,常见的原因除了方法学不一致,还因血清中可能含有对不同的嗜异体等物质,引起某些免疫交叉反应[8]。此外还有检测系统校准品的溯源性不一致,操作者本身在检测过程中未做好校准、质控、试剂稳定期、规范操作等[9]。本研究依据目前国内外实验室广泛应用的NCCLS EP9-A2文件[10]要求对血清PCT检测项目在线性范围内,采用国产的胶乳增强免疫比浊法与电化学发光免疫分析法进行比较。结果显示两种方法比对数据在方法内重复性、方法间的测定结果均无离散点,数据分布均匀[11-12]。两种检测方法的相关系数r=0.990 92,符合大于文件要求的r≥0.975的要求,直线回归方程为Y=0.037+0.992 15X,说明本研究数据取值范围合适[13],回归方程的斜率和截距可靠,且两种方法在医学决定水平2 ng/ml、10 ng/ml处的偏倚Bc%<1/2 CLIA'88允许误差10%的标准。在医学决定水平0.5 ng/ml的偏倚Bc%相对较大,主要原因是胶乳增强免疫比浊法的线性范围0.05~60 ng/ml,相对比较方法电化学发光法的最低检出限0.02 ng/ml,灵敏度低于比较方法,导致样本中PCT含量较低的时候,报告数据产生的差异相对值大,但是对于两个系统在0.5 ng/ml医学决定水平的临床阴阳结果判断差异无统计学意义(P>0.05),对细菌感染的诊断并无影响,所以表明两种方法偏倚可以接受。以电化学发光作为比较方法,两种方法的阳性符合率比较,差异无统计学意义(P>0.05)。
同时要注意的是本研究的试验方法其产品说明书上标注的试剂开瓶稳定期可达30 d,但该方法检测线性范围是0.05~60 ng/ml,临床参考限一般设定<0.5 ng/ml,由于临床参考线与该方法最低检测限相对较接近且含量较低,所以在使用过程中要严格保证校准品的质量及校准频次。本研究过程中每次检测前均进行了校准与质控,对比每次定标与不同批次校准品定标后的结果偏差,同时要认真比较每次校准的曲线空白值与吸光系数,如果多点定标中校准液低值接近或低于参考线值时需要稀释校准品中的低值校准液,或者联系厂家提供低值校准液。某些时候校准品由于批次、运输或存储过程等多方面的影响导致校准品偏倚较大[14-15]。并且两者厂家均说明了各自方法对血清抗干扰的能力如在溶血、黄疸、脂血等方面的程度要求,但是两种方法的抗干扰能力不同,为避免偏差,本研究统一选择两种方法都均不受影响的血清样本进行比对。综上所述,在对检测结果准确和快速高效的前提下,相对较低的成本、简便的操作成为检验用户及患者的目标[8]。本研究中的胶乳增强免疫比浊法与电化学发光法,在规范的质量体系和标准的操作程序下均能有效检测降钙素原且相关性良好,均能满足临床需要,适合临床实验室推广使用。

