阵发性室上性心动过速患者心房颤动的诱发及其特点
杨帆 郑亚西 杨龙 杨永曜 刘兴会
心房颤动患者的肺静脉区域独特的组织学和电生理性质是发生和维持心房颤动的主要因素。经皮心房导管肺静脉消融术(又称肺静脉电隔离术,pulmonary vein isolation,PVI)是目前心房颤动患者的主要治疗手段之一。但研究显示,起源于肺静脉以外部位的心房颤动也并非少见[1]。在心房颤动诱发试验中,采用不同刺激部位及方案诱发的成功率不同[2-3]。并且,不同研究对心房颤动诱发成功的定义也不同[2,4-6],这同样造成诱发成功率和预测复发率的偏差。目前PVI术后常以不能诱发心房颤动作为射频消融终点的意见还未获得一致认可,加之心房颤动诱发的特异性的不确定,临床对于电刺激诱发方案仍有诸多分歧[5-6]。本研究探讨阵发性室上性心动过速(paroxysmal supraventricular tachycardia,PSVT)患者刺激心房诱发出心房颤动及其心房颤动的特点。
1 对象和方法
1.1 对象 选择2015年10月至2017年2月在贵州省心血管病研究所住院成功接受射频消融术的PSVT患者65例,男29例,女36例,年龄18~65(42.6±12.7)岁。纳入标准:年龄≥18岁,且≤65岁。排除标准:(1)既往诊断有心房颤动发作史;(2)器质性心脏病、高血压、甲状腺功能亢进、肝肾功能不全、慢性肺部疾病、胸廓畸形、睡眠呼吸暂停综合征等。本实验符合本院伦理委员会要求,所有患者均告知研究内容并签署知情同意书。
1.2 方法
1.2.1 收集一般资料 采用北京索莱宝科技有限公司试剂盒检测血清钾离子浓度。采用美国GE公司Vivid E9心血管彩色超声诊断仪测量左心房前后径(left atrium anteroposterior diameter,LAD)、右心房(right atrium,RA)横径和上下径、左心室舒张末期内径(left ventricular end diastolic diameter,LVDD)、右心室舒张末期内径(right ventricular end diastolic di ameter,RVDD)、左心室射血分数(left ventricular ejection fraction,LVEF)。
1.2.2 射频消融方案 采用四川锦江电子科技有限公司电生理仪(LEAD-7000)和心脏射频消融仪(HL-100F)。根据既往常规方法[7],首先行心内电生理检查观测记录高位右心房有效不应期(high right atrial effective refractory period,HRA-ERP)、冠状窦远端有效不应期(coronary sinus distal effective refractory period,CSd-ERP)、左心房房性心动过速(left atrium atrial tachycardia,LAT)和右心房房性心动过过速(right atrium atrial tachycardia,RAT)等。通过心内刺激明确是否为房室折返性心动过速(atrioventricular reentrant tachycardia,AVRT) 或房室结折返性心动过速(atrioventricular nodal reentrant tachycardia,AVNRT)后,再予射频消融术(采用温度和功率上限控制模式,左侧旁道和房室结双径路消融温度≤55℃、功率≤30W,右侧房室旁道温度≤60℃、功率≤50W)。
1.2.3 诱发心房颤动刺激方案 刺激部位为高位右心房(high right atrial,HRA),脉宽 1.5ms,刺激电压以S1S1刺激1:1夺获最小电压,若成功诱发心房颤动则不再刺激。若未能诱发,则进行以下刺激频率方案(图1),每一步刺激次数均≤10次。记录成功诱发心房颤动的参数、持续时间及终止方式等。

图1 心房颤动诱发刺激方案路线示意图
1.2.4 诱发心房颤动指标 心房颤动诊断标准参照欧洲心脏病学会(European Society of Cardiology,ESC)2012 心房颤动指南[8],结合冠状窦(coronary sinus,CS)电极记录到A波(A波电压大小不一、间距绝对不齐,AA间距<200ms)明确心房颤动诱发成功。
1.2.5 诱发心房颤动分级 根据诱发成功与否分为诱发组和未诱发组。诱发组依据诱发出的心房颤动持续时间分为<10s、10s~<1min及≥1min等3个亚组。
1.3 统计学处理 采用SPSS17.0统计软件。计量资料先行正态性检验、方差齐性检验。符合正态分布的计量资料以表示,两组比较采用t检验,多组比较采用One-way ANOVA检验。计数资料以百分率表示,比较采用χ2检验。诱发心房颤动持续时间长短预测因子的检测采用Cox回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 诱发组及其亚组与未诱发组患者一般资料比较 诱发组 37例(56.9%),未诱发组 28例(43.1%)。所有诱发的心房颤动均自行终止。其中<10s亚组 19例(29.2%);10s~<1min亚组 8例(12.3%);≥1min亚组10例(15.4%)。诱发组及其亚组与未诱发组患者一般资料比较见表1。
由表1可见,诱发组与未诱发组性别、年龄、AVRT/AVNRT等比较,差异均无统计学意义(均P>0.05)。<10s亚组患者的LAd小于10s~<1min亚组、≥1min亚组,差异均有统计学意义(t=0.006、0.002,均 P<0.05),10s~<1min 亚组、≥1min 亚组中LAd比较,差异无统计学意义(P>0.05)。3亚组其他参数比较,差异均无统计学意义(均P>0.05)。
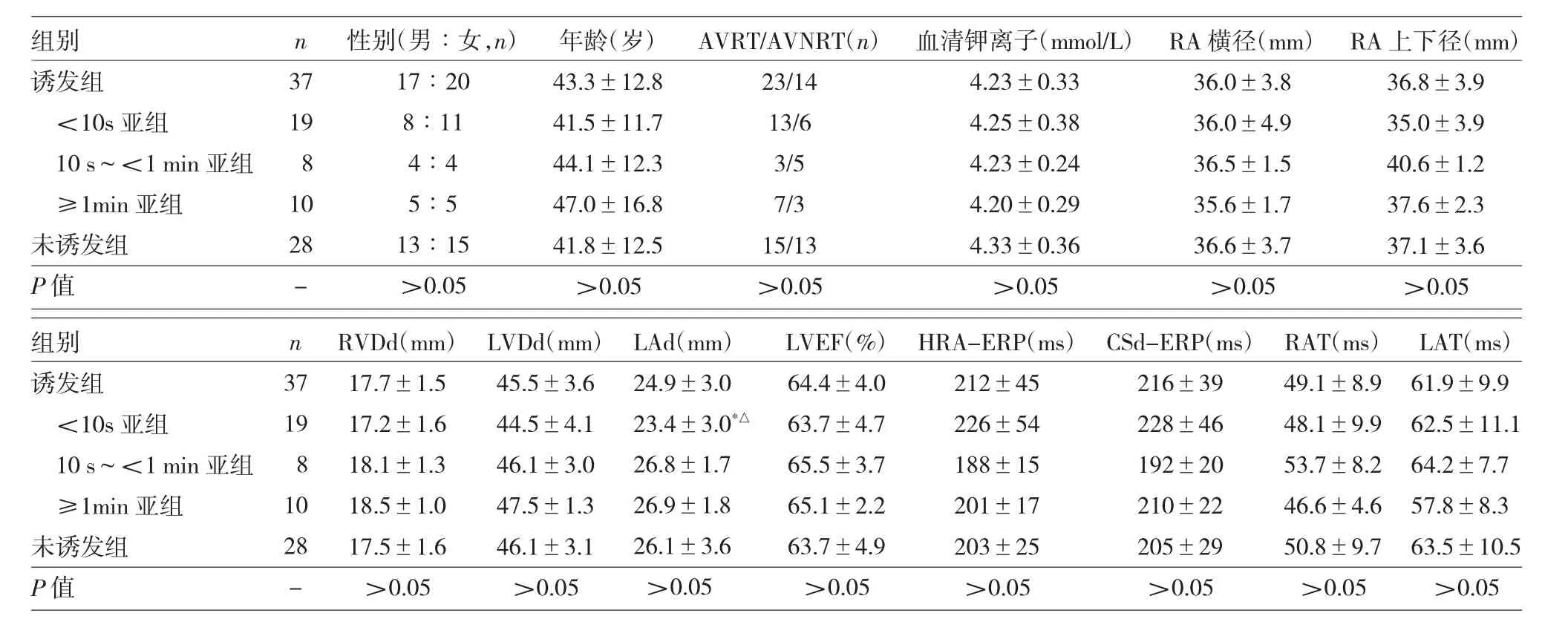
表1 诱发组及其亚组与未诱发组患者一般资料比较
2.2 诱发方案与心房颤动持续时间比较 诱发心房颤动刺激次数与心房颤动持续时间呈正相关(r=0.592,P<0.01)。进一步比较3个亚组间的诱发刺激次数,结果显示,<10s亚组平均刺激次数为(4.3±2.2)次,低于 10s~<1min 亚组(8.0±3.1)次及≥1min亚组(10.1±5.0)次,两两比较差异均有统计学意义(t=0.002、0.0002,均 P<0.05)。10s~<1min亚组与≥1min亚组比较,差异无统计学意义(P>0.05)。参照以往研究[2],将<10s亚组与10s~<1min亚组合并计算,显示<1min患者平均刺激次数为(5.4±3.0)次,明显少于≥1min亚组,两者比较,差异有统计学意义(t=0.002,P<0.01)。以上结果提示,随着刺激次数的增加,诱发心房颤动持续时间延长。
3 讨论
迄今为止,由于不同研究对心房颤动诱发成功的定义不同[5-6,9],导致心房颤动诱发成功率不同,从而对射频消融术后心房颤动复发率的预测也不同。本研究中,在无心房颤动病史、无器质性心脏病和其他合并症的PSVT患者进行射频消融术后,再给予刺激诱发心房颤动,有56.9%能够成功诱发心房颤动。并且在刺激部位和刺激节律固定情况下,诱发心房颤动的持续时间主要与诱发刺激次数(即累积刺激强度)呈正相关,此外与患者LAd大小也有关。
在刺激诱发心房颤动的三因素(刺激部位、刺激节律和刺激强度)中,就刺激部位而言,不同研究所选择的诱发刺激部位不完全一致。Huang等[10]仅在冠状窦近端刺激,另一些研究则在此基础上增加右心房游离壁及左右心耳处[8]。结果表明,刺激部位不同,诱发心房颤动成功率不一致,这可能与心房各部位的不应期及传导速度存在异质性有关。本研究采用的HRA游离壁刺激为心内电生理研究中常用和必用的刺激部位。就刺激节律而言,Huang等[10]从250ms开始,直至能1:1夺获心房的最短起搏周期的递减刺激诱发心房颤动,无论是总体诱发成功率还是持续诱发成功率均较200ms的猝发刺激明显升高。另外,Haissaguerre等[5]报道,心房期前收缩刺激的诱发成功率低于从250ms开始每次递减10ms的猝发刺激。本研究主要在于探讨刺激强度与心房颤动诱发的关系,故仅采用一种常用的HRA游离壁猝发刺激。就刺激强度而言,刺激强度包括刺激波脉宽、刺激电压、刺激频率、刺激节律、刺激次数、单次刺激持续时间和多次刺激间歇时间长短等因素。目前不同研究中重复刺激的次数不一致(2~10次不等)[2,5-6],诱发心房颤动的成功率和持续时间也不相同。本研究中发现随着刺激次数的增加,诱发心房颤动持续时间延长。本研究中,心房颤动持续时间数据分布离散,而心房颤动持续时间分级数据分布相对集中,故统计分析结果更为可靠。有趣的是,在有无成功诱发心房颤动的诱发组和未诱发组中,未诱发组给予刺激强度皆大于诱发组,而两组基线资料差异无统计学意义,目前尚无法解释此现象的原因,有待进一步探讨。
专家共识认为左心房大小是心房颤动射频消融术后复发的独立预测因子[11]。本研究发现,随着LAD增大,心房颤动成功率增加且心房颤动持续时间延长,符合上述共识。但在诱发组和未诱发组中,患者LAD大小差异无统计学意义,目前难以解释。
有研究显示,PVI术后常以不能诱发心房颤动作为射频消融终点,并且达到此终点的患者术后复发率明显降低[2,5,12-13]。但是,分析这些研究设计,发现所采用的刺激方案和对心房颤动诱发成功的定义不完全相同,因而如何评价诱发试验的价值,目前没有统一的标准。另外,有研究者采用药物(如异丙肾上腺素)和起搏刺激诱发心房颤动,也提出心房颤动诱发是否成功对远期复发有预测价值的结论[14-15]。但是也有其它研究结果表明,射频消融术后成功诱发心房颤动并不能预测其复发[6,16]。总之,迄今的研究结果尚不能确定射频消融术中诱发心房颤动对随访心房颤动射频复发的预测价值,可靠的结论需要进一步大规模、多种诱发方案对照和远期随访结果证实。