甲状旁腺激素联合低频脉冲电磁场治疗老年骨质疏松性股骨粗隆骨折的临床疗效观察
弓永顺 万超 徐毅
郑州市中医院,河南 郑州 450007
前言
骨质疏松症是现代社会影响人类健康的重大问题。它是以骨矿成分减少、骨微结构退化为特征的,导致骨脆性增加、骨折风险提高的一种全身性骨骼系统疾病,多见于中老年人群。目前中国人口老龄化严重,骨质疏松发病率正逐年提高,老年性疾病成为医学关注的重点。老年人群骨质疏松患病率多,加之运动协调力下降,故股骨粗隆骨折的发生率高。骨折后患者卧床时间长,极易导致深静脉血栓形成、褥疮和坠积性肺炎等严重并发症,具有极高的病死率和致残率[1]。目前股骨粗隆骨折的治疗原则是骨折的坚强内固定及患者术后早期肢体活动,由于股骨粗隆间骨折患者骨骼质地及愈合能力较差,即使及时选择内固定治疗,术后也不能早期活动,术后仍有部分患者出现并发症而死亡[2]。因此坚强的内固定和及时早期的愈合对骨质疏松粗隆骨折患者预后至关重要,鉴于此,本研究使用抗骨质疏松药物甲状旁腺激素联合低频脉冲电磁场结合PFNA(Proimal Femoral nail Antirotation)髓内固定系统治疗老年骨质疏松粗隆骨折,观察术后骨折愈合时间、关节功能及骨密度和骨代谢的情况,为临床上改善骨质疏松粗隆骨折治疗提供新的治疗方法。
1 资料和方法
1.1 一般资料
选取2013年7月~2015年4月间老年骨质疏松股骨粗隆间骨折患者98例,患者入院后均采用常规骨盆摄片检查确诊,经DXA骨密度仪(BMD machines)检测T值小于2.5个标准差表现患有骨质疏松。排除标准: ①类风湿关节炎、激素药物长时间口服及其他原因引发继发性骨质疏松;②伴有其它内分泌及各种代谢性骨病者如糖尿病、肾脏疾病或者严重心脑血管病和1年之内服用过影响骨代谢药物者;③药物过敏者;④因药物不良反应等各种原因中途退出研究者,使用抗骨质疏松药物治疗的患者。所有患者对治疗方法知情,愿意接受治疗并与院方签署治疗知情同意书。
将患者随机分为治疗组和对照组(每组49例)。观察组患者(男18例,女 31 例)年龄为62~80 岁,平均年龄为(68.78±6.54)岁;其受伤原因为高处坠落伤3例、车祸伤17例和行走跌伤伤29例,以及骨折分型采用 Evans 分型:Ⅱ 型 2 例、Ⅲ型28例、Ⅳ型17 例和Ⅴ型 2 例。对照组患者(男20例,女29例)年龄为63~81岁,平均年龄为(67.98±6.36)岁;其受伤原因为高处坠落伤2例、车祸伤18例和行走跌倒伤29例,以及骨折分型为Ⅱ型2例、Ⅲ型27例、Ⅳ型18例和Ⅴ型2例。两组患者的一般基线资料经比较,其差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
所有患者均使用由德格拜尔公司提供的PFNA 对股骨粗隆进行骨折闭合复位内固定手术治疗,同时每日给予一定剂量的钙剂及维生素 D:口服惠氏制药有限公司碳酸钙D3片(钙尔奇)600 mg×60 s1 次1片,1日1~2次作为基础治疗;对照组患者每天皮下注射PTH 1-34 20 μg(特立帕肽,美国礼来公司),注射部位在左下腹、右下腹或者大腿外侧;治疗组在对照组治疗的基础上给予低频电磁场治疗:天津市同业科技发展有限公司生产的 TY-PEMF-B 型 OP 治疗仪实施低频电磁场治疗,1个疗程为2月,分3个阶段,第1 个阶段每天1次,第 2 个阶段每 2 天 1 次,第3个阶段开始每 3 天 1 次,每个阶段 10 次,每次 40 min。加用连续治疗6个月比较两组患者的关节功能各指标的恢复情况。
1.3 评价指标
用视觉模拟评分法(VAS)评分治疗前后髋关节疼痛情况;髋关节Harris功能评分[3]评定患者治疗后髋关节功能差异;骨折愈合时间以临床愈合结合随访过程中X线结果来评定;使用双能X线吸收骨密度仪(LUNAR,美国)测量治疗前后的患者股骨颈及腰椎(L1-4)骨密度变化;采用双抗体夹心酶联免疫法(ELISA)和放免法测定人骨碱性磷酸酶(BALP)、人胶原交联羧基末端肽(CTX)、抗酒石酸盐酸性磷酸酶异构体 5b(TRACP-5b)及血骨钙素(BGP)水平。
1.4 统计学处理

2 结果
2.1 两组患者 VAS 疼痛评分比较
治疗前两组VAS评分比较,不具有统计学意义;治疗后1、3个月及6个月,两组患者VAS评分较治疗前均有明显的下降,且治疗组的VAS评分下降更为明显(P<0. 05),见表1。
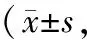
表1 两组治疗前后VAS 评分比较分)Table 1 Comparison of VAS scores before and after the treatment between the two groups scores)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05。
2.2 两组患者Harris 髋关节指数评分和骨折愈合时间比较
治疗后3及6 个月,治疗组的Harris评分均明显优于对照组(P<0.05)。骨折愈合时间治疗组较对照组明显减少(P<0.05),见表2。

表2 两组治疗后Harris评分及骨折愈合时间比较Table 2 Comparison of Harris score and fracture healing time after the treatment between the two groups
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05。
2.3 治疗后骨密度值比较
治疗前,两组各个部位的骨密度比较,无统计学意义(P>0.05);术后6个月,两组患者各部位骨密度较治疗前均有明显的提高,且治疗组较对照组提高更为显著(P<0. 05),见表3。
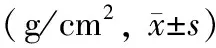
表3 两组治疗后骨密度比较Table 3 Comparison of bone mineral density after treatment between the two groups (g/cm2,
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05。
2.4 治疗后骨代谢指标的比较
治疗前,两组骨代谢指标水平比较,无统计学意义(P>0.05)。治疗6个月,两组患者的骨代谢指标较治疗前均有明显的改善,且治疗组较对照组改善更为明显(P<0. 05)。见表 4。

表4 两组治疗后骨代谢指标比较Table 4 Comparison of bone metabolism after the treatment between the two groups
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05。
3 讨论
骨质疏松症 (osteoporosis, OP)是一种以骨量低下、骨微结构破坏为特征、导致骨脆性增加、易发生骨折的全身性骨病为近年来人们关注的焦点[4],其中以髋部、椎体骨出现骨折最为常见。髋部骨折和椎体骨折作为最常见的骨质疏松性骨折。在老年人死亡率相关的调查表中,骨质疏松性髋骨骨折有着较高的死亡率,仅次于心血管和脑血管疾病,远远超过了恶性肿瘤的死亡率。由于老年人髋关节骨折的死亡率和残疾率高,近年来骨质疏松性髋部骨折治疗从早期保守治疗到现在的首选手术治疗。手术治疗可以稳定骨折,使患者能够尽快运动,从而减少可能严重影响长期卧床的各种并发症。
目前临床上对无手术禁忌证的老年骨质疏松合并股骨粗隆骨折患者,首选的治疗方法是通过手术来获得坚强固定,但是由于骨折患者多合并骨质疏松,骨质较差,一般的固定手法很难取得较好的效果,需要特殊的要求内固定物[5]。髋关节是下肢活动的关键部位,临床上常用的LISS、DHS等易造成髋关节活动度下降,同时增加严重并发症发生风险[6]。近年来一种可以有效提高骨折复位质量、减少出血、缩短手术时间、加快关节功能恢复、减少并发症发生等方面具有优势治疗老年骨质疏松粗隆骨折的治疗方法获得广泛应用,它就是有AO研制的PFNA固定系统。本研究中患者使用的治疗方法就是PFNA,取得较好的结果,从VAS评分、Harris评分及愈合时间和以前学者研究结果[6-8]相似,这表明PFNA确实是一种合适于治疗老年骨质疏松粗隆骨折的有效方法。
骨质疏松患者的破骨细胞活性相对增强,自身骨组织的愈合能力相对于正常骨组织来说比较差,骨折愈合速度明显降低;同时股骨粗隆骨折围手术期制动及卧床休息可导致骨量丢失,不利于骨折的愈合,因此,加用促进骨折愈合干预手段尤为重要。PTH是由甲状旁腺主细胞和嗜酸性粒细胞合成并分泌,在维持骨稳态的过程中介导成骨细胞合成代谢及活化破骨细胞来发挥着双重调节作用,一方面通过增加成骨细胞的数量及促进骨生长因子释放来促进骨形成;另一方面PTH可以通过刺激成骨细胞分泌白介素-1(IL-1)和白介素-6(IL-6)等因子来增强破骨细胞活性,促进骨吸收,使骨钙释放入血,因此PTH对成骨及破骨细胞活性有着重要的意义[9]。脉冲电磁场是一种治疗骨质疏松的物理方法,近年来多个临床及基础研究已经表明脉冲电磁场不仅能促进骨形成而且还通过抑制骨吸收,可以有效减少绝经后骨量丢失,增加骨密度[10, 11]。本研究证实PTH联合脉冲电磁场可以有效增加髋部及腰椎的骨密度,同时我们结果表两者联合使用明显可以加速骨折愈合,改善骨代谢异常。
我们研究表明PTH联合脉冲电磁场结合PFNA是一种有效治疗老年骨质疏松粗隆骨折的方法。我们发现治疗的VAS评分、Harris 评分在同一时期明显优于对照组,可能原因有几点:PTH联合电磁场可以加速骨折的愈合,同时增加局部的骨量,使患者疼痛明显减轻,因此VAS评分、Harris 评分中疼痛项得到改善;疼痛得到改善后,成骨增强、破骨抑制,局部疼痛减轻,患者活动增加,进一步影响Harris评分,同时活动会改善患者骨质疏松情况,也会影响到VAS评分;PTH联合电磁场对骨质疏松本身的治疗,骨密度及骨代谢改善很好的证实这点,也会影响到VAS评分、Harris 评分。
但是总的来说PTH联合脉冲电磁场结合PFNA治疗老年骨质疏松粗隆骨折是一种切实可行的方法,安全有效,值得临床推广。

