全内置式可膨胀型生物涂层脊柱前路内固定系统体外细胞毒性及肌肉植入试验
黄学良 朱双芳 林雨聪 周初松
南方医科大学珠江医院(广州 510282)
胸腰椎后路减压内固定术是治疗脊柱疾病常见的手术方式,可实现脊柱的360°环形减压、前方支撑、重建脊柱稳定性,也是脊柱外科医师最为熟悉的手术入路[1]。但对于严重的胸腰椎爆裂性骨折、椎体肿瘤等疾病,胸腰椎前路手术具有暴露充分、减压彻底、固定牢固等优势[2]。目前临床上常用的前路内固定系统有很多,各有优缺点。作者自主研发的全内置式可膨胀型生物涂层脊柱前路内固定系统(图1)由钛合金和表面羟基磷灰石涂层制成,具有全内置、可膨胀性等特点,在前期研究中已证明其具有良好的生物力学性能,可重建脊柱稳定性。本研究根据医疗器械生物学评价中的相关标准[3],采用体外细胞毒性试验和肌肉植入后局部反应试验来评价此内固定系统在这两方面的生物安全性。
1 材料与方法
1.1 实验动物 清洁级8周龄SD大鼠12只,雌雄不限,体质量180~200 g,由南方医科大学动物实验中心提供。
1.2 主要材料、仪器及浸提液的制备 全内置式可膨胀型生物涂层脊柱前路内固定螺钉(由北京富乐公司生产,并由北京航空航天大学进行螺钉表面羟基磷灰石涂层);L929小鼠成纤维细胞、胎牛血清、DMEM培养基、5%DMSO(二甲基亚砜)、MTT溶液;倒置相差显微镜、超净工作台、CO2细胞培养箱。浸提液的制备:以含10%新生牛血清的DMEM培养液为浸提介质,浸提比为0.2 g/mL,在(37±1)℃的CO2细胞培养箱浸提(72±2)h获取浸提液。
1.3 实验方法
1.3.1 体外细胞毒性试验 实验组(内固定材料在浸提液浓度为100%、75%、50%、25%时分别配制);空白对照组(浸提介质);阴性对照(密度聚乙烯);阳性对照(5%DMSO)。将培养48~72 h的细胞用胰蛋白酶消化,加入DMEM培养液稀释成密度为(2.5×104)个/mL悬液,分为7组,将细胞悬液接种至3块96孔板中,每组每块板各6孔,每孔100 μL,将其放入CO2培养箱中培养24 h。弃去各96孔板中的原培养液,磷酸盐缓冲液清洗2遍,加入相应的浸提液100 μL,于第3、5天更换1次浸提液。3块96孔板分别培养1、3、5天后,弃去原培养液,每孔加入MTT溶液 20 μL,继续培养4 h。去除孔内液体,加入150 μL DMSO后,震荡10 min,在酶标仪490 nm波长下测定其吸光度,计算相对增殖率(RGR)。RGR=(吸光度平均值/空白对照组吸光度平均值)×100%。细胞毒性分级如表1。

图1 全内置式可膨胀型生物涂层脊柱前路内固定系统的外观照Fig.1 Appearance of the built⁃in expandable bio⁃coating anterior spinal fixation system

表1 细胞毒性分级Tab.1 Cytotoxicity grades
1.3.2 肌肉植入试验 SD大鼠12只,用3%戊巴比妥钠溶液进行腹腔注射麻醉后,俯卧固定,背部备皮、消毒。切开大鼠背部正中皮肤,钝性分离肌肉,在大鼠脊柱两侧约1 cm处各分离成1个肌腔隙,将1个被测内固定材料(高8 mm,直径3 mm圆柱体)植入右侧,左侧切开但不植入,作为空白对照组,生理盐水冲洗切口并逐层缝合。术后连续3 d肌注青霉素,观察大鼠活动及切口情况。分别于术后1、4、12、26周取材,每组3只。原切口切开,先行大体观察,再取包含材料的肌肉组织及对侧肌肉组织行切片固定,常规苏木精-伊红染色(HE染色),在光学显微镜下观察组织反应情况。按照GB/T16886.6⁃1997中的组织反应分级方法分级。见表2。
评定标准(阴性对照样品应符合此标准):植入7 d:炎症细胞反应程度≤Ⅳ级,囊壁形成0级;植入15 d:炎症细胞反应程度≤Ⅲ级,囊壁形成Ⅳ级;植入30 d:炎症细胞反应程度≤Ⅱ级,囊壁形成Ⅱ级;植入60 d:炎症细胞反应程度≤Ⅰ级,囊壁形成Ⅱ级;植入90 d:炎症细胞反应程度≤Ⅰ级,囊壁形成Ⅰ级;植入180、360 d:炎症细胞反应程度I级,囊壁形成Ⅰ级。
1.4 统计学方法 采用SPSS 20.0软件进行统计分析,组间比较采用方差分析,以P<0.05为差异有显著性。
2 结果
2.1 体外细胞毒性试验 光学显微镜下可见空白对照组、阴性对照组及各材料浸提液组的细胞形态正常,以长梭形或多角形为主,贴壁生长良好。阳性对照组细胞形态多呈圆形,明显可见细胞溶解,贴壁生长差。根据各组RCG值,各材料浸提液细胞毒性分级为0~1级之间,无明显细胞毒性,各材料浸提液组在1、3、5 d的RCG值两两比较,差异无统计学意义(P>0.05);各材料浸提液组在各个时间段的RCG值与空白对照组和阴性对照组比较,差异无统计学意义(P>0.05);而各材料浸提液组、空白对照组以及阴性对照组在各个时间段的RCG值与阳性对照组比较,差异有统计学意义(P<0.05)。见表3、图2。

表2 组织反应分级Tab.2 Tissue reaction grades
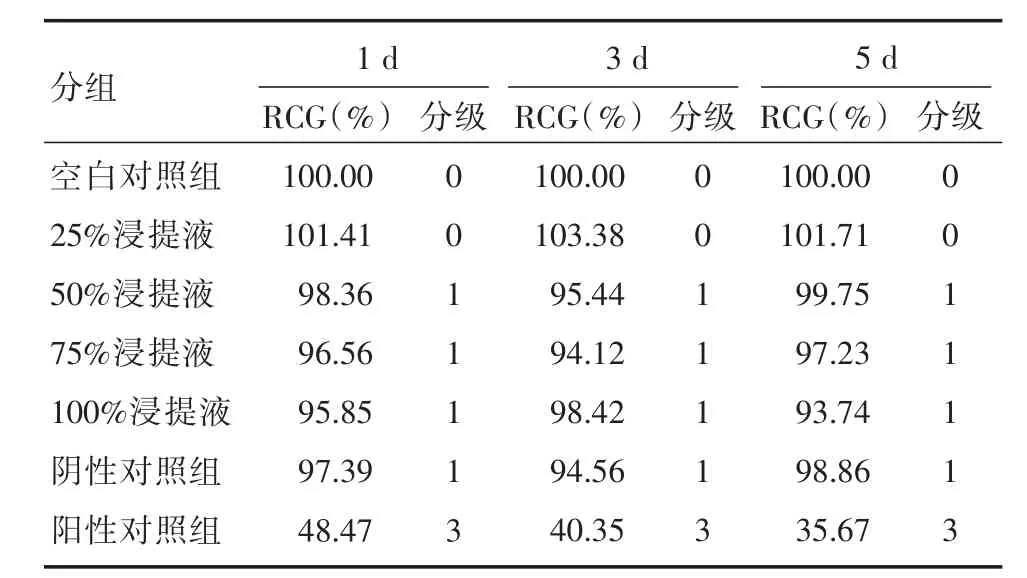
表3 各组RCG和细胞毒性分级Tab.3 RCG and cytotoxic grades of each group
2.2 肌肉植入试验 12只SD大鼠均正常存活至试验结束,切口一期愈合。术后1周,切口肿胀消退,材料与周围组织结合不紧密,未见炎性渗出或坏死组织,镜下观察可见材料周围组织有以中性粒细为主的炎症反应,无纤维囊形成,炎症细胞反应Ⅳ级,囊壁形成0级,对侧空白对照组肌肉切开部分与周围组织无明显差异,镜下亦可见炎性细胞浸润。术后4周,材料与周围组织结合稍紧密,镜下见炎性细胞明显减少,有成纤维细胞增殖,形成厚薄不一的纤维囊腔,炎症细胞反应Ⅱ级,囊壁形成Ⅱ级。术后12周,材料与周围组织结合紧密,镜下未见明显炎性细胞,材料周围形成完整较均一的纤维囊腔,炎症细胞反应Ⅰ级,囊壁形成Ⅰ级。术后26周,肌肉组织完全包裹植入材料,镜下未见炎症反应,纤维囊腔完整,炎症细胞反应Ⅰ级,囊壁形成Ⅰ级。术后4、12、26周空白对照组肌肉组织与周围组织无明显差异,镜下无明显炎性反应或囊腔形成(表4、图3)。
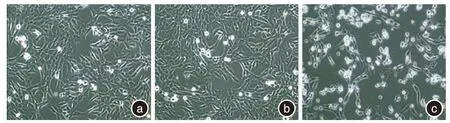
图2 各组细胞在细胞毒性试验中的光镜下观察结果Fig.2 The results of each groups in cell toxicity test

表4 各组组织反应分级Tab.4 Tissue reaction grades of each group
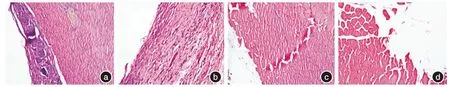
图3 被测材料植入大鼠肌肉后局部反应试验的光镜下观察结果(HE染色×100)Fig.3 The results of the local reaction test of rat muscle implantation(HE staining × 100)
3 讨论
全内置式可膨胀型生物涂层脊柱前路内固定系统由可膨胀的钉体、内芯、连接棒和螺帽组成,通过内芯的拧入,可实现钉体的膨胀[4]。在植入过程中,将螺钉及连接棒完全植入椎体及椎间隙中,实现该内固定系统的全内置,减少了钉棒对周围脏器、血管等组织的干扰。前期研究中,通过与Kaneda系统、Z⁃Plate系统的比较,发现三组内固定系统都可重建胸腰椎的即刻稳定性,具有良好的生物力学性能[5]。全内置式可膨胀型生物涂层脊柱前路内固定系统由钛合金基体及表面羟基磷灰石涂层组成,其中钛合金为钛铝合金。铝元素是人体的一种微量元素,如果体内残留过量的铝可引起阿尔兹海默病、骨软化症等疾病[6-7]。羟基磷灰石的化学成分与人体骨骼和牙齿中的矿物质组成相似度极高,是脊椎动物骨组织和牙齿重要的无机组成部分。羟基磷灰石在植入生物体后可与骨细胞在短期内形成化学键合,且具有诱导骨细胞长入涂层间隙的特点。另外,羟基磷灰石涂层还可抑制钛合金释放金属离子,是一种具有优良生物活性的医用材料[8-9]。然而,由于其机械强度不高、脆性大等特点限制了其在人体承重部位的应用[10]。本研究中的全内置式可膨胀型生物涂层脊柱前路内固定系统由钛合金和羟基磷灰石涂层组成,二者取长补短,既可发挥钛合金良好的机械性能的优势,又可发挥羟基磷灰石良好生物相容性的特点,有效提高了植入物的综合性能,且对成骨细胞、破骨细胞不具有毒性作用[7]。为进一步评价该内固定系统的生物相容性,本研究根据医疗器械生物学评价的相关标准来检测该内固定系统在细胞毒性和肌肉植入后局部反应方面的安全性。
体外细胞毒性试验是通过模拟细胞生存的环境,观察材料浸提液对细胞生长、代谢及增殖的影响,进而评价材料生物相容性的一种有效而快速的方法[11-12]。L929小鼠成纤维细胞具有增殖能力强、传代稳定、对生长环境敏感等特点,被美国质量标准协会推荐为体外细胞毒性试验中的标准细胞[13]。试验采用MTT比色法的原理在于MTT被活细胞内线粒体脱氢酶还原成蓝紫色甲臜结晶并沉积,DMSO可将其溶解成溶液,在酶标仪490 nm波长下测定其吸光度,甲臜结晶数量与存活细胞数成正比,因此可通过吸光度值反映细胞的生长情况[14-15]。本研究中,通过观察第1、3、5天各组细胞的形态和测定其吸光度值可发现,25%、50%、75%、100%四组不同浓度材料浸提液细胞形态正常,增殖良好,吸光度值在93.74%~103.38%之间,细胞毒性分级为0~1级,与空白对照组、阴性对照组无明显差异。而在各个时间点阳性对照组细胞形态大多呈圆形,贴壁生长较少,可见明显细胞溶解现象,其吸光度值在35.67%~48.47%之间,细胞毒性分级为3级。因此本研究中被测材料无细胞毒性。
植入后局部反应试验是将被测材料植入到活体动物某一部位组织内,通过在肉眼和显微镜观察水平上评价材料植入后周围组织局部反应的试验方法。本试验将被测的内固定材料植入大鼠背部脊柱旁一侧肌肉腔隙中,以对侧肌肉为空白组,通过植入术后1、4、12、26周术区肌肉的大体观察和显微镜下观察来评价被测材料的植入后局部反应。由试验结果我们可知,植入术后试验大鼠一般情况良好,未发生死亡、术区感染等不良并发症。术后1周,被测材料及空白对照周围肌肉组织可见大量炎性细胞浸润,考虑由材料局部刺激和术后应激反应引起。术后4、12、26周植入材料周围炎性细胞逐渐消失,且逐渐形成稳定的纤维包裹,而空白对照组肌肉组织与其周围肌肉组织在大体上和显微镜下观察未见明显异常。说明被测材料随着植入时间的延长,与周围肌肉组织趋于稳定状态。未发生坏死或炎症反应,提示被测材料对周围肌肉组织无毒性,植入后局部反应良好。
综上所述,全内置式可膨胀型生物涂层脊柱前路内固定系统无细胞毒性,植入后对周围肌肉组织无刺激反应。该内固定材料符合作为植入性的医用生物材料在体外细胞毒性试验、植入后局部反应试验的相关标准。

