STIC-HD live flow技术诊断胎儿完全性血管环的价值探讨
陈琳 周柳英 杨林华 舒娜 沈祥君 伍芸 程桂静 陈桦 刘凤琴
(成都市妇女儿童中心医院,四川 成都 610031)
完全性血管环[1](complete vascular ring,CVR)指主动脉弓及弓上分支发育异常,由未退化和(或)异常退化的血管组成的完全包绕气管食管的环形结构。CVR完全包绕气管食管,造成较明显呼吸吞咽困难,故产前明确诊断对孕期咨询及指导新生儿救治有重要意义。既往多采用二维联合彩色多普勒超声(two-dimensional and color doppler echocardiography,2D+Doppler)技术,通过三血管气管切面(three-vessel and trachea,3VT)发现环绕气管的“O”或“U”形血管环来诊断CVR,但因不能精确判断主动脉弓分支具体起源,不能直观反映主动脉弓上分支与气管立体空间位置关系,故而在对CVR进行精准分型上具有一定局限性[2,3]。随着三维超声的发展,运用时间-空间关联成像技术(spatio-temporal image correlation,STIC)的高分辨率仿真血流成像模式(High definition live flow,HD live flow),对心脏大血管及其内血流三维重建,直观立体显示主动脉弓及头臂分支、动脉导管空间位置关系。本研究将STIC-HD live flow技术应用于胎儿CVR的诊断,探讨其临床运用价值。
1 资料与方法
1.1 研究对象 2015年10月至2016年9月于成都市妇女儿童中心医院超声影像科经产前超声心动图检出及产后超声心动图和(或)CTA确诊的38例胎儿CVR。孕妇年龄23~40岁,平均年龄(27.0±3.6)岁,孕周23~30周,平均孕周(25.3±0.8)周。
1.2 仪器与方法
1.2.1 仪器 产前检查采用GE Voluson E10、E8彩色多普勒超声诊断仪,经腹机械凸阵三维容积探头RAB4-8D(频率4~8 MHz),仪器内配置STIC软件包,脱机分析软件采用4DView 7.0。
1.2.2 检查方法
1.2.2.1 2D+Doppler技术 ①中晚孕胎儿产科检查模式:判断胎方位、确定胎儿左右;行产科超声常规检查与测量;②胎儿心脏模式:运用Van praagh节段分析法扫查胎儿心脏各切面。
1.2.2.2 STIC-HD live flow技术容积数据采集 2D+Doppler检查于3VT切面见气管周围“O”或“U”形血管环,需确定CVR具体类型时,用STIC-HD live flow技术进行容积数据采集。①3VT和主动脉弓降部冠状切面为初始采集切面,选择高分辨血流成像,调节增益,使血流清晰显示;②选择四维STIC模式,取样框稍大于病变部位,容积扫描角度为30°~45°,采集时间约7~12秒,嘱孕妇屏气,启动STIC扫描,采集并存储三维容积数据。
1.2.2.3 STIC-HD live flow技术容积数据分析 正交三平面模式下调整A平面位置清晰显示感兴趣区域,依次切换至重建模式-彩色模式-HD live flow成像模式,旋转X、Y、Z轴线,清晰成像大动脉及分支血流。记录并存储图像资料。
1.3 验证与随访 继续妊娠者均于产后行新生儿超声心动图检查和(或)CT血管三维重建,并与产前2D+Doppler超声和STIC-HD live flow成像诊断结果对比。
2 结果
2.1 38例CVR具体分类及随访结果见表1。

表1 38例胎儿完全性血管环具体分类及随访结果
2.2 不同类型CVR 2D+Doppler超声心动图特征 正常3VT切面(图1)见:主肺动脉及动脉导管和主动脉弓均位于气管左侧,二者呈“V”形,共同汇入降主动脉(descending aorta,DAO)。右位主动脉弓(right aortic arch,RAA)伴左锁骨下动脉迷走(aberrant left subclavian artery,ALSA)、左位动脉导管(left ductus arteriosus,LDA) 3VT切面(图2、3)见:“U”形血管环形成;环的左支是位于气管左侧的动脉导管,右支是RAA,底部为与LDA相连的ALSA近端,以此为中心略侧动探头,可查见ALSA远端血管(其内血流与近端相反)。双主动脉弓(double aortic arch,DAA)3VT切面显见左右弓形成“O”形环;右弓优势型(图4)左弓较细小;左右弓平衡型(图5)则左右弓几乎等粗。镜面右位主动脉弓(mirror right aortic arch,MRAA)伴LDA(LDA-DAO)(图6)3VT切面见“U”形血管环形成;环左支及底部是动脉导管;右支是RAA;动脉导管位于气管左侧,连接DAO。
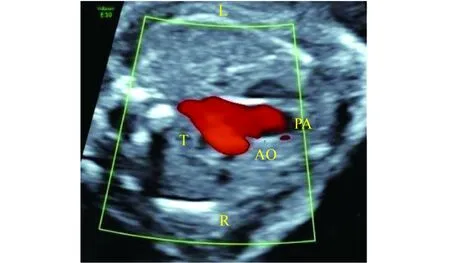
图1 正常三血管气管切面注:PA为肺动脉;AO为主动脉;T为气管
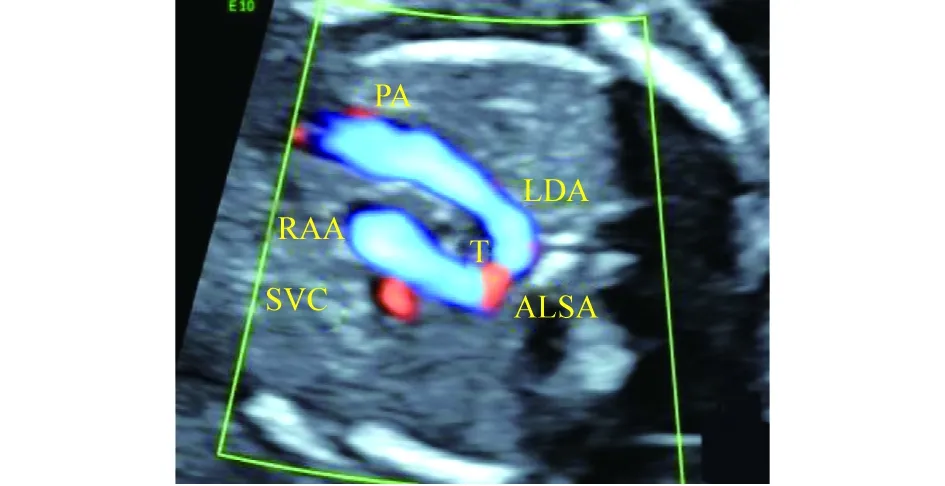
图2 三血管气管切面见“U”形血管环注:LDA为左位动脉导管;RAA为右弓;SVC为上腔静脉;ALSA为迷走左锁骨下动脉
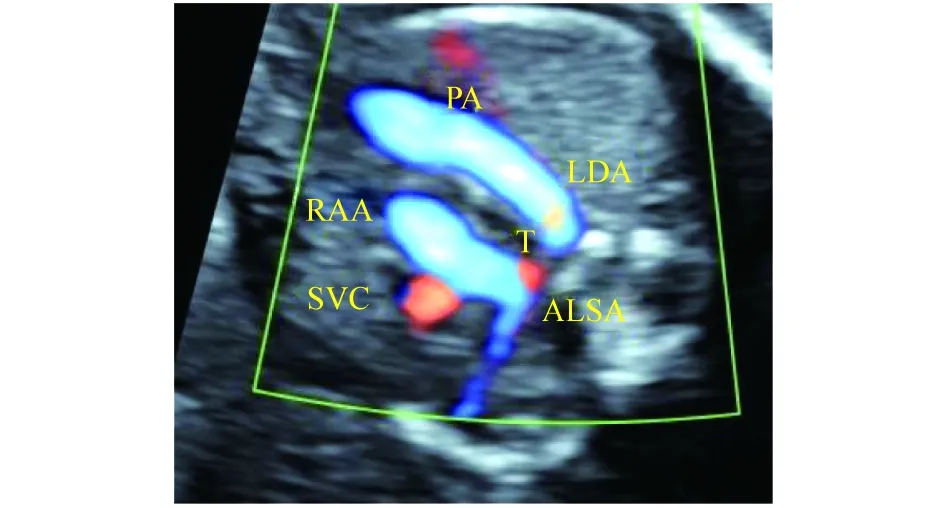
图3 以“迷走的左锁骨下动脉近端”为中心,略侧动探头,可追踪查见迷走的左锁骨下动脉远端(与近端血流方向相反)注:LDA为左位动脉导管;RAA为右弓;SVC为上腔静脉;ALSA为迷走左锁骨下动脉
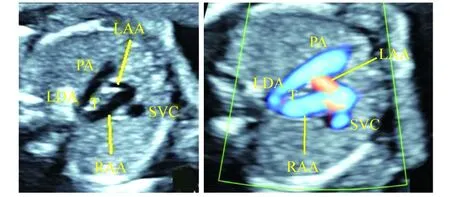
图4 双主动脉弓(右弓优势型)三血管气管切面二维(左图)和彩色多普勒图(右图),三血管气管切面见“O”形血管环;“O”形环左支为发育不良左弓近端和左位动脉导管,右支为右弓注:LAA为左弓
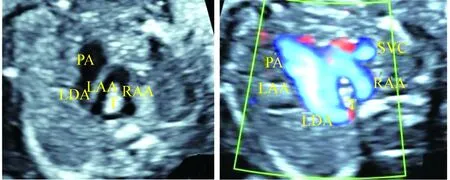
图5 双主动脉弓(左右弓均衡型)三血管气管切面二维(左图)和彩色多普勒图(右图),三血管气管切面见“O”形血管环;“O”形环左支为左弓,右支为右弓
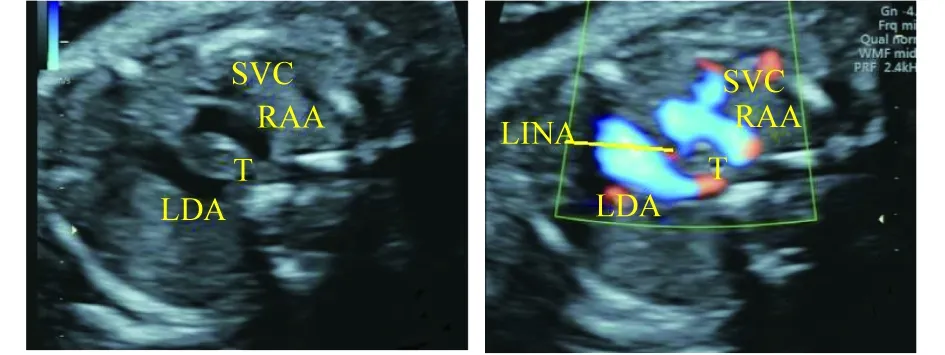
图6 镜面右位主动脉弓伴左位动脉导管(导管连接降主动脉)三血管气管切面二维和彩色多普勒图。三血管气管切面见“U”形血管环;“U”形环左支为主肺动脉和左位动脉导管,右支为右弓;右弓向左发出第一分支即左无名动脉注:LINA为左无名动脉
2.3 不同类型CVR STIC-HD live flow成像超声心动图特征 应用STIC-HD live flow技术38例CVR胎儿均获得满意的心脏容积数据。①RAA-ALSA-LDA的STIC-HD live flow技术成像(动态图1):主动脉弓上依次发出左颈总动脉(left common carotid artery,LCCA)、右颈总动脉(right common carotid artery,RCCA)及右锁骨下动脉(right subclavian artery,RSA),左锁骨下动脉(left subclavian artery,LSA)起源于DAO起始部且与LDA相连。②DAA:升主动脉分别分出左右弓,左弓发出LCCA、LSA,右弓发出RCCA、RSA后共同汇入DAO;右弓优势型(动态图2)见右弓较左弓相对粗大;左右弓平衡型(动态图3)见左右弓内径几乎相等。③MRAA-LDA(LDA-DAO)(动态图4):右弓上依次发出左无名动脉(left innominate artery,LINA)、RCA、RSA;LDA连接DAO。
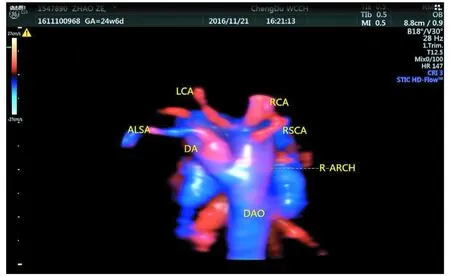
动态图1 胎儿右弓伴左锁骨下动脉迷走、左位动脉导管STIC+HD live flow成像图
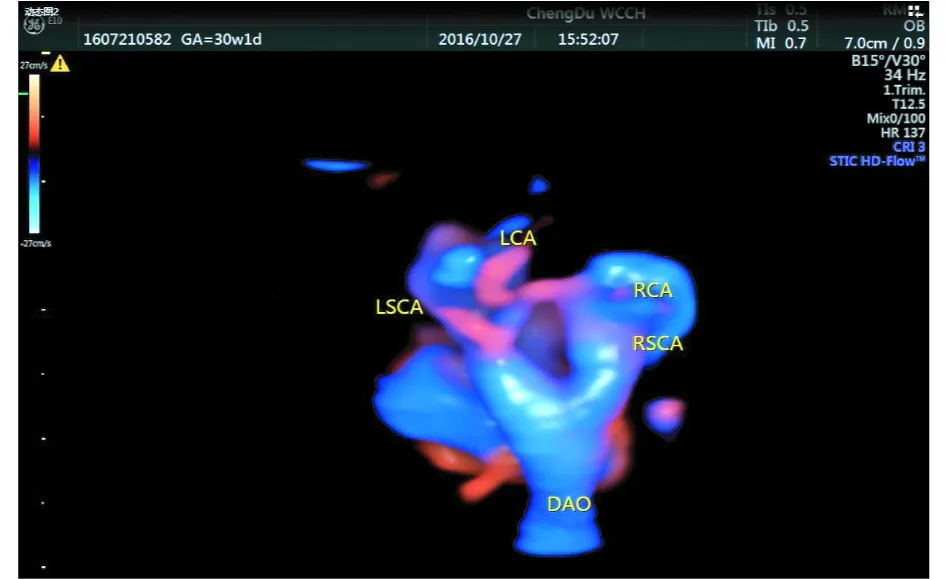
动态图2 胎儿双主动脉弓(右弓优势型)STIC+HD live flow成像图
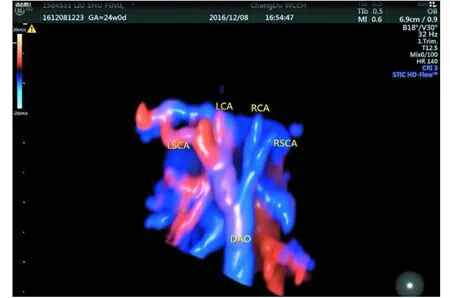
动态图3 胎儿双主动脉弓(左右弓平衡型)STIC+HD live flow成像图
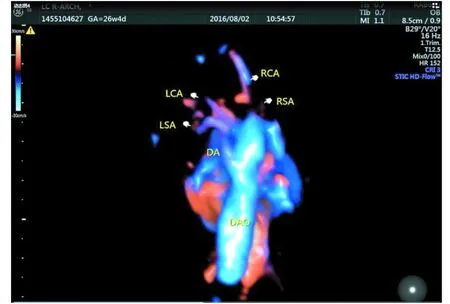
动态图4 胎儿镜面右弓伴左位动脉导管(导管连接降主动脉)STIC+HD live flow成像图
2.4 随访 本组38例CVR产后均行超声心动图和(或)CTA证实(图7~10)。其中1例产前2D+Doppler误诊为MRAA-LDA(LDA-DAO),STIC-HD live flow技术修正诊断为DAA(右弓优势型),该患儿因轻微气喘,于6个月时行手术矫治,术后情况良好;余患儿无明显症状,临床观察中。
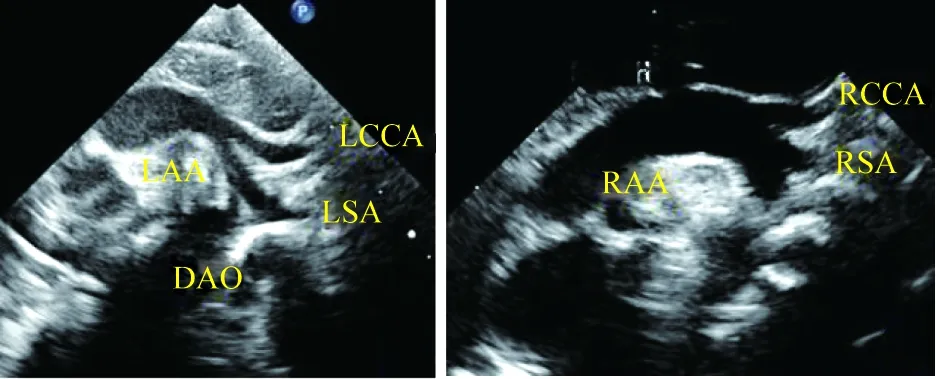
图7 双主动脉弓(右弓优势型)产后超声心动图;左图为细小左弓及弓上分支,右图为粗大右弓及弓上分支注:LCCA为左颈总动脉;LSA为左锁骨下动脉;RCCA为右颈总动脉;RSCA为右锁骨下动脉;DAO为降主动脉
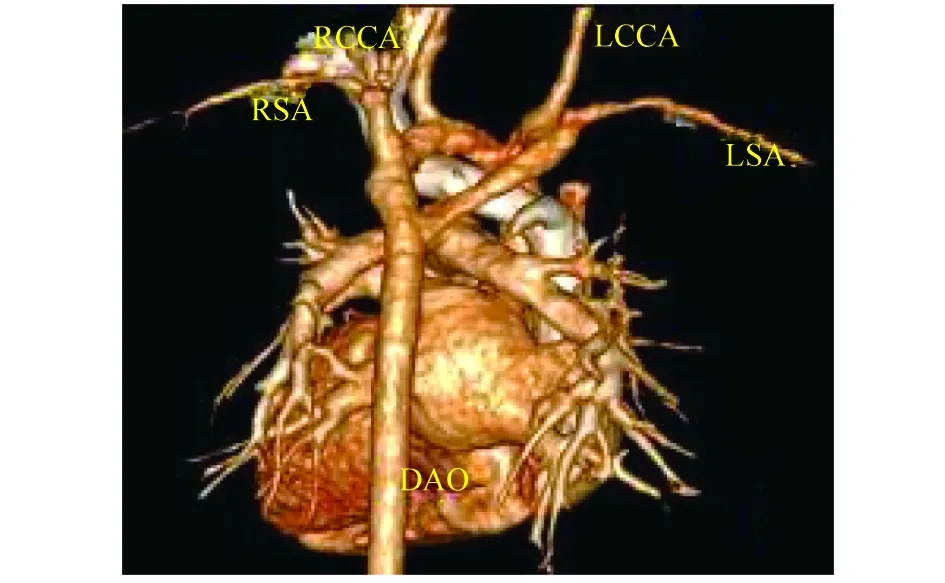
图8 双主动脉弓(右弓优势型)产后CT血管重建图
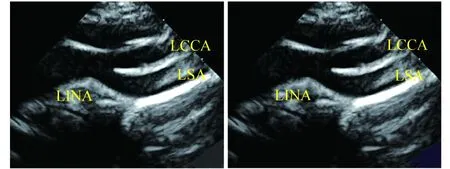
图9 镜面右位主动脉弓伴左位动脉导管(导管连接降主动脉)产后超声心动图;左图为主动脉弓发出向患儿左上方走行的第一分支,该分支再分出左颈总动脉和左锁骨下动脉;右图为粗大右弓及弓上第2、3分支
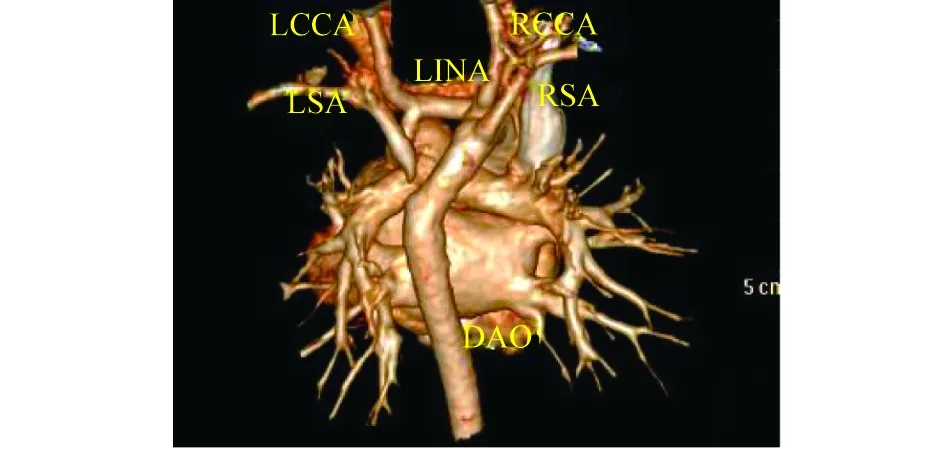
图10 镜面右位主动脉弓伴左位动脉导管(导管连接降主动脉)产后CT血管重建图
3 讨论
3.1 CVR胚胎学基础[4]Edward双主动脉弓假想模型指出胚胎4~7周内先后出现6对鳃动脉弓,第4对鳃动脉弓未退化或异常退化,形成完全包绕气管食管的血管环则为CVR。CVR常见类型包括RAA-ALSA-LDA(LDA-ALSA)、MRAA-LDA(LDA-DAO)和DAA。若LCCA与LSA间血管段和右导管退化,RAA和LDA存留,RAA上分支依次为LCCA、RCCA和RSA,LSA起源于DAO,LDA连接LSA,则形成RAA-ALSA-LDA(LDA-ALSA)。若左弓LSA远端血管段和右导管退化,RAA和LDA存留,弓上分支依次为LINA、RCCA和RSA,LDA连DAO,则形成MRAA-LDA(LDA-DAO)。若双侧第4鳃动脉弓和LDA均存留,右导管退化,左右弓上分别发出各自的颈总动脉和锁骨下动脉,则形成DAA。
3.2 2D+Dopple技术及STIC-HD live flow技术对CVR诊断价值对比 1例2D+Doppler产前误诊为MRAA-LDA(LDA-DAO),STIC-HD live flow修正诊断为DAA(右弓优势型),产后随访证实。分析误诊原因:DAA(右弓优势型)由于左弓发育不良,尤其左弓发出LSA后至汇入DAO间这段血管极度细小且走行迂曲,2D+Doppler因扫查切面、取样角度和血流速度等限制对“该段血管”检出率不高,故将DAA误诊为MRAA-LDA(LDA-DAO)[5]。产前超声鉴别二者的关键在于准确判断LSA与DAO间是否存在血管。在检出该段发育不良血管敏感性上,STIC-HD live flow技术较之于2D+Doppler具有明显优势。
3.3 STIC-HD live flow技术在胎儿CVR诊断中的应用价值分析 STIC技术是一种特殊的四维采集技术,可以对灰阶及血流(如彩色多普勒、能量多普勒、高分辨率血流等)进行容积数据采集。STIC包括多种显示模式,如Render立体渲染模式、自由剖面模式、X线断层超声波成像模式、容积分析模式等。操作者可以根据不同的研究目的对灰阶或者血流进行容积数据采集,然后对感兴趣区域运用不同成像模式进行重点成像分析,从而实现对心脏解剖结构、心脏大血管内血流的显示和先心病的诊断[6,7]。HD live flow成像[8]是基于高分辨血流能量多普勒原理,新开发的一种Render立体渲染模式下的新的四维成像模式,即高分辨仿真血流成像模式,对低速血流极其敏感,且以立体动态显示血管形态及其内血流,直观立体显示各血管空间位置关系。本研究运用STIC-HD live flow成像提高发育不良段血管的检出率,直观立体地呈现主动脉弓及弓上分支、动脉导管的空间位置关系,从而对胎儿CVR进行准确分型。本组病例中,1例2D-Doppler诊断为MRAA-LDA(LDA-DAO),以3VT和主动脉弓降部冠状切面为初始切面,运用STIC-HD live flow技术成像发现左弓发出LCCA、LSA后迂曲走行一段仍汇入DAO,该技术直观立体显示升主动脉分出左右弓,两弓分别发出各自颈总动脉和锁骨下动脉后共同汇入DAO的空间关系,故STIC-HD live flow技术修正诊断为DAA(右弓优势型)。由此可见,STIC-HD live flow技术在明确CVR具体类型具有重大价值。
总结STIC-HD live flow技术操作关键:①选择最佳容积数据采集初始平面。胎儿CVR最佳初始切面为3VT和主动脉弓降部冠状切面,因为该切面包涵气管两侧主动脉弓及弓上分支、动脉导管等重要血管信息。②容积数据采集时使主动脉弓、导管与声束尽量平行,使其内血流清晰显示等;③因STIC-HD live flow技术是获取容积数据的图像后处理技术,要求操作者熟练掌握软件操作技巧,熟悉胎儿心脏解剖结构,具有一定空间想象能力,从而能对心脏大血管立体空间关系做出正确的判断,对后期数据进行准确旋转切割。
综上所述,STIC-HD live flow成像技术在识别和追踪细小、低速血流血管具有明显优势;能直观立体显示主动脉弓及头臂分支、动脉导管等血管空间位置关系,从而提高胎儿CVR产前超声检出率并准确分型。STIC-HD live flow成像技术将成为2D+Doppler超声诊断的有力补充,为胎儿心脏及大血管立体重建提供新的方法和手段。
参考文献
[1] 接连利.胎儿心脏病理解剖与超声诊断[M].北京:人民卫生出版社,2010:260-265.
[2] 李胜利,文华轩.胎儿超声断层解剖模式图设计与应用:胎儿三血管切面及三血管气管切面异常表现[J/CD].中华医学超声杂志(电子版),2010,7(6):948-966.
[3] 张烨,何怡华,孙琳,等.胎儿孤立完全性血管环常见类型产前超声诊断研究[J/CD].中华医学超声杂志(电子版),2016,13(8):577-581.
[4] 李胜利,文华轩,罗丹丹.胎儿主动脉弓及其分支异常分型的再认识(连载一)[J/CD].中华医学超声杂志(电子版),2017,14(5):31-333.
[5] 锁仁静,李亮,穆仲平,等.时间-空间关联成像联合高分辨率血流成像诊断胎儿双主动脉弓畸形[J].中国超声医学杂志,2016,32(5):560-563.
[6] 应倩,伍育蓉,孙锟.时间-空间相关成像技术在胎儿心脏检测中的应用[J/CD].中华医学超声杂志(电子版),2016,13(9):711-714.
[7] 郭爽,张志坤.HD live技术在单绒毛膜性双胎妊娠中的诊断价值[J/CD].中国产前诊断杂志(电子版),2017,9(1):42-45.
[8] Hata T, Hanaoka U, Tenkumo C, et al. Three-and four-dimensional HD live rendering images of normal and abnormal fetuses:pictorial essay[J].Arch Gynecol Obstet,2012,286:1431-1435.

