拨开云雾见明月——化学实验题中相关计算的复习
湖北
刘利娟
一、设计思路
近年来,高考化学计算常常与化学实验、元素化合物知识、化学平衡移动等结合进行考查,特别是与难度较大的化学工业流程题结合以后,具有数据多、关系复杂、综合性强的特点,学生感到无从下笔,也是学生们在测试和考试中最难得分的一类题。高考化学计算题注重对知识的理解和应用的考查,注重对计算思路和计算方法的考查,削减了数学计算的容量,恢复了化学计算的本质。若能选择合适的方法准确快速地解决化学实验题中的计算问题,不但可以缩短解题的时间,还有助于减小计算过程的出错率,对于提高学习成绩,增强学习效率,有着重要意义。
二、考情分析
纵观近几年的高考试题,不难发现命题者更加重视对化学计算的考查,特别是对实验题中计算的考查。化学实验题中的计算题题型主要集中在以下三个方面:
1.测定样品中某物质质量分数或浓度;
2.计算产品的产率或回收率;
3.确定物质的化学式。
题型一般为非选择题,分值为2~4分。以下是近三年高考对化学实验题中计算的考查。

核心考查内容考点集锦纯度、质量分数的计算(2017·全国Ⅰ·26题)用凯氏定氮法测某甘氨酸(C2H5NO2)样品中氮的质量分数及样品纯度(2017·全国Ⅱ·26题)结合滴定法计算水泥样品中钙的质量分数(2017·北京·27题)尿素溶液中溶质的质量分数的测定(2016·浙江·29题)结合滴定实验所测数据计算无水MgBr2产品的纯度(2015·全国Ⅰ·36题)结合滴定实验所测数据计算样品中CuCl的质量分数(2015·浙江·29题)通过滴定实验计算海带中碘的百分含量(2015·上海·36题)产品中CaO2的质量分数计算

续表
三、学情分析
在化学《必修1》中学生已经学过了化学计量在实验中的应用等相关知识,也了解与物质的量计算相关公式,但是教材中涉及的知识较简单,实验流程简单,计算题较单一。而高考题中涉及的化学计算通常结合了元素化合物知识、氧化还原反应原理、酸碱中和滴定等多方面的知识,有些学生的思绪较杂乱,不知道该如何分析,无法将已知量与未知量联系起来。因此,在遇到此类习题时常常选择放弃。
四、教学方法
自主学习方法 讨论法 教师引导讲授法 练习法 归纳法
五、实验用品及教学设备
多媒体投影教学 导学案
六、教学过程
微点聚焦一 简化过程 妙用守恒
所谓“守恒”就是物质在发生变化或两种物质发生相互作用的过程中某些物理量的总量保持“不变”。一切化学反应都遵循守恒定律,在化学变化中有着各种各样的守恒,如质量守恒、元素原子守恒、得失电子守恒、电荷守恒、能量守恒等。
(一)由“元素守恒”确定关系式
1.在O2中灼烧0.44 g S和Fe组成的化合物,使其中的S全部转变为SO2,把这些SO2全部氧化转变为H2SO4。这些H2SO4可以用20 mL 0.50 mol·L-1NaOH溶液完全中和。则原化合物中S的百分含量为
( )
A.18% B.46%
C.53% D.36%
【答案】D
【解析】明确S~SO2~SO3~H2SO4中硫元素守恒,根据酸碱中和求出与NaOH的关系。
全部反应过程中,各物质的量的关系可用下式表示:
S~SO2~SO3~H2SO4~ 2NaOH
32 g 2 mol
x(0.02×0.50)mol
(二)由“电子守恒”确定关系式
2.将4.9 g Mg和Fe的混合物在过量稀HNO3中完全反应,得到标准状况下NO气体2.24 L,向反应后的溶液中加入足量烧碱溶液充分反应,求最后生成沉淀的质量。
【答案】10 g
【解析】由题意知,整个过程中存在关系:
Fe~3e-~3OH-~Fe(OH)3
Mg~2e-~2OH-~Mg(OH)2
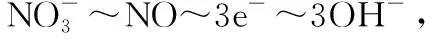
【解题模板】



微点聚焦二 解题捷径 关系式法
关系式法是表示两种或者多种物质之间“物质的量”关系的一种简化式子。在多步反应中,它可以把始态反应物与终态生成物之间物质的量关系表示出来,把多步计算简化为一步计算。正确书写关系式是关系式法解化学计算题的前提。
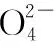
【答案】本题涉及的化学方程式或离子方程式为

5 2
n1(CaCO3)
aV2×10-3mol
n1(CaCO3)=2.5aV2×10-3mol

【解题模板】
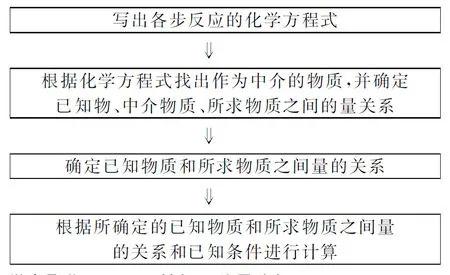
微点聚焦三 巧思妙解 差量分析
差量法的实质是算出反应体系中某些化学量从始态到终态的差量,以此作为解题的突破口。按照差量的性质来说,差量可以是质量差、体积差、物质的量的差值、压强差等。从任何一个化学反应中,均可以找到一个或多个有关量的差值,因此运用此法解题时,必须仔细分析题意,理清思路,选好相关物理量的差值,根据题意确定理论差值,再根据题目提供的实际差值,列出比例式,然后求解。
(一)确定含量


(二)确定组成
5.CuSO4·5H2O样品0.80 g受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。
试确定200 ℃时固体物质的化学式(要求写出推断过程)。


250 18n
0.80 g 0.80 g-0.57 g=0.23 g

【解题模板】


