射波刀准直器选择对原发性三*叉神经痛治疗计划影响的评估
徐 伟 解传滨 鞠忠建 戴相昆 李纪伟 葛瑞刚 王小深 徐寿平 曲宝林 潘隆盛
三叉神经痛(trigeminal neuralgia,TN)根据病因可分为原发性和继发性,由多发性硬化、中后颅窝占位病变、神经节或神经根疾病等引起者称为继发性TN;不明原因的一般称为原发性TN。发病原因一般认为是多种因素引起三叉神经根部受压,使局部神经发生脱髓鞘变化,导致神经兴奋性提高和传导异常,包括外源性冲动放电,自发或激发的后放电以及邻近传入神经的交叉兴奋等,从而产生同步化的后放电位而引起疼痛发作。NT的治疗比较棘手,治疗方式主要有药物、射频热凝、半月节球囊压迫、微血管减压手术和立体定向放射外科[1-4]。放射外科治疗NT已有50多年历史,伽玛刀因其精度高、聚焦准确及疗效好成为顽固性TN患者的首选治疗方式[5-7]。
2002年5月斯坦福(Stanford)大学开始用射波刀(cyber knife,CK)治疗TN获得成功,并取得满意的疗效[8-11]。CK与γ刀相比,在固定方式、实时位置验证、影像引导、治疗时间、正常组织保护等方面具有明显的技术优势。特别是对于TN这种长条形靶区,其优势愈加明显,剂量包绕靶区更紧密,适形度更高。而作为专用的立体定向放射治疗设备,CK通过5~60 mm不同直径大小的圆形准直器,以非共面照射方式实现对靶区的聚焦照射。因此不同的准直器计划方案势必影响计划的质量,本研究在解放军总医院应用CK治疗TN计划设计经验基础上,分析比较不同准直器选择对TN治疗计划剂量学的影响,以期为最优准直器的选择提供参考。
1 材料与方法
1.1 患者资料
选取2016年5月至2017年5月解放军总医院收治的21例TN患者,其中男性7例,女性14例;年龄44~81岁,平均年龄66.5岁;患病部位右侧14例,左侧7例。本研究只利用患者图像资料进行靶区勾画以及治疗计划设计,并进行剂量学比较,不进行临床治疗。
1.2 仪器设备
采用大孔径CT模拟定位机(德国西门子);核磁定位扫描采用GE-750W核磁定位机(美国General Electric Company);图像融合与靶区勾画采用MIM系统(美国MIM Software);计划设计采用Multiplan计划系统(美国Accuray);患者治疗采用机器人立体定向放射外科系统(CyberKnife,美国Accuray)。
1.3 模拟定位及靶区勾画
采用头肩一体板配合热塑头肩膜对患者体位进行固定。分别进行CT模拟定位扫描与核磁定位扫描,扫描层厚均为1 mm。将CT平扫图像与核磁增强图像通过医学数字成像及通信(digital imaging and communication of medicine,DICOM)网络传输到医学影像处理软件(MIM software,MIM)系统并行图像融合。以MRI为基准,将三叉神经根入桥脑段勾画为肿瘤体积(gross tumor volume,GTV),体积范围76~211 mm3,GTV外扩1.6 mm定义为计划靶区(planning target volume,PTV)。测量每例患者PTV横断面最大径及PTV边缘距离脑干最短距离,处方剂量为64 Gy/1F,见表1。
1.4 计划设计
计划设计采用非等中心投照模式,分别设计5 mm准直器、7.5 mm准直器以及5 mm联合7.5 mm双准直器3组计划,并分别定义为C5组、C7.5组及C5联合C7.5组。正常组织限量参照美国医学物理学家协会(AAPM)TG101报告,要求脑干最大受照剂量(Dmax)<15 Gy,容积剂量参数(V10)<0.5 ml。因处方剂量高、且靶区距离敏感器官较近,正常组织与靶区难以兼顾,治疗计划设计要求满足正常组织剂量限制的前提下,尽可能提升靶区覆盖率。考虑计划的临床实施效率,将总机器跳数设置为50000 MU,以控制治疗时间。

表1 病例及靶区情况
1.5 计划评估
将靶区处方剂量覆盖度(GTV-V64、PTV-V64、GTV-Dmean)、PTV新适形指数(PTV-nCI),其中Vprescription表示处方剂量线所包含的组织的体积,Vt,prescription表示处方剂量线所包含的靶区体积,Vt表示靶区体积。通过机器跳数和计划实施时间评估各计划的实施效率。
应用Multiplan计划系统autoshell功能分别在靶区外缘3 mm、1 cm、2 cm、3 cm、4 cm和5 cm处生成剂量限制壳(Shell),统计各Shell的平均剂量,以此为标准对3组靶区外剂量跌落能力进行评价分析。通过靶区体积、脑干位置与准直器选择的相关性分析为最佳准直器选择提供依据。
1.6 统计学方法
采用SPSS 22统计软件进行数据分析。使用单因素分析方法,事后多重比较LSD-t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 靶区剂量评估
通过对3组计划的PTV处方剂量覆盖率进行分析发现,C5联合C7.5组略高于C5组,但两组差异无统计学意义(F=17.811,P>0.05);C7.5组结果最差,相较于其他两组计划差异均具有统计学意义(F=17.811,P<0.05)。而在GTV处方剂量覆盖率方面,C5联合C7.5组与C5组结果相近,且均优于C7.5组;GTV平均剂量GTV-Dmean以C5联合C7.5组、C5组及C7.5组的顺序递减,且差异均具有统计学意义(F=15.068,P<0.05)。
(1)靶区适形指数方面,C5组明显优于C7.5组,且差异具有统计学意义(F=4.604,P<0.05)。而C5联合C7.5组与C5组比较,差异无统计学差异(F=4.604,P>0.05)。
(2)治疗时间方面,C5联合C7.5组优于C5组,劣于C7.5组,其差异具有统计学意义(F=152.315,P<0.05)。
(3)计划实施效率方面,C5组治疗时间最长,为78.57 min,MU最多,为47933,见表2。
2.2 靶区体积与准直器选择相关性分析
在PTV体积位于190~460(mm3)范围内,对各计划组靶区处方剂量覆盖度进行分析发现,C7.5组PTV覆盖率相对较差,随着靶区体积的变化波动较大,且无明显趋势。当PTV体积较小时(VPTV<310 mm3)C5组与C5联合C7.5组PTV覆盖率无明显差异,但随着靶区体积的增大,C5联合C7.5组的优势逐渐突出,如图1所示。

图1 不同准直器组靶区覆盖率与靶区体积的关系图
2.3 脑干位置与准直器选择相关性分析
在靶区距离脑干最短距离1.41~3.03 mm内,对3组靶区处方剂量覆盖度进行分析比较发现,靶区距离脑干最短距离为1.41~3.03 mm,3组治疗计划靶区覆盖率随着靶区距离脑干最短距离的增加,呈现出逐渐升高的趋势。且C7.5组结果随着距离的增加,与其他两组的结果越来越接近。而C5联合C7.5组在研究对象范围内,结果一直最优,如图2所示。
2.4 靶区外剂量跌落情况分析
通过对靶区外不同厚度的Shell平均剂量分析比较发现,在距离靶区较近(3 mm~1 cm)范围内,C5组平均剂量更低,在靶区远端(≥3 cm),C7.5组平均剂量更低,而C5联合C7.5组介于其两者之间,见表3。
表2 不同准直器治疗计划组统计结果
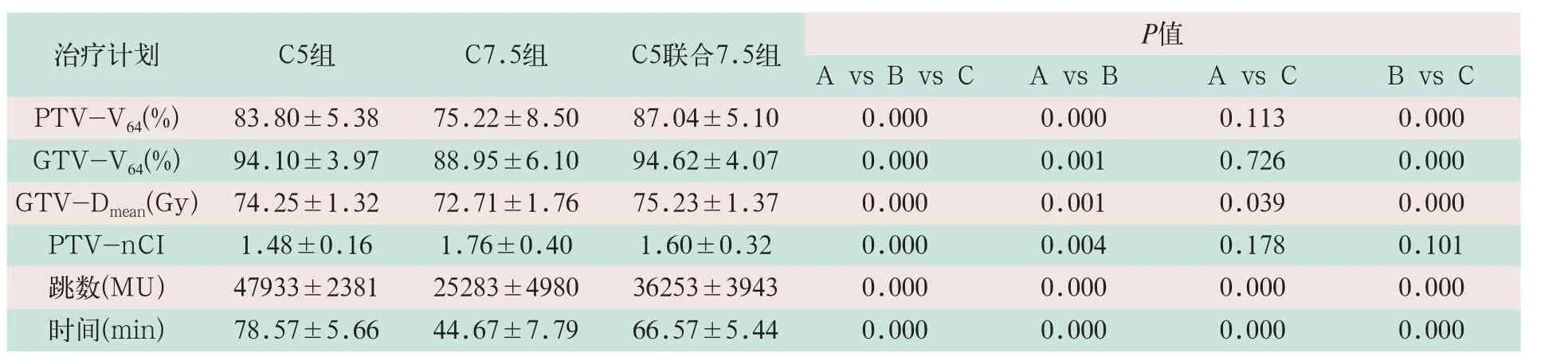
表2 不同准直器治疗计划组统计结果
治疗计划 C5组 C7.5组 C5联合7.5组 P值A vs B vs C A vs B A vs C B vs C PTV-V64(%) 83.80±5.38 75.22±8.50 87.04±5.10 0.000 0.000 0.113 0.000 GTV-V64(%) 94.10±3.97 88.95±6.10 94.62±4.07 0.000 0.001 0.726 0.000 GTV-Dmean(Gy) 74.25±1.32 72.71±1.76 75.23±1.37 0.000 0.001 0.039 0.000 PTV-nCI 1.48±0.16 1.76±0.40 1.60±0.32 0.000 0.004 0.178 0.101跳数(MU) 47933±2381 25283±4980 36253±3943 0.000 0.000 0.000 0.000时间(min) 78.57±5.66 44.67±7.79 66.57±5.44 0.000 0.000 0.000 0.000

表3 不同准直器计划与靶区外剂量跌落关系
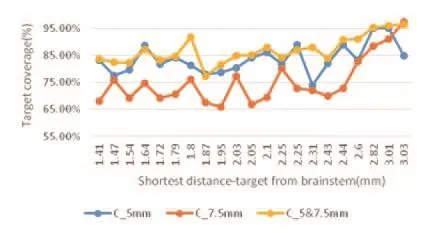
图2 不同准直器组靶区覆盖率与靶区距脑干最短距离的关系图
3 讨论
立体定向放射外科作为TN治疗方法之一,在临床上取得了较好的疗效。Kondziolka等[12]报道了应用γ刀照射三叉神经根部治疗TN的方法,经美国、法国5个单位50例临床试验确立了其有效性[13]。但由于其固定方式采用有创式金属头架,受源活度的影响其治疗时间多在1.5~2.5 h之间。CK的应用开创了立体定向放射外科以图像引导及实时验证取代有创式固定支架的新模式,在提高了治疗的精确度的同时极大改善了患者舒适度,并且其治疗时间缩短至1 h以内,对于高剂量小靶区的TN治疗带来了新的突破。
自2002年CK被用于治疗TN以来,国外已有多家医院开展此医疗技术,包括斯坦福大学医学中心、梅奥临床医学院等,而国内仅有两家医院报道开展此类临床试验[14-17]。整体病例数偏少,且其靶区定义依然延续伽马刀治疗技术,即球形规则靶区,未发挥出CK的技术优势,即其可治疗长条形非规则靶区。Villavicencio等[18]报道了CK治疗TN的多中心研究,发现增加照射的神经长度可以降低其疼痛复发率。解放军总医院自2016年开始应用CK治疗TN患者,已完成46例,其随访结果将在后续的研究中报道。
对于CK治疗TN准直器的选择问题,早前的报道证明了5 mm准直器是CK治疗TN的最佳选择[18]。而本研究中统计所得PTV体积大于其报道的数据,靶区中位体积为0.32 cm3,比之前的研究大8倍[18-19]。因此,为了实现处方剂量对靶区体积的有效覆盖,增加更大尺寸的准直器很有必要。分析发现,7.5 mm准直器能够提升治疗效率,5 mm准直器可有效保障靶区的适形度,两个准直器配合使用则可以在尽可能不牺牲靶区覆盖率的前提下,提升了治疗效率。印度学者Sudahar等[20]做了一项研究,通过对比发现,5 mm、5 mm和7.5 mm联合及7.5 mm准直器3组计划的靶区覆盖结果相似,但对于脑干的保护方面5 mm准直器更具有优势,5 mm联合7.5 mm组稍差于5 mm单准直器组,7.5 mm准直器较难实现对正常组织的有效保护,不推荐用于临床。但报道中未对靶区情况和计划设计原则进行详细描述,而且计划结果中脑干受量未满足TG101报告剂量限制要求。有报道证明了脑干的受照剂量与术后麻木的发生率直接相关[18]。因此,本研究在计划设计中严格按照TG101报告限制正常组织受量,在满足脑干(Dmax<15 Gy,V10<0.5 ml)的前提下尽可能提高靶区处方剂量的覆盖度。考虑TN靶区体积相对较小,距离敏感正常组织较近,其与正常组织相对位置关系势必对研究产生较大影响,因此对靶区体积、脑干位置与不同准直器选择的相关性进行了研究分析,其结果显示,对于TN靶区体积范围,C5组与C5联合C7.5组明显优于C7.5组,且在PTV体积较小时(VPTV<0.31 cc)C5与C5联合C7.5组PTV处方剂量覆盖率无明显差异,但随着靶区体积的增大,C5联合C7.5组的优势逐渐突出。同时3组治疗计划靶区覆盖率随着靶区距离脑干最短距离的增加,呈现出逐渐升高的趋势,且C5联合C7.5组在各距离范围内具有明显的优势。
一项关于CK治疗精度的报道[21]显示,当扫描层厚为1.25 mm时,治疗精度为(1.0±0.3)mm;另一项研究显示,使用CK治疗脑部肿瘤时,CTV与PTV之间的距离应该设定为2 mm[22]。而对于CK治疗TN的大量文献报报道显示,处方剂量都直接给予了GTV,并未考虑CK治疗精度的问题[8-13]。本研究基于本单位CK治疗的临床经验,在GTV的基础上外扩1.6 mm作为计划靶区。靶区中位处方剂量为64 Gy,80%的等剂量线作为处方剂量,这意味着Dmax接近或>80 Gy,与大多数相关研究结果一致[8-13]。此前Peddada等[23]在关于CK治疗TN医疗事故的文献中报道了1例采用SAD=65 cm的等中心照射技术对相对规则的靶区进行照射,由于CK等中心照射时无法进行逆向优化,只能通过前期设置单个射束最大跳数及单个节点最大跳数来限制靶区外高剂量,而在计划的实际设计中未对每个节点的最大MU进行限制,最终导致了患者在上唇、硬腭和舌头上出现了局灶性黏膜炎。事故分析后,研究者推荐每个射束的最大跳数应限制为150~180 MU,且每个节点的最大跳数限制为4倍的射束限制条件,以避免此类不良事件的发生。而本研究所采用的治疗技术为非等中心逆向调强治疗技术,由于治疗技术及照射靶区体积的不同,适当放宽了单个射束及单个节点的跳数限制值,跳数被设定为每个节点1200 MU,每射束600 MU。但治疗计划逆向优化中应用了严格的剂量限制条件,以避免在靶区以外的热点。
本研究针对同病例不同准直器计划设计的剂量学差异进行了分析,而对于各计划组的计划剂量验证以及患者临床治疗的随访将作为下一步研究的重点。
依照本研究对TN靶区的定义,在实施CK治疗时,5 mm联合7.5 mm双准直器计划既可以在保证正常组织剂量限制的前提下得到更为理想的靶区剂量分布,又可以保证计划实施的相对高效,可为CK治疗TN最佳准直器选择。

