决明子及炒决明子HPLC化学指纹特征及6种成分的比较研究
邹 妍,鄢海燕
(1.云南大学化学科学与工程学院,昆明 650091;2.皖南医学院药学院,安徽芜湖 241002)
决明子是豆科植物决明Cassia obtusifolia L.或小决明Cassia tora L.的干燥成熟种子,有清热明目、润肠通便的功效〔1〕,最初记载于《神农本草经》〔2〕。蒽醌类成分是其主要的活性成分,含量较高。大黄素、大黄酚、大黄酸、大黄素甲醚及橙黄决明素等在国内外研究较多,且都有明显的药理活性〔3〕。《中华人民共和国药典》(2015年版)对决明子和炒决明子以稀盐酸水解后,以大黄酚和橙黄决明素作为决明子及炒决明子化学质量控制的指标性成分〔1〕。仅以一个或两个指标成分进行质量控制不能全面地反映决明子药材的内在含量,特别是水解处理后决明子及炒决明子中的苷类成分均水解为苷元,无法充分反映决明子及炒决明子的内在化学成分的差异〔4-5〕。为此,本研究采用高效液相色谱法建立12批决明子及炒决明子未水解的化学指纹图谱并对决明子及炒决明子中橙黄决明素、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚6种成分进行定量分析,以期深入研究决明子炒制前后指纹特征、化学成分的变化,为进一步提高决明子炮制工艺及质量评价提供科学依据。
1 材料
1.1 仪器 岛津LC-20AD高效液相色谱仪(含LC-20A真空在线脱气机,LC-20AT四元泵,CTO-10AS柱温箱,SPD-M20A检测器);FA2004型电子天平(上海越平科学仪器有限公司)。
1.2 试剂 橙黄决明素(成都普菲德生物技术有限公司,批号:17032405,含量≥98%),芦荟大黄素(中药固体制剂制造技术国家工程研究中心,批号:L07-140210,含量≥98%),大黄酸(中药固体制剂制造技术国家工程研究中心,批号:D05-140210,含量≥98%),大黄素(成都普菲德生物技术有限公司,批号:17032204,含量≥98%),大黄酚(中药固体制剂制造技术国家工程研究中心,批号:D02-140210,含量≥98%),大黄素甲醚(中药固体制剂制造技术国家工程研究中心,批号:D04-140210,含量≥98%)。12批决明子的药材来源见表1。经皖南医学院药学院邹纯才副教授鉴定为豆科植物小决明(Cassia tora L.)的干燥成熟种子。炒决明子为实验室参照《中华人民共和国药典》(2015年版)〔1〕自制,即:取决明子,照清炒法〔6〕炒至微鼓起、有香气。

表1 药材来源
2 方法
2.1 溶液制备
2.1.1 对照品溶液 分别取橙黄决明素、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚对照品适量,以甲醇溶解,配置质量浓度分别为96、176、112、168、148、108 μg∕mL的对照品溶液。
2.1.2 样品溶液的制备 决明子及炒决明子粉碎,过40目筛,各取1 g,精密称定,分别加100 mL二氯甲烷回流80 min,所得二氯甲烷层回收溶剂后,分别以甲醇定容于25 mL容量瓶中,得0.04 g∕mL(每mL含原药材0.04 g)的溶液,0.22 μm微孔滤膜过滤,备用。
2.2 色谱条件 色谱柱为YMC-Pack ODS-A C18(250 mm×4.6 mm,5 μm),以乙腈为流动相A,0.1%磷酸溶液为流动相B,梯度洗脱(流动相A:0~15 min,35%→35%;15~18 min,35%→32%;18~23 min,32%→32%;23~25 min,32%→35%;25~45 min,35%→50%;45~63 min,50%→55%;63~85 min,55%→55%;85~100 min,55%→90%),流速为1.0 mL∕min;柱温25 ℃;DAD检测器,检测波长287 nm,进样量10 μL。
2.3 相似度计算 采用国家药典委员会《中药色谱指纹图谱相似度评价系统》(2012.130723版本)进行多点校正、Mark峰及全谱峰匹配、生成对照图谱并进行相似度计算。
2.4 统计学处理 实验数据以均数±标准差(xˉ±s)表示,用SPSS 11.5软件进行统计学处理。两组间比较采用独立样本t检验,P<0.05为差异有统计学意义。
3 结果
3.1 决明子及炒决明子指纹特征的研究
3.1.1 决明子及炒决明子指纹图谱 橙黄决明素、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚6种成分的混合对照品、决明子及炒决明子样品的色谱图,见图1~3。

图1 混合对照品的色谱图

图2 决明子的HPLC色谱图

图3 炒决明子的HPLC色谱图
3.1.2 决明子及炒决明子共有模式的建立 采用国家药典委员会《中药色谱指纹图谱相似度评价系统》(2012.130723版本)对12批决明子、炒决明子样品指纹图谱进行多点校正、峰匹配、生成对照图谱,见图4~5。
3.1.3 相似度评价 采用国家药典委员会《中药色谱指纹图谱相似度评价系统》(2012.130723版本),对图4~5中的指纹图谱进行处理。设置S1为参照图谱,经多点校正,分别进行全谱峰匹配和Mark峰匹配,生成对照图谱,计算各样品与对照图谱的相似度。见表2。
3.2 决明子及炒决明子6种成分的定量分析

图4 12批决明子的HPLC指纹图谱及对照图谱

图5 12批炒决明子的HPLC指纹图谱及对照图谱
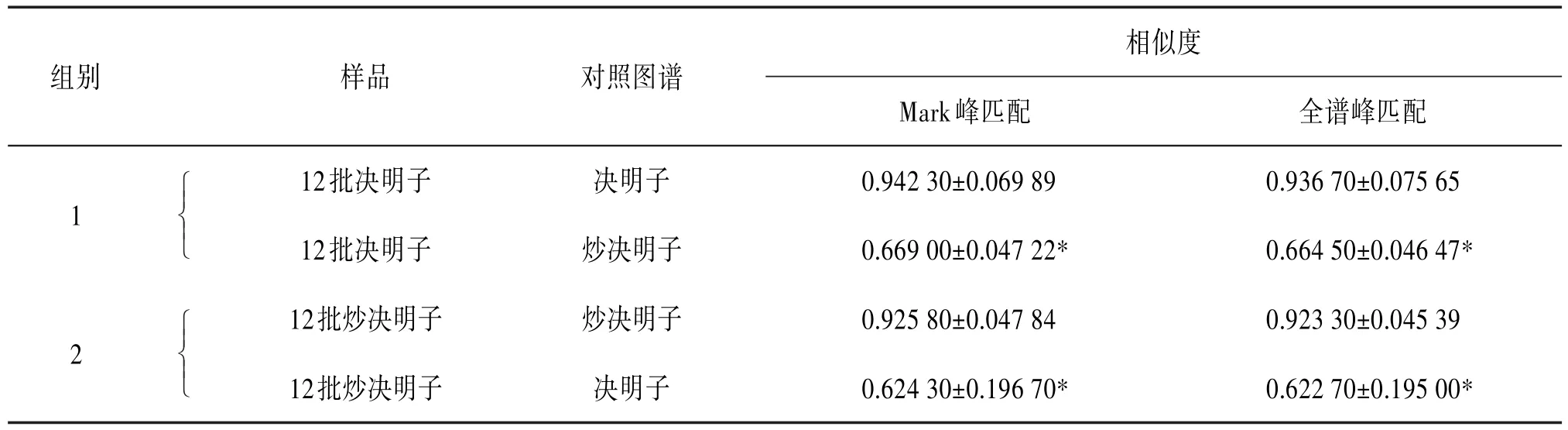
表2 相似度计算结果(xˉ±s,n=12)
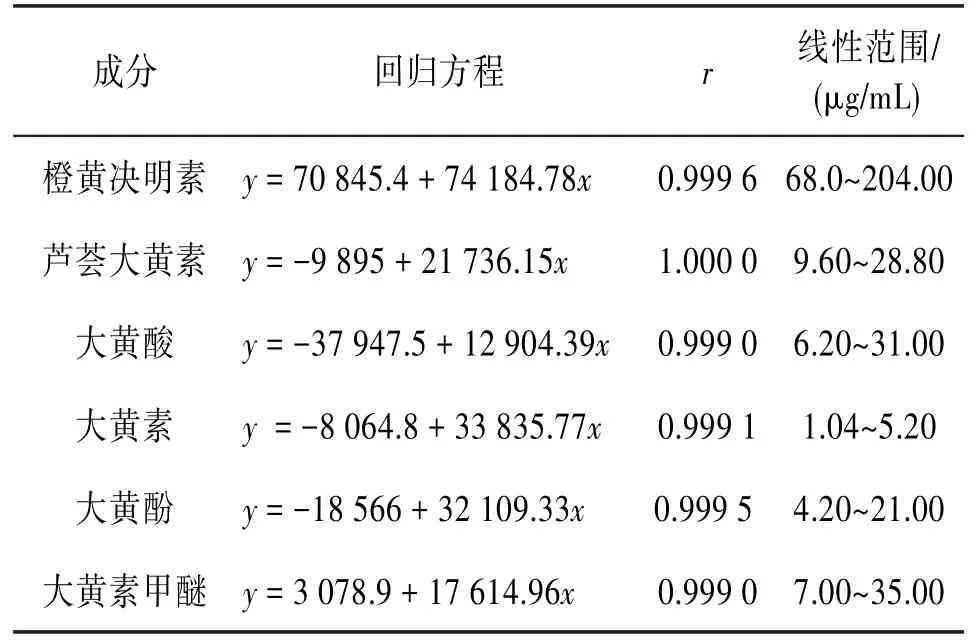
表3 决明子中6种成分的回归方程
3.2.1 标准曲线的建立 取对照品适量,以甲醇为溶剂分别配制系列混合对照液,并逐步稀释为5个系列浓度,按照“2.2”项下色谱条件进样。以对照品溶液的质量浓度(x)为横坐标、峰面积(y)为纵坐标进行线性回归。见表3。3.2.2 方法学考察 ①精密度:精密吸取决明子(批号为170401)样品溶液,按照“2.2”项下色谱条件,连续进样5次。结果显示橙黄决明素、芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚峰面积的RSD分别为0.38%、1.24%、1.32%、0.49%、0.40%和1.60%,表明仪器精密度良好。
②稳定性:取决明子(批号为170425)的样品溶液,按照“2.2”项下的色谱条件,分别在0、6、12、18、24 h进行测定。结果橙黄决明素、芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚峰面积的RSD分别为0.33%、1.53%、1.28%、0.46%、0.44%、3.72%,表明样品溶液在24 h内稳定性良好。
③重复性:取决明子(批号为170425)样品5份,按“2.1.2”项下方法预处理,按“2.2”项下色谱条件分别进样。结果橙黄决明素、芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚百分含量的RSD分别为2.21%、4.85%、3.30%、3.63%、4.83%、4.44%,表明方法精密度良好。
④加样回收率:取决明子(批号为170425)的样品9份,分为3组,每组3份,每组按照橙黄决明素、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚已测得含量的80%、100%、120%精密加入对照品。按“2.1.2”项下方法制备溶液,按照“2.2”项下的色谱条件进行测定。见表4。

表4 加样回收率结果

续表4
3.2.3 样品分析 按“2.1.2”的方法对12批决明子及炒决明子进行处理,按“2.2”项下色谱条件,对12批决明子及炒决明子中橙黄决明素、芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚进行定量分析,见表5。
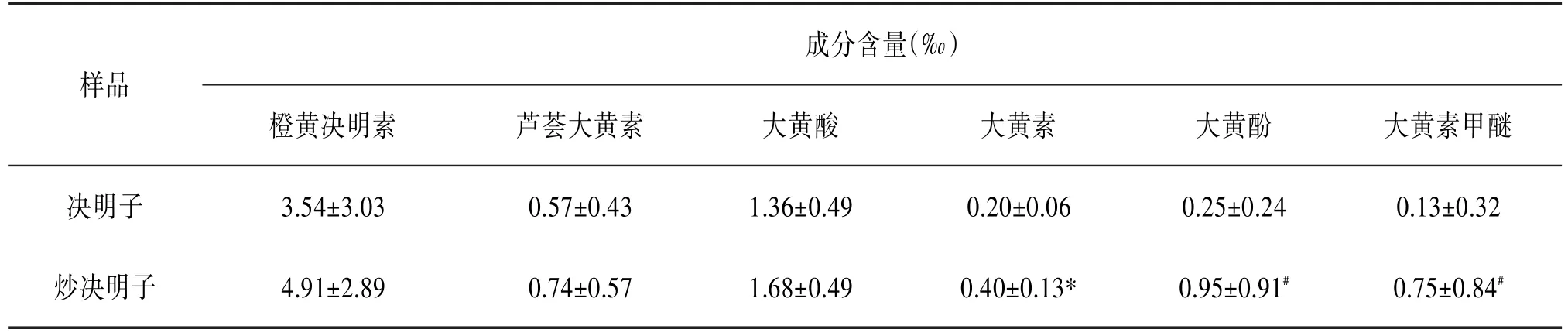
表5 决明子及炒决明子6种成分的定量分析(xˉ±s,n=12)
4 讨论
在实验中针对决明子中蒽醌类化合物这一主要有效成分来进行流动相的筛选〔7〕,考察了甲醇、乙腈与磷酸、醋酸的混合系统作为流动相的梯度洗脱条件,并对YMC-Pack ODS-A C1(8250 mm×4.6 mm,5 μm)、Synergi Hydro-RP C18(250 mm×4.6 mm,4 μm)、Kinetex XB-C1(8100A,250 mm×4.6 mm)、Agilent TC-C1(8250 mm×4.6 mm,5 μm)等几种色谱柱的分离效果进行了考察,以色谱柱为YMC-Pack ODS-A C18(250 mm×4.6 mm,5 μm),乙腈-0.1%磷酸溶液为流动相进行梯度洗脱效果最佳。同时综合各蒽醌类化合物的紫外吸收特征,选择检测波长为287 nm。本实验中,样品处理方法参照《中华人民共和国药典》(2015年版)〔1〕,但省略了甲醇提取过程并用二氯甲烷代替三氯甲烷进行萃取,降低试剂毒性,同时也满足决明子及炒决明子未水解处理条件下指纹特征及成分含量比较的要求。
中药指纹图谱就其本质而言,应可视为中药的一种依赖于不同提取方法所得的活性化学组分的相对浓度谱〔8〕,为国内外广泛接受的一种中药质量评价模式。《中华人民共和国药典》(2015年版)及现有研究多对决明子及炒决明子进行水解处理后的样品进行分析,难以评价决明子及炒决明子内在化学成分上的差异。为此,参考有关文献〔10-11〕,本实验建立了12批决明子及炒决明子未水解样品的指纹图谱,结果发现12批决明子与决明子对照图谱及炒决明子对照图谱比较,相似度分别为0.94和0.67,二者间差异有统计学意义(P<0.01);12批炒决明子与炒决明子对照图谱及决明子对照图谱比较,相似度分别为0.92和0.62,二者间差异有统计学意义(P<0.01)。因此,采用指纹图谱技术可进行决明子及炒决明子的鉴别。通过实验结果可知,不同产地的决明子间化学成分有一定差异,因此,应按《中药材生产质量管理规范》和决明子规范化种植标准操作规程开展决明子药材的种植生产,以保证药材质量〔12〕。炒决明子相似度较决明子低,可能原因是决明子本身内在化学成分的差异经过炒制后更加凸显。
本实验对决明子及炒决明子中的橙黄决明素、芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚等成分的定量分析结果表明,决明子及炒决明子未经水解处理,炒决明子中6种成分的含量均较决明子高,其中大黄素、大黄酚及大黄素甲醚差异有统计学意义(P<0.01或0.05),说明炒制过程中,部分结合型苷类成分解离成了苷元,应注意炒制过程的质量监控。鉴于决明子及炒决明子未水解样品中6种成分含量的差异性,特别是与决明子相比,炒决明子中大黄素、大黄酚及大黄素甲醚差异有统计学意义(P<0.01或0.05)。因此,决明子及炒决明子未水解样品中大黄素、大黄酚和大黄素甲醚用于决明子炒制前后内在成分含量变化的评价更为合理。
〔1〕国家药典委员会.中华人民共和国药典:一部〔M〕.北京:中国医药科技出版社,2015:145.
〔2〕侯长军,张平平,霍丹群.决明子的应用研究进展〔J〕.海峡药学,2007,19(7):7-9.
〔3〕王淑红,杨春娟,刘璐,等.HPLC测定决明子中6种游离蒽醌含量〔J〕.哈尔滨医科大学学报,2015,49(1):22-26.
〔4〕赖日明.不同炮制方法对决明子中蒽醌类成分含量的影响〔J〕.中国民族民间医药,2015,24(20):5.
〔5〕寇真真.炮制对决明子主要成分及药效影响研究〔D〕.郑州:河南中医药大学,2016.
〔6〕国家药典委员会.中华人民共和国药典:四部〔M〕.北京:中国医药科技出版社,2015:31.
〔7〕李文莉,黄晓燕,丁野,等.不同来源决明子的质量分析〔J〕.药物分析杂志,2013,33(8):1411-1415.
〔8〕谢培山.中药色谱指纹图谱〔M〕.北京:人民卫生出版社,2005:141.
〔9〕罗国安,粱琼麟,王义明.中药指纹图谱—质量评价、质量控制与新药研发〔M〕.北京:化学工业出版社,2009:18.
〔10〕杨美丽,张少杰,杨金蕊,等.决明子的特征图谱研究及质量分析〔J〕.中国药业,2015,24(22):75-78.
〔11〕张杰,张振秋,米宝丽,等.HPLC测定不同来源决明子饮片中9个成分的含量〔J〕.药物分析杂志,2013,33(10):1665-1671.
〔12〕张成,李勇军,李永,等.决明子规范化种植标准操作规程(SOP)〔J〕.现代中药研究与实践,2015,29(2):5-7.

