姜酚的热稳定性及其热分解动力学研究
杨 鹏, 徐 颖, 王 展, 沈汪洋, 于 博
(1.武汉轻工大学食品科学与工程学院,湖北武汉 430023; 2.湖北文理学院化学工程与食品科学学院,湖北襄阳 441053)
生姜是姜科(Zingiberaceae)多年生草本植物姜(ZingiberofficinaleRosc.)的新鲜根茎,是我国自古以来广泛种植的药食两用植物资源[1],它的主要成分为挥发性油类、姜辣素、二苯基庚烷,其中姜辣素是生姜辣味的主要成分[2]。酚类物质是姜辣素中含量最高且具有生物活性的化合物,也是生姜的主要辣味物质,由一系列的6-姜酚、8-姜酚、10-姜酚和 12-姜酚等同系物组成,其结构如图1所示,其中6-姜酚的含量最高。姜酚具有降血脂、抗肿瘤、驱虫等多种功能活性[3],是生姜具有多种药用价值的主要原因[4]。
在医疗保健领域,姜酚可用来防治类风湿[5]、慢性粒细胞白血病[6]、糖尿病、肾病[7]等疾病,还具有抗凝血[8]、抗氧化[9]等功能。在食品领域,6-姜酚可以有效改善鲈鱼产品的色泽及质构[10-11],还可以延长鱼糜的保质期[12]及牛肉的货架期[13]。除此之外,姜酚还应用于化妆品、漱口液等产品或领域中。虽然姜酚具有良好的生物活性,但由于其分子中存在愈创木酚结构和β-羟基酮结构,使其非常不稳定,易发生降解、脱水等反应[14],导致其难以分离及扩大生产,这也成为姜酚应用的一大瓶颈。
热分析是在控温条件下对物质的物理性质与温度的关系进行测定的技术。热分析技术具有操作简单快捷、热转换少、可重复性好等优点,可以很好地揭示物质的热稳定性及其分降解规律,因此被广泛应用于各个领域。热分析按升温方式可以分为等温法和非等温法,按照数据处理方式可以分为积分法和微分法。由于非等温法和积分法可以很好地减小误差,所以这2种方法应用更为广泛。目前,关于6-姜酚的热稳定性及其热分解动力学的研究报道很少。为此本研究通过热重分析-差示扫描量热(TG-DSC)联用的方法对6-姜酚的热稳定性及其热分解动力学进行研究,探讨6-姜酚的热稳定性规律并揭示其热分解机制,为其热稳定性的评价及实际应用提供一定的科学依据。
1 材料与方法
1.1 试剂与试剂
6-姜酚,上海阿拉丁生化科技股份有限公司,质量分数≥98%。
1.2 仪器与设备
SDTQ600同步TGA/DSC分析仪,美国TA仪器[沃特世科技(上海)有限公司)]。
1.3 试验方法
1.3.1 试验条件 样品的TG和DSC曲线在SDTQ 600同步TGA/DSC分析仪上获得,仪器在试验前用纯金属铟校正。准确称取适量(≤5 mg)样品放入Al2O3坩埚中,用相同的坩埚作参比。在N2保护下,先于70 ℃保温10 min(对样品进行一段时间的后烘干),再分别以5.0、10.0、15.0、20.0、25.0 ℃/min的速率从40 ℃升温至500 ℃。DSC曲线的测定条件与TG曲线相同。数据采集使用仪器配套TA Instrument Explorer软件。
1.3.2 动力学数据处理方法 分别用Friedman-Reich-Levi法和Ozawa-Flynn-Wall法计算6-姜酚热分解的活化能。Friedman-Reich-Levi法和Ozawa-Flynn-Wall法的公式分别表示如下:
Friedman-Reich-Levi法:
ln[(dα/dT)β]=ln[Af(α)]-E/(RT)。
(1)
Ozawa-Flynn-Wall法:
lnβ=ln{AE/[RG(α)]}-5.330 5-1.051 6E/(RT)。
(2)
式中:β为升温速率,℃/min;A为指前因子,min-1;E为活化能,kJ/mol;α为转化率;R为气体常数,8.314 J/(K·mol);T为温度,℃。
利用Friedman-Reich-Levi法计算活化能,在处理数据时,用Δα/ΔT来代替dα/dt,取(αi,Ti)两边相邻的2个点(αi-1,Ti-1)和(αi+1,Ti+1)利用(dα/dt)i≈(Δα/ΔT)i=(αi+1-αi-1)/(Ti+1-Ti-1)进行取点计算,采用线性拟合的方法对活化能E进行求解。
利用Ozawa-Flynn-Wall法计算活化能,在处理数据时,取αi与相邻的αi-1及αi+1的平均值作为αi的值,取Ti与相邻的Ti-1及Ti+1的平均值作为Ti的值进行取点计算,采用线性拟合的方法对活化能E进行求解。
2 结果与分析
2.1 6-姜酚的热分解过程
本研究测试了不同升温速率对6-姜酚的热重及热流的影响。试验结果表明,6-姜酚热分解过程只有1个阶段,升温速率的改变对其温度范围有微小的影响;随着升温速率的增大,热重曲线向高温方向移动,但失质量率变化不大。
图2为在升温速率为20.0 ℃/min下6-姜酚的TG-DSC曲线,可以看出,6-姜酚分解过程温度范围为 153.82~350.00 ℃,其TG曲线只有1个热分解台阶,失质量率为98.03%,推测主要是6-姜酚分子骨架大规模解体所致,DSC曲线表明其热分解过程为吸热过程。
2.2 6-姜酚热分解动力学分析
2.2.1 动力学参数的获得 多元非线性拟合法是对不同升温速率下的多条TG曲线进行分析,从而较好地描述固相反应体系的一种方法。由于一些仪器及热反应过程的影响,研究热力学时α的范围常选择在0.2~0.8内[15]。f(α)和G(α) 均为α的函数,则当α一定时,f(α)和G(α)均为常数。对于Friedman-Reich-Levi法,取相同α时,以ln[(dα/dT)β]对1/T作图,由经最小二乘法拟合所得的直线斜率即可求出E。对于Ozawa-Flynn-Wall法,在不同升温速率β下选择几个相同的α,以各个α对应的lnβ对1/T作图,由经最小二乘法拟合所得的直线斜率即可求出E[16]。图3是采用Friedman-Reich-Levi法计算6-姜酚分解活化能时,ln[(dα/dT)β] 对1/T在转化率为0.3~0.7时的线性拟合图。图4是采用Ozawa-Flynn-Wall法时,lnβ对1/T在转化率为0.3~0.7时的线性拟合图。线性关系几乎都在 0.990 0 以上,拟合效果较好。表1分别列出了通过2种方法计算的6-姜酚分解活化能的结果。2种方法计算所得的结果相差不大,但由于计算过程难免会产生误差,因此取2种方法平均值作为分解过程活化能。由表1可知,6-姜酚热分解过程活化能为101.00 kJ/mol。

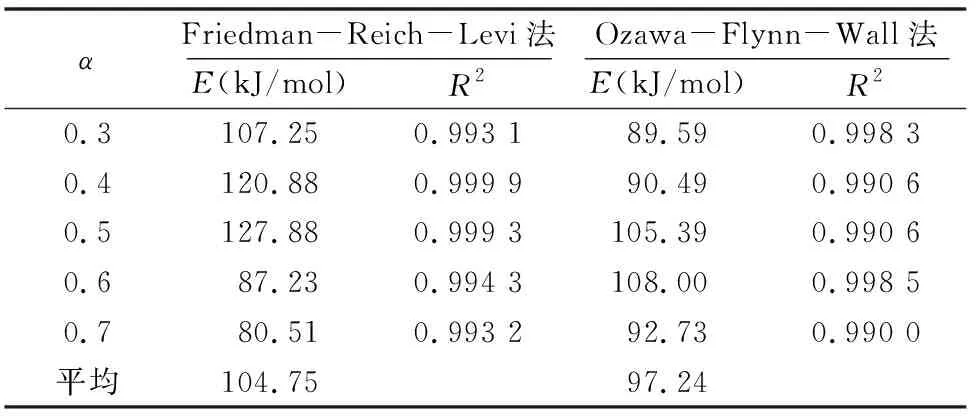
表1 用不同方法计算的6-姜酚热分解活化能
2.2.2 最概然机制函数的判定 双等双步法是在等转化率法和变形的等转化率法的基础上,利用不同升温速率的TG曲线,对定温度和定转化率处的数据进行分析,进而求取活化能、指前因子以及机制函数,具有活化能与机制函数的求取互不影响的优点[17]。
由公式(2)可得:
lnG(α)=ln(AE/R)-5.330 5-1.051 6E/(RT)-lnβ。
(3)
将不同TG曲线上同一温度处的α值与不同升温速率β以及表2中常见的21种固体反应机制函数G(α)带入公式(3)中,以lnG(α)对lnβ作图,用最小二乘法进行线性拟合,找出线性关系较好且斜率接近-1者所对应的机制函数,即为该反应的最概然机制函数,结果见表3。将不同TA曲线上同一α值处的温度和升温速率及已经确定的机制函数G(α) 带入公式(2),以lnβ对1/T作图,用最小二乘法进行线性拟合,由斜率求E,由截距求A,结果见表4。由表3可知,方程y=-1.005 4x+2.859 1(r2=0.986 3)的斜率最接近 -1,拟合效果较好,因此,6-姜酚的分解机制函数为G(α)=-ln(1-α),热分解机制属于随机成核和随后生长反应。由表4可知,根据公式(3)以lnG(α)对lnβ作图所得活化能E为 88.11 kJ/mol,与根据公式(2)以lnβ对1/T作图所得活化能E为97.24 kJ/mol相差不大, 说明该方法拟合所得的动力学参数具有较高可信度。因此,指前因子lnA为27.24 min-1。

表2 常见动力学机制函数的积分表达式

表3 6-姜酚热分解反应机制拟合结果

表4 6-姜酚热分解动力学参数拟合结果
2.2.3 动力学补偿效应 在均相或多相的反应中,经常可以发现对反应速率的影响相反的活化能E和指前因子A存在着“同增同减”的补偿关系,这种关系称为动力学补偿效应。动力学补偿效应的表达式为lnA=kE+b(其中k、b为补偿参数)。利用判定所得的机制函数求得的E与lnA,用最小二乘法进行拟合。结合表4的数据,可得6-姜酚热分解动力学补偿效应方程为lnA=0.222 6E+7.626 6(r2=0.993 5)。
3 结论
采用多重扫描速率法研究了6-姜酚的热稳定性,发现其热重曲线有且仅有1个明显的失重平台,可能是该物质的分子骨架大规模解体,温度范围在153.82~350.00 ℃。采用热分析动力学的方法求得6-姜酚热分解活化能E为 101.00 kJ/mol,指前因子lnA为27.24 min-1,其分解机制函数为G(α)=-ln(1-α),分解机制符合随机成核和随后生长机制。热分解动力学补偿效应表达式为lnA=0.222 6E+7.626 6(r2=0.993 5)。
参考文献:
[1]国家药典委员会. 中华人民共和国药典:一部[M]. 北京:中国医药科技出版社,2015:101.
[2]项佳媚,许利嘉,肖 伟,等. 姜的研究进展[J]. 中国药学杂志,2017,52(5):353-357.
[3]王少鹏,杨 光. 姜酚生物活性研究进展[J]. 中国公共卫生,2013,29(10):1549-1552.
[4]张雪红,刘红星. 姜酚的研究进展[J]. 广西师范学院学报(自然科学版),2009,26(1):110-113.
[5]马武开,姚血明,黄 颖,等. 姜酚对类风湿关节炎模型大鼠血清白细胞介素-17及白细胞介素-23的影响[J]. 中国中医药信息杂志,2014,21(9):43-45.
[6]韩新爱,曾慧兰,古 晨,等. 姜酚和姜酚肟对K562细胞增殖和凋亡的影响[J]. 中药材,2009,32(10):1584-1586.
[7]陈燕玲,罗 婷,吴秀香,等. 6-姜酚对丙酮醛诱导的HK-2肾小管上皮细胞损伤的保护作用[J]. 临床医药文献电子杂志,2017,4(57):11095-11096.
[8]蒋苏贞,宓穗卿,王宁生. 姜酚抗血小板作用及其药效动力学研究[J]. 中药药理与临床,2010,26(3):10-13.
[9]翟兴月. 6-姜酚对过氧化氢致INS-1细胞DNA损伤的保护作用及机制探讨[D]. 大连:大连医科大学,2017:21-22.
[10]蔡路昀,马 帅,曹爱玲,等. 6-姜酚协同超高压处理对花鲈挥发性成分的影响[J]. 水产学报,2016,40(2):255-266.
[11]马 帅,曹爱玲,冯建慧,等. 6-姜酚结合超高压处理对海鲈鱼冷藏期间品质及风味变化的影响[J]. 食品工业科技,2016,37(14):313-319.
[12]米红波,王 聪,赵 博,等. 6-姜酚对草鱼鱼糜凝胶特性及贮藏稳定性的影响[J]. 食品科学技术学报,2017,35(1):21-27.
[13]刘 伟. 姜酚抑菌作用及姜酚-壳聚糖复合膜性质与应用研究[D]. 北京:中国农业大学,2015:79-89.
[14]杨 鹏,于 博,汤尚文,等. 姜酚及其应用研究进展[J]. 现代食品,2017,2(4):78-81.
[15]戚桂斌,刘庆阳,贝逸翎,等. 三种糖类物质的热降解动力学研究[J]. 山东大学学报(理学版),2007,42(7):19-21.
[16]胡荣祖. 热分析动力学[M]. 2版. 北京:科学出版社,2016:57-58.
[17]任 宁,张建军. 热分析动力学数据处理方法的研究进展[J]. 化学进展,2006,18(4):410-416.

