血红蛋白水平及CAMI-STEMI评分对急性ST段抬高型心肌梗死患者PCI术后预后的预测价值
罗二飞,鄢高亮,钱昊,秦雨涵,刘钜川,马长乐,彭中兴,汤成春
(1.东南大学 医学院,江苏 南京 21009; 2.东南大学附属中大医院 心内科,江苏 南京 21009)
冠心病医疗结果评价和临床转化(China PEACE)研究对2001年至2011年13 815例ST段抬高型心肌梗死(ST segment elevation myocardial infarction, STEMI)患者的分析数据显示,急性心肌梗死患者住院率呈逐年上升趋势[1]。早期、快速和完全地开通梗死相关动脉是改善STEMI患者预后的关键,经皮冠状动脉介入治疗(percutaneous coronary intervention, PCI)是目前广泛开展的心肌再灌注治疗的有效手段[2-3]。同时,早期风险分层对预后判断和指导诊疗决策有重要意义。贫血和高血红蛋白(hemoglobin, Hb)水平在STEMI患者中都较常见,但目前Hb水平对STEMI患者预后的影响仍存在一定争议。贫血是急性冠脉综合征(acute coronary syndrome, ACS)患者住院期间和30 d 之内的近期发生心血管事件的独立预测因子[4],但贫血对ACS患者长期预后的预测作用存在不同的看法,al Falluji等[5]发现,贫血对这些患者的1年死亡率没有直接预测作用。并且贫血在不同类型心肌梗死(STEMI与Non-ST-segment elevation myocardial infarction,NSTEMI)患者中的预测价值也不尽相同[6]。有研究称,在STEMI患者中,入院时贫血应被视为一个额外的风险因素[4]。与此同时,高Hb水平与心血管风险是否具有相关性仍然不清楚。有研究指出,过低或者过高的Hb水平都将增加心血管不良事件的发生率[7]。与此同时,目前临床常用的几种危险分层评分针对的是ACS患者,均来自于国外的模型,也不是专门针对STEMI或NSTEMI的模型。Yang等[8]在2017欧洲心脏病学会(European Society of Cardiology,ESC)年会上公布了中国心肌梗死注册登记研究-ST段抬高型心肌梗死(the China Acute Myocardial Infarction registry-ST segment elevation myocardial infarction, CAMI-STEMI)评分,与同类的其他评分相比,CAMI的这个评分简单实用,不需要抽血化验及问病史,在中国STEMI患者住院死亡率的预测精度与心肌梗死溶栓治疗临床试验(the thrombolysis in myocardial infarction,TIMI)评分、全球急性冠状动脉综合征注册(the Global Registration of Acute Coronary Syndromes Events, GRACE)评分相似。本研究拟探讨Hb水平及CAMI-STEMI评分对STEMI患者PCI术后预后的预测价值,为进一步完善STEMI危险分层及优化心肌梗死治疗方案提供思路。
1 对象与方法
1.1 研究对象
连续选择2013年6月至2016年4月于东南大学附属中大医院住院的经临床确诊为STEMI并行PCI的病例。纳入标准:符合文献[2]关于STEMI的诊断标准。排除标准:近期(3个月)内有重大手术、外伤及出血史;有抗凝和抗血小板治疗禁忌证;有严重的肝、肾功能损伤;患有恶性肿瘤;临床资料或冠状动脉造影资料不全。
1.2 方法
1.2.1 分组 根据患者入院第1次Hb值分为3组,组1(男姓Hb<120 g·L-1,女姓Hb<110 g·L-1,共42例)、组2(男姓120 g·L-1≤Hb<160 g·L-1,女姓110 g·L-1≤Hb<150 g·L-1,共278例)、组3(男姓Hb≥160 g·L-1,女姓Hb≥150 g·L-1,共40例)。
1.2.2 Hb水平检测 入院后24 h内采集静脉血检测Hb水平,并测定血糖、血脂、肌酐等生化指标。
1.2.3 CAMI-STEMI评分计算 ESC公布的CAMI-STEMI评分包括7个变量:女性(1分),心率(HR)≥100次·min(2分),年龄≥70岁(2分),收缩压≤115 mmHg(2分),Killip分级>1(2分),心跳骤停(4分)和前壁梗死(1分)。记录各患者上述资料情况并计算CAMI-STEMI评分。
1.2.4 PCI PCI包括对梗死相关血管进行球囊扩张术和(或)支架置入术。所有患者术前均口服阿司匹林300 mg、替格瑞洛180 mg或氯吡格雷300 mg,术后长期口服阿司匹林(100 mg,每天1次)、替格瑞洛(90 mg,每天2次)或氯吡格雷(75 mg,每天1次)。术中常规肝素化,术后肝素酌情使用;术中和术后替罗非班酌情使用,无禁忌情况下3组患者均常规使用他汀类药物、β受体阻滞剂、硝酸酯类药物及血管紧张素转换酶抑制剂。
1.2.5 事件及定义 主要不良心脑血管事件(major adverse cardiovascular and cerebral events, MACCE)包括全因死亡、靶血管病变重建、随访期间发生的心肌梗死、需要住院治疗的不稳定心绞痛和心功能衰竭、脑卒中或者一过性脑缺血。终点为随访期间(PCI术后30 d、6个月)出现MACCE。
1.2.6 临床随访 所有患者随访由心血管内科医生完成,随访方式包括电话随访及门诊随访。所有纳入该研究的患者均自愿参加本临床研究并签署知情同意书。
1.3 统计学处理
2 结 果
2.1 基线临床资料
3组患者基线临床资料见表1,血细胞分析及生化指标见表2,冠脉造影及心脏彩超结果见表3。本研究378例患者入选,失访18例(占4.8%),最终360例患者纳入研究。3组间在年龄、女性比例、体质指数(BMI)、吸烟史、心率、Killip分级>1比例、钾离子浓度、白蛋白、丙氨酸转氨酶、天冬氨酸转氨酶、肌酸激酶、肌酐、总胆固醇、低密度脂蛋白、术中行血栓抽吸比例等方面比较差异有统计学意义(P<0.05),余指标3组间差异无统计学意义。平均年龄组3<组2<组1,女性患者比例组3<组2<组1。
表13组患者基线临床资料比较
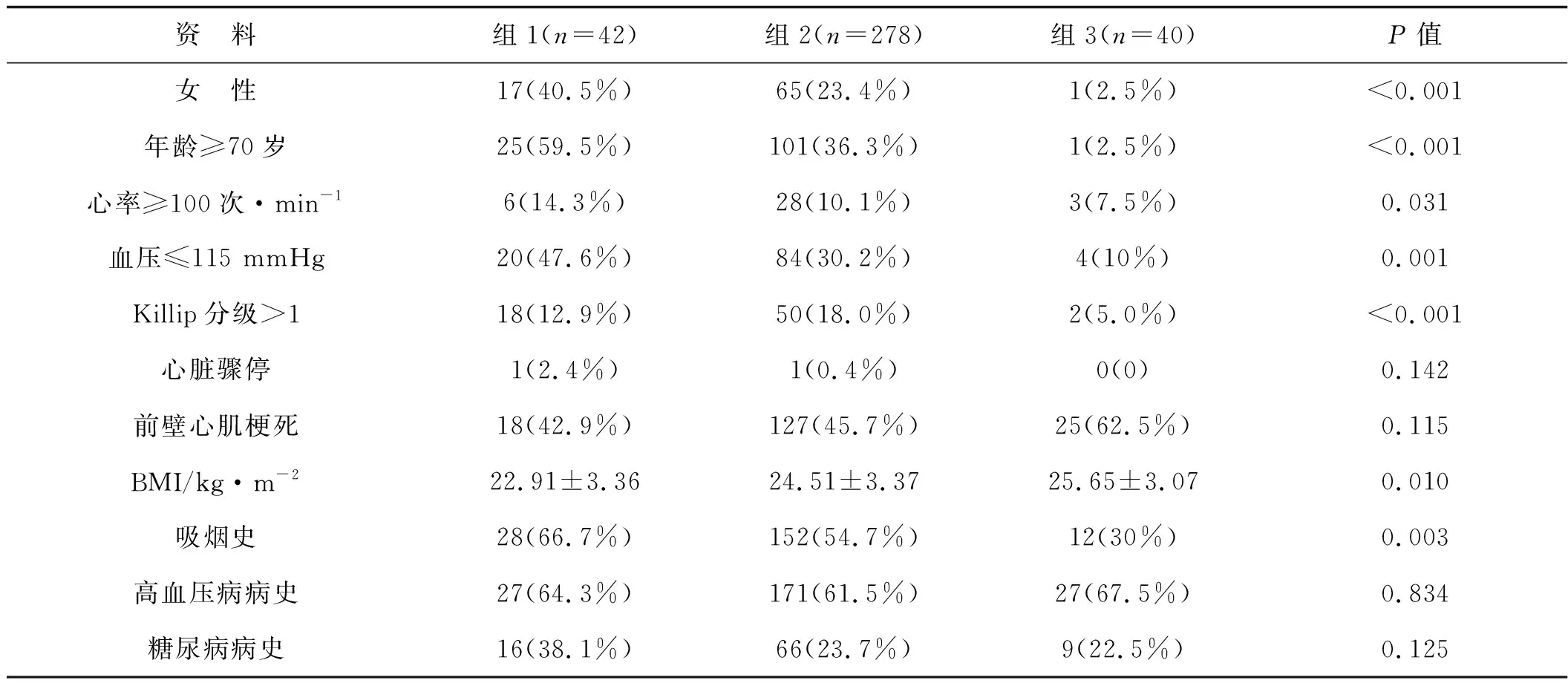
资 料组1(n=42)组2(n=278)组3(n=40)P值女 性17(40.5%)65(23.4%)1(2.5%)<0.001年龄≥70岁25(59.5%)101(36.3%)1(2.5%)<0.001心率≥100次·min-16(14.3%)28(10.1%)3(7.5%)0.031血压≤115 mmHg20(47.6%)84(30.2%)4(10%)0.001Killip分级>118(12.9%)50(18.0%)2(5.0%)<0.001心脏骤停1(2.4%)1(0.4%)0(0)0.142前壁心肌梗死18(42.9%)127(45.7%)25(62.5%)0.115BMI/kg·m-222.91±3.3624.51±3.3725.65±3.070.010吸烟史28(66.7%)152(54.7%)12(30%)0.003高血压病病史27(64.3%)171(61.5%)27(67.5%)0.834糖尿病病史16(38.1%)66(23.7%)9(22.5%)0.125
注:表中数据单位除标注者外均为例;括号内为所占比例
表23组患者血细胞分析及生化指标比较

指 标组1(n=42)组2(n=278)组3(n=40)P值Hb浓度/g·L-1108(99~112)139(130~147)168(161~174)0.000K+浓度/mmol·L-13.9(3.6~4.3)3.8(3.5~4.0)3.6(3.3~3.9)0.010白蛋白水平/g·L-132.5±5.337.4±4.539.4±5.4<0.001丙氨酸转氨酶活性/IU·L-126(15~53)37(25~58)48(34~82)0.001天冬氨酸转氨酶活性/IU·L-185(31~141)112(46~202)114(59~266)0.034肌酸激酶活性/IU·L-1560(139~1 288)1 028(279~2 043)1 249(275~2 267)0.018肌酐浓度/mmol·L-1107(72~141.5)81(69~97)85.5(69.5~100)0.006总胆固醇水平/mmol·L-13.7(3.4~4.4)4.6(3.9~5.4)4.8(4.3~5.6)<0.001低密度脂蛋白水平/mmol·L-12.4(2.0~2.7)2.9(2.4~3.4)2.8(2.5~3.4)0.001
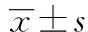
表33组患者冠脉造影及心脏彩超结果比较

检查项目组1(n=42)组2(n=278)组3(n=40)P值冠脉造影 病变支数3(2~4)3(2~4)3(1.5~3)0.089 三支病变20(47.6%)146(52.5%)13(32.5%)0.058 冠脉内血栓19(45.2%)169(60.8%)27(67.5%)0.091 血栓抽吸16(38.1%)162(58.3%)26(65.0%)0.026术后心脏彩超 左心室射血分数0.53(0.4~0.62)0.54(0.47~0.61)0.56(0.5~0.63)0.242 室壁节段性运动异常27(64.3%)200(71.9%)30(75%)0.513
注:表中病变支数和左心室射血分数用P50(P25~P75)表示,其余指标单位均为例,且括号内为所占比例
2.2 临床随访及结果
各组患者CAMI-STEMI评分及术后随访情况见表4。通过Kaplan-Meier曲线描绘出3组患者随访MACCE-free生存曲线,见图1。多因素Cox逐步回归显示,在校正其他因素后,CAMI-STEMI评分是患者术后30 d MACCE发生率的独立预测因子(OR为1.225,95%CI为1.067~1.406,P=0.004),30 d的Cox 回归模型包括:CAMI-STEMI评分、血红蛋白分组、白蛋白、术中行血栓抽吸比例、左心室射血分数(LVEF);贫血是患者术后6个月MACCE发生率的独立预测因子(OR为2.071,95%CI为1.178~3.461,P=0.011),无糖尿病的患者术后6个月MACCE发生率较低(OR为0.585,95%CI为0.363~0.944,P=0.028),6个月的Cox回归模型包括CAMI-STEMI评分、Hb分组、糖尿病病史、肌酐。
表43组患者CAMI-STEMI评分及随访结果

组别CAMI-STEMI评分术后30 d内发生MACCE例数术后6个月内发生MACCE例数组14(3~6)10(23.8%)16(38.1%)组22(1~4)31(11.2%)57(20.5%)组31(0.5~1)2(5.0%)5(12.5%)P值<0.0010.0210.014
注:表中CAMI-STEMI评分用P50(P25~P75)表示,其余指标括号内为所占比例
3 讨 论
既往研究显示,贫血在ACS患者中很普遍,因各个临床研究应用的诊断标准和研究人群不同,贫血在ACS患者中的发生率从10%~43.4%不等[9]。一项关于ACS患者贫血与预后的系统回顾和Meta分析显示:与非贫血患者相比,贫血患者的短期死亡率、长期死亡率及心力衰竭、心源性休克、大出血发生率均增加;贫血可能成为ACS患者危险分层的独立预测因子[10]。Younge等[11]研究显示,贫血的存在和严重程度是ACS后高住院率和高长期死亡率的重要预测指标。STEMI是严重威胁人类生命的危重症,以往Hb水平对冠心病患者预后影响的研究多集中在ACS患者中,针对STEMI患者的研究较少。贫血和高Hb水平在STEMI患者中都较常见,但目前Hb水平对STEMI预后的影响仍存在一定争议[12]。王崇慧等[13]研究发现,对于行PCI的STEMI患者,基线Hb水平<120 g·L-1与随访期间不良反应、MACE发生率及死亡率升高有显著相关性。Zhang等[14]研究发现,对于STEMI患者,入院时Hb水平降低可独立预测1年MACE,特别是LVEF>48%的患者。同时,Reinecke等[15]研究显示,Hb水平与冠心病预后的关系呈J/U型,显示高Hb水平与冠心病预后差相关。李全等[16]研究显示,高Hb水平与冠心病患者的不良心血管事件连续相关,是冠心病预后的独立预测因素,临床工作中需要注意Hb水平对冠心病的预后意义,从而进一步优化临床治疗方案。
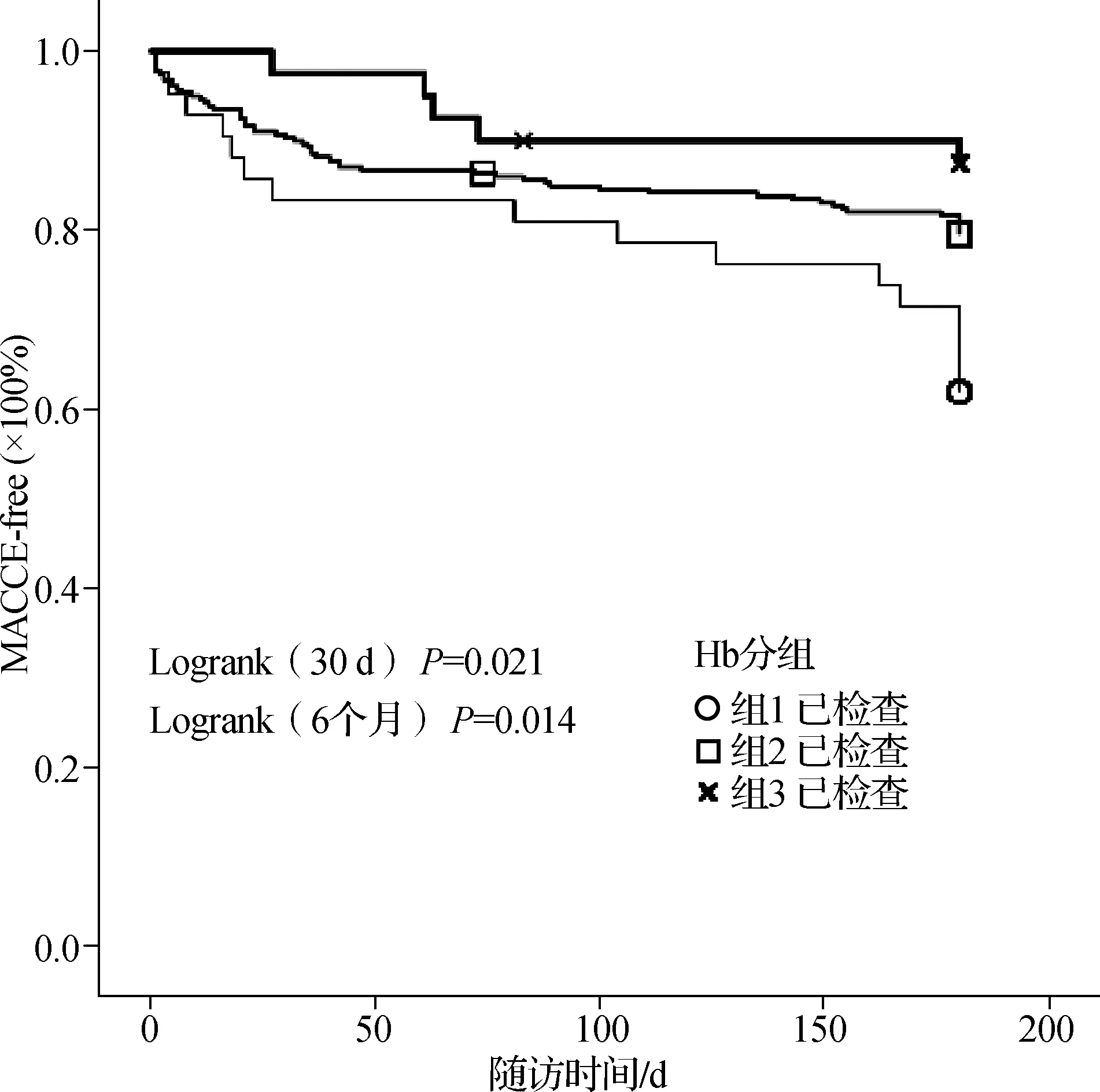
图13组患者随访MACCE-free生存曲线
本研究结果显示,男性及吸烟的STEMI患者Hb水平较高,而且随着年龄的增加,Hb水平明显下降。低Hb水平的STEMI患者,白蛋白、丙氨酸转氨酶、天冬氨酸转氨酶、肌酸激酶、总胆固醇、低密度脂蛋白水平及术中行血栓抽吸的比例也偏低,且钾离子浓度、肌酐浓度、Killip分级>1比例高于高Hb水平的STEMI患者。通过Kaplan-Meier曲线描绘出3组患者随访MACCE-free生存曲线提示,3组PCI术后30 d、6个月MACCE发生率均随Hb水平的降低而增高。CAMI-STEMI评分是最新公布的一种简单实用的危险分层评分系统,不需要抽血化验及问病史,在中国STEMI患者住院死亡率的预测精度与TIMI评分、GRACE评分相似。本研究显示,CAMI-STEMI评分是患者术后30 d MACCE发生率的独立预测因子。Hb水平是STEMI患者住院早期最广泛使用的实验数据,是临床最常用最经济的检查之一,且结果稳定,易于观察。本研究显示,贫血是患者术后6个月MACCE发生率的独立预测因子,但与Reinecke等研究结果不同的是,高Hb水平对术后6个月MACCE发生率无明确的预测作用。
本研究的局限性在于:系回顾性研究,患者仅限于东南大学附属中大医院且数量有限,本研究不是标准的随机对照试验,存在选择偏倚。对于急性心肌梗死患者,虽然美国心脏协会(AHA)、美国心脏病学会(ACC)指南建议对ACS患者进行筛选并纠正贫血,但由于缺乏足够的临床资料的支持,尚未确定理想的靶Hb水平[9],有待更大样本量、更多Hb亚组、更长随访时间、多中心的试验进一步确定,为优化心肌梗死治疗方案提供思路,改善患者预后。
[参考文献]
[1] 国家卫生计生委合理用药专家委员会,中国药师协会.冠心病合理用药指南[J].中国医学前沿杂志:电子版,2016,8(6):19-108.
[2] 中华医学会心血管病学分会,中华心血管病杂志编辑委员会.急性ST段抬高型心肌梗死诊断和治疗指南[J].中华心血管病杂志,2015,43(5):380-393.
[3] 韩雅玲.中国经皮冠状动脉介入治疗指南(2016)解读[J].中国循环杂志,2016,31(z2):5-8.
[4] BOLINSKA S,SOBKOWICZ B,ZANIEWSKA J,et al.The significance of anaemia in patients with acute ST-elevation myocardial infarction undergoing primary percutaneous coronary intervention[J].Kardiol Pol,2011,69(1),33-39.
[5] al FALLUJI N,LAWRENCE-NELSON J,KOSTIS J B,et al.Effect of anemia on 1-year mortality in patients with acute myocardial infarction[J].Am Heart J,2002,144:636-641.
[6] 孙钊,杨树森,樊瑛,等.贫血对急性心肌梗死患者预后独立预测的价值[J].国际心血管病杂志,2012,39(1):41-43.
[7] SABATINE M S,MORROW D A,GIUGLIANO R P,et al.Association of hemoglobin levels with clinical outcomes in acute coronary syndromes[J].Circulation,2005,111:2042-2049.
[8] YANG J G,LIU H F,XU H Y,et al.Simple risk prediction model to assess hospital mortality in chinese patients with st elevation myocardial infarction based on a machine learning approach:from china acute myocardial infarction (CAMI)[J].Eur Heart J,2017,38(Suppl):1199.
[9] 方唯一,施鸿毓.急性冠状动脉综合征与贫血[J].心肺血管病杂志,2007,26(3):182-184.
[10]LIU Y,YANG Y M,ZHU J,et al.Anaemia and prognosis in acute coronary syndromes:a systematic review and meta-analysis[J].J Int Med Res,2012,40(1):43-55.
[11]YOUNGE J O,NAUTA S T,AKKERHUIS K M,et al.Effect of anemia on short-and long-term outcome in patients hospitalized for acute coronary syndromes[J].Am J Cardiol,2012,109(4):506-510.
[12]LIU C W,LIAO P C,CHEN K C,et al.Baseline hemoglobin levels associated with one-year mortality in ST-segment elevation myocardial infarction patients[J].Acta Cardiol Sin,2016,32(6):656-666.
[13]王崇慧,金晓峰,方全,等.血红蛋白水平对冠状动脉介入治疗急性ST段抬高心肌梗死患者远期预后的影响[J].中华医学杂志,2011,91(42):3003-3006.
[14]ZHANG E,LI Z,CHE J,et al.Anemia and inflammation in ST-segment elevation myocardial infarction[J].Am J Med Sci,2015,349(6):493-498.
[15]REINECKE H,TREY T,WELLMANN J,et al.Haemoglobin-related mortality in patients undergoing percutaneous coronary interventions[J].Eur Heart J,2003,24:2142-250.
[16]李全,高阅春,何继强,等.高血红蛋白水平与冠心病患者的不良预后相关分析[J].心肺血管病杂志,2013,32(1):49-52.

