5-氟尿嘧啶/α-氰基丙烯酸酯载药医用胶的制备与特性研究
柏自奎,彭国富,龚年华,郭 强,沈 月,向 春,周应山
5-氟尿嘧啶/α-氰基丙烯酸酯载药医用胶的制备与特性研究
柏自奎1,2,彭国富1,龚年华1,郭 强1,沈 月1,向 春1,周应山2
(1. 人福医药集团医疗用品有限公司,湖北 武汉 430206;2.武汉纺织大学 湖北省纺织新材料及其应用重点实验室,湖北 武汉 430073)
以α-氰基丙烯酸酯为载体,采用静电喷的方法制备5-氟尿嘧啶与α-氰基丙烯酸酯的载药微球。将制备的载药微球分散入α-氰基丙烯酸酯中,即制备成载药医用胶。IR和SEM对微球及载药医用胶进行的结构表征和形态观察,紫外分光光度仪对载药医用胶在模拟体液中的释药性能进行考察,测试了载药医用胶的力学性能变化,结果表明,5-氟尿嘧啶和α-氰基丙烯酸酯之间有比较强的分子间作用力,微球表面呈褶皱状,粒径分布在0.2µm-5µm之间;载药医用胶具有良好的药物控释性能,释药速率随微球加入量的增多而加快、随模拟体液pH值的降低而减缓。掺入少量微球后,医用胶的粘接性能会随着加入微球量的增多而增强。
5-氟尿嘧啶;微球;医用胶;释药性能
手术创面的缝合以及通过创面通道来促进病灶及手术面的愈合一直都是临床上亟待解决的重大问题之一。目前,用于手术缝合功能的医用胶已经是广大病友接受的手术缝合方式,具有止血快、不需要包扎、创面无印记的特点。而对于切除术而言,减少手术出血、防止术后病灶复发及促进创面愈合抑制炎症是外科手术面临的主要困难。手术野病灶残留、术后增殖是术后病灶复发的主要原因,口服药物对人体都将产生很大的毒副作用。目前还没有在手术局部长期给药来抑制术后病灶复发及促进伤口愈合的有效手段。本文针对此问题,提出医用胶的功能化,将药物复合于医用胶中,通过医用胶在手术野均匀分布、与组织细胞直接接触并逐渐降解的特性,在病灶部位持续释放,维持有效的药物浓度,从而有效减少术后病灶复发并促进创面愈合,减少口服及注射药物。5-氟尿嘧啶(5-Fu)是临床常用抗癌化疗及抑制肿瘤细胞增殖的药物,其在血浆中停留半衰期短且毒副作用大。近年来,通过化学修饰或将5-Fu包裹于载体材料形成药物控释体系以减少用药量,降低5-Fu的毒副作用,提高药物利用率和提高药效已成为研究热点。
药物控释体系以载药微球形式具多,微球的形貌和功能也呈现出多样性变化,微球形态包括实心[1]、中空[2]、多孔、哑铃形、雪花形、草莓和花瓣形[3]等,其功能发展到双亲性[4,5]、光敏[6]、pH响应性、温敏性、磁性和生理相容性等。同时在制备方法上,已从传统的乳液聚合[7]、悬浮聚合[8]、分散聚合[9],发展到无皂乳液聚合[10]、种子乳液聚合[3]、种子溶胀聚合、大分子单体参与的分散共聚合[11,12]、喷雾干燥法、熔融挤出法、液体干燥法以及自组装[1]等新的制备方法。然而上述制备微球方法中都要用到较多的有机溶剂、表面活性剂及赋型剂等添加剂,并且不容易调节微球中药物的含量,在临床中主要是用于静脉注射或口服用药,还没有能直接应用于手术创面而又不影响医用胶性能的载药微球。
本文采用医用胶α-氰基丙烯酸酯作为药物载体材料来制备5-Fu载药微球,再将微球分散入医用胶中,形成一种功能化的载药医用胶。因为制备过程中除需要少量酒精外,不需其它有机溶剂、表面活性剂及赋型剂等添加剂,所以微球与医用胶结合紧密,降解速度一致,随胶的降解缓慢释放5-Fu,不会对创面产生新的生化刺激,微球的加入不会影响医用胶的性能。
1 实验部分
1.1 仪器和试剂
仪器:高压直流电源,数控超声波清洗器,85-1型磁力搅拌器,JSM-B510LV型电子扫描显微镜,INSTRON-5566型万能试样机,冲击试验机,TENSOR-27 TGA-IR型红外光谱仪(德国布鲁克),TG 209F1型热重分析仪(德国耐驰),UV-2550型紫外可见分光光度计(日本岛津),恒温烘箱,SHA-B双功能水浴振荡器。
试剂:5-Fu,α-氰基丙烯酸酯,其它试剂均为国产分析纯。
1.2 实验方法
1.2.1 载药微球的制备及其形貌观察:
将5-Fu溶入乙醇中,磁搅拌后获得5-Fu/乙醇溶液,再在溶液中,加入α-氰基丙烯酸酯,密封的条件下搅拌均匀,获得5-Fu与α-氰基丙烯酸酯的复合溶液;将复合溶液吸入静电纺用的纺丝液管中,将平底圆形玻璃容器置于磁搅拌器平台上,在平底圆形玻璃容器内置入导电圆环电极,导电圆环电极接地,将蒸馏水倒入平底圆形玻璃容器中,使导电圆环电极完全浸没在蒸馏水内,将纺丝液管的喷嘴垂直置于平底圆形玻璃容器中心上方,并在纺丝液管的纺丝头上接入高压电源,制备载药微球装置示意图如图1。

图1 高压静电法制备载药微球示意图
(1-纺丝液管, 2-纺丝针头, 3-平底玻璃器皿, 4-接地导电圆环, 5-磁搅拌子, 6-磁搅拌器)
复合溶液喷完以后,收集落在水中的物质,经冷冻干燥,得到的产物即为5-Fu/α-氰基丙烯酸酯复合微球。
1.2.2 载药医用胶体外释放实验
配制5-FU/模拟体液标准溶液,用紫外分光光度法绘制标准曲线。将制备的载药微球按照微球与α-氰基丙烯酸酯质量比为1/15、3/15、5/15、7/15的组分配制医用胶。以脱脂纱布为胶体的载体,将相同体积的不同组分比的医用胶均匀涂于相同面积的纱布上,制备释放样品。将释放样品分别浸在50ml模拟体液中,在37℃水浴振荡器中做释放实验,于不同时间点取少量模拟体液做紫外测试,并在原溶液中加入等量的新鲜模拟体液。根据标准曲线,计算不同时间段溶液中的实际浓度,绘制5-Fu在载药医用胶中的累积释药百分率曲线。
1.2.3 载药医用胶体外降解实验
取微球与α-氰基丙烯酸酯质量比为3:15的等质量的医用胶释放样品6块,分别浸在50ml模拟体液中,在37℃水浴振荡器中做降解实验,分别于1、8、12、16、20、25天后各取一块样品,清洗烘干后用电子扫描显微镜观察胶体表面,分析胶体降解情况,通过对比推测载药医用胶的降解过程。
1.2.4 模拟体液pH值对释药速率的影响
微球与α-氰基丙烯酸酯质量比为3:15的医用胶释放样品2块,分别浸在pH=3.9、7.4的模拟体液中,在37℃水浴振荡器中做释放特性测试,绘制载药医用胶的累积释药百分率曲线。
1.2.5 载药医用胶粘接性能的测试
将载药微球分散于α-氰基丙烯酸酯,制备成载药量不同的医用胶,自然聚合后进行红外光谱测试。同时对载药量不同的医用胶依照GB/T 7124-2008的标准制作粘接板,GB/T 21526-2008的标准对样品板进行粘接前的表面处理,在试样机上测试胶接板的拉伸剪切强度,冲击强度和弯曲强度。
2 结果与讨论
2.1 微球形貌
5-Fu载药微球如图2所示,微球为白色粉末状,粒径均匀。微球表面呈褶皱状,形状像一朵花,粒径分布在0.2µm-5µm之间。这是因为复合溶液从纺丝针头喷出到达水面过程中,溶剂酒精完全挥发,5-Fu与α-氰基丙烯酸酯的复合体落入水面,由水的引发作用迅速聚合对5-Fu形成包埋作用,同时在水面上形成微小薄膜,由水面的波动形成褶皱状微球。采用这种方法制备的5-Fu载药微球具有以下特点:(1)微球具有较高的载药量;(2)载药量容易调节;(3)不需要其他有机溶剂,表面活性剂及赋型剂等添加剂。

图2 5-FU/α-氰基丙烯酸酯载药纳米微球
2.2 医用胶的红外光谱分析
红外吸收光谱又称为分子振动转动光谱,常用于分子结构的基础研究和化学组成分析。在载药微球的研究中常用红外吸收光谱来分析载体材料与药物分子的相互作用。当药物与高分子载体间发生某种作用时会导致红外吸收峰位移或峰强度的改变。以光谱的变化来探究微球中载体材料与药物在结构上的变化及两者间之间是否发生化学反应。
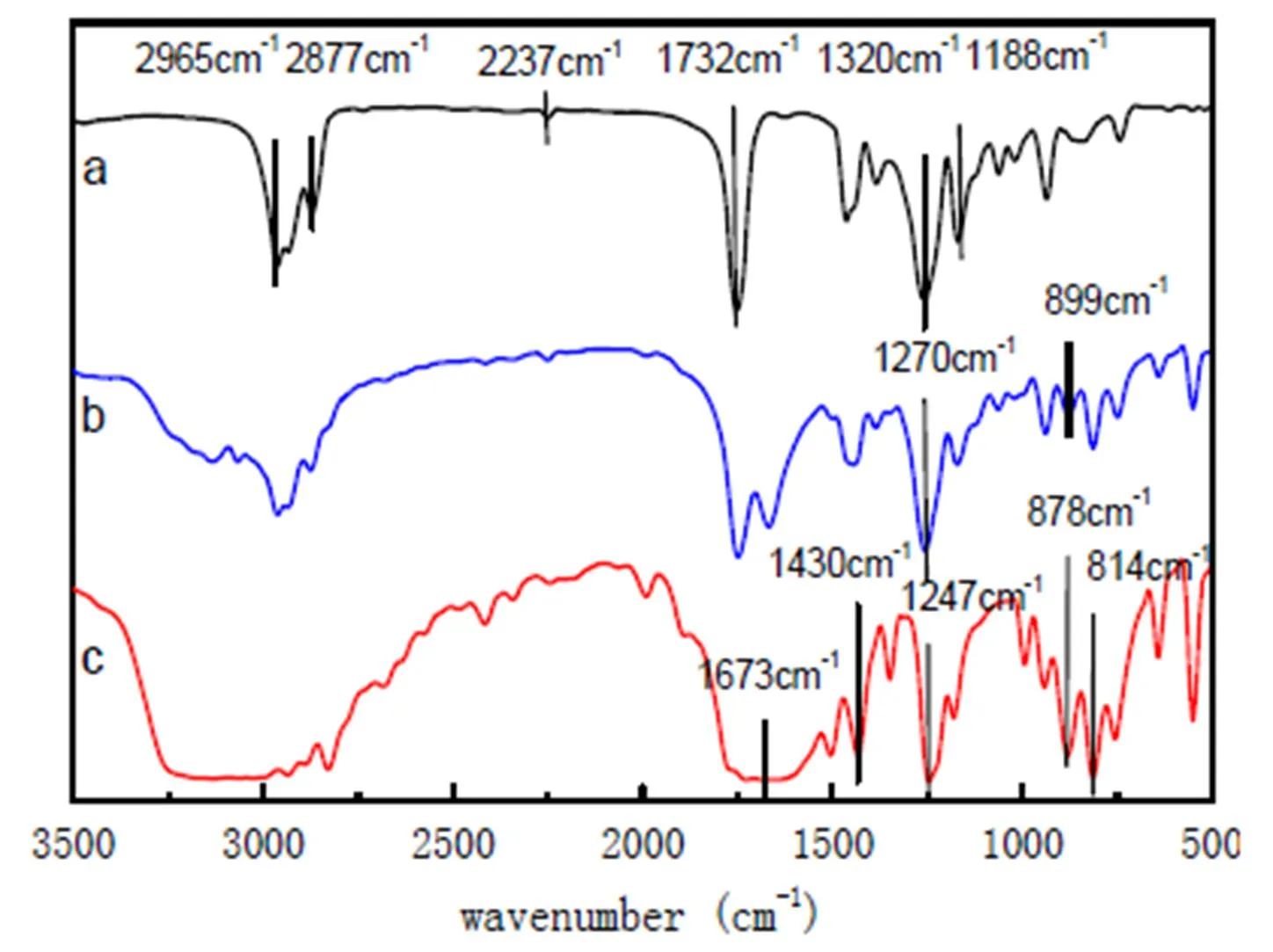
图3 红外光谱图,聚α-氰基丙烯酸酯(a)、5-Fu/α-氰基丙烯酸酯载药微球(b),5-Fu(c)

图4 微球与α-氰基丙烯酸酯质量比分别5:15(a), 3:15(b),1:15(c)的医用胶累积释药曲线
由图3(a)可以看出聚α-氰基丙烯酸酯的特征吸收峰1616cm-1、1188cm-1、1732cm-1分别为C=C伸缩振动峰,C-(C=O)-O变形振动峰,C=O伸缩振动峰;图(c)中5-Fu的特征吸收峰878cm-1为-CF=CH-中的C-H的面外弯曲振动;1673cm-1为C=O和C=C伸缩振动的重合吸收峰;1430cm-1为-CF=CH-中的C—H的面内弯曲振动。对比图(b)、(c)可以看出载药微球红外光谱中,在1270cm-1处出现了5-Fu中的C-N伸缩振动红移的吸收峰,在899cm-1处出现了5-Fu中的-CF=CH-中的C-H的面外弯曲振动红移的吸收峰,这表明载药微球中,α-氰基丙烯酸酯的存在削弱了5-Fu分子之间的作用力,使吸收峰红移。对比图(a)、(b)可以看出微球酯基上的羰基伸缩振动峰和甲基的弯曲振动峰相对于α-氰基丙烯酸酯有了一定的偏移;微球中甲基的伸缩振动峰偏移很小,而峰的强度变化较明显。这些峰位和峰强度的变化都说明,在微球中5-Fu与α-氰基丙烯酸酯之间没有发生明显的基团反应,α-氰基丙烯酸酯的特征基团吸收峰强度减弱,这可能是因为微球中一些基团经过缠绕而使峰强度减弱。同时,5-Fu的有此吸收峰在微球的光谱中基本消失,说明5-Fu在微球内部分散较为均匀,没有发生局部聚集的现象,5-Fu与α-氰基丙烯酸酯相容性较好。
2.3 微球加入量对医用胶释药性能的影响
释药性能是评价载药医用胶的重要指标之一,微球加入量对载药医用胶释药性能的影响如图4所示,从图中可以看出在实验前24小时,释药速率较快,表现出一定的“突释现象”,持续时间相差不大,之后释药速率逐步趋于平缓,药物缓慢释放,表现出很好的缓释特性。随着微球量的增加,释药百分率提高。产生上述现象的主要原因,可能是载药医用胶的释药行为主要受胶体的降解和药物在胶体中的扩散两个因素决定[13]。我们可以将药物释放分为三个阶段:突释阶段,扩散阶段,降解阶段,而后两个阶段可统称为缓释阶段。
第一阶段为突释阶段,是由于部分微球裸露,嵌在微球表面的5-Fu,通过溶解或扩散作用渗透出来。加入的微球越多,裸露在胶体表面的微球就越多,5-Fu的溶解或扩散速度很快,所以随着微球量的增加,释药百分率在增加。
第二阶段为扩散阶段,胶体溶蚀,高分子链变得疏松,成为一种网状结构,部分5-Fu从水溶性孔道以扩散方式释放。由于胶体的溶蚀速度比较慢,所以药物释放缓慢,曲线趋于平缓。
第三阶段为降解阶段,为模拟体液进入胶体内部,孔隙附近处的分子链优先溶蚀,开始降解,降解产物是链短、相对分子质量小且能溶于水的化合物,致使胶体内部孔隙增多、增大,胶体的骨架结构加速破坏,降解中伴随着扩散,药物进一步充分释放,释药曲线斜率增大。
从整个释放过程看出:载药医用胶有明显的药物缓释特性,制备微球的过程可能有少许5-Fu溶于水中,造成微球的实际载药量要小于理论载药量,因此计算的理论释药百分率要比实际数值低。
2.4 载药医用胶在降解过程中的表面形貌变化
载药医用胶在模拟体液中降解过程的形貌变化如图5所示。在实验1天和8天的样品表面平整,比较光滑,两者间无明显变化,这是因为初期降解缓慢,不显著。随时间的延长降解量增大,胶体表面开始出现少许小孔,如图5(c),小孔使内部的5-Fu能溶解到模拟体液中,又为模拟体液渗入胶体内部提供空间,加速胶体的降解,随时间的进一步延长,胶体表面变得更粗糙,表面孔隙数量减少,孔径变大,如图5(d)、(e)、(f)显示,药物释放速率也增大,与如图4的结果一致。

图5 载药医用胶降解过程中的形貌变化
2.5 模拟体液pH值对载药医用胶释药性能的影响
如图6所示,在药物的突释阶段模拟体液pH值对其影响较小,而在缓释阶段,模拟体液pH值对释药性能影响较大,且在酸性条件下的释药百分率要比在中性条件下的释药百分率小。说明酸性条件下,载药医用胶降解速率变慢。

图6 模拟体液pH值为7.4(a)、3.9(b)累积释药曲线
其原因可能为:一方面是胶体聚α-氰基丙烯酸酯的降解首先发生在可水解的酯基上,酯基分解成羟基和羧基是可逆反应,与中性条件相比,在酸性条件下酯基的分解更为不易;另一方面,5-Fu是一种酸性药物,在水中的溶解度受pH值的影响比较大,在中性条件下比酸性条件下更易被电离成带负电的离子,从胶体中扩散出来,溶解度增大[14]。
2.6 载药医用胶的粘结特性
图7显示了不同质量的载药微球加入等质量的医用胶中形成载药医用胶的粘结特性的变化曲线,结果表明随着微球加入量的增多,胶体的冲击强度、拉伸剪切强度、弯曲强度都逐渐增强。医用胶粘接性能的增强可能是因为载药微球的基体材料是聚α-氰基丙烯酸酯,医用胶聚合前是α-氰基丙烯酸酯,当它们混合后α-氰基丙烯酸酯发生聚合反应,微球与胶体间有很强的结合力。当载药医用胶受到外界作用力时,微球的存在,产生应力集中效应,并吸收外界的作用力,使载药医用胶中的裂纹扩展受阻,最终终止裂纹,不致发展成破坏性裂纹,从而达到提高医用胶的黏结性、增强、增韧的效果。
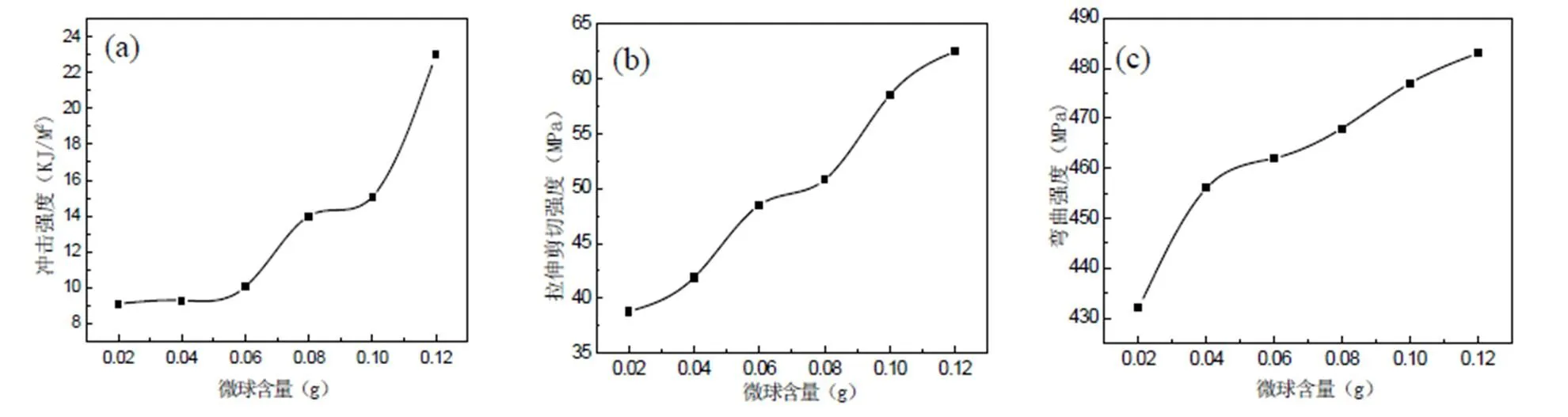
图7 微球量对胶体冲击强度(a)、拉伸剪切强度(b)、弯曲强度(c)的影响
3 结论
以α-氰基丙烯酸酯为载体,采用静电喷的方法制备5-Fu与α-氰基丙烯酸酯的质量比为1:2的载药微球,再将制备的载药微球分散入α-氰基丙烯酸酯中,制备成载药医用胶的方法是完全可行的。5-Fu和α-氰基丙烯酸酯之间有比较强的分子间作用力,微球表面呈褶皱状,粒径分布在0.2µm-5µm之间;载药医用胶具有良好的药物控释性能,释药速率随微球加入量的增多而加快、随模拟体液pH值的降低而减缓。载药医用胶的粘接性能会随着加入微球量的增多而增强。
[1] Liu X Y, Jiang M, Yang S L, et al.Micelles and hollow nano spheres based on ε-caprolactone-containing polymers in aqueous[J].Angewandte Chemie International Edition, 2002, 114 (16) : 2950-2953.
[2] 华慢, 杨伟, 薛乔, 等.两亲性嵌段共聚物PS-b-PMAA的合成与胶束化行为研究[J].化学学报,2005,63 (7) : 631-636.
[3] 王红艳, 倪忠斌, 杨成, 等.PSt种子与“花瓣”形PSt/PAN复合颗粒的制备[J].高分子学报,2007,(6) : 503-508.
[4] Chen M Q, Kaneko T, Zhang M, et al.Preparation of uniform nano spheres with a hydrophilic core and a hydrophobic corona by the macro monomer method[J].Chemistry Letters,2003, 32 (12) : 1138-1139.
[5] 陈明清, 张明, 张坤, 等.PAm-g-PMAA亲水性聚合物微球的合成[J].高分子学报,2004,(5) : 673-678.
[6] Jiang J Q, Qi B, Lepage M, et al.Polymer micelles stabilization on demand through reversible photo-cross-linking [J].Macromolecules,2007, 40: 790-792.
[7] Okubo M, Lu Y.Preparation of a heter geneous polymer film from the blend emulsion by the stepwise heterocoagulation method[J].Colloid and Surfaces,1999, 153: 609-615.
[8] 张洪刚, 陆书来, 成国祥.悬浮聚合法制备磁性分子印迹聚合物微球[J].功能高分子学报,2007, 19 (3) :257-261.
[9] Huang J X, Yuan X Y, Yu X L, et al.Dispersion copolymerization of methyl methacrylate and acrylic acid in polar media: effects of action parameters on the particle size and size distribution of the copolymer microspheres[J].Polymer International,2003, 52: 819-826.
[10] 王志英, 范丽恒, 杨成, 等. 无皂乳液共聚制备纳米微球[J].化工新型材料,2006, 34(3):43-45.
[11] Chen M Q, Serizawa T, Kishida A, et al.Particle size control of poly ( ethylene glycol) coated polystyrene nano particles by macro monomer method[J].Journal Polymer Science PartA: Polymer Chemistry, 1999, 37 (13) : 2155-2166.
[12] 陈明清, 刘晓亚, 杨成, 等.分散共聚体系中高分子纳米颗粒的合成与反应机理[J].江南大学学报(自然科学版),2002, 1(3) : 254-258.
[13] 符旭东, 高永良.缓释微球的释放度试验及体内外相关性研究进展[J].中国新药杂志,2003,12(8):608-611.
[14] 何强芳,李国明,巫海珍,等.5-氟尿嘧啶壳聚糖微球的制备及其释药性能[J].2004,21(2): 192-196.
Preparation and Properties of the α-cyanoacrylate Medical Adhesive with 5-fluorouracil Composite Microspheres
BAI Zi-kui1,2, PENG Guo-fu1, GONG Nian-hua1, GUO Qiang1,SHEN Yue1, XIANG Chun1, ZHOU Ying-shan2
(1.Humanwell Healthcare Group Medical Supplies Co.LTD. Wuhan Hubei 430206, China;2.Key Laboratory for New Textile Materials and Applications of Hubei Province,Wuhan Textile University, Wuhan Hubei 430073, China)
5-fluorouracil-loaded microspheres were prepared using α-cyanoacrylate as the carrier material by using the method of electrostatic spray. The medical adhesive with 5-fluorouracil was fabricated by dispersing the 5-fluorouracil-loaded microspheres into α-cyanoacrylate medical adhesive. The composite microspheres and the medical adhesive with 5-fluorouracil were characterized by Scanning Electronics Microphotograph (SEM), fourier transform infrared spectroscopy (FTIR) and Ultraviolet spectrophotometer. The 5-fluorouracil release kinetic was also systematically studied. The adhesive properties of the medical adhesive with 5-fluorouracil were tested. The results indicated that there are strong interactions between the 5-fluorouracil and a-cyanoacrylate in the composite microspheres with the diameter of 0.2µm-5µm. The 5-fluorouracil release rate increased with the increase of 5-fluorouracil-loaded microspheres in the medical adhesive and decreased with the decrease of simulated body fluid pH value. The adhesive property of medical adhesive with the composite microspheres increases with the increase of the composite microspheres.
5-fluorouracil; composite microspheres; medical adhesive; release property
柏自奎(1971-),男,副教授,博士,研究方向:功能医用材料.
第九批“3551光谷人才计划”创新人才资助项目(2016);武汉纺织大学湖北省纺织新材料及其应用重点实验室开放基金项目(Fzxcl2017011).
R979.1
A
2095-414X(2018)03-0031-06

