双倍氯吡格雷维持剂量与替格瑞洛对慢代谢型患者的临床效果
申文彬,白静,陈素芳,刘会君,李国庆,王明昭,张瑞霞,苏邵萍,王禹*
(解放军371中心医院:1心血管内科,3肿瘤科,4财经处,5药械科,新乡 453000;解放军总医院:2心血管内科,6门诊部干部诊疗科,北京 100853)
冠心病患者行经皮冠状动脉介入(percutaneous coronary intervention,PCI)术后使用双联抗血小板(阿司匹林+氯吡格雷)预防主要不良心血管事件(major adverse cadiovascular events,MACEs)的发生已成为一种经典方法[1]。人群对阿司匹林药物反应的差异较小,发生阿司匹林药物抵抗的概率较低[2]。然而,人群中约1/3冠心病患者存在氯吡格雷药物抵抗现象[3],造成人群对氯吡格雷药物存在抵抗的原因很多,主要是氯吡格雷药物代谢基因不同、是否为急性冠状动脉综合征、是否合并糖尿病等因素[1,4-6]。文献报道,与氯吡格雷药物代谢相关基因的研究热点有细胞色素P450基因超家族(cytochrome P450 proteins,CYP)、对氧磷酶1(paraoxonase 1,PON1)、人ATP结合盒转运体B1(human ATP binding cassette transporter B1,ABCB1)等基因[6-8]。其中CYP基因多态性与氯吡格雷药物抵抗相关性较强[1,9],CYP2C19基因野生型为CYP2C19*1,而CYP2C19*2或CYP2C19*3携带患者对氯吡格雷药物抵抗的发生率明显升高[4]。降低氯吡格雷药物抵抗的方法有增加氯吡格雷药物负荷剂量、维持剂量或更换为替格瑞洛等[10-12]。既往研究未明确何种方法的效果更优,本研究针对慢代谢型患者使用双倍氯吡格雷维持剂量与替格瑞洛两者间的效果进行探讨。
1 对象与方法
1.1 研究对象
选取2014年6月至2016年9月解放军总医院心血管内科行PCI且CYP基因检测结果为慢代谢型(CYP2C19*2/*2、CYP2C19*2/*3、CYP2C19*3/*3)患者205例[6],随机数字表法分为氯吡格雷组103例和替格瑞洛组102例。纳入标准:年龄大于18岁;行PCI且CYP2C19检测结果为慢代谢型患者。排除标准:对阿司匹林、氯吡格雷或替格瑞洛过敏患者;不能持续口服双联抗血小板药物达12个月者;同时服用华法林等抗凝药物患者;估计肾小球滤过率(estimated glomerular filtration rate,eGFR)<30 ml/(min·1.73m2)的患者;预期寿命<1年患者。
1.2 基因检测
基因检测由解放军总医院药学实验室承担,方法为核酸芯片杂交法,检测设备为BE-2.0生物芯片识度仪、BR-526-24全自动杂交仪,由上海百傲科技有限公司生产。患者入院当天抽取静脉血3 ml,加入依地酸二钠(ethylenediaminetetraacetate,EDTA)抗凝,按照外周血细胞DNA提取试剂盒步骤说明提取DNA后,琼脂糖凝胶电泳检测目的条带。聚合酶链反应(polymerase chain reaction,PCR)仪扩增后,按照核酸芯片杂交试剂盒步骤说明应用DNA测序仪进行基因测序,分析患者CYP2C19基因型。
1.3 冠状动脉造影及PCI
经桡或股动脉入路, 6F或7F动脉鞘经桡动脉时动脉鞘内给予维拉帕米1 mg,造影后对狭窄血管进行PCI,包括球囊扩张、支架置入、血栓抽吸等。术中采用比伐芦定或肝素抗凝。支架置入成功定义为残余管腔狭窄<25%,无内膜撕裂或夹层,PCI术后血流心肌梗死溶栓试验(thrombolysis in myocardial infarction,TIMI) 评分3级[3]。
1.4 PCI术后用药
根据检测结果按照美国食品和药品管理局建议调整给药剂量[6]。氯吡格雷组患者给予硫酸氢氯吡格雷[赛诺菲(杭州)制药有限公司,国药准字H20056410]300 mg负荷剂量,双倍维持剂量150 mg/d,3个月后更改为75 mg/d;替格瑞洛组患者每天给予替格瑞洛(阿斯利康制药有限公司,国药准字J20130020)180 mg负荷剂量,90 mg维持剂量,2次/d,所有患者使用双联抗血小板药物时间均为12个月。并于12个月后进行电话随访。
1.5 比较指标
比较2组患者MACEs的发生。MACEs包括支架内血栓、脑卒中、靶血管再次血运重建、心源性死亡、再次发作胸痛、因胸痛再次入院治疗。支架内血栓:明确的支架内血栓,由冠状动脉造影确认。心源性死亡:由任何原因引起的因心脏导致的死亡,也包括未知原因死亡与PCI并发症相关死亡。脑卒中:任何原因引起的缺血性或出血性事件导致局部神经功能障碍,至少持续24 h。靶血管再次血运重建:靶血管任何的再次介入或者搭桥治疗,其中靶血管包括病变血管的上游、下游和分支血管。再次发作胸痛:胸痛症状较术后明显加重,包括活动后、静息时以及胸痛时心电图改变的患者。因胸痛再次入院治疗:术后因胸痛再次入院治疗,不包括正常复查患者[13]。
1.6 统计学处理
2 结 果
2.1 2组患者基线资料比较
2组患者年龄、性别、体质量指数(body mass index,BMI)、血小板计数、eGFR、ST段抬高型心肌梗死(ST-segment elevation myocardial infarction,STEMI)、非ST段抬高型心肌梗死(non-ST-segment elevation myocardial infarction,Non-STEMI)、高血压、高脂血症和既往是否行PCI等差异无统计学意义(P>0.05;表1)。
2.1 2组患者PCI情况比较
2组患者左主干病变、左前降支病变、左回旋支病变、右冠状动脉病变、单支病变、双支病变、三支病变、置入支架、支架总长度、支架直径、球囊预扩张比例、球囊后扩张压力和球囊后扩张比例差异无统计学意义(P>0.05)。球囊预扩张和支架展开压力差异有统计学意义(P<0.05;表2)。
2.2 2组患者MACEs发生率比较
2组患者支架内血栓(stent thrombus, ST)、靶血管再次血运重建(target vessel revascularization, TVR)、再次发作胸痛(recurrent angina pectoris,RAP)、心源性死亡、因胸痛再次入院(hospitalization because of angina pectoris,PBAP)差异无统计学意义(P>0.05)。氯吡格雷组MACEs发生率较替格瑞洛组明显升高[14.6%(15/103)vs5.9%(6/102)],差异具有统计学意义(P=0.040;表3)。
3 讨 论
冠心病患者中约1/3存在氯吡格雷药物抵抗,从而导致PCI术后MACEs发生率明显升高[14]。增加患者氯吡格雷药物抵抗的原因有很多,如糖尿病、急性冠脉综合征、不同药物代谢基因型等[5,8],在此主要针对氯吡格雷药物代谢基因CYP进行讨论。
氯吡格雷在肝脏需经过两步代谢才能转化为有活性的产物[4],CYP2C19在这个过程中发挥了主导作用[4]。CYP2C19基因的野生型为(CYP2C19*1),功能丧失的CYP2C19基因多态性(CYP2C19*2、CYP2C19*3)与较高的氯吡格雷药物抵抗发生率有关,进而增加了PCI术后MACEs的发生率。CYP2C19*2、CYP2C19*3基因型在不同种人群中的发生率存在差异,CYP2C19*2在亚洲人群的发生率约为30%,而高加索人群和非洲、美洲人群的发生率分别为13%和18%[4,15,16]。 CYP2C19*3在东亚人群和高加索人群的发生率分别为(5%~10%)和0%[4,15,16]。东亚人群中氯吡格雷慢代谢型几乎100%是由这两种基因变异导致的[15]。氯吡格雷药物抵抗会增加PCI术后围手术期心肌梗死(peri-operative myocardial infarction,PMI)的发生率,并明显增加MACEs的发生率[15]。数据显示,慢代谢性型患者PMI的发生率较快中代谢型患者明显升高,而快代谢型与中代谢型患者的PMI发生率差异无统计学意义[15]。降低氯吡格雷药物抵抗的方法有增加氯吡格雷剂量或更改药物等方法[10,12],本研究针对慢代谢性患者使用双倍氯吡格雷药物维持剂量或使用替格瑞洛的方法。结果提示,相比替格瑞洛组患者,双倍氯吡格雷组患者MACEs发生率明显升高,提示针对慢代谢型患者采用双倍维持剂量的方法效果较差。

表1 2组患者基线资料比较
BMI: body mass index; eGFR: estimated glomerular filtration rate; Non-STEMI: non ST-segment elevation myocardial infarction; STEMI: ST-segment elevation myocardial infarction; HLP: hyperlipidemia; DM: diabetes mellitus; PCI: percutaneous coronary intervention
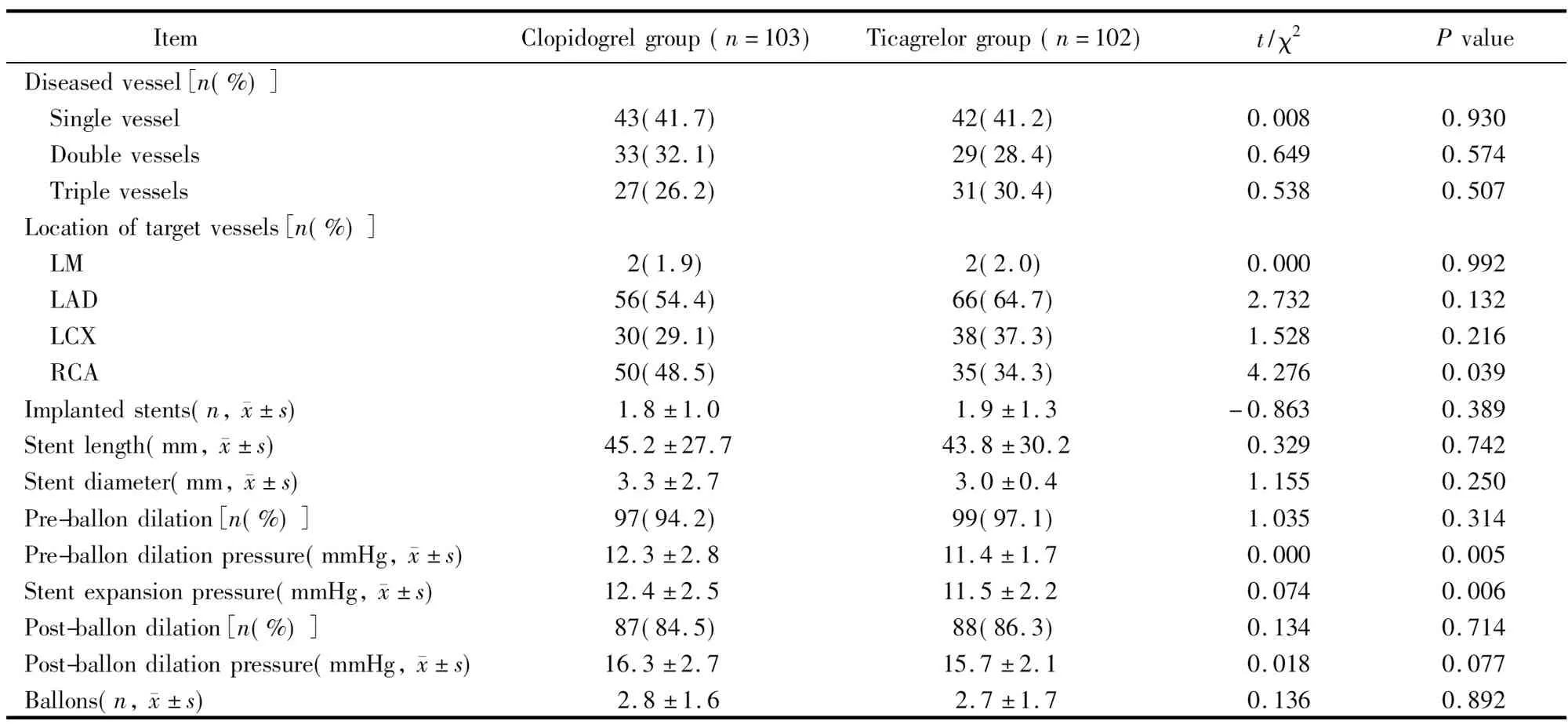
表2 2组患者PCI情况比较
PCI: percutaneous coronary intervention; LM: left main stem; LAD: left anterior descending coronary artery; LCX: left circumflex artery; RCA: right coronary artery. 1 mmHg=0.133 kPa
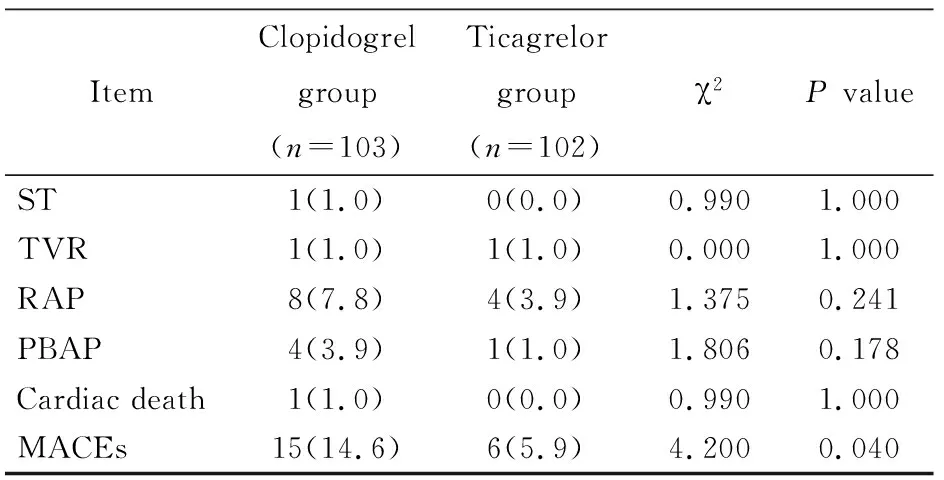
表3 2 组患者MACEs发生率比较
MACEs: major adverse cadiovascular events; ST: stent thrombus; TVR: target vessel revascularization; RAP: recurrent angina pectoris; PBAP: hospitalization because of angina pectoris
虽然双倍氯吡格雷维持剂量可降低氯吡格雷药物抵抗的发生率,但其抗血小板效果仍无法与替格瑞洛相比[17]。研究提示,糖尿病患者往往伴随更高的氯吡格雷抵抗发生率,研究者曾经将糖尿病患者氯吡格雷的负荷剂量增加到600 mg,仍未能达到非糖尿病患者同样的抗血小板效果[5];也有研究者针对糖尿病患者将氯吡格雷维持剂量增加到150 mg,在60%的患者中仍存在氯吡格雷药物抵抗[18]。研究者针对CPY2C19进行了类似的研究,针对中代谢型、慢代谢性患者增加氯吡格雷维持剂量,结果提示,与中代谢型患者的抗血小板效果相比,慢代谢型患者明显较差[6,19]。结合本研究结果提示针对慢代谢型患者,使用替格瑞洛可能会取得更优的临床效果。本研究不足之处是样本量较少,观察时间较短,其有效性和安全性还有待大样本多中心临床研究进一步评价。
【参考文献】

