连续性动态颅内压监测在高血压脑出血患者治疗中的应用价值
宿小满,张 静
高血压性脑出血是高血压较为常见但最为严重和凶险的并发症之一,具有较高的致残率和死亡率,临床预后较差[1]。脑出血发生后,病情发展迅速,早期即可因出血量扩大而引起颅内压急骤升高,脑疝从而导致呼吸循环衰竭。目前临床上对于脑出血的治疗包括手术治疗及药物保守治疗,但对于具体治疗方案的把握,如手术时机、脱水药物用量等,则需要依靠有经验的神经科医生的综合判断,主观性较强。目前临床尚缺乏针对脑出血患者治疗方案的可量化的客观指标。应用颅内压监护仪对颅内压进行连续监测可反映患者实时颅内压力的实时变化,是观察颅脑疾病患者病情变化、手术时机选择、指导临床用药和判断预后的常用手段[2,3],目前已广泛应用于颅脑损伤的患者[4]。本文就连续性动态颅内压监测技术在高血压脑出血患者临床治疗中的应用价值进行初步研究和探讨。
1 研究对象与方法
1.1 研究对象
研究对象为锦州医科大学附属第一医院2016年12月~2018年1月期间收治的高血压脑出血患者共95例。通过随机数表法随机分为监测组和对照组。所有入选对象均符合中国高血压防治指南修订委员会2010制定并发布的《中国高血压防治指南》中相关诊断标准,且高血压病史大于5 y;患者入院后均进行头部CT检查结合临床表现确诊为脑出血,血肿位于幕上,体积在20 ml以上;格拉斯哥昏迷量表GCS评分在3~12分范围内;年龄在30~80岁范围内;排除因各种原因(长期服用华法林、肝病、血友病等)造成的凝血机制障碍患者;排除由外伤、动脉瘤破裂、动静脉畸形等所致脑出血的患者;排除合并全身其它系统严重疾病的患者;排除处于妊娠期及哺乳期的患者。所有患者或其授权直系家属均对本研究知情并愿意配合相关检查及随访,并签署知情同意书,本研究已获我院伦理委员会批准。
1.2 方法
所有患者于重症监护病房密切观察生命体征,瞳孔大小及意识变化,两组患者均根据目前脑出血指南接受常规治疗(包括脱水、调整血压、维持水、电解质及酸碱平衡、营养支持、必要的镇静、并发症的预防等)及必要时手术治疗(根据病情选择小骨窗开颅脑内血肿清除、血肿腔细孔穿刺外引流术、侧脑室穿刺置管外引流手术),其中监测组患者依据连续监测的颅内压数值调整脱水药物(甘露醇)用量、及病情、手术时机判断,而对照组则根据患者的意识状态、影像学资料、瞳孔变化等临床信息经验性调整脱水药物用量以及选择手术时机。
1.2.1 颅内压监测技术
本研究仪器选用CF01-MPM-1颅内压监护仪(美国INTEGRA公司生产),选用脑室内颅内压监测方法进行监测。监测组患者给予行颅骨钻孔并放置传感器,整个操作过程中严格按照无菌操作要求,术后严密进行连续颅内压监护及术后护理。正常的颅内压为5~15 mmHg,根据颅内压监测结果对颅内压升高的严重程度分类:15~20 mmHg范围内判定为轻度;20~40 mmHg范围内判定为中度;超过40 mmHg判定为重度。一般将颅内压增高值报警上限设定为20 mmHg,需要进行相应的降低颅内压处理。
1.2.2 研究方案
两组患者根据病情需要随时调整治疗方案,具体如下:对照组除上述常规治疗外,密切关注患者出血量、血肿位置、瞳孔改变、意识状态,GCS评分,必要时随时复查头部CT。根据GCS评分给予相应的脱水强度:GCS大于9分,给予甘露醇125 ml,3/d,静点;GCS 6~9 分的患者给予125 ml甘露醇,3~4/d,静点,同时给予呋塞米20~40 mg,3/d,静推;GCS在3~5分的患者,同时给予甘露醇125 ml和呋塞米40 mg,4/d,并加用甘油果糖、白蛋白等辅助脱水。若治疗过程患者出现脑疝症状,头部CT证实出血量≥40 ml,存在中线偏移及脑疝等情况应予以立即手术;若治疗过程中意识状态逐渐好转,GCS评分升高2分以上,且复查头部CT证实颅内情况好转(中线结构移位减少、血肿的占位效应较前减轻等),则开始减少甘露醇使用频次。监测组患者除上述常规治疗外,需根据连续监测的颅内压数值调整脱水强度及手术时机。对于颅内压持续高于20 mmHg的患者应用甘露醇125 ml,3~4/d,静点;此期间颅内压仍高20 mmHg持续15 min以上,则给予患者呋塞米20~40 mg静推或甘露醇125 ml静滴,白蛋白静脉滴注等。若患者应用脱水药物后颅内压仍在较高位震荡,则应给予患者复查头部CT,若CT提示出血量≥40 ml,证实中线偏移及脑疝,结合颅内压变化趋势等情况,应予以立即手术,术后继续行连续颅内压监测。根据患者的颅内压监测数值减少甘露醇使用频次,若数值持续小于20 mmHg且波动幅度较小,则考虑减量。监测组非手术治疗患者则在监护7 d后若病情平稳,监测数值持续小于20 mmHg即可拔除引流。
1.3 患者随访
发病3 m后通过门诊随访和电话随访的方式了解患者神经功能恢复情况,应用格拉斯哥预后评分(GOS)进行评估。5分表示痊愈良好,恢复正常生活,尽管有些小的残疾;4分表示中度残疾,但尚可独立生活,可以在保护下工作;3分表示严重残疾,日常生活不能独立,需要照顾;2分表示长期持续的植物生存状态,存在眼部的活动和睡眠周期;1分表示死亡。
1.4 统计学分析
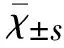
2 结 果
2.1 基线资料
本研究共纳入高血压脑出血患者95例,其中监测组48例,对照组47例,两组患者在性别、年龄、入院GCS评分、手术治疗比例均无统计学差异(见表1)。其中监测组患者入院行急诊手术者18例,余患者暂行保守治疗,后有12例患者经积极降颅压治疗颅内压仍在较高位震荡,复查头部CT后其中11例符合手术指征行手术治疗,另1例继续给予保守治疗,调整脱水强度后颅内压监测结果好转;对照组患者入院行急诊手术患者16例,余患者保守治疗,后有14例患者在积极保守治疗过程中出现意识状态改变、瞳孔改变,复查头部CT后其中11例行手术治疗,另3例均保守治疗。
2.2 甘露醇开始减量时间及应用总量的比较
监测组在甘露醇开始减量时间和应用总量上均显著低于对照组(P<0.05)(见表2)。
2.3 住院期间常见并发症发生的比较
监测组的水电解质紊乱的发生率显著低于对照组(P<0.05),两组患者在肾功能不全、肺部感染、应激性溃疡的发生率差异无统计学意义(见表3)。
2.4 临床预后的比较
监测组临床预后GOS评分显著高于对照组(Z=2.876,P=0.036)(见表4)。
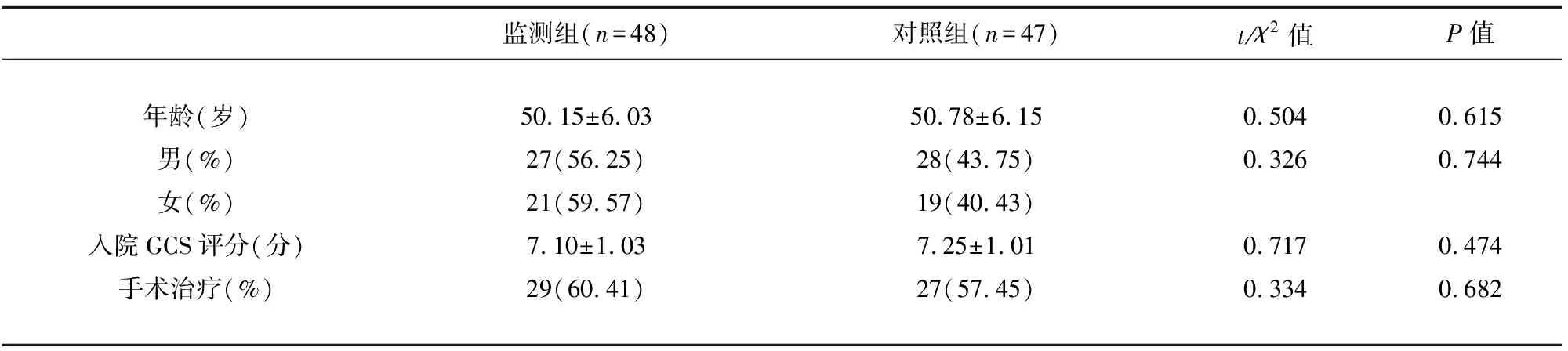
表1 两组患者基线资料的比较

表2 两组患者脱水药物开始减量时间和应用总量的比较

表3 两组患者住院期间常见并发症的比较

表4 两组患者临床预后GOS评分的比较
3 讨 论
高血压性脑出血是神经外科临床常见的急危重症,是临床预后较差的脑血管病类型之一。脑出血发生后,血肿的占位效应及水肿的发生导致的颅内压升高,脑灌注压降低,正常人可通过脑血流自动调节功能而维持脑灌注的稳定,而脑出血的患者脑血流自动调节机能受损[5,6],随之出现脑灌注不足,脑组织缺血缺氧,加重脑水肿程度,从而形成恶性循环引发脑疝及死亡[7]。目前针对脑出血的治疗方式非常有限,如何能够优化脑出血患者的治疗体系是目前临床研究的热点问题。动态颅内压监测技术是通过由传感器和监护仪组成的动态颅内压监护仪实现的,目前已成为监测高颅压最直观和准确的方法,也是观察颅脑疾病患者病情变化、判断手术时机、指导临床用药和评估预后的必备手段之一,广泛用于颅脑损伤的患者[8]。近几年,有学者在相关研究中指出,动态颅内压监测技术或可对高血压脑血压患者病情判断及针对性治疗方案的选择及有重要意义,为临床脱水药物的应用提供了数据支持[9~13]。在上述研究的基础上,我们对连续动态颅内压监测技术在高血压脑血压患者中的应用进行更深入的探讨。
本次研究中,我们比较颅内压监测指导下治疗和常规治疗的两组患者中脱水药物的调整时间及应用总量、常见并发症发生情况及临床转归。共选取近期收治的95例高血压脑出血患者进行随机分组对比研究,主要结局指标为患者3 m的临床预后GOS评分,其他结局指标包括甘露醇开始减量时间,应用甘露醇总量,住院期间常见并发症(包括水电解质紊乱肾功能不全、肺部感染、应激性溃疡),结果得出监测组甘露醇开始减量时间缩短,总用量显著降低,住院期间水电解质紊乱发生率显著降低,且3 m GOS评分显著高于对照组,上述结果均与相关研究报告一致[9~13]。结合多位学者相关报告,我们对颅内压监测在临床中应用的优势进行了综合分析,具体阐述如下:(1)对手术时机的选择提供可靠的临床依据。血肿形成及早期血肿扩大所导致的占位效应是引起早期颅内压升高的主要原因,也是影响临床预后最为关键的因素。当发生血肿扩大时,通过对患者意识、瞳孔变化的判断通常滞后于病情的发展,导致手术时机的延迟,虽然患者生命得以维持,但并不能从根本上改善患者的临床预后。而通过连续颅内压监测,可对患者颅内压变化进行实时监测,在患者出现颅内压升高超过警戒值时可采取相应的治疗及手术,使得早期病情恶化及时发现及处理。本研究中,监测组3 m GOS评分显著高于对照组,且预后良好(GOS评分4~5分)的比例较高,因此我们认为持续性颅内压监测对于量化颅内压和判断手术时机有着重要的意义,可作为危重高血压脑出血患者的常规监测指标。(2)为临床脱水药物应用强度提供了数据支持。水电解质紊乱和肾功能损害为脑出血后应用脱水药物的常见并发症,而在临床上对于甘露醇往往存在过度应用,造成并发症比例相对较高,严重则可因并发症危及生命。在而本次研究中我们发现颅内压监测组甘露醇开始减量时间缩短,甘露醇总用量显著低于对照组,住院期间水电解质紊乱发生率显著降低,因此动态颅内压监测可为脱水剂的使用提供更加安全、准确的治疗方案,结合患者颅内压水平决定甘露醇使用频次,减少并发症的产生,从而改善患者的临床预后。
综上所述,通过对高血压脑出血患者应用连续性动态颅内压监测,可对治疗过程中脱水药物的使用、手术时机的选择提供可靠的临床依据,减少因甘露醇使用产生的并发症,改善患者的临床预后,值得临床推广应用。未来有望在脑出血患者深入探索基于连续性动态颅内压监测的诊治流程,以便对高血压脑出血患者提供个体化的治疗。
[参考文献]
[1]van Asch CJ,Luitse MJ,Rinkel GJ,et al. Incidence,case fatality,and functional outcome of intracerebral haemorrhage over time,according to age,sex,and ethnic origin:a systematic review and meta-analysis[J]. Lancet Neurol,2010,9:167-176.
[2]Harary M,Dolmans RGF,Gormley WB. Intracranial Pressure Monitoring-Review and Avenues for Development[J]. Sensors,2018,18(2):465.
[3]Zhang X,Medow JE,Iskandar BJ,et al. Invasive and noninvasive means of measuring intracranial pressure:a review[J]. Physiol Meas,2017,38:143-182.
[4]Smith M. Monitoring intracranial pressure in traumatic brain injury[J]. Anesth Analg,2008,106:240-248.
[5]Ma H,Guo ZN,Liu J,et al. Temporal Course of Dynamic Cerebral Autoregulation in Patients With Intracerebral Hemorrhage[J]. Stroke,2016,47:674-681.
[6]Reinhard M,Neunhoeffer F,Gerds TA,et al. Secondary decline of cerebral autoregulation is associated with worse outcome after intracerebral hemorrhage[J]. Intensive Care Med,2010,36:264-271.
[7]Rincon F,Mayer SA. Intracerebral hemorrhage:clinical overview and pathophysiologic concepts[J]. Transl Stroke Res,2012,3:10-24.
[8]Chesnut R,Videtta W,Vespa P,et al. Intracranial pressure monitoring:fundamental considerations and rationale for monitoring[J]. Neurocrit Care,2014,21(Suppl 2):S64-S84.
[9]王文德. 持续颅内压监测在高血压脑出血手术时机及甘露醇用量调控中的应用[J]. 中国实用神经疾病杂志,2017,20(3):108-110.
[10]何 川,陈慎之,潘建南,等. 高血压脑出血患者应用持续颅内压监测的临床意义[J]. 中国实用神经疾病杂志,2016,19(18):1-3.
[11]陈劲飞,肖化选,钟素雯,等. 持续颅内压监测联合NIHSS量表在高血压脑出血患者的应用[J]. 新医学,2016,47(6):393-396.
[12]祝 涛,安晓静,金昌洙. 持续颅内压监测在高血压脑出血的个体化治疗中的应用[J]. 滨州医学院学报,2014,37(3):189-193、237.
[13]李 想,陈新生. 持续有创颅内压监测在高血压脑出血治疗中的应用[J]. 安徽医药,2013,17(5):825-827.

