微波消解-原子荧光光谱法测定鸡蛋各组分中硒含量
孙亚波,夏芳芳,唐婧,张平,汪建飞
(安徽科技学院资源与环境学院,安徽滁州233100)
硒在自然环境中是普遍存在的元素之一,随着人们对硒元素研究的不断深入,从2003年国家标准[1]中规定硒为食品中污染物到2012年国标[2]中取消了对硒的限量规定,使得人们逐渐认识到硒的摄入量对人体的健康有着紧密的联系,摄入量过少会引起各种不同程度的疾病[3-5]。临床医学研究证明,低硒或缺硒都会威胁人类健康和生命,如癌症、胃病、放化疗疾病、视力、甲状腺疾病、生殖系统疾病等[6-7]。据不完全统计,全世界范围内有大部分的土地面积属于缺硒地区,我国有72%的地区和人口存在缺硒状况[8-9],缺硒已成为当代社会人类健康发展的重要限制因素之一。世界卫生组织(World Health Organization,WHO)和世界粮农组织(Food and Agriculture Organization of the United Na tions,FAO)对人体日硒摄入量推荐的安全范围为50μg~400 μg,中国营养学会推荐成人每天摄入量为50 μg~250 μg[10-13]。因此,科学补硒刻不容缓,食品是人们日常生活中补硒的主要来源,鸡蛋则是人们饮食生活中最常见的食物之一,参照国家食品标准中富硒食品的标准来研究富硒鸡蛋的安全性,合理控制鸡蛋中硒含量就显得极其重要,并对人们生活有着切合实际的意义。
目前测定硒的方法有紫外分光光度法[14-15]、荧光法[16]、原子吸收法[17-19]、气相色谱法[20-21]、电化学法[22-23]等。氢化物发生—原子荧光法[24-27]具有高的选择性和灵敏度,近年来发展迅速,在食品和医药卫生领域中的应用日益广泛[28]。微波消解作为当前新的样品制备手段,具有穿透力强的优点,可以直接作用于样品内部,加热快、升温高、消解能力强,整个消解过程消耗的试剂量少,降低了空白值,避免了处理过程中挥发的损失和样品的污染,样品的回收率试验效果好,也提高了分解的准确度和精密度。本研究将微波消解和原子荧光法结合起来应用于鸡蛋各组分中硒含量的检测,以期为鸡蛋中硒含量的检测提供新的方法。
1 材料与方法
1.1 材料与试剂
硝酸(优级纯)、盐酸(优级纯)、硒标准储备液(1 000 μg/mL):国家标准物质研究中心;过氧化氢(30%)、硼氢化钾、铁氰化钾溶液(100 g/L)、试验用水为超纯水(电导率18 MΩ·cm),以上试剂均为分析纯:阿拉丁试剂公司;普通鸡蛋:当地市场;营养鸡蛋:凤阳县化喜科技养殖有限公司。
XT-9800型多用预处理加热仪:上海新拓分析仪器科技有限公司;Jupiter-B多通量微波消解/萃取系统:上海新仪微波化学科技有限公司;PF3原子荧光光度计:北京普析通用仪器有限公司;超纯水装置(Labonova Direct):Think-lab 公司。
1.2 仪器工作条件
原子荧光光度仪器工作条件设置见表1所示。
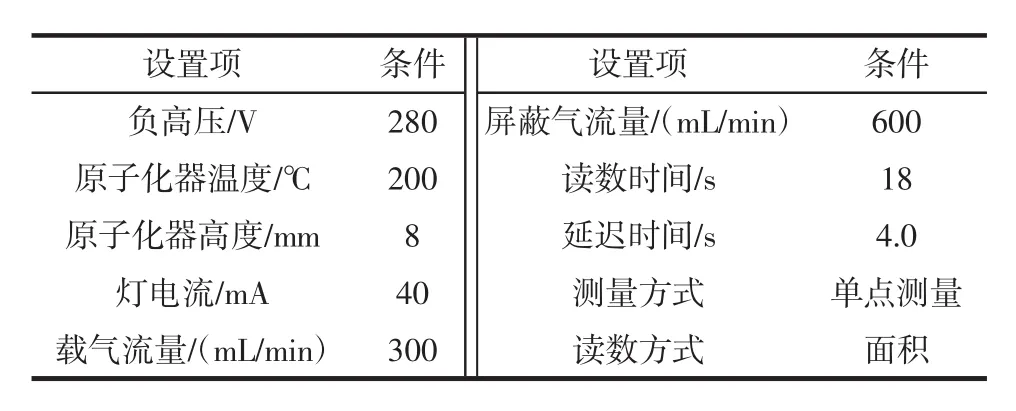
表1 原子荧光光度仪的工作条件Table 1 The conditions of atomic fluorescence spectrometer
1.3 标准曲线的绘制
取硒标准使用液0.1 μg/mL至25 mL容量瓶,标准溶液浓度梯度分别为 0.000 4、0.004、0.008、0.016、0.032、0.08μg/mL。以此取10 mL溶液至离心管中,添加2 mL盐酸(优级纯)和1 mL铁氰化钾溶液摇匀,待测。
1.4 样品前处理
取新鲜鸡蛋,将蛋壳、蛋黄和蛋清分离,称取待测试样0.2 g(精确到小数点后4位)分别放置于微波消解罐内。其中,放置蛋壳的消解罐内直接加入10 mL硝酸进行预处理;放蛋清的消解罐内加入8 mL硝酸和1 mL过氧化氢进行预处理;放蛋黄的消解罐内加入10 mL硝酸和2 mL的过氧化氢进行预处理。摇晃均匀待消解罐内气体散尽后将消解罐放置至反应转子上按设定的程序进行消解,微波消解仪要在使用前预热20 min。程序运行结束后,待消解仪器显示屏上气压为0,温度低于60℃时方可取出反应装置,待反应装置冷却一段时间至室内温度时,可将消解罐取出放置于赶酸架上150℃赶酸至2 mL左右取下加入5 mL盐酸(6 mol/L)溶液,继续放置到加热板上加热赶酸至溶液变为清亮透明无色并伴有白烟出现,将消解罐取下,冷却后用去超纯水定容至25 mL容量瓶中,待测,同时做空白试验。微波消解仪器设置条件如表2所示。
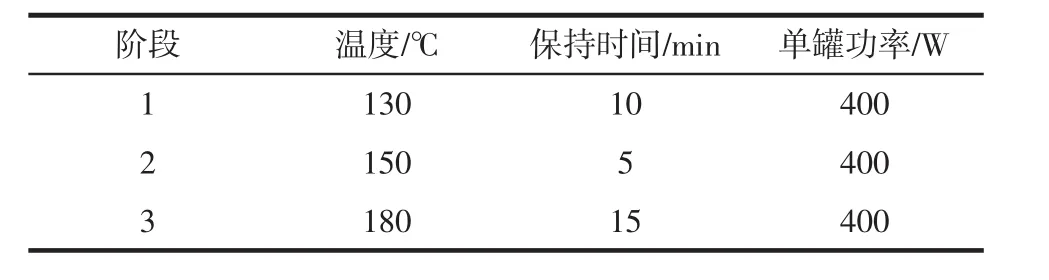
表2 微波消解程序Table 2 The conditions of microwave instrument
1.5 样品测定
微波消解后定容至25 mL容量瓶,取10 mL溶液放置到原子荧光仪的离心管中,向离心管中添加2 mL优级纯的盐酸和1 mL铁氰化钾溶液混合摇匀待测。其中,原子荧光分析中载流溶液为5%浓度的盐酸溶液,还原剂为10 g/L浓度的硼氢化钾溶液。
2 结果与讨论
2.1 基本原理
试验样品经酸加热消解后,通过加热板赶酸冷却后,在6 mol/L的盐酸介质中,将试样中的六价硒还原成四价硒,然后再通过用硼氢化钾溶液作为还原剂,将样品中的四价硒在盐酸介质中还原成硒化氢,再由载气和氩气带入原子化器中进行原子化,在原子化仪器中的硒空心阴极灯照射下,可以使得硒原子产生荧光,其荧光强度与硒含量成正比。
2.2 原子荧光试验条件的考察
2.2.1 负电压的选择
试验中考察不同的负高压对荧光强度的影响,其变化曲线如图1所示。
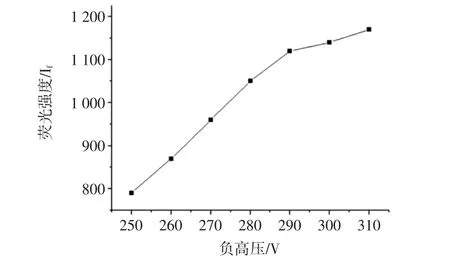
图1 负高压对硒荧光强度的影响Fig.1 Effects of high negative voltage on Ifof Se
从图1可以看出,荧光强度随着负高压的增大而增强,但噪声也随之增大。试验结果表明,当负高压超过290 V后,荧光强度与Se的浓度反而不呈线形,因此选择负高压为280 V。
2.2.2 灯电流的选择
试验中考察不同的灯电流对荧光强度的影响,其变化曲线如图2所示。

图2 灯电流对硒荧光强度的影响Fig.2 Effects of lamp current on Ifof Se
由图2可知,随着灯电流的增加,硒的荧光强度增大,但是当灯电流超过40 mA,反而强度下降,可能是由于发生自吸导致。从灯的寿命和强度综合考虑,选择40 mA作为最佳电流。
2.2.3 原子化器高度的选择
原子化器的高度是试验中重要的参数,高度较高虽然背景噪音较小但是相应荧光强度较弱,高度过低噪音较大,综合考虑,在本试验中选取原子化器的观测高度为8 mm最为合适。
2.2.4 载气、屏蔽气流量的选择
样品与还原剂反应后生成的气态氢化物由载气携带进入原子化器,因此必须考察载气流量对试验的影响,结果见图3。
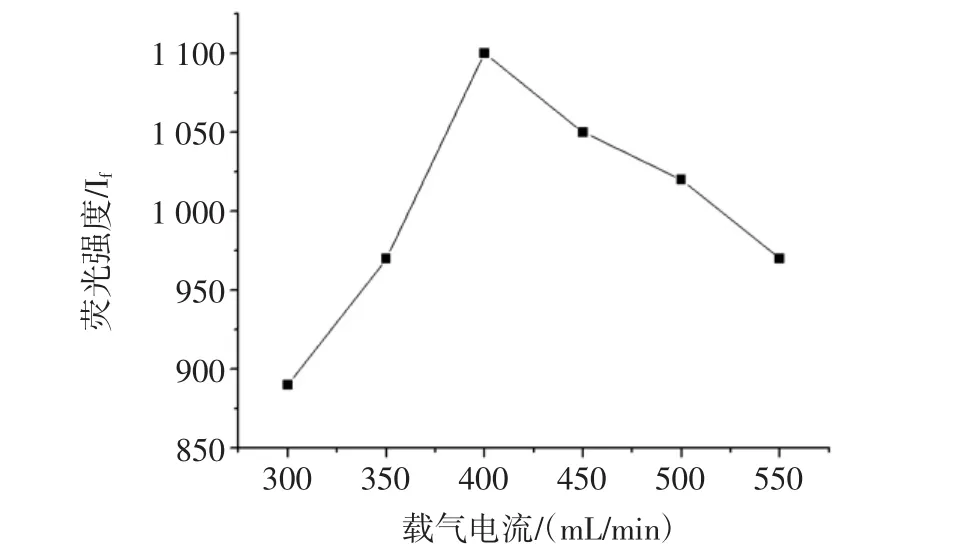
图3 载气流量对硒荧光强度的影响Fig.3 Effects of flow rate of carrier gas on Ifof Se
从图3可见,随着载气流量的增大,硒的荧光强度也随着增加。当载气流量过大,对气态氢化物的浓度有所稀释,其强度反而下降。因此最合适的载气流量为400 mL/min。
屏蔽气在这里可以起到防止气态原子在原子化器中扩散,增加荧光强度的作用,试验考察不同流量屏蔽气下荧光强度的影响,结果见图4。
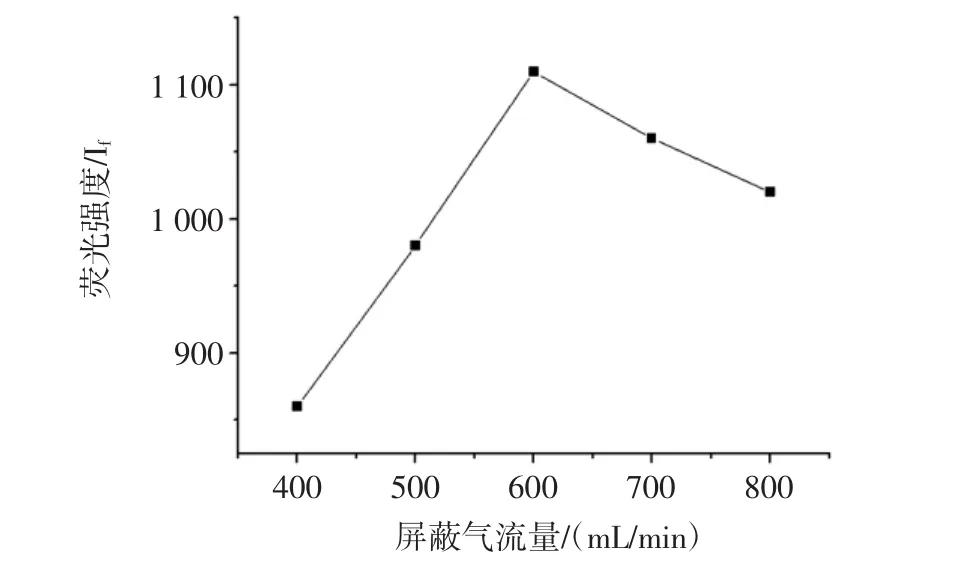
图4 屏蔽气流量对硒荧光强度的影响Fig.4 Effects of flow rate of Ar on Ifof Se
从图4可知,当氩气屏蔽气的流量为600 mL/min,试验效果最佳。
2.2.5 载流及酸度的选择
分别采用盐酸、硝酸和硫酸作为酸介质,考察不同酸介质对试验结果的影响。硝酸本身氧化性太强,容易氧化样品,硫酸具有较强的腐蚀性,从试验的结果来看,最合适作为载流的是盐酸,其试验效果最佳。不同浓度盐酸对荧光强度的影响结果见图5。
从图5可知,当盐酸浓度较小时,容易出现峰拖尾现象,而当盐酸浓度为5%时,硒的荧光强度信号趋于稳定。因此,选择5%盐酸作为酸度介质。
2.2.6 硼氢化钾浓度的选择
考察了不同浓度的还原剂硼氢化钾浓度对荧光强度的影响,见图6。
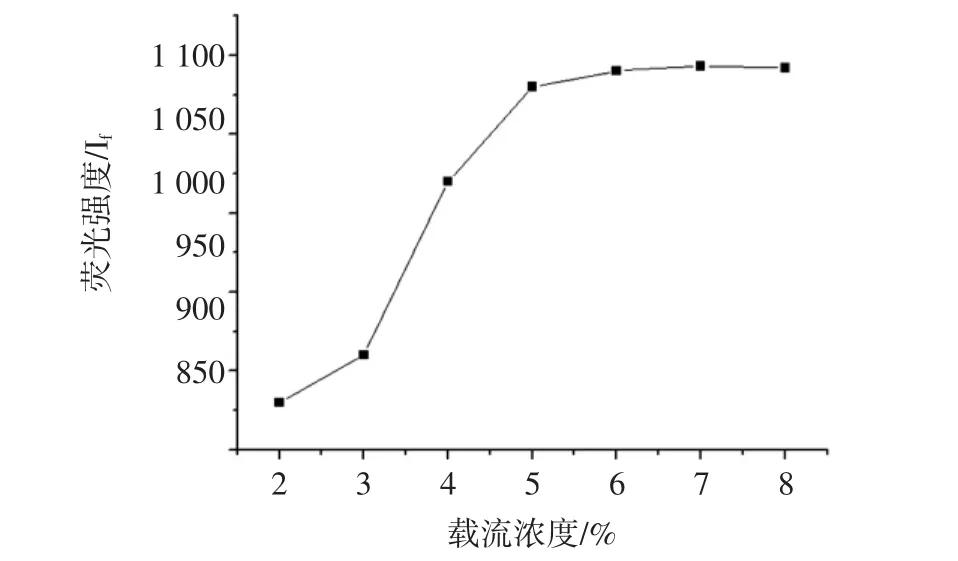
图5 盐酸浓度对硒荧光强度的影响Fig.5 Effects of concentration of HCl on Ifof Se

图6 硼氢化钾浓度对硒荧光强度的影响Fig.6 Effects of concentration of KBH4 on If of Se
如图6所示,随着硼氢化钾用量的增加,其荧光值强度随之降低,是因为产生的大量氢气对硒原子蒸气的稀释作用而造成的[29],因在浓度为10 g/L~15 g/L之间,本试验选取10 g/L硼氢化钾溶液作为最佳条件。
2.2.7 共存离子干扰的影响
鸡蛋中含有较多的锰、钙、铜、锌、镁、铁等元素,在本试验中,考察不同元素对硒含量测定的干扰,试验结果表明,当钾、钠、镁等碱金属、碱土金属元素是硒的5 000倍不会对硒的测量产生干扰,当锰、锌、铁元素是硒的100倍不会对对硒的测量产生干扰,在这里干扰来自于铜元素,在后续试验中会加入掩蔽剂排除干扰。
2.3 方法与分析结果
2.3.1 线性范围
在优化的试验条件下考察硒标准溶液的线性范围,硒的浓度在 0.000 4 μg/mL~0.08 μg/mL 之间呈良好线性关系,线性方程为y=37 349x-2.281 7,其中相关系数达到0.999 9。
2.3.2 精密度
按照仪器工作条件和样品处理条件对浓度为10、20、30、40、50 μg/L 的硒标液重复测定 5 次,对方法的精密度进行试验,从数据的标准偏差和变异系数表明本方法具有良好的试验重现性。见表3。
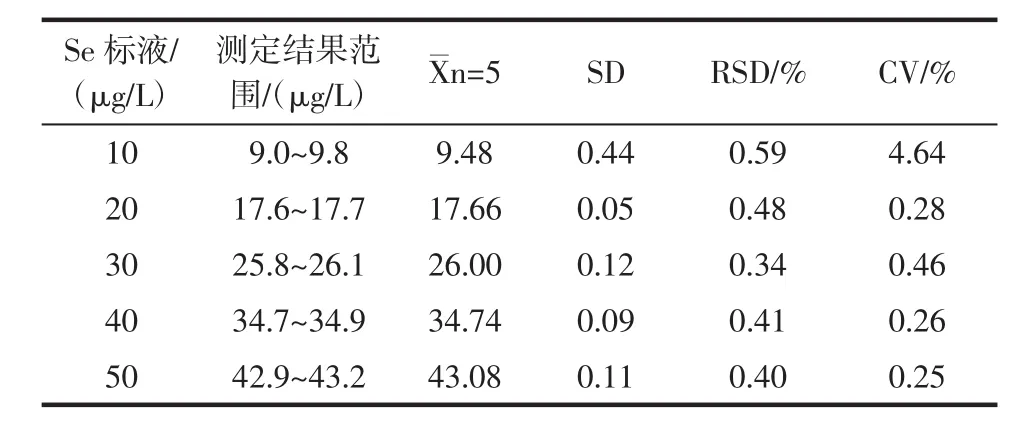
表3 原子荧光法测定Se的精密度Table 3 The precision of the Se by atomic fluorescence method
2.3.3 样品测定
样品测定结果见表4。
对于鸡蛋的前处理消解中,采用了不同的方法(具体方法见1.4所述),一是蛋壳中碳酸钙与酸发生反应后能迅速消解;二是蛋黄中含有成份较复杂,消解中添加更多硝酸和过氧化氢能使消解完全。
将样品溶液按照试验方法测定和加标回收试验,向鸡蛋各组分中加入Se标准溶液,按照蛋清、蛋黄、蛋壳依次加入0.03 mL的标液并各自重复3次并对实际值取均值(如表4),样品Se的回收率为93.5%~107.8%,试验所测富硒鸡蛋中的硒含量在0.728 μg/g~0.750 μg/g之间。
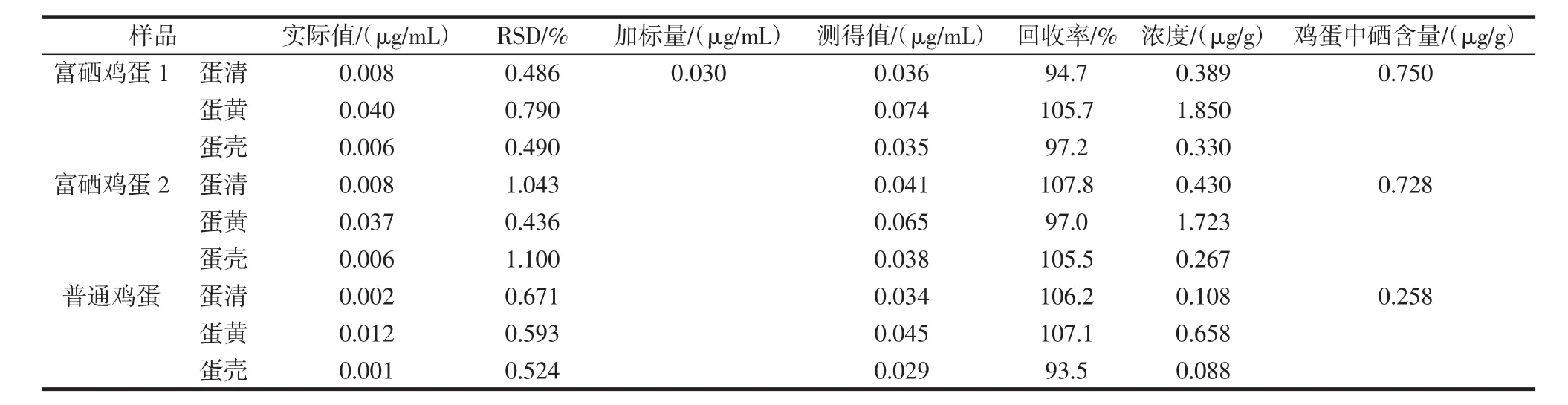
表4 样品测定结果(n=3)Table 4 Determination results of samples(n=3)
通过对富硒鸡蛋1、2两个样品各组分之间的测定,可以得到鸡蛋各组分之间硒含量的差异。鸡蛋1、2两样品之间各部位硒含量显著性差异较小,鸡蛋中蛋清、蛋黄和蛋壳三者之间显著性差异较大,三者之间硒含量比较为蛋黄>蛋清>蛋壳,且蛋黄和蛋清硒含量中质量比约为4∶1,其中蛋黄中硒含量明显高于蛋清和蛋壳中硒含量,而蛋清和蛋壳两者之间硒含量几乎接近。普通鸡蛋与富硒鸡蛋相比较而言,鸡蛋中各组分之间硒含量差异性显著,且富硒鸡蛋与普通鸡蛋中含硒量质量比约为3∶1。
此次试验中所用的富硒鸡蛋是通过喂养富硒饲料得到的,利用原子荧光法检测出鸡饲料中的硒含量在 2.90 μg/g~3.08 μg/g之间。见表 5。
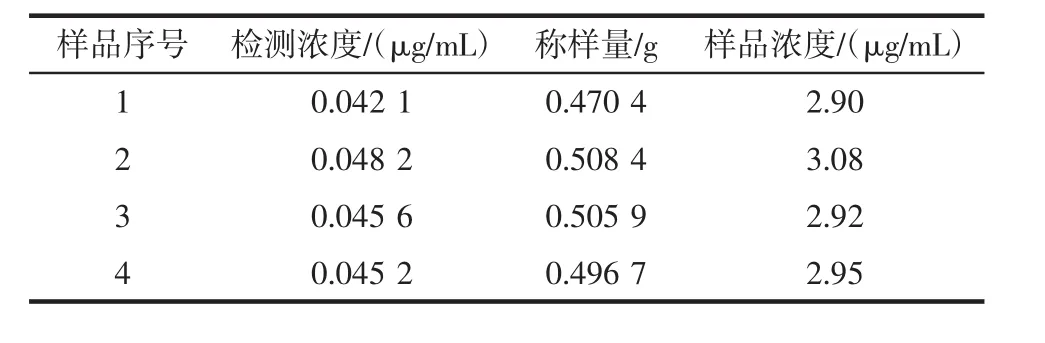
表5 鸡饲料中硒含量检测结果Table 5 Determination of selenium content in chicken feed
3 结论
采用方便快捷的微波消解进行前处理,这种方法可将样品消解完全,相比于传统前处理方法,这种方法大大降低了处理过程中硒的流失。检测技术选用原子荧光分光法,仪器价格便宜,适用性强,操作简捷。从结果来看,通过饲料喂养的方法确实可以增加鸡蛋中的硒含量。该方法分析结果准确,可以应用于鸡蛋各组分中硒含量的检测,并有望用于更多富硒产品的检测研究。
参考文献:
[1]北京市卫生防疫站,卫生部食品卫生监督所和中国预防医学科学院营养与食品卫生研究所.GB/T 5009.93-2003食品中硒的测定[S].北京:中国标准出版社,2003
[2]中华人民共和国卫生部.GB 2762-2012食品安全国家标准食品中污染物限量[S].北京:中国标准出版社,2012
[3]朱传风,贾三春.甘肃省土壤中硒背景值的调查研究[J].甘肃环境研究与检测,1991,14(2):4-7
[4]ABDULAH R,MIYAZAKI K,NAKAZAWA M,et al.Chemical forms of selenium for cancer prevention[J].J Trace Elem Med Bio,2005,19(2):141-150
[5]王梅,张红香,邹志辉,等.原子荧光光谱法测定富硒螺旋藻片中不同形态、价态的硒[J].食品科学,2011,32(6):179-182
[6]Vivtma J,Valkella E,Alfthan G,er al.Serum Selenium and Risk of cancer A prospective follow-up of nine years[J].Cancer,1987,60:145-149
[7]王家明,王砚英.饲料加硒对鸡蛋硒含量的影响 [J].食品科学,1993,14(10):46-47
[8]周漴棠,谢英彪.来自微量元素的报告[M].北京:人民军医出版社,2005:258
[9]徐文军.顺序注射氢化物发生-原子荧光光谱法测定富硒鸡蛋中的硒[J].食品科学,2007,28(8):318-321
[10]祁嘉义.临床元素化学[M].北京:化学工业出版社,2000
[11]田园,朱超,范志影,等.微波消解-原子荧光光谱法测定鸡蛋中的硒[J].分析仪器,2012(1):105-108
[12]李莹,张丽,崔小军,等.原子荧光法测定营养鸡蛋中的微量硒[J].食品研究与开发,2002,23(6):97-98
[13]TAYKIR J B,MARCHELLO M J,FINLEY J W,et al.Nutritive value and display-life attributes of selenium-enriched beef-muscle foods[J].Journal of Food Composition and Analysis,2008,21:183-186
[14]刘有芹,杨庆辉,黄函,等.紫外分光光度法测定枸杞子、陈皮、生姜中硒含量[J].理化检验(化学分册),2010,46(3):329-330
[15]李岱.分光光度法测定香菇中硒的研究[J].光谱实验室,2000,17(6):656-657
[16]熊远福,刘军鸽,文祝友,等.荧光法测定水样中硒(Ⅳ),硒(Ⅵ)和有机硒[J].分析科学学报,1999,15(2):154-157
[17]冯尚彩,韩长秀.塞曼石墨炉原子吸收法直接测定血清中的硒[J].分析实验室,2002,21(4):52-53
[18]刘恒,马盼,黄婷,等.氢化物发生-原子荧光光谱法测定富硒杂粮中的有机硒和无机硒[J].食品科学,2014,35(10):170-173
[19]Omemark U,Pettersson J,Olin A.Determination of total selenium in water by atomic-absorption spectromrtry after hydride generation and preconcentration in a cold trap system[J].Talanta,1992,39(9):1089-1096
[20]农晋琦,蔡端瑞,欧阳政.硒半胱氨酸和硒胱氨酸的间接气相色谱测定-溴化氢-气相色谱法[J].色谱,1994,12(1):28-31
[21]Iscioglu B,Henden E.Determination of selenoamino acids by gas chromatography-massspectrometry[J].AnalyticaChimicaActa,2004,505:101-106
[22]杨培慧,政志雯,冯德雄,等.硒代胱氨酸和硒代蛋氨酸电化学检测得比较[J].分析化学,2003,32(2):194-197
[23]曹璨,吴志刚.微波消解—原子荧光光谱法测定鸡蛋中痕量硒[J].光谱实验室,2008,25(5):796-800
[24]肖辉,吴向阳,仰榴青,等.氢化物-原子荧光法测定姬松茸子实体中硒含量[J].食品科学,2010,31(10):247-249
[25]CAPEIO J L,FERNANDEZ C,PEDRAS B,et al.Trends in selenium determination/speciation by hyphenated techniques based on AAS or AFS[J].Talanta,2006,68(5):1442-1447
[26]SEHLOSKE L,WALDNER H.Marx optimization of sample pretreatraent in the HG-AAS selenium analysis[J].Analytical Biochemistry,2002,372(2):700-704
[27]SMRKOL J P,STIBILJ V.Determination of selenium in vegetables by hydride generation atomic fluorescence spectrometry[J].Analytica Chimica Acta,2004,512(1):11-17
[28]李明远.微波消解-氢化物原子荧光光谱法测定食品中的微量元素硒[J].光谱实验室,2007,24(3):618-620
[29]李连平,范威,庄峙夏,等.蔬菜中硒总量及形态的氢化物发生-原子荧光光谱测定方法[J].光谱学与光谱分析,2008,28(12):2975-2978

