干预前后美罗培南使用情况分析及药学干预效果评价Δ
武明芬,贾自力,崔喜凤,李春钰,郭 哲
(北京丰台医院药剂科,北京 100071)
当前,细菌耐药已成为全球公共健康领域的重大挑战,也是各国政府和社会广泛关注的世界性问题[1]。细菌耐药问题已经从卫生领域扩大到了政治、经济领域[2]。我国是抗菌药物的生产和使用大国,细菌耐药问题日益突出[3-5]。原国家卫生计生委高度重视抗菌药物临床应用管理,积极应对细菌耐药带来的挑战,努力提高抗菌药物科学管理水平。自2012年全国抗菌药物专项整治活动以来,我国逐步加强对抗菌药物的使用管理。2016年8月25日,原国家卫生计生委制定了《遏制细菌耐药国家行动计划(2016—2020年)》[6];2017年1月,组建了“抗菌药物临床应用与细菌耐药评价专家委员会”,对我国用于预防和治疗感染的抗菌药物进行临床综合评价,并对我国抗菌药物临床应用、细菌耐药形势、感染性疾病谱及细菌耐药经济负担等进行研究。碳青霉烯类作为一种广谱抗菌药物深受临床青睐,其的使用越来越多,造成近年来细菌对其的耐药率越来越高[7]。2017年3月,原国家卫生计生委办公厅发布《进一步加强抗菌药物临床应用管理遏制细菌耐药的通知》,强化对碳青霉烯类抗菌药物以及替加环素等药物的管理[8]。碳青霉烯类作为特殊使用级抗菌药物,一直是北京丰台医院(以下简称“我院”)监测的重点。2016年对我院抗菌药物的系统监测结果发现,美罗培南的使用量出现明显异常,其使用量排序在抗菌药物中居第2位,我院高度警惕,医务处联合医院感染控制委员会与药事管理委员会共同制订了一系列管控措施,2017年1月药师开始对美罗培南的使用进行干预。故现回顾性对比分析药学干预前后我院住院患者美罗培南的使用情况,以期为后续管理提供依据,最大限度减少耐药菌的出现。
1 资料与方法
1.1 资料来源
通过医院信息系统,检索2016—2017年我院使用美罗培南的出院患者病案号,共1 130例,以2017年1月1日为时间节点,分为干预前和干预后(其中干预前600例,干预后530例)。按照检索到的病历号,从病案室查询所有病历资料,记录与美罗培南有关的患者信息、疾病信息、用药信息和实验室检查信息。
1.2 方法
根据《美罗培南使用点评医嘱表》和病历信息,设计制作《北京丰台医院美罗培南使用信息统计表》,按照病历记录填写记录表格,包括登记患者的基本信息(姓名、性别、年龄、体质量、入院科室及病历号)、疾病信息(诊断、住院日期、住院时间及过敏史等)、美罗培南使用信息(用药原因、用法与用量、用药起止时间、医嘱权限、是否紧急使用、是否会诊、联合用药信息及用药金额)、用药前后病原学检查结果(微生物送检率、细菌培养结果、耐药菌及药物敏感试验等)、用药指征(体温、血液检查、生化检查、血沉、聚合酶链式反应及肝肾功能等)和用药结果(感染控制清况、对原患疾病的影响及治疗结果等)。采用Excel 2013软件进行数据汇总分类、统计分析,从抗菌药物使用评价指标、用药合理性评价及经济学效益等3个维度来评价美罗培南的药学干预效果。
1.3 评价标准
1.3.1 抗菌药物使用评价指标:选取用药频度(defined daily dose system,DDDs)、抗菌药物使用强度(antibiotics use density,AUD)、使用量、使用率和使用量排序等5个指标评价抗菌药物使用情况[9]。依照药物利用评价分析方法,采用世界卫生组织推荐的限定日剂量(defined dialy dose,DDD)[参考《新编药物学》(17版)、《中华人民共和国药典·临床用药须知》(2010版)[10]和药品说明书确定DDD值]计算美罗培南的DDDs。DDDs=某药的总用量(g或mg)/该药的DDD,其值越大,说明临床对该药的使用频率越高,药物应用就越广泛。AUD=DDDs×100/[同期出院患者人数×同期患者平均住院时间(d)]。
1.3.2 用药合理性评价指标:从药物利用指数(drug utilization index,DUI)、微生物送检率、药物敏感试验结果、处方医师权限、会诊率、用法与用量及联合用药等7个方面评价用药合理性[11]。DUI=DDDs/实际用药时间(d),DUI>1.0,说明临床实际使用日剂量>DDD,存在不合理用药倾向;DUI接近1.0,说明临床实际使用日剂量接近DDD,表明用药合理。
1.3.3 经济学评价指标:从患者平均住院费用、年销售金额、限定日费用(defined daily cost,DDC)、药占比及住院时间(d)等5个方面评价药物经济性[12]。DDC=某药年销售金额/该药的DDDs。
1.4 药学干预措施
(1)参照美罗培南的药品说明书、临床指南和药物专论,制订美罗培南合理使用标准。(2)执行抗菌药物分级管理制度、处方医师权限制度和特殊使用级抗菌药物会诊制度。(3)成立美罗培南医嘱点评专项小组,每月对美罗培南的使用进行专项点评。(4)抗感染专业临床药师同感控中心人员一起进行药学专项查房,对不合理用药进行及时干预。
1.5 统计学方法
采用SPSS 19.0统计学软件进行数据处理,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 干预前后患者的基本情况比较
1 130例患者中,男性592例,女性538例;年龄19~94岁。干预前后患者的基本情况比较,差异无统计学意义(P>0.1),见表1。

表1 干预前后患者的基本情况比较Tab 1 Basic information of patients before and after intervention
2.2 干预前后美罗培南抗菌药物使用指标评价结果
与干预前比较,干预后美罗培南的DDDs、AUD分别降低14.80%、22.09%,使用量、使用率分别降低14.81%、12.84%;干预前,美罗培南的使用量排序在全院抗菌药物中居第2位,干预后降至第15位,上述差异均有统计学意义(P<0.01),见表2。按季度对美罗培南的使用量进行汇总分析,结果显示,干预前其使用量每季度都在递增,干预后迅速降低,逐渐降至合理水平,见图1。
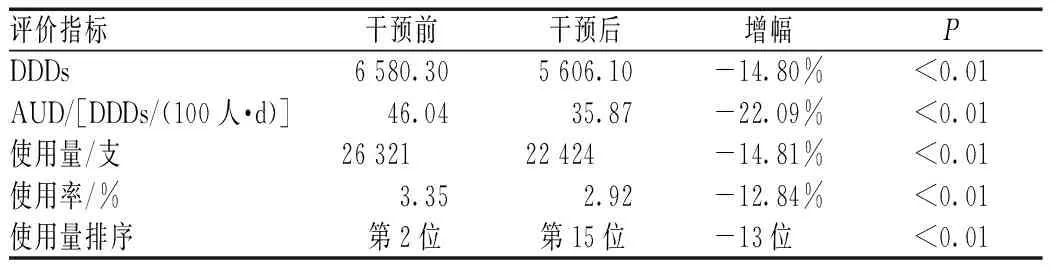
表2 干预前后美罗培南抗菌药物使用指标评价结果Tab 2 Results of evaluation indices of antibiotics on meropenem before and after intervention
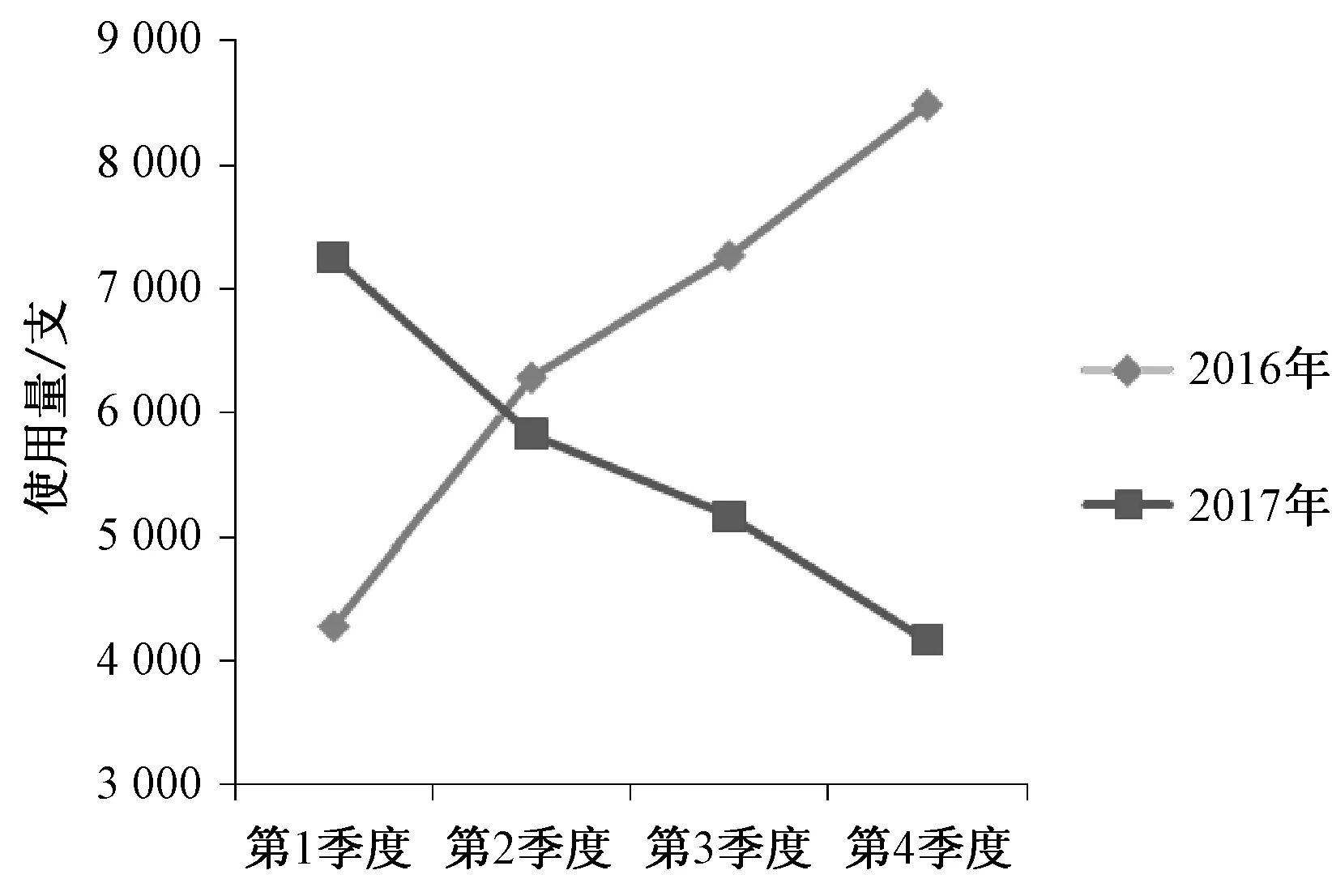
图1 干预前后各季度美罗培南使用量比较Fig 1 Comparison of usage amount of meropenem at different quarters before and after the intervention
2.3 干预前后美罗培南用药合理性评价结果
干预前,美罗培南的DUI为1.6,存在明显的不合理用药倾向,干预后降为1.05,接近于1,用药趋于合理;干预后,微生物送检率和药物敏感试验率分别提高了41.13%和46.38%,但仍需进一步加强;干预后,处方医师权限符合率达100%,用药前会诊率也达到了89.56%;干预前后用药时间基本无变化,见表3。美罗培南和丙戊酸钠联合应用能降低后者的血药浓度,引起癫痫发作,应特别提醒临床医师注意,干预后还存在两者联合应用的情况。

表3 干预前后美罗培南用药合理性评价结果Tab 3 Results of rationality evaluation of meropenem before and after intervention
2.4 干预前后美罗培南药物经济学评价结果
干预后,患者平均住院费用减少了1 324.61元,药占比、DDC分别下降18.35%、20.22%,美罗培南年销售金额降至233.74万元,降幅达32.03%,与干预前的差异均有统计学意义(P<0.05),见表4。干预前,美罗培南的销售金额随季度呈升高趋势,干预后直线下降,回归合理范围,见图2。
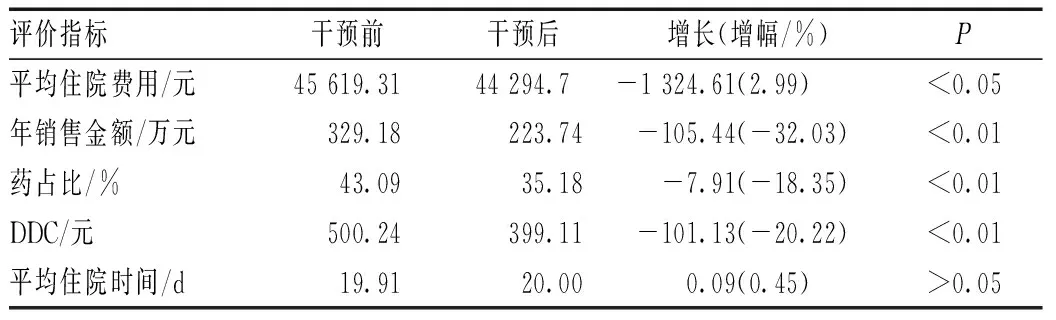
表4 干预前后美罗培南药物经济学评价结果Tab 4 Results of economic evaluation of meropenem before and after intervention
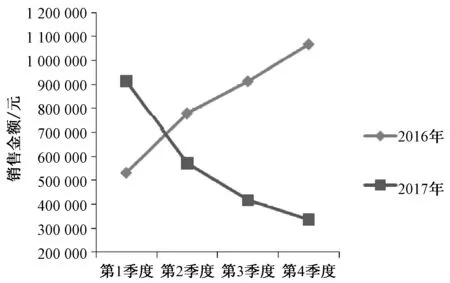
图2 干预前后美罗培南各季度销售金额变化趋势Fig 2 Variation trends of consumption sum of meropenem at different quarters before and after the intervention
3 讨论
3.1 药学干预措施评价
作为特殊使用级抗菌药物,2016年我院美罗培南的使用量排序在抗菌药物中居第2位,显然有不合理使用的可能。我院定期监测抗菌药物的DDDs和销售金额,对超长使用的药品进行预警,制订专项药学干预措施加强管理。干预后,抗菌药物中,美罗培南的使用量排序降至第15位,干预效果显著。干预后,美罗培南的AUD、DDDs、使用量和使用率均显著降低,用药合理性、微生物送检率和药物敏感试验率都有大幅提升,用药前会诊率达到100%,联合用药率进一步降低,表明美罗培南的使用日趋规范,销售金额、DDC和药占比的降低极大地减轻了患者的经济负担。针对美罗培南的药学干预措施可以为其他药品的管理提供方向和参考依据。
3.2 美罗培南使用管理存在的不足和改进措施
3.2.1 微生物送检率和药物敏感试验率仍不达标,应进一步加强管理:原国家卫计委《进一步加强抗菌药物临床应用管理遏制细菌耐药的通知》[8]要求,接受特殊使用级抗菌药物治疗的住院患者用药前微生物送检率应不低于80%。干预后,微生物送检率有大幅提升,但还未达到80%,尤其脑外科和普外科的微生物送检率比较低,目前只有50%~60%,今后应加强管理,使微生物送检率达标。神经外科和消化内科很多病例没有药物敏感试验结果,经验性用药率较高,甚至还存在不根据药物敏感试验结果选药的情况,造成耐药菌的产生。今后,临床药师查房时应重点检查各科室用药前微生物送检及药物敏感试验情况,要求在规定时间留取标本送检,并依据细菌
培养及药物敏感试验结果及时调整药物;提醒医师不宜盲目全覆盖用药,并在处方前置审核系统做好预警,一旦有使用美罗培南的申请,药师可及时对用药合理性、处方医师权限和会诊记录进行检查。
3.2.2 避免无循证依据联合用药:美罗培南不易发生神经系统的不良反应,可用于产超广谱β-内酰胺酶细菌引起的中枢神经系统感染[13]。临床上,很多医师更倾向于联合应用碳青霉烯类与氨基糖苷类抗菌药物治疗产超广谱β-内酰胺酶细菌引起的感染,我院脑外科也存在使用美罗培南与氨基糖苷类抗菌药物联合治疗颅内感染的情况,但目前仍无临床证据表明联合用药的疗效是否优于单用碳青霉烯类抗菌药物[14]。药师应对不必要的联合用药及时干预,避免无循证医学的联合用药。
3.2.3 避免美罗培南与丙戊酸钠联合应用:国内外文献均有报道,美罗培南与丙戊酸钠联合应用能导致丙戊酸钠血药浓度明显降低,甚至诱发癫痫发作[15-16]。美罗培南的药品说明书也明确禁止其与丙戊酸钠联合应用。两者的相互作用不能通过改变丙戊酸钠的剂量而缓解,临床上使用丙戊酸钠时如确需联合应用美罗培南,可改用卡马西平或苯妥英钠等药物替代[17]。目前,神经外科还存在美罗培南与丙戊酸钠联合应用的情况,药师应提醒医师避免两者联合应用,减少临床不良事件的发生。
综上所述,针对美罗培南的药学干预效果显著,干预措施得当。但还存在不足之处,今后应针对实验室检查和循证用药等方面重点进行药学干预,规范碳青霉烯类抗菌药物的使用,进一步减少耐药菌的产生,合理使用抗菌药物。
[2]Jethwa S.Confronting the growing problem of antibiotic resistance[J].Prescriber,2016,27(2):50-51.
[3]Paterson DL,Van DD.China’s antibiotic resistance problems[J].Lancet Infect Dis,2017,17(4):351-352.
[4]夏培元.抗菌药物耐药的管理——研究现状和展望[J].药物不良反应杂志,2017,19(2):81-83.
[5]胡付品,郭燕,朱德妹,等.2016年中国CHINET细菌耐药性监测[J].中国感染与化疗杂志,2017,17(5):481-491.
[6]遏制细菌耐药国家行动计划:2016—2020年[J].药物不良反应杂志,2016,18(5):398-400.
[7]张艳君,秦琴,李虎,等.耐碳青霉烯类肠杆菌科细菌的分布特点与耐药性分析[J].中华医院感染学杂志,2016,26(2):245-247.
[8]国家卫生计生委办公厅.关于进一步加强抗菌药物临床应用管理遏制细菌耐药的通知[S].国卫办医发〔2017〕10号.2017-02-27.
[9]张楠,陆红柳,杨慧鹃,等.某院碳青霉烯类抗菌药物的临床应用调查与用药合理性评估[J].中国药房,2016,27(29):4047-4050.
[10] 国家药典委员会.中华人民共和国药典·临床用药须知:化学药和生物制品卷[S].2010年版.北京:中国医药科技出版社,2011:697-699.
[11] 陈琳,杨小燕,许小敏,等.加强对碳青霉烯类抗菌药物使用管理的效果评价[J].中华医院感染学杂志,2017,27(8):1897-1900.
[12] 顾红燕,金锐,谢猛,等.药学干预在医院美罗培南不合理使用管理中的作用[J].中国医院药学杂志,2016,36(14):1209-1212.
[13] 唐景云,秦晓林.加强抗菌药物管理对产超广谱β-内酰胺酶肺炎克雷伯菌耐药性的影响[J].海南医学,2016,27(5):753-755.
[14] 潘鹏玉,甄健存.美罗培南在国内外临床指南中的推荐[J].临床合理用药杂志,2015,8(23):180-181.
[15] 黄秀华.注射用美罗培南与丙戊酸钠的药物相互作用分析[J].中国医药指南,2012,10(25):426-427.
[16] 齐晓涟,高冉,韩建,等.癫痫患者抗感染药合理应用案例分析[J].中国药房,2010,21(6):570-572.
[17] 李冬梅,闫赋琴,孙慧萍.碳青霉烯类抗菌药物与丙戊酸存在临床意义的药物相互作用[J].中华医院感染学杂志,2011,21(19):4133-4134.

