艾迪注射液佐治弥漫性大B细胞淋巴瘤的临床观察
,,
弥漫性大B细胞瘤(Diffuse large B cell lump,DLBCL)是非霍奇金淋巴瘤中最常见的一个亚型,具有侵袭性。R-CHOP方案是治疗DLBCL的一线用药方案[1],虽然疗效较好,但副作用也较大。艾迪注射液是一种具有良好抗肿瘤效果的复方中成药制剂,且一定程度上改善肿瘤患者的全身免疫功能[2]。可溶性白细胞介素2受体(sIL-2R)是一种可以和白介素-2结合的免疫抑制剂,其可中和T淋巴细胞周围的IL-2,从而影响T细胞的增值,在DLBCL中具有较高表达,因而其表达水平可作为DLBCL疾病进展的判断依据。本文旨在探究艾迪注射液辅助常规R-CHOP方案治疗DLBCL的疗效及对患者sIL-2R水平的影响。现报道如下。
1 资料与方法
1.1一般资料 选取2016年1月-2017年9月本院收治的89例DLBCL住院患者,均经活检后确诊为弥漫性大B细胞淋巴瘤[3],经骨髓穿刺检验无骨髓侵犯,ZPS评分1-2之间且预计存活期>6个月,可耐受放化疗治疗。排除其它干扰疾病和药物禁忌者,随机数字表法将其分成两组。常规组:44例,男24例,女20例;年龄37~49(42.50±2.50)岁;Ⅲ期淋巴瘤29例,Ⅳ期淋巴瘤15例。联合组:45例,男26例,女19例;年龄39~48(43.50±2.50)岁;Ⅲ期31例,Ⅳ期14例。两组患者一般资料有可比性(P>0.05)。所有患者均签署知情同意书,该研究也得到医院伦理委员会的批准。
1.2方法 常规组:予R-CHOP治疗:第1天用利妥昔单抗注射液(国药准字J20080054,上海罗氏制药有限公司)375 mg/m2,静滴,滴前予5 mg地塞米松防过敏,由慢至快,控制滴速<400 mg/h,第2天开始用环磷酰胺(C)(国药准字H32020857,江苏恒瑞医药有限公司,用法:800 mg/m2,静滴,1d)+阿霉素(H)(国药准字H20041318,浙江海正药业股份有限公司,用法:50 mg/m2,静滴,1d)+长春新碱(O)[国药准字H33020421,上海医药(集团)有限公司华联制药厂,用法:1.4 mg/m2,静滴,1 d]+泼尼松(P)(国药准字H33021207,浙江仙琚制药股份有限公司,用法:60 mg/m2,口服,5d)。21 d为1个疗程,共6个疗程。
联合组:在R-CHOP基础上加用艾迪注射液(国药准字Z52020236,贵州益佰制药有限公司)50 ml加入到250 ml10%葡萄糖溶液中,静滴,1次/d,3周1疗程,共2疗程。
1.3观察指标及判定标准 观察两组近期疗效、血清sIL-2R水平、KPS评分以及不良反应情况。近期疗效参考中国DLBCL诊疗指南[4]:完全缓解(CR):CT检查所有病灶消失,PET检查阴性;部分缓解(PR):CT检查可测量病灶SPD缩小≥50%,无新病灶出现,病变部位个别PET阳性;疾病稳定(SD):CT显示病灶大小无变化,无新病灶出现,PET仍为阳性;进展或复发(PD):CT检查有新病灶出现或原病灶SPD增加≥50%,且PET显示阳性。不良反应主要观察两组患者骨髓抑制情况,包括:白细胞、血小板和血红蛋白含量。治疗前后用Karnofasky评分对患者功能状态进行评分。
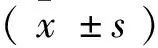
2 结果
2.1近期疗效比较 联合组近期总有效率高于常规组,差异有统计学意义(χ2=5.97,P=0.015)。见表1。
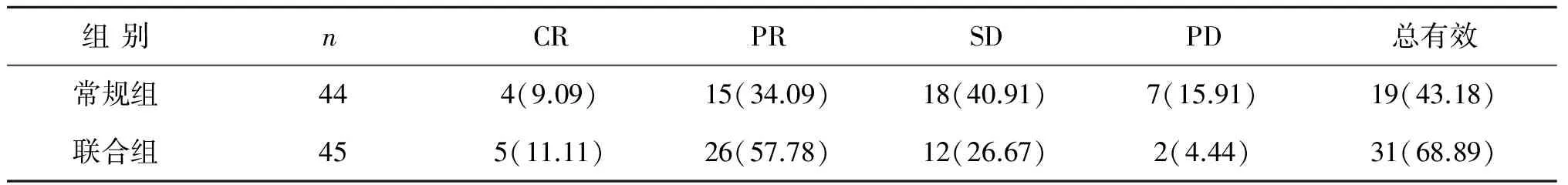
表1 两组患者近期治疗效果比较(n,%)
2.2血清sIL-2R水平 两组治疗后sIL-2R水平均明显降低,且联合组sIL-2R水平明显低于常规组,差异有统计学意义(t=3.33,P=0.001)。见表2。
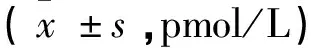
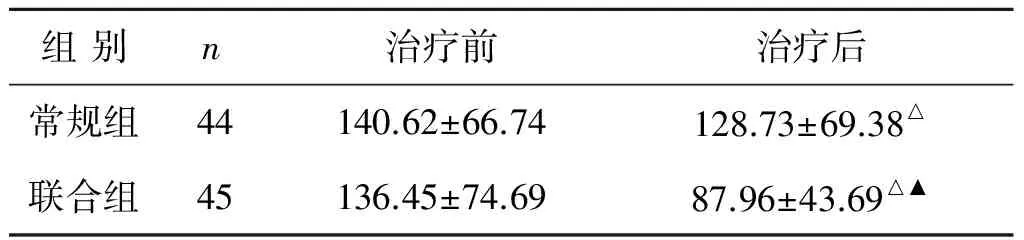
组别n治疗前治疗后常规组44140.62±66.74128.73±69.38△联合组45136.45±74.6987.96±43.69△▲
注:△组内治疗前后比较P<0.01;▲组间治疗后比较P<0.05。
2.3治疗前后两组KPS评分比较 治疗后,两组KPS评分均升高,且联合组高于常规组(t=4.10,P<0.01)。见表3。
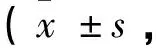
表3 两组治疗前后KPS评分比较分)
注:※治疗前后组内比较P<0.05;*治疗后两组间比较P<0.05。
2.4不良反应 治疗过程中,常规组共有12例患者出现不良反应,其中血小板减少4例,白细胞减少9例,血红蛋白减少12例,不良反应发生率27.27%(12/44)。联合组共有10例患者出现不良反应,其中血小板减少3例,白细胞减少8例,血红蛋白减少11例,不良反应发生率为22.22%(10/45)。差异无统计学意义(χ2=0.31,P>0.05)。
3 讨论
DLBCL原发于淋巴结或淋巴结外,弥漫性生长发展,半数以上患者都有淋巴结外浸染,最常见弥漫于胸腺和骨髓[2]。R-CHOP方案是治疗DLBCL的一线用药方案,其中的利妥昔单克隆抗体对于CD20阳性的中立细胞具有较强的杀伤作用,对大B细胞淋巴瘤治疗预后效果良好,其中环磷酰胺、阿霉素、长春新碱等化疗药有骨髓抑制作用,且副作用较大,需较长时间的用药间隔,使治疗周期延长,疗效降低。艾迪注射液是一种具有良好抗肿瘤效果的复方中成药制剂,其主要成分为斑蝥、人参、黄芪和刺五加,其中人参具有益气补血的效果,黄芪中的黄芪多糖和刺五加中的多糖都具有增强人体免疫功能的效果,主药斑蝥主要有效成分为斑蝥素,斑蝥素具有一定的刺激毒性,可使肿瘤细胞的DNA得到抑制,从而达到杀死肿瘤细胞的目的[5],另有研究表明[6],斑蝥素对患者的骨髓也有一定的刺激作用,可诱使造血干细胞分化,使粒细胞增加,使白细胞水平增加。本研究显示,治疗后,联合组的总疗效高于对照组;两组患者治疗前sIL-2R均有较高表达,治疗后联合组sIL-2R水平低于对照组,说明联合组方案可显著降低DLBCL患者血清中sIL-2R的表达,表明艾迪注射液可通过降低sIL-2R水平,影响T细胞的增值;患者KPS评分明显升高且优于对照组,表明艾迪注射液与R-CHOP方案联合治疗DLBCL可有效提高患者机体功能状态,提升患者生存质量;此外,两组不良反应发生率比较无统计学意义,表明艾迪注射液与常规R-CHOP方案联合用药的安全性没有降低。
综上所述,艾迪注射液辅助常规R-CHOP方案治疗DLBCL,可降低患者血清sIL-2R的表达水平,减少放化疗引起的不良反应,提高患者生存质量,近期治疗效果良好。
[1] 王连静,郭炜,刘丽宏.淋巴瘤中RAS相关区域家族5A基因启动子区甲基化状态及其mRNA表达与患者临床表现的关系[J].中国肿瘤生物治疗杂志,2016,23(4):537-544.
[2] 武四超.艾迪注射液联合化疗治疗食管鳞状细胞癌疗效观察[J].实用中医药杂志,2017,33(8):946-947.
[3] 陈一峰,何佩,姚锡虎,等.转化性CD20阴性弥漫性大B细胞淋巴瘤的临床病理观察[J].诊断病理学杂志,2016,23(11):875-876,880.
[4] 陆国权,周晓红,陈红,等.艾迪注射液辅助利妥昔单抗联合CHOP化疗方案治疗弥漫性大B细胞淋巴瘤[J].中国实验血液学杂志,2016,24(3):733-737.
[5] 吕秀玮,孔庆志,袁昌劲,等.艾迪注射液对Lewis肺癌荷瘤裸鼠的放射增敏作用及机制研究[J].华中科技大学学报(医学版),2018,47(1):16-19.
[6] 王明雪,殷杰,张立刚,等.艾迪注射液抗肿瘤作用及其对Th1/Th2免疫调节机制探讨[J].广州中医药大学学报,2017,34(2):299-302.

