原生硫酸盐对水泥熟料矿物形成的影响
宋文娟,曲生华,黄黎明,杨正宏
(1.同济大学 材料科学与工程学院,先进土木工程材料教育部重点实验室,上海 201804;2.中国新型建材设计研究院,浙江 杭州 310022)
0 引言
本文将来自熟料、混合材中的硫酸盐归类为原生硫酸盐。水泥熟料的主要矿物组成为 C3S、C2S、C3A、C4AF,C3S 决定着水泥熟料的主要关键性能。生料中掺入硫酸盐引入杂质离子,影响水泥熟料的烧成反应,并最终影响烧成矿物的组分和晶型,主要探讨对C3S、C2S的影响。
由于煅烧条件和外掺微量组分的不同,C3S矿物呈现7种晶型:3种三斜(triclinic)晶型 T1、T2和 T3,3种单斜(monoclinic) 晶型 M1、M2 和 M3,1 种六方晶型(rhombohedral)R。加热时,C3S矿物会发生晶型转变:

在对C3S晶型的研究中,由于X射线衍射峰型相似和多晶转变焓非常低,晶型很难用普通方法加以鉴别。J W等用热分析[1-2]、显微镜[3-4]和X射线衍射[5-6]对C3S不同晶型进行了鉴别。在纯C3S中,M3只能用高温显微镜观察到。SO3含量在一定范围内时,可以降低水泥熟料煅烧时液相初析的温度和粘度,并且增加液相量[7-8],当SO3含量过多时,会导致烧成矿物C3S晶核的形成速率变慢,使得C3S晶体生长的速度加快[8]。最终反映为较少的C3S晶核生长为尺寸大的晶体,但因其成核变慢,一定时间内形成的晶核数量减少,其晶体的总数量减少[9]。较多的SO3存在,会阻碍C2S进一步吸收CaO,不利于C3S的形成[10]。此外,SO3会倾向于与烧成熟料矿物中的C3A发生反应,形成水化硫铝酸钙(CaO·Al2O3·CaSO4·31H2O)[10-11]。
熟料中C3S的含量及其晶型晶貌特征在很大程度上决定了水泥熟料矿物水化后的性能,熟料中C3S含量越高,结晶越完整,则熟料参与水化反应后形成的水泥石强度越高[12]。在水泥熟料体系中掺加杂质离子,可以降低熟料矿物烧成时的液相形成温度及液相粘度,从而改变了C3S的晶体结构,产生畸变或缺陷,使熟料C3S形成的温度降低,水化活性提高[13]。
C2S由CaO和SiO2反应生成,多晶转变发生在1450℃以下的温度环境中。C2S在室温下有水硬性的α、αH′、αL′、β四种晶型转变,处于介稳状态,有转变为γ型的趋势。β型C2S转变为γ型C2S,体积会膨胀10%,致使物料有一定程度的粉化。在高温下,不同晶型与C2S所固溶的氧化物种类、数量有关,烧成产物冷却的起始温度与速率也会影响不同晶型的生成,据此可以生产出不同的C2S高温晶型[14]。α型与α′型的晶体强度有可能较β型高,且生成温度较高。
当前有关硫酸盐对水泥水化硬化性能影响的研究颇多,但将硫酸盐掺入水泥生料进行熟料煅烧,进而研究原生硫酸盐类型和含量对熟料矿物形成影响的研究较少,原生硫酸盐作为引入的杂质,影响熟料矿物烧成体系,改变熟料矿物组成和矿物微结构,进而在熟料水化过程中对熟料的水化性能产生影响,因此研究原生硫酸盐对水泥熟料矿物组成和矿物微结构的影响有重要意义。
1 试验
1.1 试验材料
硫酸盐:CaSO4、Na2SO4、K2SO4,分析纯。
水泥熟料:在实验室烧制而成,由 CaCO3、SiO2、Al2O3、Fe2O34种纯化学试剂按一定的比例混料,本实验采用的生料配比石灰饱和系数(KH)、硅率(SM)和铝率(IM)主要参照国内大型水泥生产厂的常用率值,取KH=0.915,SM=2.5,IM=1.76。掺CaSO4、Na2SO4、K2SO4烧成水泥熟料的样品配比分别见表1~表3,所有硫酸盐掺量均折合成SO3掺量计算。

表1 掺CaSO4烧成水泥熟料的样品配比

表2 掺Na2SO4烧成水泥熟料的样品配比

表3 掺K2SO4烧成水泥熟料的样品配比
1.2 试样制备
将 CaCO3、SiO2、Al2O3、Fe2O3四种分析纯化学试剂混合为基准组,依据表1~表3配比分别掺入CaSO4、Na2SO4、K2SO4,球磨机以500 r/min速度均匀混合3 min,用钢模将粉末压成直径为20 mm的圆饼,放入高温炉内,在90 min内升温至1450℃煅烧至f-CaO含量小于1%,从高温炉取出,在空气中急冷制得含原生硫酸盐的水泥熟料。
1.3 性能测试方法
利用X射线荧光光谱分析(XRF)测试烧成产物的化学成分;X射线衍射仪(XRD)测试烧成熟料矿物的组成和微结构,X射线衍射仪的工作条件:CuKα,管电压40 kV,管电流30 mA,步进扫描,步进宽度为0.05°,步进时间为4 s。
2 结果与讨论
2.1 原生CaSO4对水泥熟料矿物形成的影响
2.1.1 原生CaSO4对水泥熟料矿物组成的影响
(见图1)

图1 不同CaSO4掺量的烧成水泥熟料试样XRD图谱
由图1可知,掺加不同质量的CaSO4烧成的熟料基本矿物组成都为 C3S、C2S 和 C3A,还有少量的 C4AF(2θ=33.8°处),并且在所有的试样中都未发现有CaO的衍射峰,说明CaCO3分解以后完全反应生成熟料矿物。虽然基本组成相同,但是每种矿物的成分比例有差别。可以看出,随着CaSO4掺量的增加,C2S的含量有所增加。不掺CaSO4的试样中C3A含量明显比掺入CaSO4的试样含量高,主要原因是加入CaSO4后,熟料烧成过程中形成了较多的C4A3S,与矿物组分中的Al结合反应,Al参加反应后被消耗,在一定程度上抑制了C3A的形成[15]。试样C2(掺CaSO4,折合SO3掺量为2.4%)的XRD图谱中,C3S的衍射峰明显强于其它试样,这与C3S在形成过程中的晶型转变有关。
2.1.2 原生CaSO4对水泥熟料矿物微结构的影响
在硅酸盐水泥熟料组成矿物中,其中2种矿物C2S和C3S的晶体结构有多种。C2S具有岛状结构,主要有5种晶型,分别是α型、αH′型、αL′型、β型和γ型,纯C2S在常温下呈γ型,具有典型的橄榄石结构,但当外来离子固溶进C2S晶体结构时,可以阻止在温度降低过程中高温晶型向低温晶型的转变[16-17]。原生CaSO4对水泥熟料矿物微结构的影响见图2。

图2 不同CaSO4掺量的烧成水泥熟料试样在2θ为31°~33°和 51°~53°范围的 XRD 图谱
分析图2可以得出,掺有CaSO4烧成的水泥熟料中存在的C2S主要为β型,有少量的γ型。为了减小表面能,β-C2S和γ-C2S成核时晶核的晶界上会吸附大量的稳定离子,稳定离子的存在阻碍了晶核晶界运动,使得晶核难以长大。C2S由α型向β型转变属于位移转变,不需要克服很高的能量势垒,晶界表面的离子产生的阻碍能量不足以阻止α型向β型的转变。β型向γ型的转变属于重建型转变[18],需要克服的势垒能量较高,晶界表面少量的稳定离子便可以阻碍β型向γ型的转变,从而阻碍γ-C2S成核和长大[19]。
C3S有T1型、T2型、T3型、M1型、M2型、M3型和R型7种晶体结构。常温下,纯的C3S是以T型存在的,掺加杂质离子后,普通硅酸盐水泥熟料矿物中C3S主要是R型,在掺入其它微量元素以后,也可能是以M型存在。本文采用的分析方法是根据 X 射线衍射角 2θ=32°~33°和 2θ=51°~52°的衍射峰型变化来判断C3S的晶型,衍射角在51°~52°处的峰型变化最为明显,在此处单衍射峰为R型C3S,双衍射峰为M型C3S,三衍射峰为 T 型 C3S[4,20]。
从图2可以看出,未掺CaSO4时,试样的XRD衍射图谱具有较好的对称性,在2θ为32°~33°出现了2个明显的衍射分叉峰,对称性良好,在 51°~52°范围内出现以(220)晶面为对称的峰型,判定为R型C3S。掺CaSO4,折合SO3掺量达到2.4%时,2θ=32°~33°处的衍射峰不对称性明显增强,但是 51°~52°范围内在2θ=51.6°的衍射峰明显出现了分裂峰,并随着掺量增加到3.6%时,此处的峰更为明显的分裂为(420)和(240)峰,随着CaSO4掺量的增加,C3S从R型转变为M1型。折合SO3掺量大于2.4%时,C3S衍射峰突变的非常强,晶型结构发生变化,可以认为CaSO4的掺入会导致C3S结构转变,发生晶型突变,结晶度提高。
2.2 原生Na2SO4对水泥熟料矿物形成的影响
2.2.1 原生Na2SO4对水泥熟料矿物组成的影响
(见图3)

图3 不同Na2SO4掺量的烧成水泥熟料试样XRD图谱
分析图3可知,在生料中掺入1.2%Na2SO4时,烧成的水泥熟料矿物成分主要是C3S,有少量的C2S、C3A。掺Na2SO4,折合SO3掺量达到2.4%时,熟料矿物中还存有较多未参加吸收反应的CaO。观察C3S和C2S的衍射峰强度,与折合SO3掺量为1.2%的比较,掺量为2.4%时样品的C3S衍射峰明显减弱,C2S的衍射峰明显增强,说明当掺Na2SO4,折合SO3掺量达到2.4%时,Na2SO4的掺入抑制了C2S吸收CaO参与反应,从而抑制了C3S的生成。当折合SO3掺量达到3.6%时,C2S与CaO的生成量增加,生成少量的C3S和C3A,说明Na2SO4掺量的增加对C2S吸收CaO参与反应的抑制效果更加明显。此外还有一个很强的Ca(OH)2衍射峰,这是CaO吸湿与水反应的结果。
由图3可以看出,随着Na2SO4掺量的增加,烧成水泥熟料中C3S的衍射峰越来越弱,C2S和CaO的衍射峰逐渐增强,说明Na2SO4的掺入会对C2S在高温下吸收CaO的反应起到抑制作用。
2.2.2 原生Na2SO4对水泥熟料矿物微结构的影响(见图4)
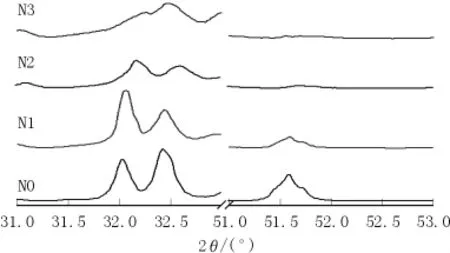
图4 不同Na2SO4掺量的烧成水泥熟料试样在2θ为31°~33°和 51°~53°范围的 XRD 图谱
由图4可见,掺Na2SO4烧成的熟料矿物中,2θ为32.0°和32.1°处,C2S的衍射峰最强,参考《材料图谱手册》分析,确定为β型C2S。当掺Na2SO4,折合SO3掺量达到2.4%、3.6%时,2θ为32.5°处也有较强的C2S衍射峰,此处衍射峰最强的为γ型C2S。说明Na2SO4的掺入促进了β型C2S向γ型C2S的转变。
掺 Na2SO4,折合 SO3掺量为 1.2%时,2θ为 31°~33°范围内的衍射峰明显不对称,并且在2θ为51°~53°范围内的衍射峰分叉成2个峰,此时熟料中的C3S主要为M型,结合衍射峰的不对称性,进一步确定C3S的晶型为M1型。折合SO3掺量达到2.4%时,此时虽然在2θ为51°~53°处的衍射峰比较弱,但是此处开始出现3个分叉峰,且在2θ为31°~33°范围内出现第3个衍射峰,此时的C3S晶型应为T1型。
图4显示,烧成的水泥熟料矿物中C2S的含量很高,在2θ为31°~33°范围内的衍射峰已经被C2S影响,无法用来准确判断C3S的晶体结构,虽然2θ为51°~53°范围内的衍射峰非常弱,但还是可以看出较为明显的3个对称性好的衍射峰,可以认为,掺Na2SO4,当折合SO3掺量达到3.6%时,烧成的水泥熟料中少量的C3S晶型为T2型。
2.3 原生K2SO4对水泥熟料矿物形成的影响
2.3.1 原生K2SO4对水泥熟料矿物组成的影响
(见图5)

图5 不同K2SO4掺量的烧成水泥熟料试样XRD图谱
分析图5可知,掺K2SO4,折合SO3掺量为1.2%的烧成水泥熟料中矿物组成主要是C3S、C2S、C3A和少量的C4AF。掺有K2SO4的熟料矿物中C3A含量少于未掺K2SO4的熟料试样。随着K2SO4掺量的增加,C3A的衍射峰强度逐渐变弱,可能是因为液相粘度降低导致C3A的含量降低。并且随着K2SO4掺量的增加在2θ=33.8°处C4AF的衍射峰也更加明显,说明液相粘度的降低促进了C4AF的生成。当折合SO3掺量为3.6%时,2θ=30.7°处的衍射峰明显强于其它几组,该处的衍射峰为K2SO4的衍射峰,说明K2SO4掺量较大时,经过高温煅烧后,还有部分K2SO4未参与反应,残存于熟料当中。
2.3.2 原生K2SO4对水泥熟料矿物微结构的影响
(见图 6)

图6 不同K2SO4掺量的烧成水泥熟料试样在2θ为31°~33°和 51°~53°范围的 XRD 图谱
由图6可以看出,掺入K2SO4烧成的水泥熟料中有少量的 C2S,衍射峰主要在 2θ为 30.9°、31.8°、32.5°和 34.2°。其中主要为β型C2S,另外还有少部分的γ型C2S。当在水泥生料中掺入 K2SO4,折合 SO3掺量为 1.2%时,2θ为 31°~33°处的衍射峰对称性较差,并且呈现为左高右低的形态;在2θ为51°~53°处的衍射峰出现分叉,此时生成的是M1型C3S。当折合SO3掺量达到2.4%时,生成的C3S的结构变化不大,但是衍射峰有向2θ值变大的方向移动,根据布拉格公式2dsinθ=nλ,说明K2SO4掺量的增加导致了d值的减小。当折合SO3掺量达到3.6%时,在2θ为31°~33°处的衍射峰的对称性很高,且在2θ为 51°~53°之间出现了(040)和(620)2个峰,可以判断此时生成的是M2型C3S。
3 结论
(1)未掺硫酸盐时,烧成的熟料矿物组成以C3S、C3A为主,含有少量的C2S与C4AF。矿物中C2S主要为β型,少部分的为γ型,C3S为对称性较好的R型。
(2)掺入CaSO4烧成水泥熟料,烧成熟料的主要矿物组成是C3S,CaSO4的掺入使熟料中C3A的含量减少。掺入CaSO4对生成矿物中C2S的结构没有很大的影响,C3S的结构由R型向M2型转变。
(3)Na2SO4对烧成熟料矿物组成和结构的影响最大,抑制了C3S的生成,提高了C2S的生成量,促进了C3A的生成。Na2SO4的掺量对C3S的晶型影响明显,随着掺量的增加,C3S的晶型向M1、T1、T3型转变。Na2SO4有利于β型C2S的稳定。
(4)K2SO4的掺入降低了熟料烧成过程中的液相粘度,利于C3S和C4AF的形成,抑制C3A的生成,当掺量较大(3.6%)时,部分 K2SO4不能参与反应。K2SO4的掺量影响C3S的晶型转变,随着掺量的增大,C3S晶型逐渐向M1、M2型转变。K2SO4都有利于β型C2S的稳定。
[1] Jeffery J W.Crystal Structure of Tricalcium Silicate and Cobalt-Mercury Thiocyanate[D].London:London University,1950.
[2] Jeffery J W.The crystal structure of tricalcium silicate[J].Acta Crystallographica,1952,5(1):26-35.
[3] Jeffery J W.The Tricalcium Silicate Phase[C]//Proc.of the 3rd ISCC,London,1954:30-48.
[4] BIGARé M,Guinier A,Mazières C,et al.Polymorphism of Tricalcium Silicate and Its Solid Solutions[J].Journal of the American Ceramic Society,2006,50(11):609-619.
[5] Guinier A,Regourd M.Structure of Portland cement minerals[C]//Proc.of the 5th ISCC,Tokyo,1968:1-41.
[6] Regourd M.Polymorphisme du silicate tricalcique.Nou velles donnee′s de la diffraction des rayons X,C.R.[J].Acad.Sci.,Sci.Paris Terre,1979,289:17-20.
[7] 沈威,黄文熙,闵盘荣.水泥工艺学[M].武汉:武汉工业大学出版社,1991.
[8] 王善拔.复合矿化剂理论和实践中的几个问题[J].水泥,1995(9):1-5.
[9] 赵改菊.水泥生料的固硫行为及硫铝酸盐的形成机理研究[D].武汉:武汉理工大学,2004.
[10] 毛若卿,熊家国,潘国耀,等.F、Cl、SO3对C2AS形成的影响[J].武汉理工大学学报,1997(4):13-15.
[11] Regourd M,Bolkova A.Chemistry,structure,properties and quality of clinker[C]//Proceedings of the 9th International Congress of the Chemistry of Cement,New Delhi,1992:3-45.
[12] 郭向阳.掺杂BaO/BaSO4对高阿利特水泥熟料合成及性能的影响[D].济南:济南大学,2010.
[13] 马素花,沈晓冬,钟白茜.掺杂对高胶凝性水泥熟料矿物形成影响的研究进展[J].材料导报,2006,20(10):92-96.
[14] 吕辉,钟景裕,樊粤明.少量异组分对贝利特性能的影响[J].华南理工大学学报,1996,24(2):92-96.
[15] 谢峻林,肖飞燕,韩春华,等.高硫煤燃烧对水泥熟料矿物形成过程的影响[J].武汉理工大学学报,2007,29(5):31-33.
[16] Mondal P,Jeffery J W.The crystal structure of tricalcium aluminate,Ca3Al2O6[J].Acta Crystallographica,1975,31(3):689-697.
[17] NishiF,TakéuchiY.The Al6O18,ringsoftetrahedra in the structure of Ca 8.5 NaAl6O18[J].Acta Crystallographica,1975,31(4):1169-1173.
[18] Regourd M,Bigare M,Guinier A.Synthesis and crystallographic investigation of some belites[J].Journal of Analytical Atomic Spectrometry,1968,14(11):1743-1748.
[19] 冯修吉,龙世宗.微量离子对β-C2S稳定性的影响及其机理研究[J].硅酸盐学报,1985(4):34-42.
[20] TaylorH F W.Cement chemistry[M].2ndEdition.London:Thomas Telford Publishing,1997.

