聚3,4-乙烯二氧噻吩在海洋微生物燃料电池阳极改性中的应用
陈占飞,郑 智,宋宇宁,刘红豆,王 珊,徐方成
(厦门大学化学化工学院,福建 厦门 361005)
微生物燃料电池(MFC)是一种特殊的燃料电池,它以微生物为催化剂,废弃生物质、有机废水等有机物作为燃料,通过生物氧化产生电能.常规燃料电池的阳极和阴极都是化学电极,而MFC的阳极是生物电极,阴极仍然是化学电极[1].因此,MFC的阴极可以借助传统燃料电池技术进行设计,而其阳极必须开展基础研究.传统燃料电池的催化剂一般是一次性固定在电极表面,而MFC的阳极催化剂(也就是阳极表面生物膜)是在MFC启动过程中逐渐形成的.有机物通过扩散传递到生物膜内,被产电菌氧化分解,产生的一部分电子通过胞外电子传递途径传递到细胞外部,再经过生物膜内细胞与细胞之间的传递,最终到达电极表面.现有研究已发现,产电微生物主要通过细胞外膜上的细胞色素C、纳米导线以及分泌可溶性电子介体3种途径实现胞外电子传递[2-3].MFC的阳极实际上是微生物与电极相互作用的结果,其性能不仅与产电微生物的种类和电化学活性有关,而且电极材料对其也有重要影响.
目前,MFC的阳极设计仍然缺乏系统的理论指导[4].大多数研究采用碳材料作为MFC的阳极,如石墨块、碳纸、碳布和碳毡[5].尽管碳材料质量轻,抗腐蚀性好,但碳材料脆性大,二次加工困难,而且也不太容易吸附微生物.高分子聚合物普遍具有耐腐蚀、易加工和成本低的优点,将导电聚合物涂布在普通基材表面,可以简单、快速地改变电极特性,该方法已经逐渐成为MFC电极改性的一个新的发展方向.常见的导电聚合物有聚苯胺、聚吡咯、聚噻吩等以及其衍生物[6].与其他导电聚合物相比,聚3,4-乙烯二氧噻吩(PEDOT)具有极好的化学稳定性、高电导率和良好的生物相容性,很适合作为MFC的电极涂层.近年来,已有将PEDOT用作MFC的阳极涂层或黏结剂的研究报道[7-9].Liu等[7]采用电化学聚合法,在碳纸、碳毡表面合成了一层PEDOT膜,并认为三维纳米多孔结构是PEDOT提高Shewanellaloihica产电的原因.Wang等[8]以大肠杆菌(Escherichiacoli)为测试菌种,PEDOT作为纳米石墨烯黏结剂,考察了石墨烯对MFC产电的影响.Kang等[9]以活性污泥作为菌种来源,研究了PEDOT修饰的石墨板、石墨毡和碳布对产电的影响.Yong等[10]以S.oneidensisMR-1作为产电菌,导电聚合物改用聚苯胺作为黏结剂,将纳米石墨烯固定在碳毡表面,考察了石墨烯对MFC产电的影响.这些研究主要采用来自陆地环境的产电菌纯种或活性污泥作为阳极催化剂,并指出MFC产电能力的提高主要得益于导电聚合物改进了阳极表面的三维立体结构,增加了电极的比表面积.
研究PEDOT对MFC产电的作用,不仅要考虑PEDOT的导电作用和三维立体结构作用,而且应该考虑PEDOT本身的化学性质作用.尽管掺杂纳米颗粒能提高PEDOT的导电特性和电极的比表面积,从而进一步提高MFC产电,但掺杂有可能劣化PEDOT在基材表面的附着能力以及材料的长期稳定性.是采用比较平整的纯PEDOT膜,还是采用含有高电导率的纳米材料(如石墨烯)掺杂的复合膜,需要从MFC性能、电极制备难易程度、材料长期稳定性等多方面综合考虑,来进一步优化PEDOT在MFC中的应用.
本研究采用循环伏安法在石墨电极表面聚合形成PEDOT薄膜,以海洋产电菌Shewanellasp. S2为菌种材料,制成MFC,并探讨PEDOT对海洋产电菌产电的影响及机制.
1 材料与方法
1.1 电极制备和PEDOT膜检测分析
电极采用大小为28 mm×7 mm×3 mm的高纯石墨块(99.9%,天津艾达恒晟科技发展有限公司),用100~5 000目的氧化铝砂纸,从粗到细将石墨表面抛光.再通过酸洗和碱洗除去表面的金属氧化物和油污.采用直径0.2 mm 的细钛丝(外面套耐高温绝缘管)与石墨块相连.
石墨块表面聚合PEDOT薄膜的制备方法如下:石墨块作为工作电极,Ag/AgCl(3 mol/L KCl)和Pt棒分别作为参比电极和对电极,在电化学工作站CHI660E(上海辰华仪器有限公司)控制下采用循环伏安法聚合;扫描电压范围为0~1.2 V,扫描速率为0.01 V/s,扫描圈数为10 圈;乙烯二氧噻吩(EDOT)的浓度为0.01 mol/L,高氯酸锂作为引发剂.聚合完成后用大量去离子水冲洗,除去表面残留的EDOT溶液,制备好的电极浸泡在去离子水中备用.
采用能谱(EDS)仪(日本HITACHI公司,S-4800)通过测量元素C以及PEDOT特征元素(O和S)判断PEDOT是否聚合在石墨基材表面.石墨电极标记为G,PEDOT修饰的石墨电极标记为PEDOT/G.
1.2 产电菌菌种和培养基
测试菌株来自厦门近海的海洋产电菌Shewanellasp. S2[11],采用2216E培养基(西宝生物科技股份有限公司)好氧培养.配制M6溶液模拟海水基础盐溶液[12],在M6溶液中加入20 mmol/L乳酸钠和1 g/L氯化铵,作为Shewanellasp. S2在MFC阳极室的产电培养基,即阳极溶液.所有化学试剂均为分析纯,购自国药集团化学试剂有限公司.
1.3 U型MFC的制作和启动
采用U型MFC分析PEDOT修饰阳极对产电的影响.U型MFC由两个带球形接头的L型玻璃弯管(内径20 mm)对接而成,中间夹一片质子交换膜(杜邦N112,上海河森电气有限公司)和O型密封圈,用平行夹夹紧密封.外接510 Ω电阻,用多通道万用数字电表(Keithley 2700,Keithley Instruments,Inc.,美国)测量510 Ω电阻两端电压,每5 min采集一次.阴极溶液为含有50 mmol/L铁氰化钾的0.1 mol/L磷酸盐缓冲液(pH 7.0).两室的装液量均为25 mL左右,预先通过渗透实验用NaCl调整阴极室的离子强度,以保证质子交换膜两侧的渗透压平衡.设立两组MFC,一组阳极为PEDOT/G,另一组为G.两组MFC的阴极均采用PEDOT/G电极.产电菌采用2216E培养基培养到对数末期,在7 000 r/min下离心5 min 后,菌泥用M6溶液悬浮后接种到阳极室.阳极溶液中的生物量用溶液在600 nm的吸光度(即菌浊度A600)表示,初始A600为0.3~0.4.产电培养基中的乳酸钠,待MFC电压曲线的基线平稳后,单独用注射器加入.
1.4 极化曲线测量和电化学阻抗分析
传统燃料电池的阳极催化剂是固定的,但MFC的阳极催化剂是在人工电子受体(即阳极)胁迫下逐步建立起来的.通常在电极表面生物膜达到稳定后,通过外电阻法或线性伏安扫描法获得极化曲线[13].本研究采用线性伏安扫描法,扫描从开路电压开始,0 V 结束,扫描速率为1 mV/s.
电化学阻抗谱(EIS)的测量:工作电极分别为G电极和PEDOT/G电极,参比电极和对电极分别为Ag/AgCl电极和Pt网电极;振幅为10 mV,频率从1 000 kHz到0.01 Hz,起始电压为开路电压.本研究采用Lu等[14]报道的EIS方法和等效电路模型:将整个MFC简化为R0(R1C1)(R2C2) 等效电路,其中R0为溶液和隔膜的电阻,R1和C1分别为阳极的电阻和电容,R2和C2分别为阴极的电阻和电容.采用的EIS模拟软件为ZsimDemo 3.30d.
1.5 阳极表面细胞形态分析
MFC运行结束之后,取出阳极,先在2.5%(体积分数)戊二醛溶液中浸泡4 h以灭活细胞;然后在装有0.1 mol/L磷酸盐缓冲液(pH 7.0)的离心管(5 mL)中换液浸泡2~3次,每次15 min左右;再将阳极依次浸入梯度乙醇溶液(体积分数为30%,50%,70%和100%)中进行脱水处理,每个梯度浸泡15 min;最后将阳极放入真空干燥箱内保存.用S-4800扫描电镜(SEM,日本HITACHI公司)观察产电菌在电极表面的形态.
2 实验结果
2.1 阳极PEDOT修饰
从图1可知:在0~0.1 V,氧化电流从-2 mA增加到1 mA;在0.1~0.7 V,氧化电流基本没有变化;在0.7~1.2 V,氧化电流由1 mA迅速增加到12 mA左右,这表明PEDOT是在高电位下聚合而成的.在高电位,EDOT单体在高氯酸锂的氧化下形成阳离子自由基,然后自由基之间发生聚合形成短链,随着反应时间延长聚合链长度不断增加,最终形成PEDOT薄膜.
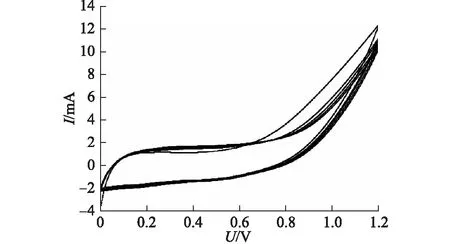
0.01 mol/L EDOT溶液,扫描速率10 mV/s,扫描范围0~1.2 V (vs. Ag/AgCl).图1 石墨阳极表面聚合PEDOT的循环伏安图Fig.1 Cyclic voltammograms of PEDOT modification on graphite anode

图2 石墨阳极(a,b)和PEDOT修饰石墨阳极(c,d)的SEM和EDS图Fig.2 SEM and EDS images of pure graphite anode (a,b) and PEDOT modified graphite anode (c,d)
图2是两种电极的SEM和EDS的表征结果.从SEM图看,G电极表面比较平坦;PEDOT在PEDOT/G电极表面总体呈片状,并带有一些颗粒状凸起(直径约200 nm).EDS分析表明,未修饰的G电极只有C元素,而修饰后的PEDOT/G电极除了C元素以外还有O和S元素,这两种元素只能来自PEDOT分子,说明PEDOT已经聚合到石墨电极表面.
2.2 MFC产电量分析

箭头所示为乳酸纳加入时间点.图3 PEDOT修饰石墨阳极对MFC产电的影响Fig.3 Effects of PEDOT modified graphite anode on MFC current production
MFC的产电曲线如图3所示,开始产生的电流不是产电菌产生的电流,而是由阳极室和阴极室的离子强度差异等因素造成的.由于加入的产电菌本身也是一类特殊的带电粒子,有一定的离子强度,但无法精确估计,所以等电压信号基本归零(基线平稳)后,再用注射器将乳酸钠注入到阳极室.从图3可知:加入乳酸钠后MFC电流迅速上升.在稳定期,以PEDOT/G为阳极的电流密度可以达到约173.6 mA/m2,是以G为阳极(74.4 mA/m2)的2.33倍.前期研究[11]表明,采用以G为阳极的H型MFC时,Shewanellasp. S2产生的电流密度可以达到66.1 mA/m2.本研究采用U型MFC,缩短了阳极和阴极之间的距离从而减少了内阻,提高了产电量,但提高幅度不大;而采用PEDOT修饰石墨阳极后,电流密度得到显著提高,说明PEDOT修饰是一种提高MFC产电量的有效方法.产电结束时乳酸钠已经消耗完毕,理论上产电量为289.5 C,利用Origin软件对产电曲线进行积分和换算,以G和PEDOT/G为阳极的MFC的产电量分别为33.8和98.6 C,二者的库伦效率分别为11.7%和34.1%.

图4 未修饰(a)和PEDOT修饰(b)石墨阳极的MFC极化曲线和功率密度曲线Fig.4 Polarization and power density curves of MFCs with unmodified (a) and PEDOT modified (b) graphite anodes

图5 未修饰(a)和PEDOT修饰(b)的石墨阳极MFC启动阶段的EIS Nyquist图Fig.5 Nyquist plots of EIS test during start-up stage of MFCs with unmodified (a) and PEDOT modified (b) graphite anodes
2.3 极化曲线分析
当MFC运行一定时间后,产电曲线基本稳定,达到相对稳态,此时将MFC装置与电化学工作站相连接进行线性伏安扫描,测得MFC的极化曲线.再将极化曲线进行线性拟合,所得斜率的绝对值即为电池的表观内阻.如图4所示,通过线性拟合得到以PEDOT/G为阳极的电池表观内阻为390 Ω,是以G为阳极(471 Ω)的83%.二者的最大功率密度分别为40和26 mW/m2.
2.4 EIS的比较
从图3可知,运行到第7天(168 h),两种MFC的产电都进入稳定期,因此,图5的EIS分析只记录前7 d的数据.采用等效电路R0(R1C1)(R2C2) 拟合图5的EIS数据,得到两种MFC的阳极电阻和电容(图6).结果表明,无论是PEDOT/G 电极还是G 电极,阳极电阻R1均随着MFC运行时间增加呈下降趋势.在起始阶段,PEDOT/G和G电极的R1分别约为8.1和19 kΩ;运行7 d后,R1分别降至0.135和2 kΩ左右.从图3可知,第1天生物膜还没有形成,第7天生物膜已经达到稳定值.EIS模拟结果显示,无论是否形成生物膜,PEDOT修饰后的R1都小于未修饰的石墨阳极,而阳极电容C1则都大于未修饰的石墨阳极,表明PEDOT修饰石墨阳极能降低阳极电阻并增大电容.
3 讨 论

图6 两种MFC启动阶段的阳极电阻R1(a)和电容C1(b)Fig.6 Resistance R1 (a) and capacitance C1 (b) of anodes of two types of MFC during start-up stage
原核生物的呼吸链在细胞膜上,其呼吸作用属于胞内电子传递.产电菌用的是胞外电子传递链,代谢产生的电子沿着呼吸链传递一段距离后,最终通过细胞表面的细胞色素C或纳米导线传递给电极.MFC的阳极是生物电极,阳极电位不仅与外膜上的氧化还原载体的种类和数量有关,而且还和胞外电子传递路线、生物膜结构等很多因素有关[15].50 mmol/L铁氰化钾的氧化还原电位在0.2 V(vs. Ag/AgCl)左右,结合极化曲线图(图4),可知在本研究条件下阳极电势在0 V(vs. Ag/AgCl)左右.从图1可知,在0~0.6 V(vs.Ag/AgCl)范围内PEDOT没有氧化还原峰,说明PEDOT用于Shewanellasp. S2产电的电化学性质是稳定的.PEDOT能促进海洋产电菌Shewanellasp. S2产电(图3).

图7 未修饰(a)和PEDOT修饰(b)的石墨阳极吸附产电菌的SEM图Fig.7 SEM images of exoelectrogenic cell adsorption on unmodified (a) and PEDOT modified (b) graphite anodes
关于PEDOT促进MFC产电的机制,目前还缺乏详实的研究数据和结论.很多学者认为PEDOT通过促进电极表面形成高度立体结构,提高了电极比表面积从而促进产电[7-9,16].因此,把PEDOT和聚苯胺等导电聚合物用作黏结剂,将氧化石墨烯等高导电物质黏结在电极表面以促进MFC产电[8,10].但本研究中,如图2所示,导电聚合物PEDOT在石墨基材表面比较平整,有一些直径200 nm左右的PEDOT凸起(表面粗糙度),并未形成明显的三维结构,而海洋产电菌Shewanellasp. S2为直径0.7 μm、长1.5 μm的杆菌,其宽度和长度远大于阳极表面的粗糙度,因此,可以排除PEDOT的三维立体结构作用,且粗糙度对单位电极表面产电菌数量的影响几乎可以忽略不计.从图7可知,海洋产电菌Shewanellasp. S2没有完全覆盖两种电极的表面,但PEDOT修饰电极表面的细菌密度明显高于未修饰的石墨电极.PEDOT是带正电的高分子聚合物,而细胞表面通常是带负电的,电荷的相互作用促进了更多产电菌吸附在PEDOT/G电极表面.产电菌增加意味着阳极有更多的催化剂用于催化分解有机物,从而促进MFC产电.这说明MFC产电能力的提高主要是由于PEDOT本身的化学特性,而不是其空间几何形态.
4 结 论
本研究采用循环伏安法在石墨电极表面聚合PEDOT薄膜,制备的以PEDOT/G为阳极的MFC在稳定期的电流密度达到173.6 mA/m2,产电量为98.6 C,库伦效率为34.1%,最大功率密度为40 mW/m2,均比以G为阳极的MFC有明显提高,且PEDOT修饰石墨电极后,电池表观内阻和阳极电阻均有所下降,而阳极电容上升.SEM表征结果显示,PEDOT修饰电极表面的粗糙度远小于产电菌的尺寸,推测其MFC产电能力的提高主要是由于PEDOT与产电菌间的电荷相互作用,提高了修饰电极表面的产电菌吸附量.
[1] LOGAN B E.Microbial fuel cells[M].Hoboken,New Jersey:John Wiley & Sons,Inc.,2008:4-6.
[2] LOVLEY D R.Microbial fuel cells:novel microbial physiologies and engineering approaches[J].Current Opinion in Biotechnology,2006,17(3):327-332.
[3] FRAIWAN A,CALL D F,CHOI S.Bacterial growth and respiration in laminar flow microbial fuel cells[J].Journal of Renewable and Sustainable Energy,2014,6(2):023125.
[4] LOGAN B E.Scaling up microbial fuel cells and other bioelectrochemical systems[J].Applied Microbiology and Biotechnology,2010,85(6):1665-1671.
[5] FOLEY J M,ROZENDAL R A,HERTLE C K,et al.Life cycle assessment of high-rate anaerobic treatment,microbial fuel cells,and microbial electrolysis cells[J].Environmental Science & Technology,2010,44(9):3629-3637.
[6] ATES M,KARAZEHIR T,SARAC S A.Conducting polymers and their applications[J].Current Physical Che-mistry,2012,2(3):224-240.
[7] LIU X,WU W G,GU Z Z.Poly (3,4-ethylenedioxythiophene) promotes direct electron transfer at the interface betweenShewanellaloihicaand the anode in a microbial fuel cell[J].Journal of Power Sources,2015,277:110-115.
[8] WANG Y,ZHAO C E,SUN D,et al.A graphene/poly(3,4-ethylenedioxythiophene) hybrid as an anode for high-performance microbial fuel cells[J].ChemPlusChem,2013,78(8):823-829.
[9] KANG Y L,IBRAHIM S,PICHIAH S.Synergetic effect of conductive polymer poly (3,4-ethylenedioxythiophene) with different structural configuration of anode for microbial fuel cell application[J].Bioresource Technology,2015,189:364-369.
[10] YONG Y C,DONG X C,CHAN-PARK M B,et al.Macroporous and monolithic anode based on polyaniline hybridized three-dimensional graphene for high-perfor-mance microbial fuel cells[J].ACS Nano,2012,6(3):2394-2400.
[11] 王彪,黄杰勋,章晓波,等.一株海洋产电菌Shewanellasp. S2的筛选和产电分析[J].微生物学通报,2010,37(3):342-348.
[12] XU F,MOU Z,GENG J,et al.Azo dye decolorization by a halotolerant exoelectrogenic decolorizer isolated from marine sediment[J].Chemosphere,2016,158:30-36.
[13] PÉREZ-RODRGUEZ P,OVANDO-MEDINA V M,MARTNEZ-AMADOR S Y,et al.Bioanode of polyurethane/graphite/polypyrrole composite in microbial fuel cells[J].Biotechnology and Bioprocess Engineering,2016,21(2):305-313.
[14] LU Z,GIRGUIS P,LIANG P,et al.Biological capacitance studies of anodes in microbial fuel cells using electrochemical impedance spectroscopy [J].Bioprocess and Biosystems Engineering,2015,38(7):1325-1333.
[15] BARON D,LABELLE E,COURSOLLE D,et al.Electrochemical measurement of electron transfer kinetics byShewanellaoneidensisMR-1[J].Journal of Biological Chemistry,2009,284(42):28865-28873.


